Morbo di Alzheimer AD Alzheimers Disease AD patologia

Morbo di Alzheimer (AD = Alzheimer’s Disease)

AD: patologia neurodegenerativa 1906, Alois Alzheimer Descrizione di una demenza senile non correlabile semplicemente all’età Sintomi Perdita della memoria Disorientamento Confusione Allucinazioni Paranoia Agitazione Aggressività Ansia Depressione Insonnia

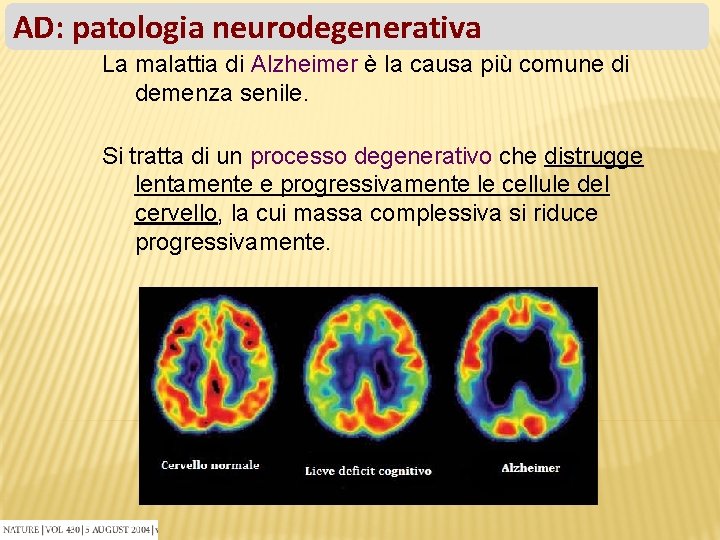
AD: patologia neurodegenerativa La malattia di Alzheimer è la causa più comune di demenza senile. Si tratta di un processo degenerativo che distrugge lentamente e progressivamente le cellule del cervello, la cui massa complessiva si riduce progressivamente.
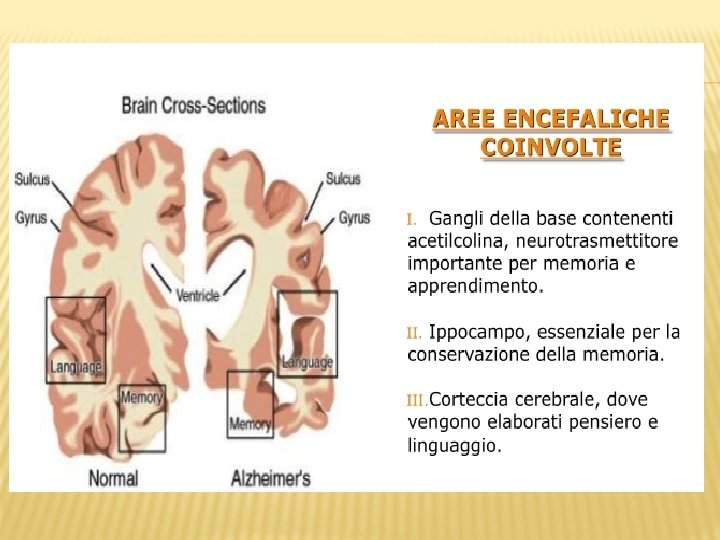

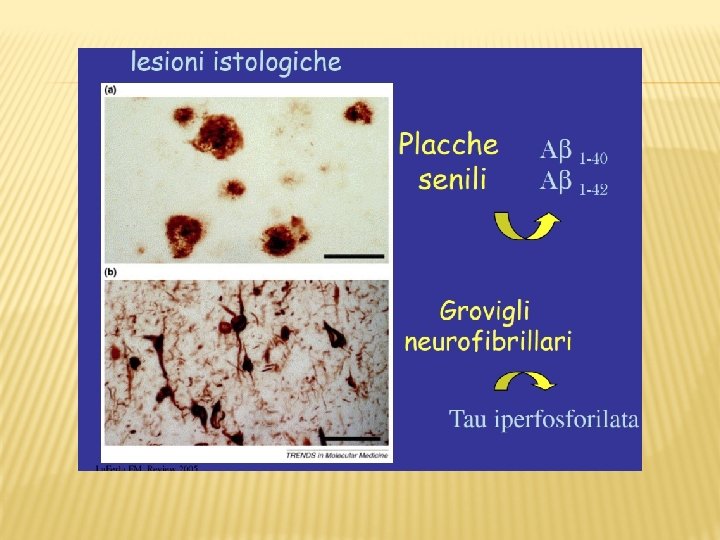
AD: marchi della patologia (hallmarks) • Placche cerebrali (cerebral plaques) Densi accumuli extracellulari di natura proteica (A , -amiloide come principale componente) circondati da neuroni danneggiati • Ammassi neurofibrillari (neurofibrillary tangles) Aggregati intracellulari costituiti prevalentemente da una forma iperfosforilata della proteina TAU • Sono semplicemente “marchi” o anche cause della patologia? • Se cause, quali dei due marchi è associato agli eventi iniziali della patologia?
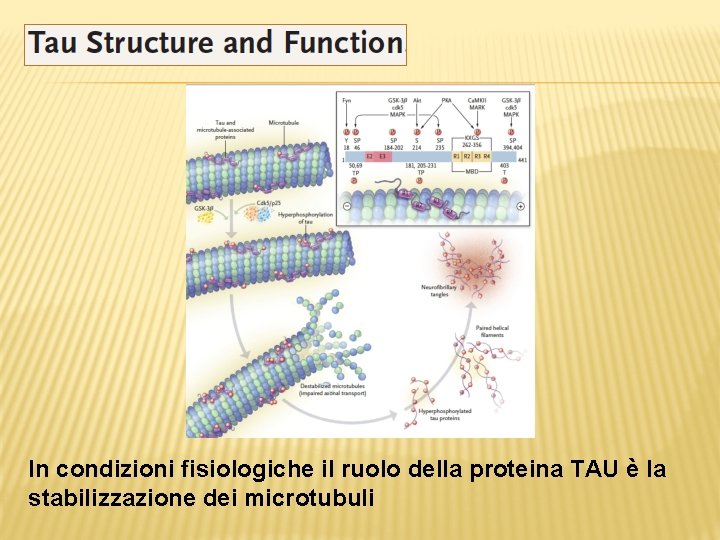
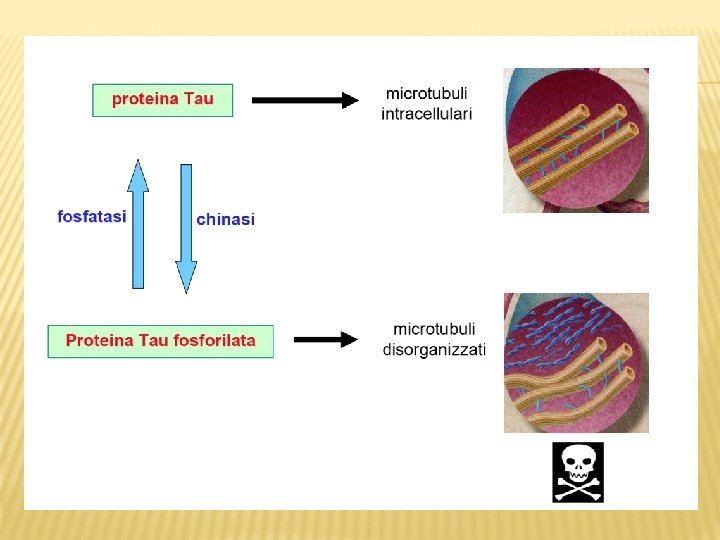
In condizioni fisiologiche il ruolo della proteina TAU è la stabilizzazione dei microtubuli
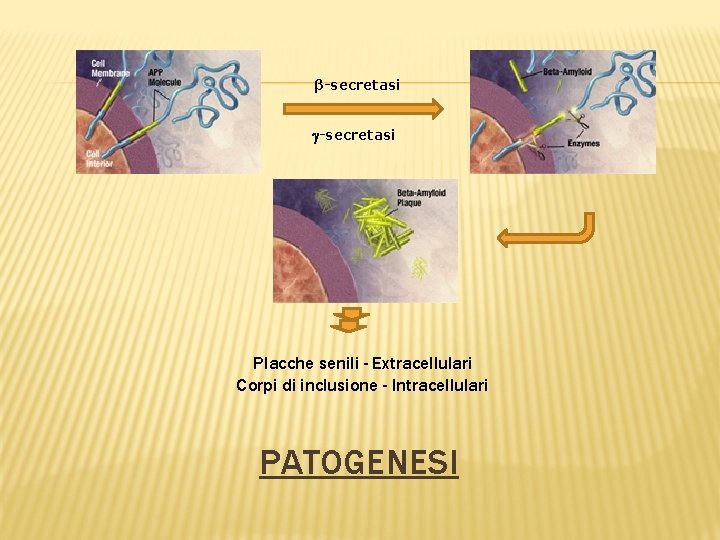
β-secretasi Placche senili - Extracellulari Corpi di inclusione - Intracellulari PATOGENESI
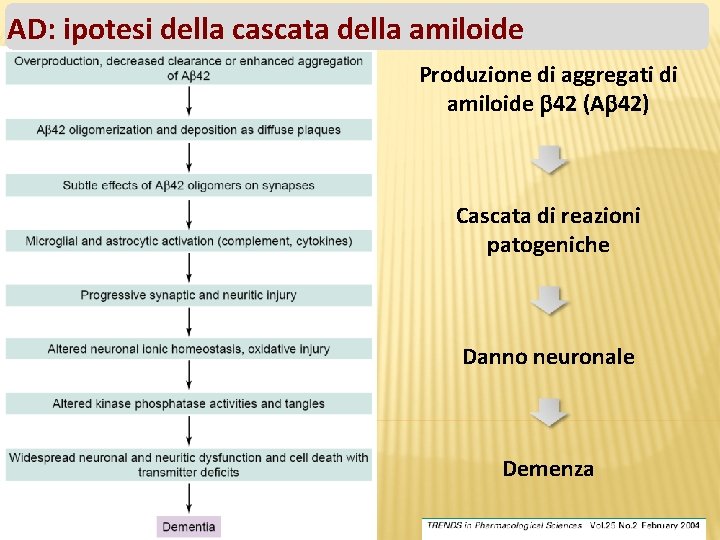
AD: ipotesi della cascata della amiloide Produzione di aggregati di amiloide 42 (A 42) Cascata di reazioni patogeniche Danno neuronale Demenza

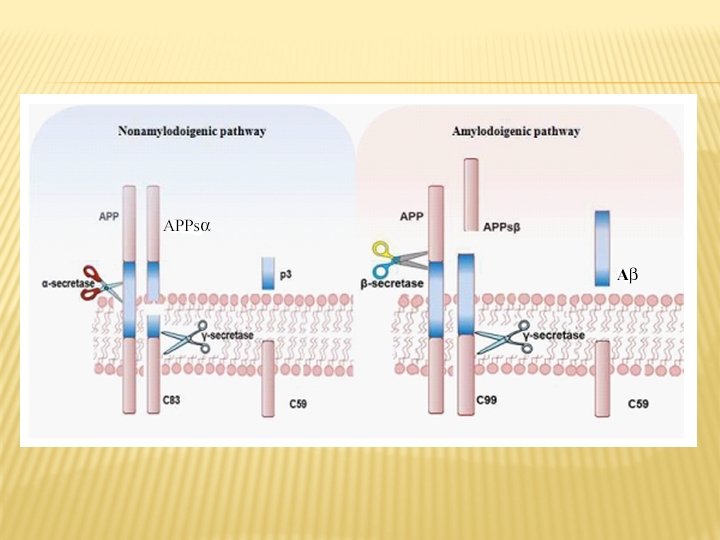
� La APP (Amyloid precursor protein, Proteina Progenitrice dell'Amiloide) che viene prodotta, è degradata durante il processo di trasporto sulla superficie cellulare (processo di degradazione della APP) e vede coinvolti tre enzimi che operano tagli proteolitici: la � α-secretasi β-secretasi in un primo γ-secretasi. Attraverso due e la momento e successivamente la tagli successivi operati prima dall'α-secretasi e poi dall'γsecretasi, viene prodotto un peptide innocuo chiamato p 3. La β -secretasi opera un taglio differente che, in seguito al successivo taglio da parte della γ-secretasi, porta alla produzione (pathway amiloidogenico) di due peptidi di 40 e 42 aminoacidi, chiamati beta-amiloide (Aβ 1 -40 e Aβ 1 -42): il secondo (Aβ 142) è considerato il più tossico a livello neuronale. Nei soggetti sani il processo di degradazione della APP sembra essere operato principalmente dalla α-secretasi. Per motivi non totalmente chiariti, nei soggetti malati l'enzima che interviene sull'APP non è l'α-secretasi ma la β-secretasi, con una larga produzione di proteina beta-amiloide. Tale beta-amiloide non presenta le caratteristiche biologiche della forma naturale, ma tende a depositarsi in aggregati extracellulari sulla membrana dei neuroni.
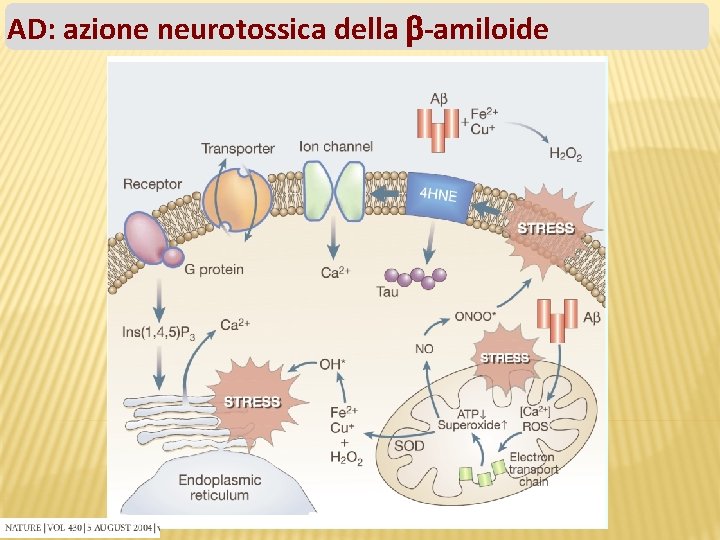
AD: azione neurotossica della -amiloide
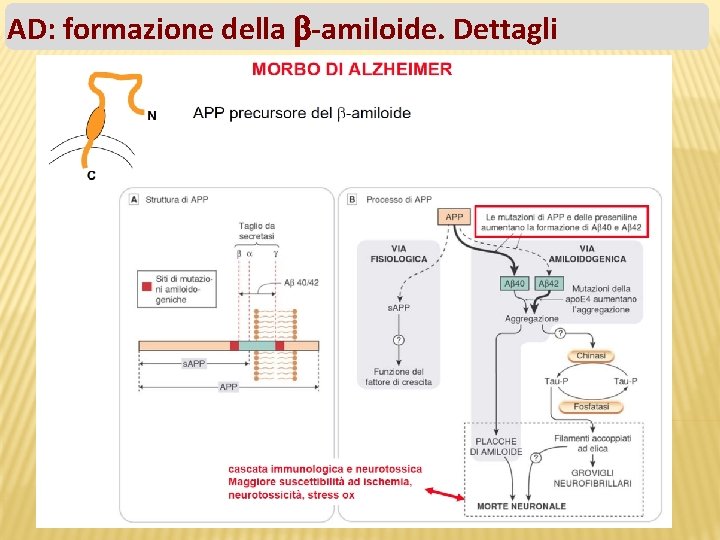
AD: formazione della -amiloide. Dettagli

AD: strategie terapeutiche A) Trattamento dei sintomi Symptoms management therapies • Unici farmaci in commercio; • Intervento farmacologico finalizzato a ridurre i sintomi della patologia; • Non arrestano il decorso della patologia B) Trattamento della causa Disease modifying therapies Intervento farmacologico sulle cause della patologia
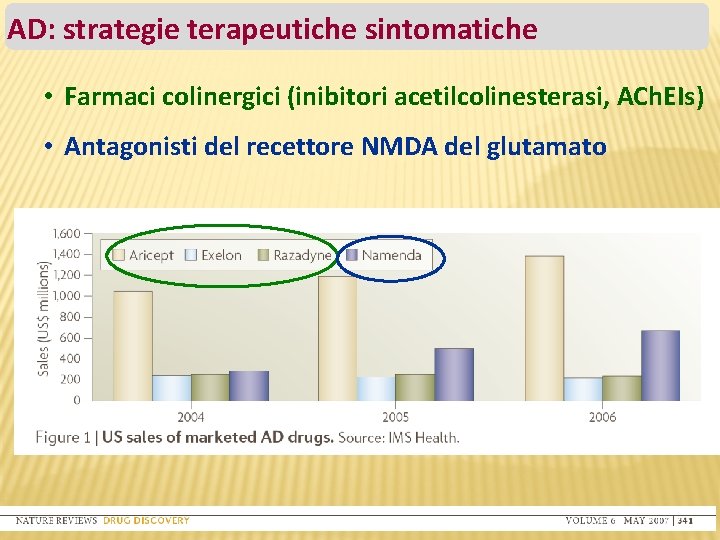
AD: strategie terapeutiche sintomatiche • Farmaci colinergici (inibitori acetilcolinesterasi, ACh. EIs) • Antagonisti del recettore NMDA del glutamato
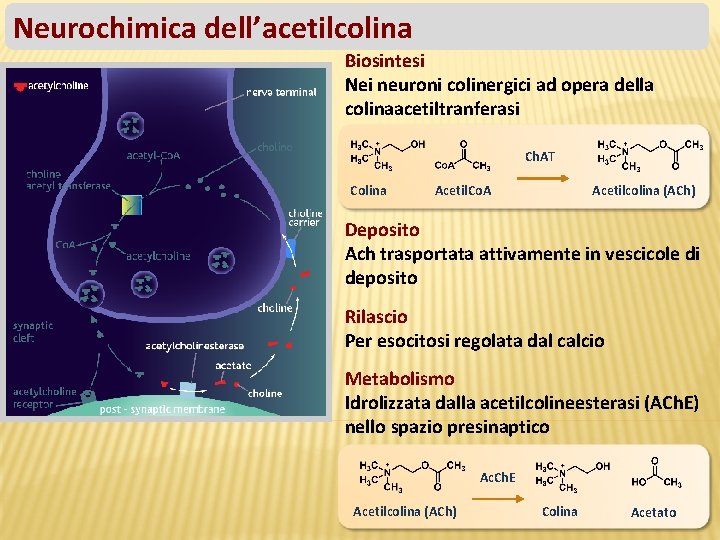
Neurochimica dell’acetilcolina Biosintesi Nei neuroni colinergici ad opera della colinaacetiltranferasi Ch. AT Colina Acetil. Co. A Acetilcolina (ACh) Deposito Ach trasportata attivamente in vescicole di deposito Rilascio Per esocitosi regolata dal calcio Metabolismo Idrolizzata dalla acetilcolineesterasi (ACh. E) nello spazio presinaptico Ac. Ch. E Acetilcolina (ACh) Colina Acetato
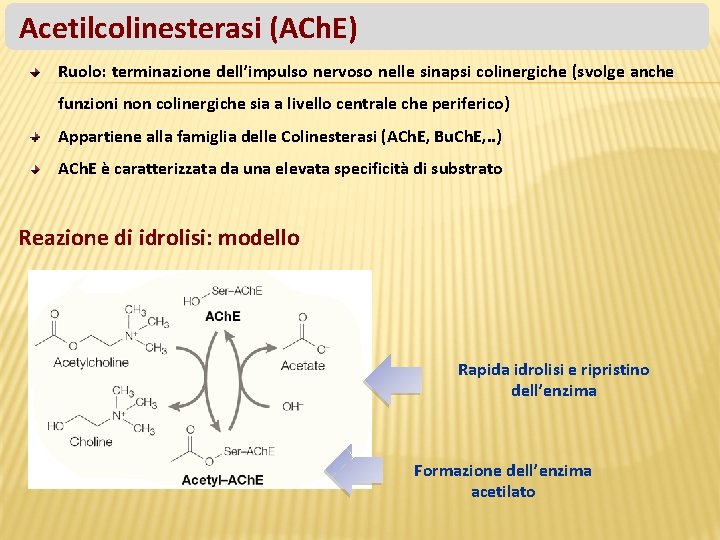
Acetilcolinesterasi (ACh. E) Ruolo: terminazione dell’impulso nervoso nelle sinapsi colinergiche (svolge anche funzioni non colinergiche sia a livello centrale che periferico) Appartiene alla famiglia delle Colinesterasi (ACh. E, Bu. Ch. E, . . ) ACh. E è caratterizzata da una elevata specificità di substrato Reazione di idrolisi: modello Rapida idrolisi e ripristino dell’enzima Formazione dell’enzima acetilato

Inibitori della acetilcolinesterasi (ACh. EIs): impieghi Aggressivi chimici per uso bellico Insetticidi Farmaci • Avvelenamento da pachicurari • Miastenia grave • Glaucoma (abbassamento della pressione intraoculare) • Morbo di Alzheimer 20
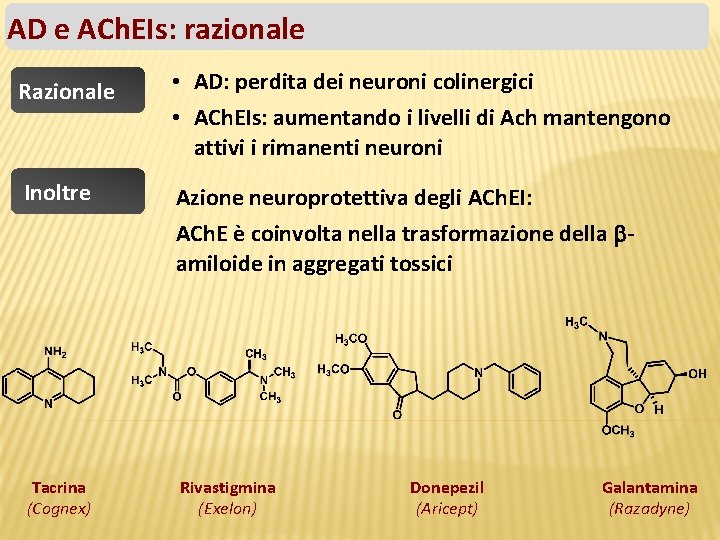
AD e ACh. EIs: razionale Razionale • AD: perdita dei neuroni colinergici • ACh. EIs: aumentando i livelli di Ach mantengono attivi i rimanenti neuroni Inoltre Azione neuroprotettiva degli ACh. EI: ACh. E è coinvolta nella trasformazione della amiloide in aggregati tossici Tacrina (Cognex) Rivastigmina (Exelon) Donepezil (Aricept) Galantamina (Razadyne)

Inibitori della acetilcolinesterasi (ACh. EIs): tipi Irreversibili Aggressivi chimici per uso bellico Insetticidi Reversibili Farmaci • con gruppo carbammico: legame covalente all’enzima • senza gruppo carbammico: legame non covalente all’enzima 22
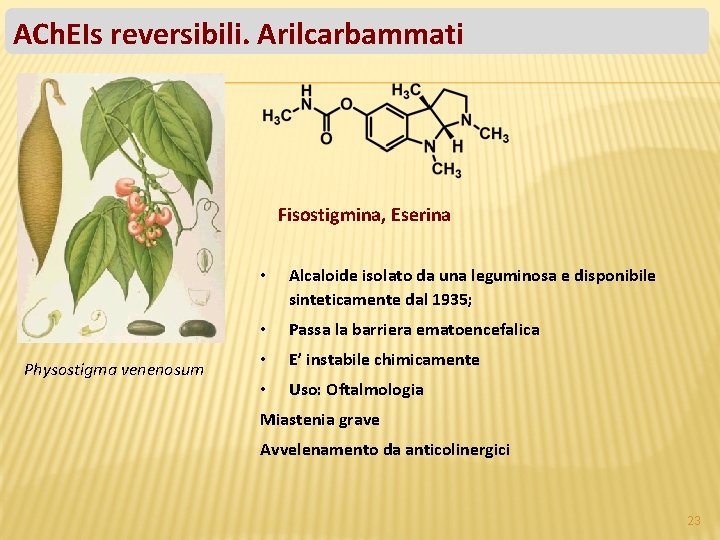
ACh. EIs reversibili. Arilcarbammati Fisostigmina, Eserina Physostigma venenosum • Alcaloide isolato da una leguminosa e disponibile sinteticamente dal 1935; • Passa la barriera ematoencefalica • E’ instabile chimicamente • Uso: Oftalmologia Miastenia grave Avvelenamento da anticolinergici 23
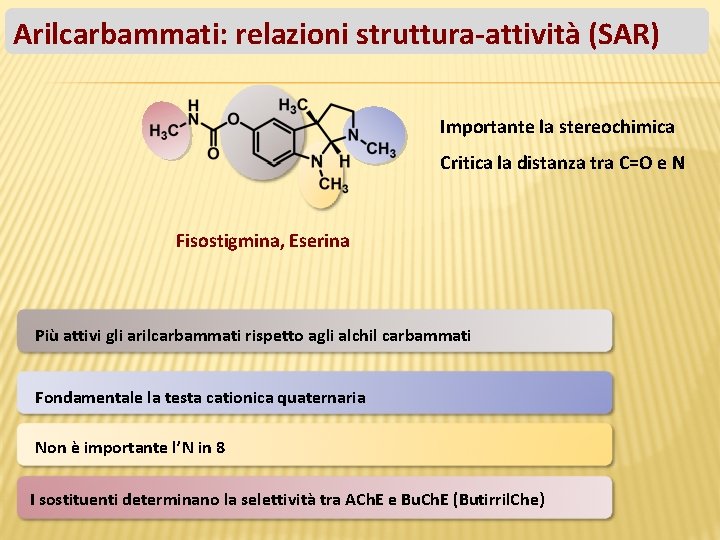
Arilcarbammati: relazioni struttura-attività (SAR) Importante la stereochimica Critica la distanza tra C=O e N Fisostigmina, Eserina Più attivi gli arilcarbammati rispetto agli alchil carbammati Fondamentale la testa cationica quaternaria Non è importante l’N in 8 I sostituenti determinano la selettività tra ACh. E e Bu. Ch. E (Butirril. Che)
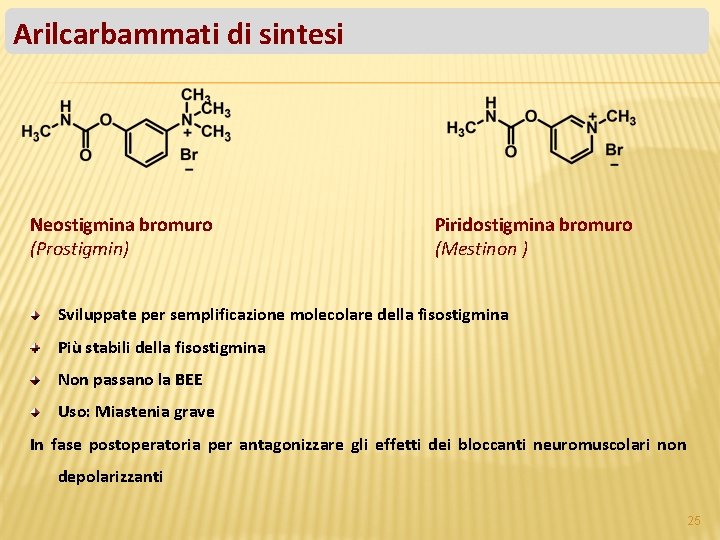
Arilcarbammati di sintesi Neostigmina bromuro (Prostigmin) Piridostigmina bromuro (Mestinon ) Sviluppate per semplificazione molecolare della fisostigmina Più stabili della fisostigmina Non passano la BEE Uso: Miastenia grave In fase postoperatoria per antagonizzare gli effetti dei bloccanti neuromuscolari non depolarizzanti 25

Arilcarbammati di sintesi Rivastigmina (Exelon) Approvato per il trattamento del AD (1997) e per il trattamento della demenza associata al morbo di Parkinson (2006) Ha una emivita bassa (2 h) ma blocca ACh. E per circa 10 h Blocca sia ACh. E che Bu. Ch. E: effetti collaterali (nausea a vomito) La attività è selettiva in zone del cervello clinicamente rilevanti 26

ACh. EIs reversibili senza porzione carbammica Tacrina (Cognex) Sintetizzata nel 1930 Primo farmaco approvato nel trattamento AD Non selettivo nei confronti della ACh. E: effetti collaterali (nausea, diarrea, incontinenza urinaria, grave epatotossicità) Scarsa biodisponibilità: sono necessarie 4 somministrazioni giornaliere
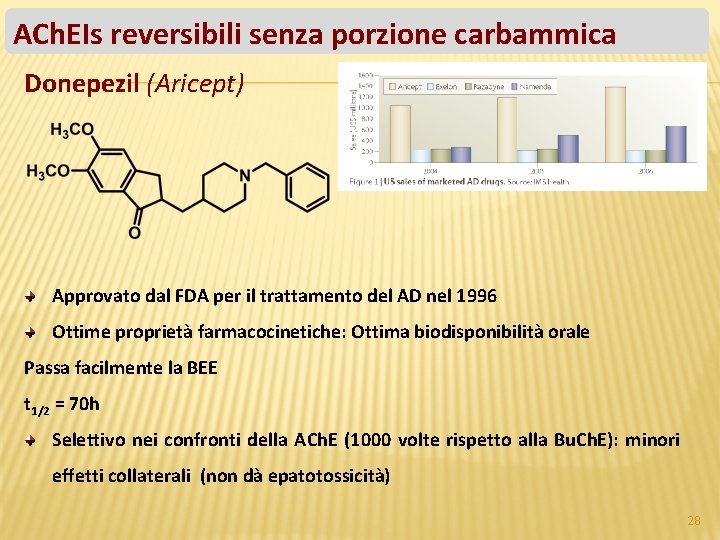
ACh. EIs reversibili senza porzione carbammica Donepezil (Aricept) Approvato dal FDA per il trattamento del AD nel 1996 Ottime proprietà farmacocinetiche: Ottima biodisponibilità orale Passa facilmente la BEE t 1/2 = 70 h Selettivo nei confronti della ACh. E (1000 volte rispetto alla Bu. Ch. E): minori effetti collaterali (non dà epatotossicità) 28
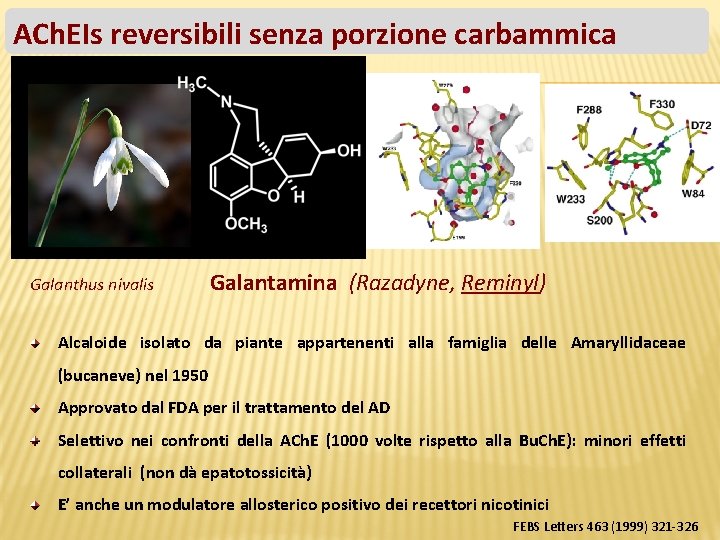
ACh. EIs reversibili senza porzione carbammica Galanthus nivalis Galantamina (Razadyne, Reminyl) Alcaloide isolato da piante appartenenti alla famiglia delle Amaryllidaceae (bucaneve) nel 1950 Approvato dal FDA per il trattamento del AD Selettivo nei confronti della ACh. E (1000 volte rispetto alla Bu. Ch. E): minori effetti collaterali (non dà epatotossicità) E’ anche un modulatore allosterico positivo dei recettori nicotinici FEBS Letters 463 (1999) 321 -326

Galantamina Scarsa disponibilità della pianta Elevati costi di estrazione e purificazione $50 000 / Kg) Riportate numerose sintesi totali A) Coupling ossidativo del fenolo (Approccio biomimetico) B) Coupling di Heck intramolecolare 30
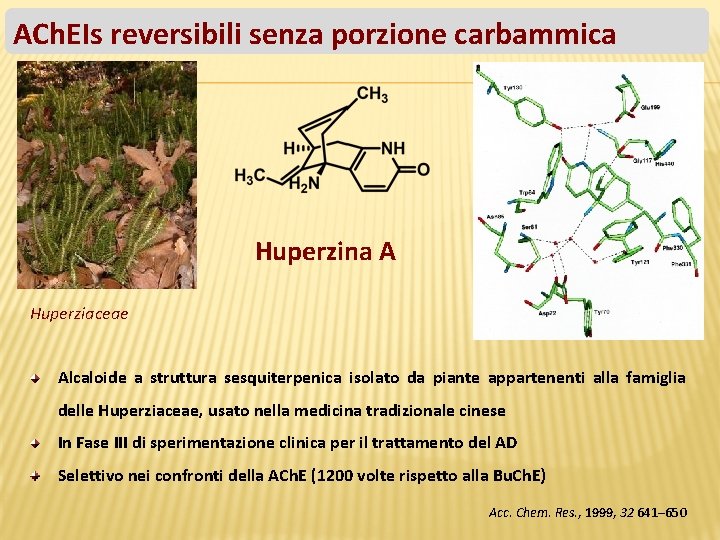
ACh. EIs reversibili senza porzione carbammica Huperzina A Huperziaceae Alcaloide a struttura sesquiterpenica isolato da piante appartenenti alla famiglia delle Huperziaceae, usato nella medicina tradizionale cinese In Fase III di sperimentazione clinica per il trattamento del AD Selettivo nei confronti della ACh. E (1200 volte rispetto alla Bu. Ch. E) Acc. Chem. Res. , 1999, 32 641– 650
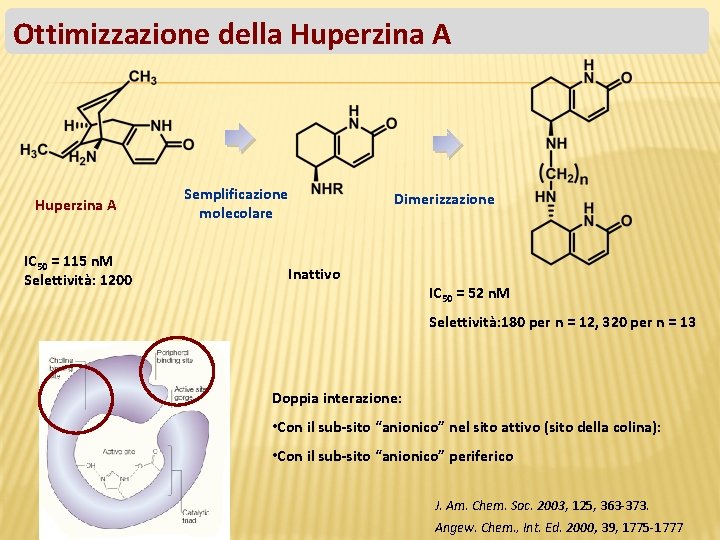
Ottimizzazione della Huperzina A IC 50 = 115 n. M Selettività: 1200 Semplificazione molecolare Dimerizzazione Inattivo IC 50 = 52 n. M Selettività: 180 per n = 12, 320 per n = 13 Doppia interazione: • Con il sub-sito “anionico” nel sito attivo (sito della colina): • Con il sub-sito “anionico” periferico J. Am. Chem. Soc. 2003, 125, 363 -373. Angew. Chem. , Int. Ed. 2000, 39, 1775 -1777
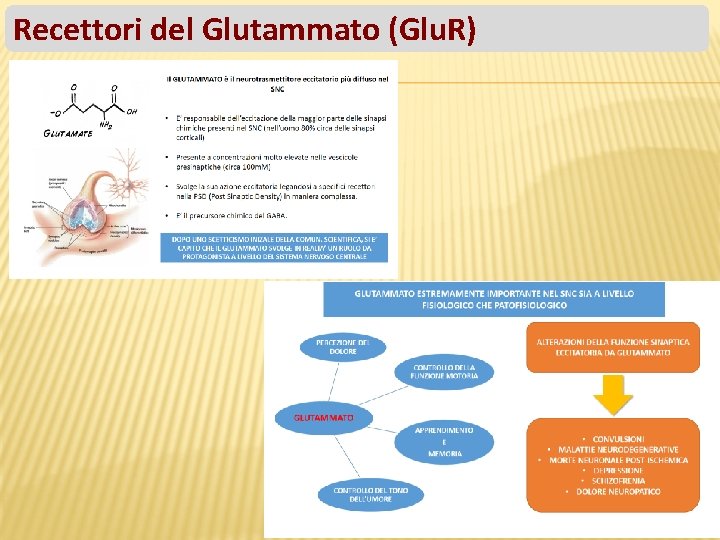
Recettori del Glutammato (Glu. R)
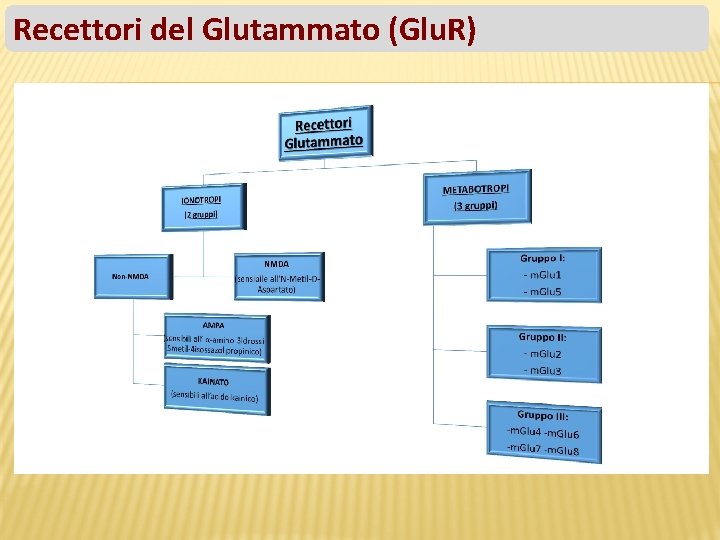
Recettori del Glutammato (Glu. R)
![Recettori del glutammato ionotropici (i. Glu. Rs) AMPA/KA ( ↑ Na+ , [↑ Ca++]) Recettori del glutammato ionotropici (i. Glu. Rs) AMPA/KA ( ↑ Na+ , [↑ Ca++])](http://slidetodoc.com/presentation_image_h2/e7d53c4374f4c33b8a6cf9df58d83e07/image-35.jpg)
Recettori del glutammato ionotropici (i. Glu. Rs) AMPA/KA ( ↑ Na+ , [↑ Ca++]) NMDA (↑ Na+, ↑ Ca++)

AD: Antagonisti del recettore NMDA del glutamato Razionale L’aumentata concentrazione di Glu determina il danno eccitotossico Aβ induce cambiamenti di tipo ossidativo che alterano la funzione dei trasportatori del Glu (GLT-1) e GS; L’elevata attività dei NMDARs è associata alla iperfosforilazione della proteina tau Nature Reviews Drug Discovery, 2006, 5, 160 -17 CNS Drugs, 2003, 17, 641 -652.
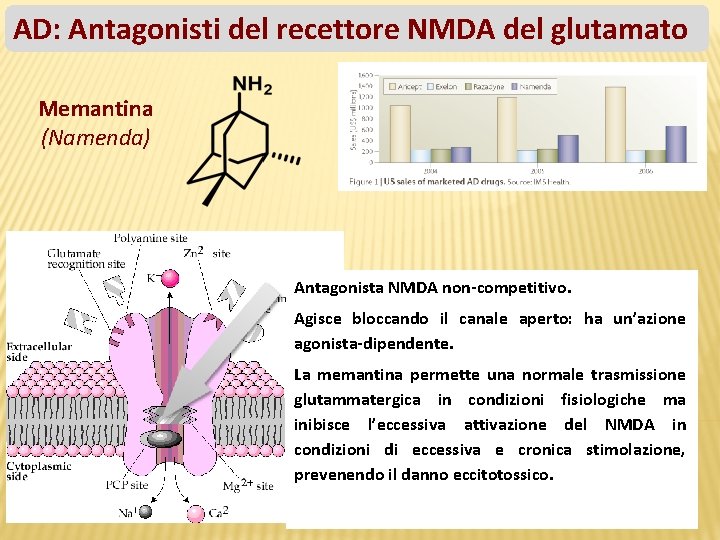
AD: Antagonisti del recettore NMDA del glutamato Memantina (Namenda) Antagonista NMDA non-competitivo. Agisce bloccando il canale aperto: ha un’azione agonista-dipendente. La memantina permette una normale trasmissione glutammatergica in condizioni fisiologiche ma inibisce l’eccessiva attivazione del NMDA in condizioni di eccessiva e cronica stimolazione, prevenendo il danno eccitotossico.

AD: strategie terapeutiche causali Modulatori delle secretasi • Inibitori della attività della β secretasi • Inibitori della attività della γ secretasi • Induttori della attività della α secretasi Inibitori della biosintesi del colesterolo Inibitori della aggregazione della Aβ Approcci immunologici
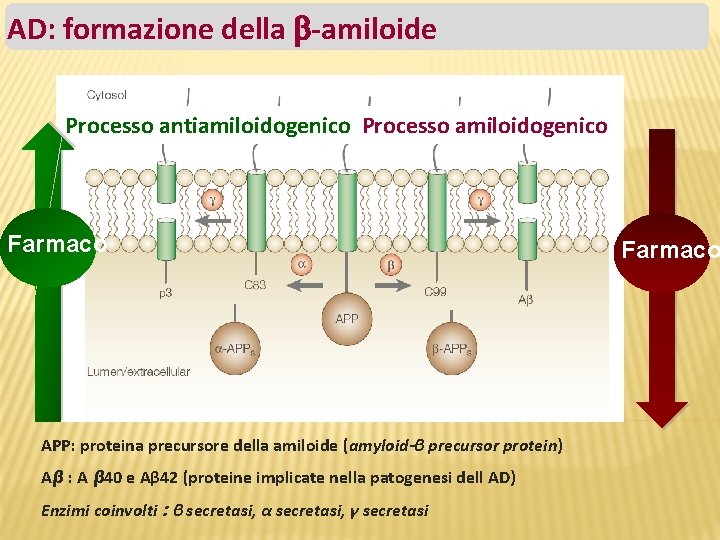
AD: formazione della -amiloide Processo antiamiloidogenico Processo amiloidogenico Farmaco APP: proteina precursore della amiloide (amyloid-β precursor protein) Aβ : A β 40 e Aβ 42 (proteine implicate nella patogenesi dell AD) Enzimi coinvolti : β secretasi, α secretasi, γ secretasi Farmaco
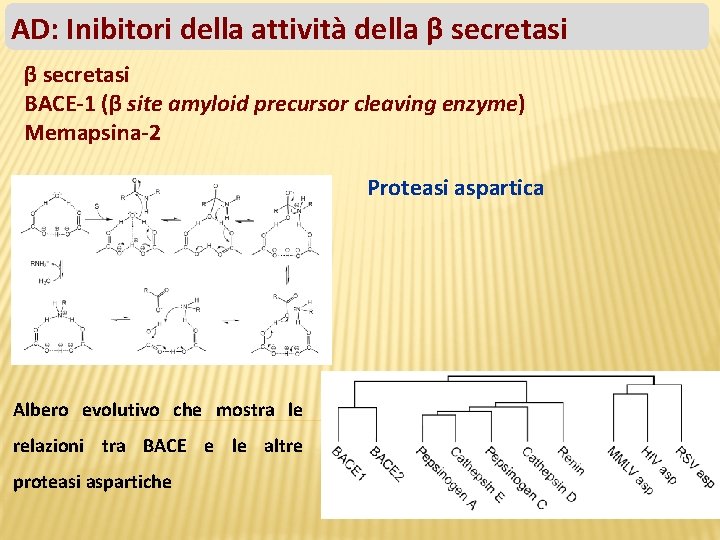
AD: Inibitori della attività della β secretasi BACE-1 (β site amyloid precursor cleaving enzyme) Memapsina-2 Proteasi aspartica Albero evolutivo che mostra le relazioni tra BACE e le altre proteasi aspartiche
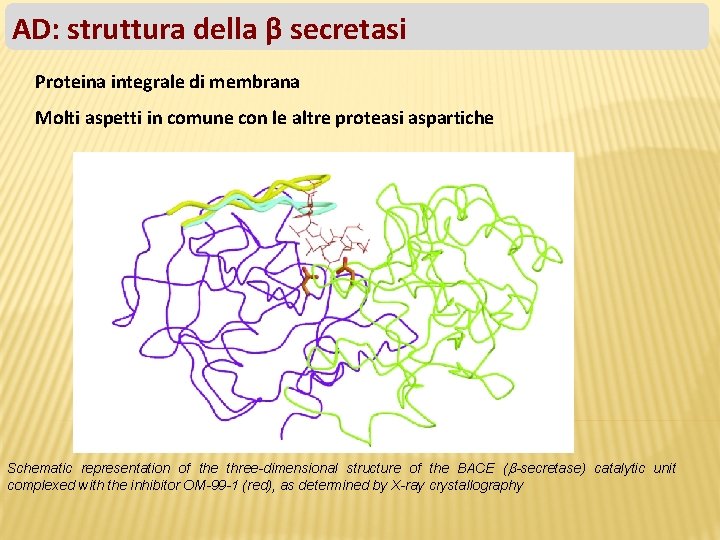
AD: struttura della β secretasi Proteina integrale di membrana Molti aspetti in comune con le altre proteasi aspartiche Schematic representation of the three-dimensional structure of the BACE ( -secretase) catalytic unit complexed with the inhibitor OM-99 -1 (red), as determined by X-ray crystallography

AD: Inibitori della attività della β secretasi Inibitori basati sulla struttura del substrato Substrate based approach Inibitori non peptidomimetici Small molecules
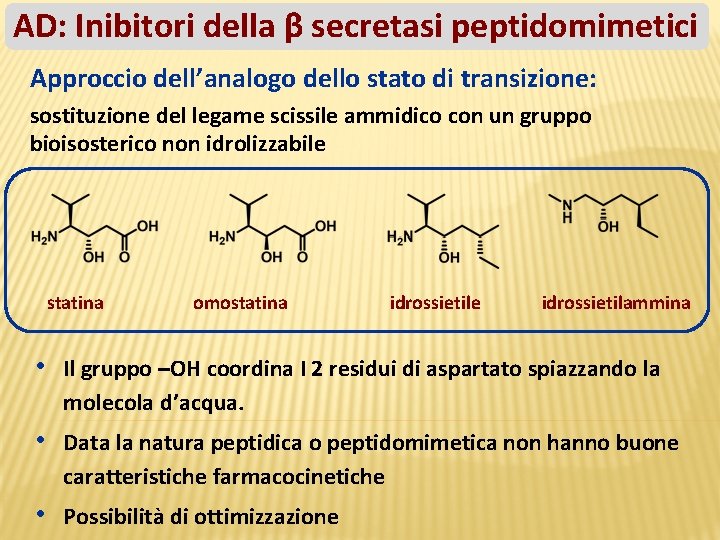
AD: Inibitori della β secretasi peptidomimetici Approccio dell’analogo dello stato di transizione: sostituzione del legame scissile ammidico con un gruppo bioisosterico non idrolizzabile statina omostatina idrossietile idrossietilammina • Il gruppo –OH coordina I 2 residui di aspartato spiazzando la molecola d’acqua. • Data la natura peptidica o peptidomimetica non hanno buone caratteristiche farmacocinetiche • Possibilità di ottimizzazione
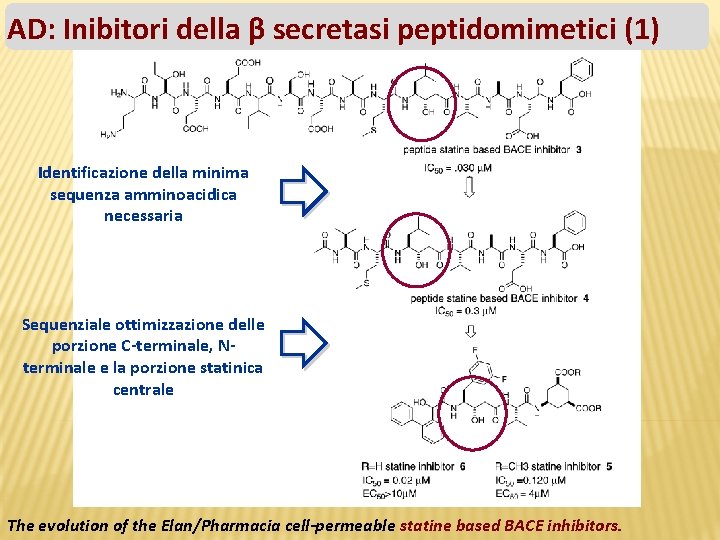
AD: Inibitori della β secretasi peptidomimetici (1) Identificazione della minima sequenza amminoacidica necessaria Sequenziale ottimizzazione delle porzione C-terminale, Nterminale e la porzione statinica centrale The evolution of the Elan/Pharmacia cell-permeable statine based BACE inhibitors.
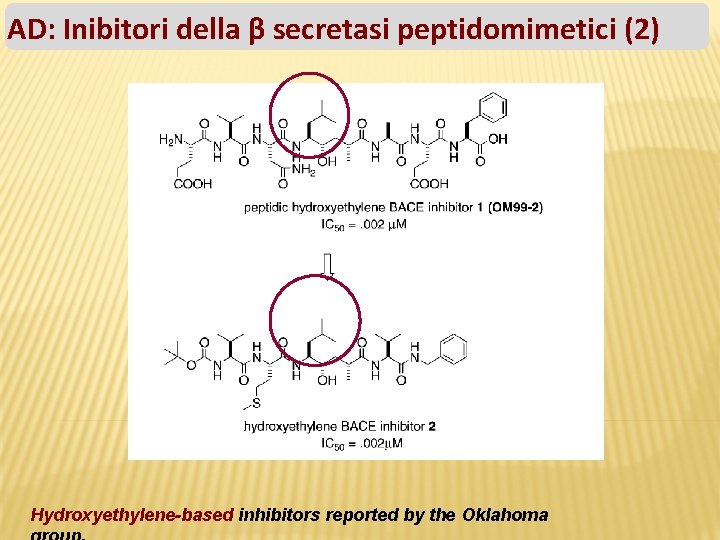
AD: Inibitori della β secretasi peptidomimetici (2) Hydroxyethylene-based inhibitors reported by the Oklahoma
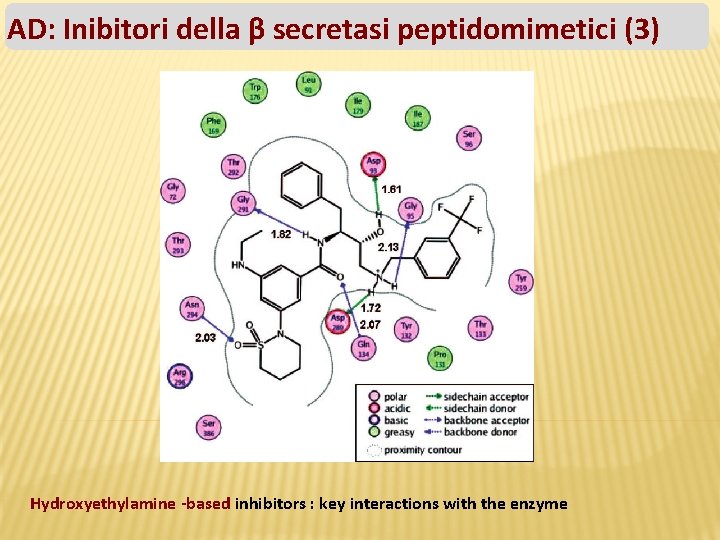
AD: Inibitori della β secretasi peptidomimetici (3) Hydroxyethylamine -based inhibitors : key interactions with the enzyme
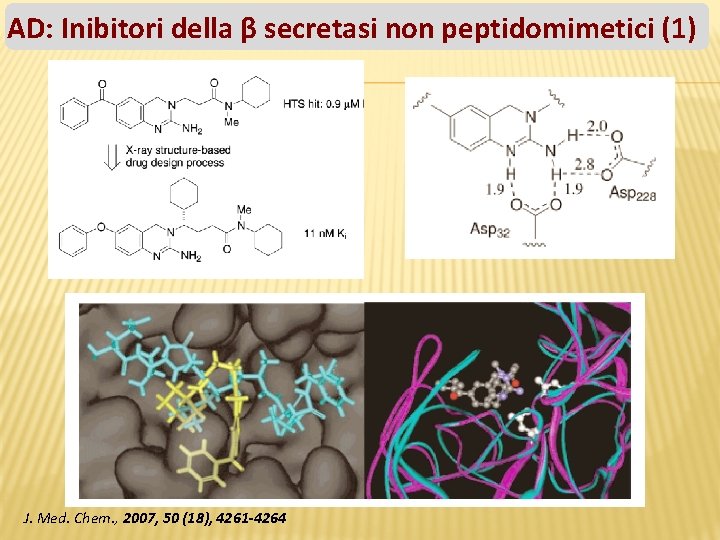
AD: Inibitori della β secretasi non peptidomimetici (1) J. Med. Chem. , 2007, 50 (18), 4261 -4264
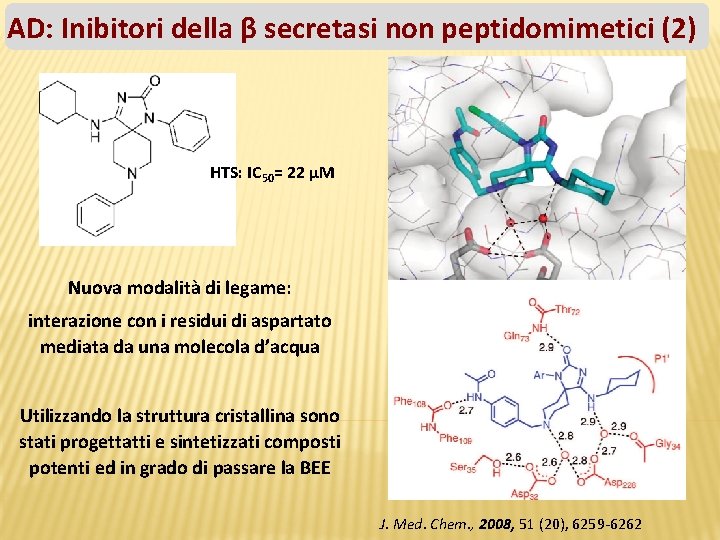
AD: Inibitori della β secretasi non peptidomimetici (2) HTS: IC 50= 22 μM Nuova modalità di legame: interazione con i residui di aspartato mediata da una molecola d’acqua Utilizzando la struttura cristallina sono stati progettatti e sintetizzati composti potenti ed in grado di passare la BEE J. Med. Chem. , 2008, 51 (20), 6259 -6262
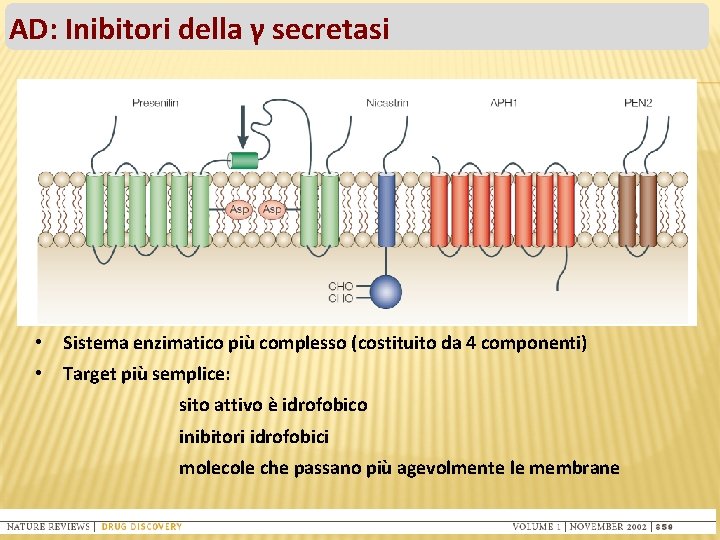
AD: Inibitori della γ secretasi • Sistema enzimatico più complesso (costituito da 4 componenti) • Target più semplice: sito attivo è idrofobico inibitori idrofobici molecole che passano più agevolmente le membrane
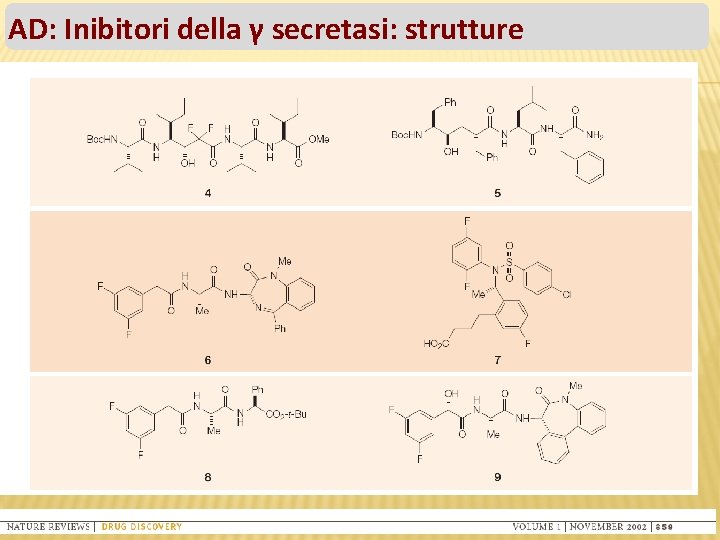
AD: Inibitori della γ secretasi: strutture

AD e FANS: ruolo della γ secretasi Studi epidemiologici: I FANS riducono i rischi per AD L’azione non è correlata alla inibizione della COX I FANS riducono la formazione del frammento amiloidogenico Aβ 42 I FANS modulano l’azione della γ-secretasi

AD: Attivatori della α secretasi Razionale α secretasi : catalizza un processo antiamiloidogenico Incrementandone l’azione si dirotta l’APP verso la produzione di peptidi diversi dalla Aβ 42 Attivatori della α secretasi Agonisti M 1 e M 3
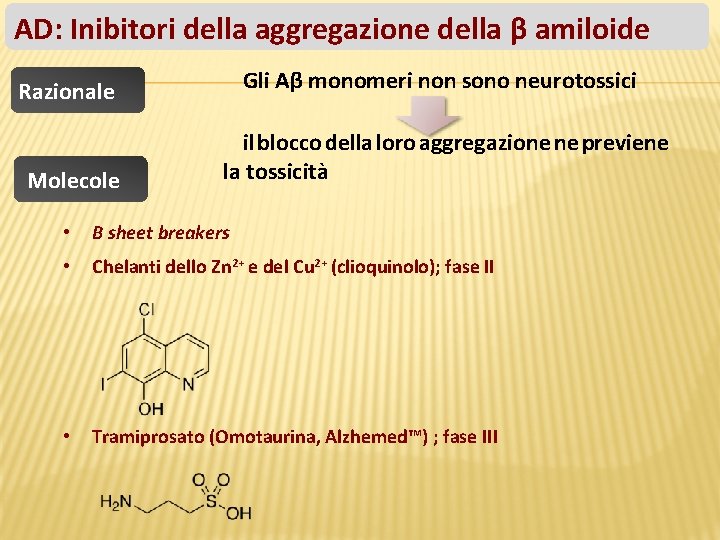
AD: Inibitori della aggregazione della β amiloide Razionale Gli Aβ monomeri non sono neurotossici Molecole il blocco della loro aggregazione ne previene la tossicità • Β sheet breakers • Chelanti dello Zn 2+ e del Cu 2+ (clioquinolo); fase II • Tramiprosato (Omotaurina, Alzhemed™) ; fase III

AD: Inibitori della biosintesi del colesterolo Correlazione tra il metabolismo del colesterolo e AD • Evidenze § Studi epidemiologici correlano alti livelli di colesterolo con l’incremento della incidenza di AD; § La terapia con statine diminuisce l’ incidenza di AD; § Esperimenti su animali • Meccanismo: non noto. Ipotesi: I livelli di colesterolo, modulando la fluidità delle membrane, modulano l’azione delle secretasi • Farmaci: § Statine § Inibitori ACAT (acilcoenzima A-colesterolo aciltransferasi)
- Slides: 54