Monothrapies dIP boost Rsultats des principaux essais Dr

Monothérapies d’IP boosté Résultats des principaux essais Dr Jade GHOSN Service de Médecine Interne & Maladies Infectieuses CHU Bicêtre

Monothérapie d’IP/r en maintenance chez des patients pré-traités en succès virologique

Traitement de maintenance par IDV/r en monothérapie • Étude pilote chez 12 patients ayant une charge virale < 50 copies sous IDV/r + 2 INTI et n’ayant pas présenté d’échec virologique documenté • Dose IDV adaptée pour obtenir une Cmin entre 500 et 2000 ng/ml (400 bid: 1; 600 bid: 4; 800 bid: 7) • Critère de jugement principal = Échec 1 CV > 400 cp/ml ou 3 CV successives supérieures à 200 cp/ml • 4 patients ont développé une néphrotoxicité • Maintien de l’indétectabilité (50 cps ) à S 48 • Pas de modification sur DEXA à S 48 Kahlert et al AIDS 2004

Essai ACTG 5201 : Traitement de maintenance par ATV/r en monothérapie • Étude pilote prospective ouverte non randomisée • Critères d’inclusion – Patient en 1ère ligne thérapeutique (2 INTI + 1 IP/r) – CD 4 > 250 /mm 3 – Charge virale < 50 copies /ml depuis 48 semaines • Objectif principal : évaluer le risque d’échappement virologique ( 2 charges virales successives > 200 copies/ml) sur 24 semaines Swindells et al JAMA 2006

Résultats • 36 patients inclus dans l’essai • Succès à S 24 : 33 patients / 36 • Parmi les 33 patients en succès de la stratégie – Absence de patients avec 2 mesures successives supérieures à 50 copies /ml • Mesure de la charge virale dans le sperme (n=8) – CV < seuil de détection pour les 8 patients Swindells et al JAMA 2006

OK-04: traitement de maintenance par Kalétra® versus 2 INTI + Kalétra ® CV <50 c/ml depuis > 6 mois l Pas d'ATCD d'échec virologique sous IP l Sous LPV/r + 2 INTI depuis > 1 mois l LPV/r SGC 400/100 mg x 2/j (groupe OK) (n = 100) 96 semaines LPV/r SGC 400/100 mg x 2/j + 2 INTI (groupe Tri) (n = 100) Suivi : sélection, J 0, S 4, S 12, puis toutes les 12 semaines jusqu'à S 96 • Critère de jugement principal : absence d'échec à S 48 • Définition de l'échec : – 2 CV > 500 c/ml espacées de 2 semaines (sans re-négativation de la CV après ré-induction avec 2 INTI dans le groupe OK), OU – Modification du traitement alloué pour autre chose qu'une réinduction, OU – Arrêt de traitement, OU Arribas J. , IAC 2006
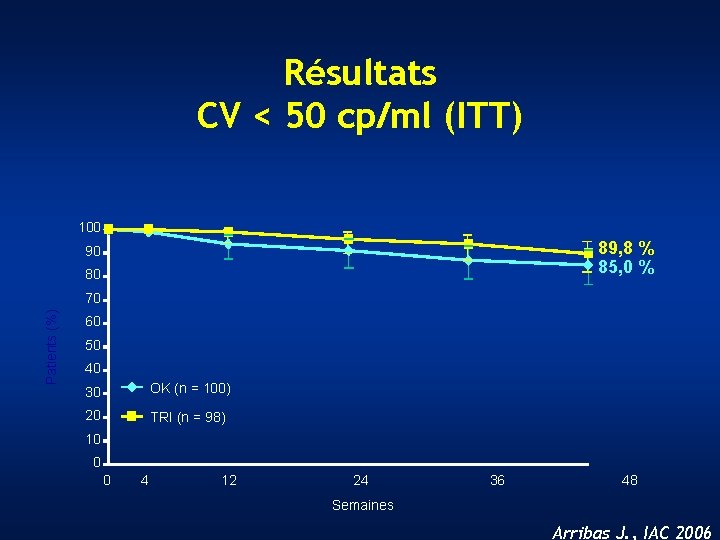
Résultats CV < 50 cp/ml (ITT) 100 89, 8 % 85, 0 % 90 80 Patients (%) 70 60 50 40 30 OK (n = 100) 20 TRI (n = 98) 10 0 0 4 12 24 36 48 Semaines Arribas J. , IAC 2006

Échecs virologiques: résistance • Test génotypique de résistance chez tous les patients avec une CV > 500 c/ml, blips > 500 c/ml inclus OK (n = 100) Tri (n = 98) 11 (11 %) 4 (4 %) Souches avec mutations primaires IP 2 [10 F, 46 I, 82 A/V] [54 V, 77 I, 82 A] 1 [54 V, 63 P, 71 V, 82 A] Souches sans mutations primaires IP 9 3 n Arribas J. , IAC 2006

Stratégie Induction - Maintenance
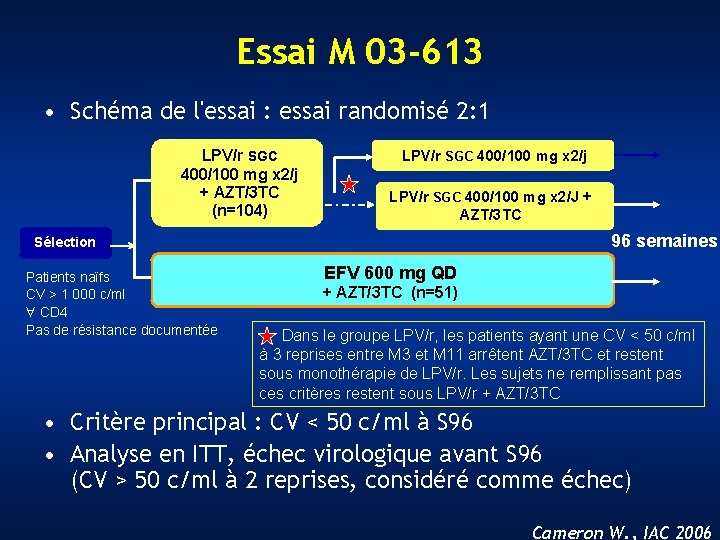
Essai M 03 -613 • Schéma de l'essai : essai randomisé 2: 1 LPV/r SGC 400/100 mg x 2/j + AZT/3 TC (n=104) LPV/r SGC 400/100 mg x 2/j LPV/r SGC 400/100 mg x 2/J + AZT/3 TC 96 semaines Sélection Patients naïfs CV > 1 000 c/ml " CD 4 Pas de résistance documentée EFV 600 mg QD + AZT/3 TC (n=51) Dans le groupe LPV/r, les patients ayant une CV < 50 c/ml à 3 reprises entre M 3 et M 11 arrêtent AZT/3 TC et restent sous monothérapie de LPV/r. Les sujets ne remplissant pas ces critères restent sous LPV/r + AZT/3 TC • Critère principal : CV < 50 c/ml à S 96 • Analyse en ITT, échec virologique avant S 96 (CV > 50 c/ml à 2 reprises, considéré comme échec) Cameron W. , IAC 2006
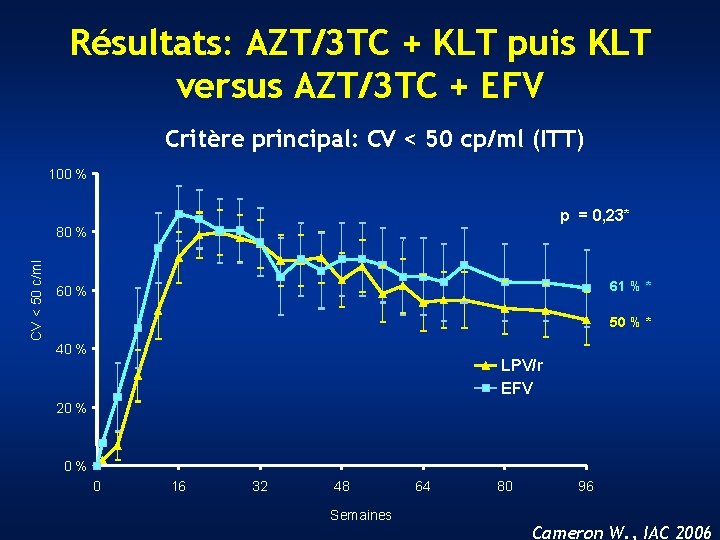
Résultats: AZT/3 TC + KLT puis KLT versus AZT/3 TC + EFV Critère principal: CV < 50 cp/ml (ITT) 100 % p = 0, 23* CV < 50 c/ml 80 % 61 % * 60 % 50 % * 40 % LPV/r EFV 20 % 0% 0 16 32 48 Semaines 64 80 96 Cameron W. , IAC 2006
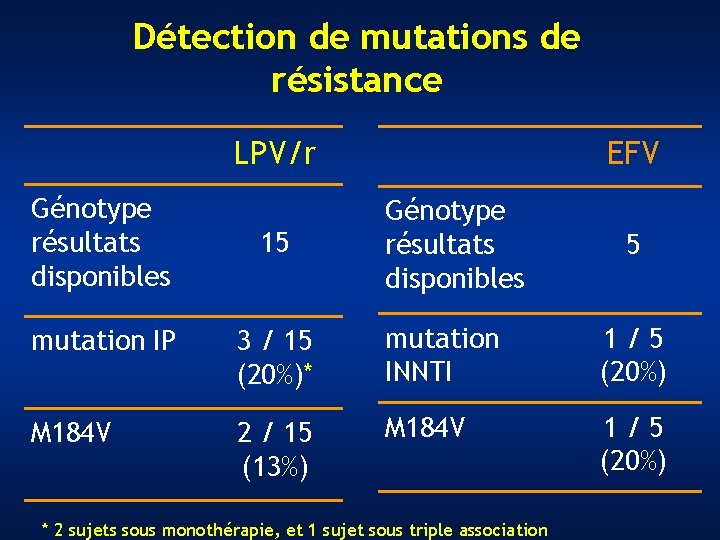
Détection de mutations de résistance LPV/r Génotype résultats disponibles 15 EFV Génotype résultats disponibles 5 mutation IP 3 / 15 (20%)* mutation INNTI 1/5 (20%) M 184 V 2 / 15 (13%) M 184 V 1/5 (20%) * 2 sujets sous monothérapie, et 1 sujet sous triple association

Monothérapie d’IP/r en initiation de traitement
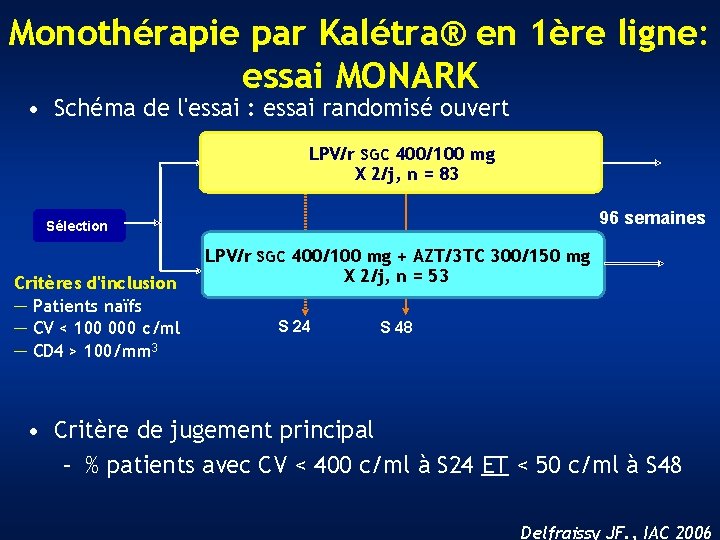
Monothérapie par Kalétra® en 1ère ligne: essai MONARK • Schéma de l'essai : essai randomisé ouvert LPV/r SGC 400/100 mg X 2/j, n = 83 96 semaines Sélection Critères d'inclusion ─ Patients naïfs ─ CV < 100 000 c/ml ─ CD 4 > 100/mm 3 LPV/r SGC 400/100 mg + AZT/3 TC 300/150 mg X 2/j, n = 53 S 24 S 48 • Critère de jugement principal – % patients avec CV < 400 c/ml à S 24 ET < 50 c/ml à S 48 Delfraissy JF. , IAC 2006
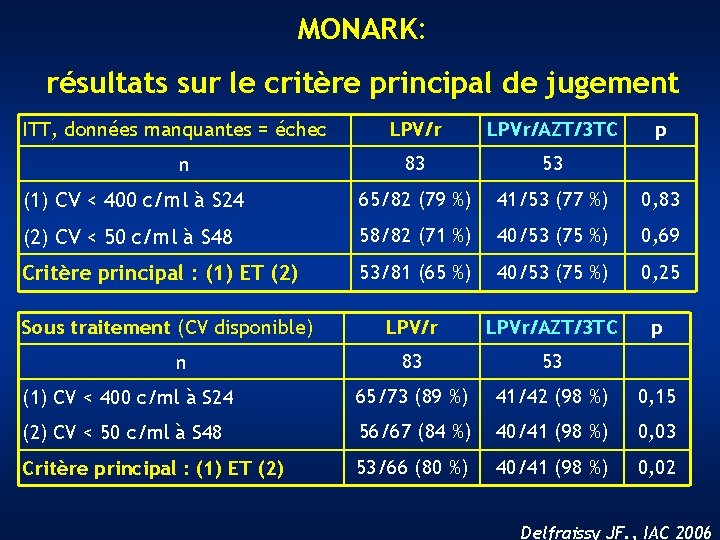
MONARK: résultats sur le critère principal de jugement ITT, données manquantes = échec LPV/r LPVr/AZT/3 TC 83 53 (1) CV < 400 c/ml à S 24 65/82 (79 %) 41/53 (77 %) 0, 83 (2) CV < 50 c/ml à S 48 58/82 (71 %) 40/53 (75 %) 0, 69 Critère principal : (1) ET (2) 53/81 (65 %) 40/53 (75 %) 0, 25 LPV/r LPVr/AZT/3 TC p 83 53 (1) CV < 400 c/ml à S 24 65/73 (89 %) 41/42 (98 %) 0, 15 (2) CV < 50 c/ml à S 48 56/67 (84 %) 40/41 (98 %) 0, 03 Critère principal : (1) ET (2) 53/66 (80 %) 40/41 (98 %) 0, 02 n Sous traitement (CV disponible) n p Delfraissy JF. , IAC 2006

MONARK: Étude des mutations de résistance • Etude des mutations de résistance, réalisée – au moment de l'échec virologique (CV > 500 c/ml après un nadir < 400 c/ml) – ou à la demande du clinicien investigateur LPV/r + AZT/3 TC (n = 83) (n = 53) Patients justifiant d'un test de résistance Résultats disponibles Patients avec mutation de résistance IP Patients avec mutation de résistance AZT Patients avec mutation de résistance 3 TC 21 (25 %) 3 (6 %) 21 3 2/21 0/21 0/3 1/3 Delfraissy JF. , IAC 2006
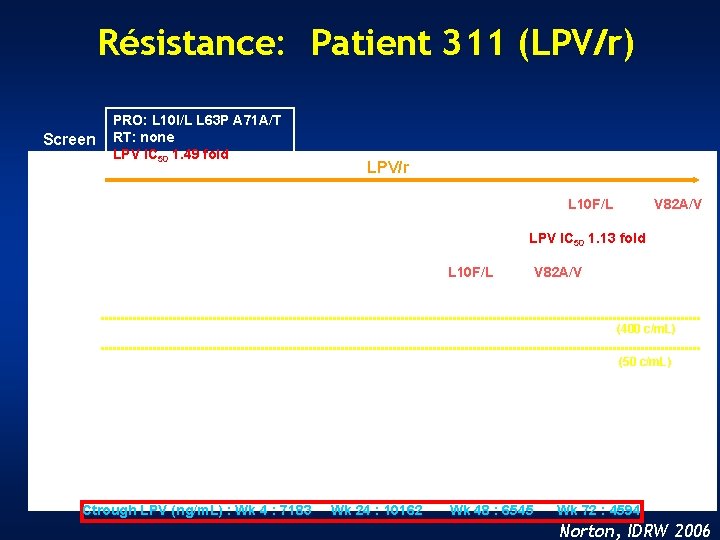
Résistance: Patient 311 (LPV/r) Screen PRO: L 10 I/L L 63 P A 71 A/T RT: none LPV IC 50 1. 49 fold LPV/r PRO: L 10 F/L L 63 P V 82 A/V RT: none LPV IC 50 1. 13 fold PRO: L 10 F/L L 63 P V 82 A/V RT: none (400 c/m. L) (50 c/m. L) MONARK Ctrough LPV (ng/m. L) : Wk 4 : 7183 Wk 24 : 10162 Wk 48 : 6545 Wk 72 : 4594 Norton, IDRW 2006
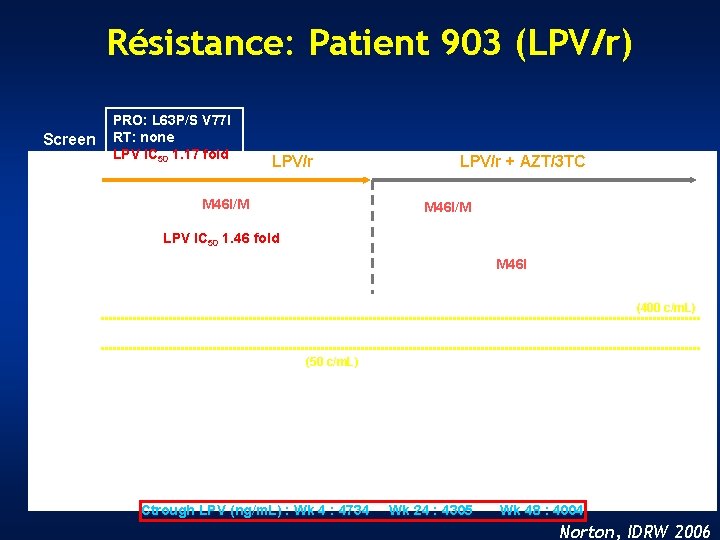
Résistance: Patient 903 (LPV/r) Screen PRO: L 63 P/S V 77 I RT: none LPV IC 50 1. 17 fold LPV/r PRO: M 46 I/M L 63 P/S V 77 I RT: none LPV IC 50 1. 46 fold LPV/r + AZT/3 TC PRO: M 46 I/M L 63 P V 77 I RT: none PRO: M 46 I L 63 P V 77 I RT: none (400 c/m. L) (50 c/m. L) MONARK Ctrough LPV (ng/m. L) : Wk 4 : 4734 Wk 24 : 4305 Wk 48 : 4004 Norton, IDRW 2006

Résistance Patient 5102 + AZT/3 TC) Screen (LPV/r PRO: L 33 I L 63 P A 71 T RT: none LPV/r + AZT/3 TC LPV/r + AZT + dd. I PRO: L 33 I A 71 T RT: M 184 V PRO: L 33 I L 63 P A 71 T RT: none (400 c/m. L) (50 c/m. L) MONARK Ctrough LPV (ng/m. L) : Wk 4 : <75 Wk 24 : <75 Retest : 1625 Wk 48 : <75 Norton, IDRW 2006

Monothérapie d’IP/r: Conclusions (1) • Chez les patients en succès virologique: - Maintien de l’indétectabilité dans la majorité des cas - Fréquence plus élevée de virémie entre 50 et 500 copies/ml dans le groupe monothérapie - Pas de risque plus élevé de sélection de mutants résistants dans les études avec LPV/r - Les échappements virologiques peuvent être facilement et rapidement contrôlés par la réintroduction de 2 INTIs - Beaucoup de données avec LPV/r: extrapolables à la classe des IP? - Barrière génétique en monothérapie? - Concentration cible? - Réservoirs profonds?

Monothérapie d’IP/r: Conclusions (2) • Chez les patients naïfs - Un seul essai: MONARK - La monothérapie de LPV/r s’est avérée moins efficace qu’une triple association (critère < 50 cp/ml) - En cas d’échec, les options de 2ème ligne n’ont pas été compromises - Ne peut être recommandée en 1ère ligne , mais peut représenter une option chez près de 80% des patients ++++ Impact sur la qualité de vie des patients? Y a-t-il une place pour ce type de stratégie actuellement? Si oui, facteurs prédictifs du succès d’une monothérapie en 1ère ligne? Réservoirs profonds?
Compartiment génital • IP/r en première ligne: Sous-étude de l’essai Monark • 10 patients (5 sous LPV/r seul, 5 sous CBV + LPV/r) • A l’inclusion: p. CV 4. 36 log 10 cp/ml; CD 4 221/mm 3 • Suivi : 48 semaines • plasma ARN-VIH S 48: < 50 cp/ml pour tous les patients • CV liquide séminal à S 48: < 200 cp/ml pour les 5 patients CBV + LPV/r < 200 cp/ml pour les 5 patients LPV/r seul p. Cmin LPV= 4896 ng/ml, LSCmin LPV < 30 ng/ml Ghosn, XIV IWHIVR, 2006


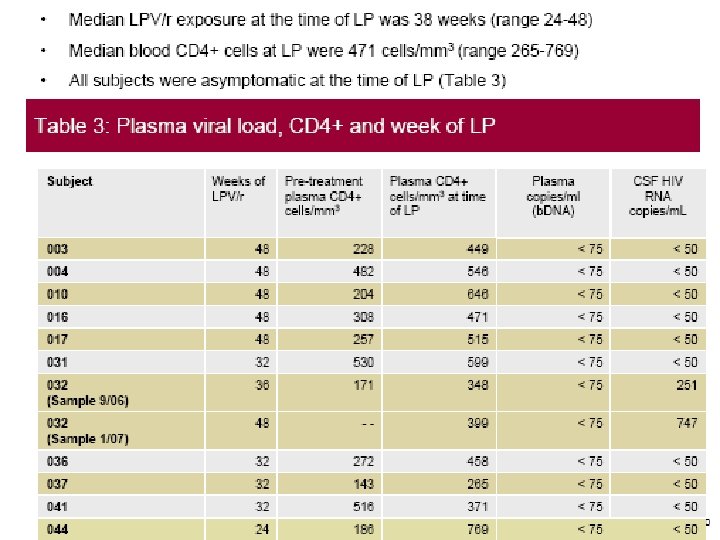
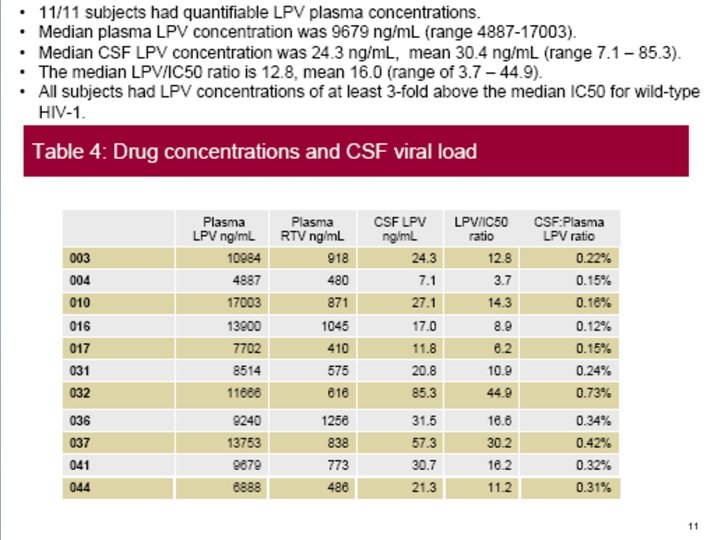
- Slides: 26