MONITORIZACIN DE FRMACOS BIOLGICOS INHIBIDORES DE TNF FACTOR

MONITORIZACIÓN DE FÁRMACOS BIOLÓGICOS INHIBIDORES DE TNF

FACTOR DE NECROSIS TUMORAL (TNF) • El TNFα es miembro de un grupo de citocinas que estimulan la fase aguda de la reacción inflamatoria. • Es una hormona glucopeptídica formada por 185 aa , que procede de un propéptido formado por 212 aa. • El gen de TNF está ubicado en el cromosoma 6, región 6 p 21.

• Su liberación produce activación local del endotelio vascular, vasodilatación y aumento de la permeabilidad vascular reclutamiento de cél inflamatorias, Ig y complemento, provocando la activación de los linfocitos T y B. • Aumenta la activación y adhesión plaquetarias, y probablemente la oclusión vascular sea la causa de la necrosis tumoral, de donde proviene su nombre. • Sus funciones son por unión a dos recep diferentes (TNFR 1 y TNFR 2) que se localizan en neutrófilos, células endoteliales y fibroblastos.

• Importante papel en mec defensa y rta frente una agresión local, pero cuando se encuentra en exceso produce una inflamación extemporánea con el conseceunte daño tisular. • Esta en ↑ en LS de articulaciones inflamadas, en tejido intestinal en EII, mediador de daño epitelial en psoriasis…
• Es posible la inhibición de TNFα o de su receptor celular con los llamados fármacos biológicos. Drástico cambio en el tto de estas enfermedades: • Se utilizan en tratamientos de medicina altamente específica que semodernos puede aplicar de modo personalizado varias enfermedades autoinmunitarias y con escasos efectos adversos como la AR, espondiloartropatías, EII y la psoriasis.

FARMACOS BIOLOGICOS • Son moléculas generadas o derivadas de células vivas, de base proteica y estructura muy compleja. • Son fabricados por ADN recom y/o métodos de expresión génica controlada. • Los inhibidores de TNF pueden ser quiméricos, humanizados o “totalmente humanos”.

• Hay 5 inhibidores de TNF en uso: - 3 son ac monoclonales completos - 2 son prot de fusión (frag de Ig unido a otra molécula) • Por ser estruc moleculares complejas de base proteica son muy inmunogénicos. • Evaluar su inmunogenicidad (producción de ac anti-fco) es requerimiento de la EMA para su comercialización. EMA European Medicines Agency

INFLIXIMAB (REMICADE®) • Ac monoclonal quimérico Ig. G 1 kappa. • Región variable (Fv) murina y región constante (Fc) con secuencias de Ig. G 1 humana. • En 1998 aprobado en conjunto con MTX para AR con poca rta. • Actual/ uso recomendado desde inicio en AR. Tb en EII, Psoriasis, EA y artritis psoriásica.

ADALIMUMAB (HUMIRA®) • Primer Ac totalmente humano, Ig. G 1 humana. • Aprobado en 2002. • Menos inmunogénico. • Mismas indicaciones que IFX.

GOLIMUMAB (SIMPONI®) • Ig. G 1 totalmente humana. • Aprobado en 2009 como terapia subcutánea para AR y más recientemente xa resto de indicaciones.

CERTOLIZUMAB PEGOL (CIMZIA®) • Proteína de fusión compuesta en Fv por Ac monoclonal recombinante y humanizado conjugado a polietilenglicol de 40 k. Da. • Carece de la región Fc del ac. • Aprobado en 2008 xa AR en combinación con MTX.

ETANERCEPT (ENBREL®) • Proteína de fusión dimérica totalmente humana, x tecnología de ADN recombinante. • Formada por parte extracelular del receptor TNFR 2 y Fc de cadena pesada de Ig. G 1. • Aprobado en 1998 para AR y posterior/ xa el resto.
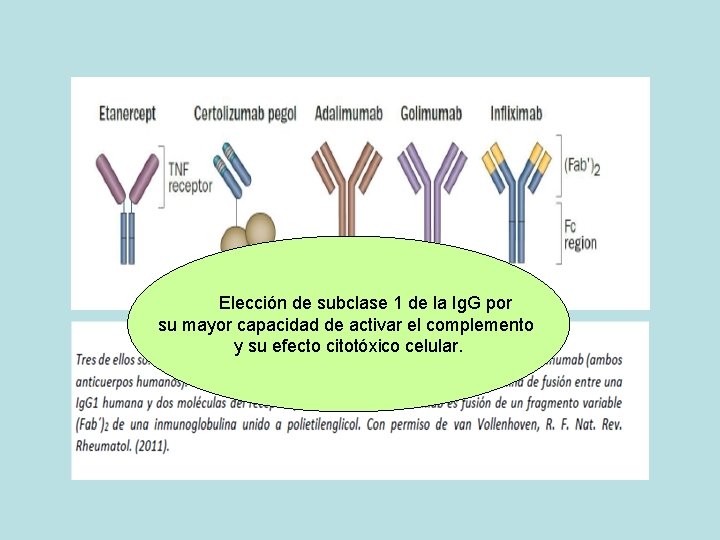
Elección de subclase 1 de la Ig. G por su mayor capacidad de activar el complemento y su efecto citotóxico celular.

FARMACOCINÉTICA • Admón iv (IFX) o subcutánea (resto). • Al ser Ig los procesos catabólicos son en tejidos, no en híago o riñón, jugando papel esencial el stma retículo-endotelial. • Influye la abundancia de antígeno diana, inmunogenicidad, edad, sexo, peso, alb… • Gran varaibilidad interindividual • Medidas en valle, momento de menor [

INMUNOGENICIDAD • Producción de ac frente al fco (agente externo) es la rec normal del stma inmune. • Ruta subcut. menos inmunogénica q iv. • Influye la estructura de la proteína, genética del pac y admón de inmunosupresores. • *La detección de ac anti-fco puede estar enmascarada por dosis altas de fco.

• Los ac anti-fco pueden ser neutralizantes (bloquean unión fco-TNF) o no neutralizantes. • Forman IC con el fco, su aclaramiento y [ fracaso del tto. • Los 3 ac monoclonales (IFX, ADL, GOLI) son bivalentes. • Las 2 proteínas (CTZ, ETN) son monovalentes y forman IC más pequeños

• Los AAF neutralizantes contribuyen al fracaso terapéutico de modo directo al interferir en la unión fco-TNF.

Frecuencia de aparición de AAF • La frec publicada es muy variable. • En su medida influye el método empleado, mto temporal (6 meses, 1 año tto…), dosis (↑ dosis ETN baja inmunogenicidad detección de por ac), tto concomitante (MTX el diseño de su molécula: Proteína de fusión* formada por parte inmunogenicidad)… del receptor TNFR 2 y Fc de cadena pesada de Ig. G 1 • • IFX: 25 -35% para AR, hasta 61% en EC *reconocida como propia por el organismo ADL: 15 -25% GOLI: 2 -5%. CTZ: 4 -8% ETN: no se han encontrado ac anti-ETN

¿Cómo influir en la inmunogenicidad? • Modulada de dos maneras: - Aumento de dosis - Admón conjunta de inmunosupresores • Los estudios muestran menor AAF en pac con MTX.

BIOSIMILARES • Una vez patente del fco ha expirado. • “Producto médico biológico que contiene una versión de la sustancia activa de un producto médico biológico original autorizado (producto médico de referencia)”. • Certificación de bioequivalencia. • Dirigidos frente los mismos epítopos antigénicos , producen los mismos AAF. • IFX y ETN

MÉTODOS DE MEDIDA DE NIVELES DE FCO Y AAF 1. • • 2. • • FÁRMACO: ENZIMOINMUNOENSAYOS (ELISA) RADIOINMUNOENSAYOS (RIA) BIOENSAYOS HPLC AAF ELISA PUENTE RIA BIOENSAYOS HPLC
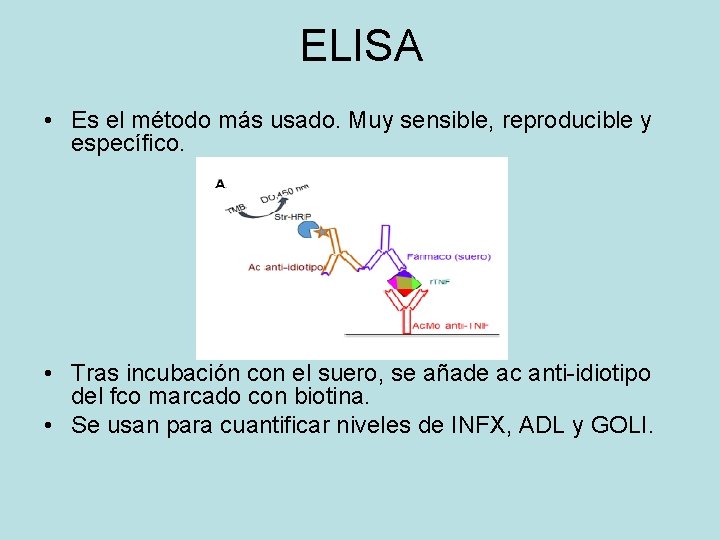
ELISA • Es el método más usado. Muy sensible, reproducible y específico. • Tras incubación con el suero, se añade ac anti-idiotipo del fco marcado con biotina. • Se usan para cuantificar niveles de INFX, ADL y GOLI.

• Captura del fco sobre placa recubierta con el F(ab´)2 de un ac monoclonal anti-fco y revelado con ac anti-idiotipo. • Se usan para cuantificar niveles de ETN y CTZ.
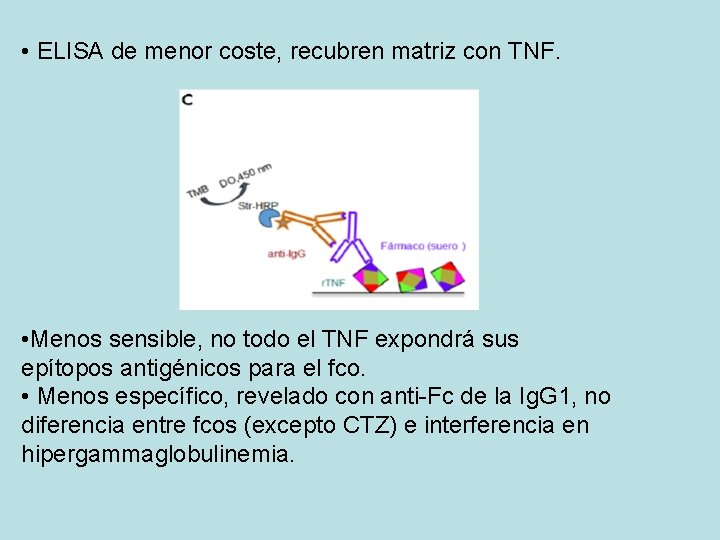
• ELISA de menor coste, recubren matriz con TNF. • Menos sensible, no todo el TNF expondrá sus epítopos antigénicos para el fco. • Menos específico, revelado con anti-Fc de la Ig. G 1, no diferencia entre fcos (excepto CTZ) e interferencia en hipergammaglobulinemia.

RIA • Fundamento igual que el ELISA pero revelado con ac marcados con 125 I. • Menos utilizados (instalaciones radioactiv)

BIOENSAYOS • Utiliza células (líneas celulares K 562, HEK 293) que responden a la presencia de TNF emitiendo luminiscencia. • Fco anti-TNF detectado x la inhibición de la luminiscencia emitida por una cantidad de TNF conocida. • Dificultad del manejo de células vivas y disponer de luminómetro.
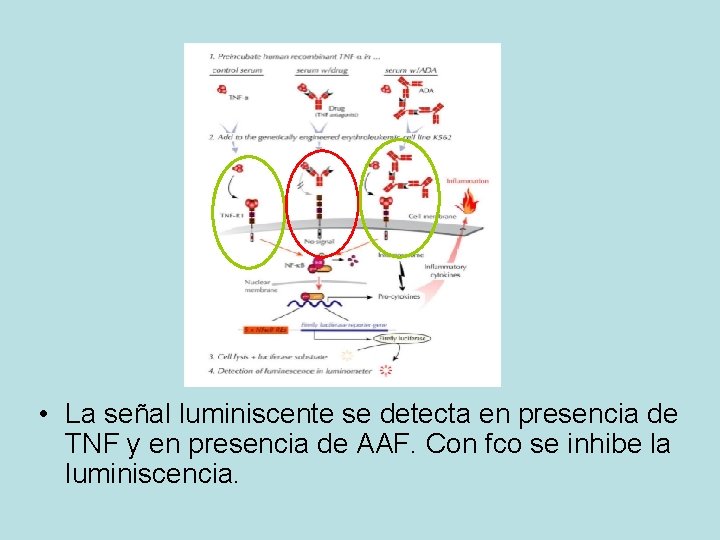
• La señal luminiscente se detecta en presencia de TNF y en presencia de AAF. Con fco se inhibe la luminiscencia.

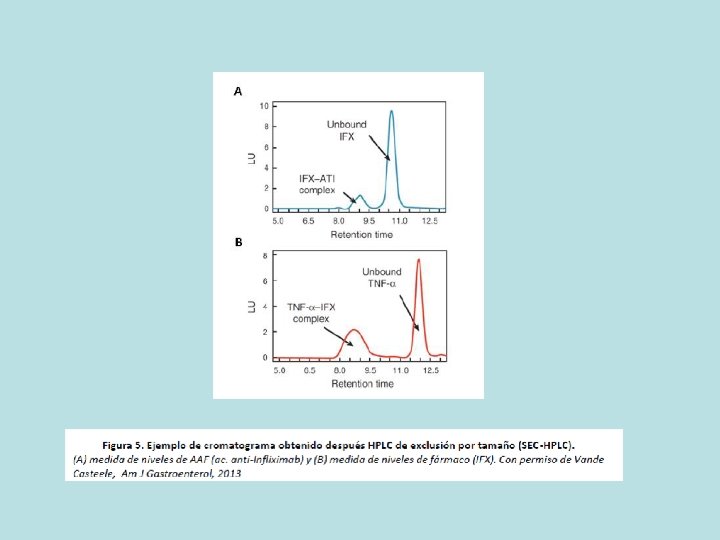
HPLC • HPLC de exclusión por tamaño (SEC-HPLC) • Se incuba una mezcla de una cantidad en exceso de TNF (TNF-alexa 488) con el suero con el fco y se aplican a una columna. • El primer pico será TNF-Fco (mayor peso molecular) y 2º pico el TNF sólo • Necesario en cada carrera control + y – y la curva de calibración. • Elevado coste y baja rta, tiempo excesivo…

NIVELES DE AC ANTI-FCO (AAF) • Su dificultad es detectar ac en presencia a su vez de ac (el ppo fco). • Los métodos más usados son el RIA y el ELISA puente

ELISA PUENTE • Método de los kits comerciales. Reproducible, sencillo y barato. • Aprovecha la capacidad de los AAF (moléculas Ig. G bivalentes y monoespecíficas) para “puentear” y unir dos moléculas idénticas. • Fco unido a placa y fco marcado enzimáticamente
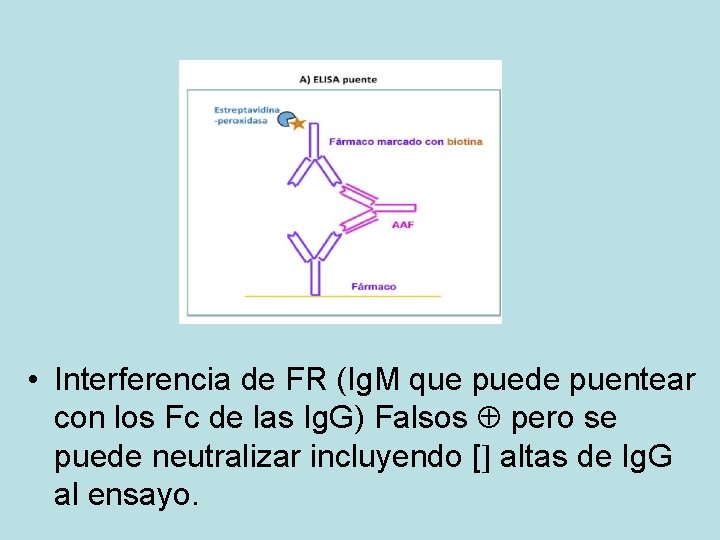
• Interferencia de FR (Ig. M que puede puentear con los Fc de las Ig. G) Falsos pero se puede neutralizar incluyendo [ altas de Ig. G al ensayo.

RIA • El suero del pac se hace pasar por una columna de Proteína A-Sefarosa donde queda retenida todas la Ig. G de la muestra. • Para detectar la Ig. G anti-fco, se incuba con la Fv del fco marcada con I radiactivo.
BIOENSAYOS Y HPLC

INTERFERENCIA DE FCO • Tanto RIA como ELISA puente sólo detectan AAF cuando están en exceso sobre la de fco. • Nuevos ensayos con paso previo de disociación de inmunocomplejos Fco-AAF y bloqueo. • Detección temprana de AAF pero cautela con cambios precoces de tto si no interfieren en la clínica. • Repercusión clínica de los AAF es cuando el fco no ejerce su acción por estar total/ bloqueado.
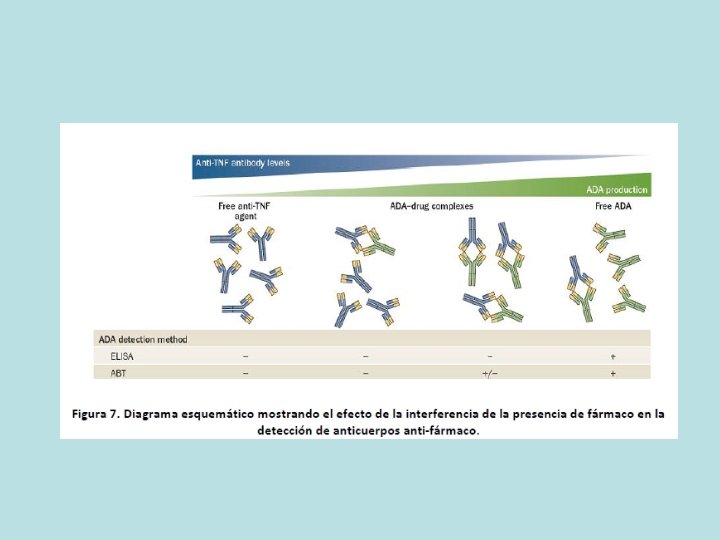

MONITORIZACIÓN PERSONALIZADA (Therapeutic drug monitoring o TDM) • Relacionar la rta clínica a un fco con un parámetro medible en suero ( [ fco o AAF). • Seguimiento de la actividad clínica del fco para individualizar la terapia. • La alterac de los valores en suero suele ser anterior a variaciones de índices de activ clínicos, que además son subjetivos.
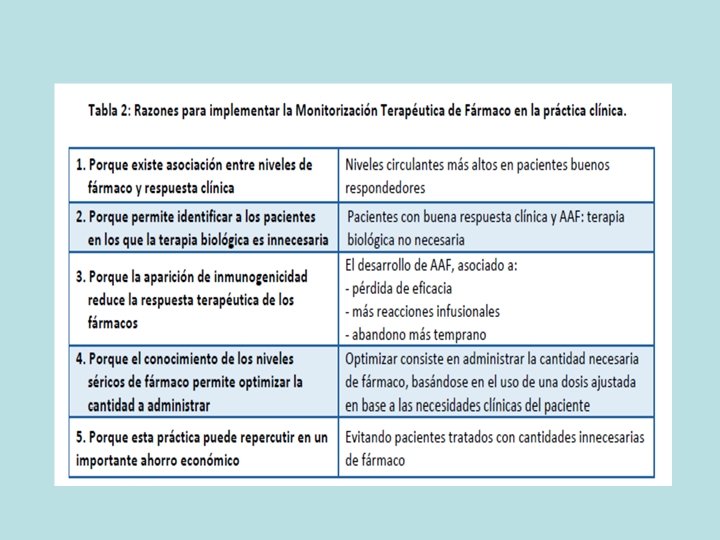
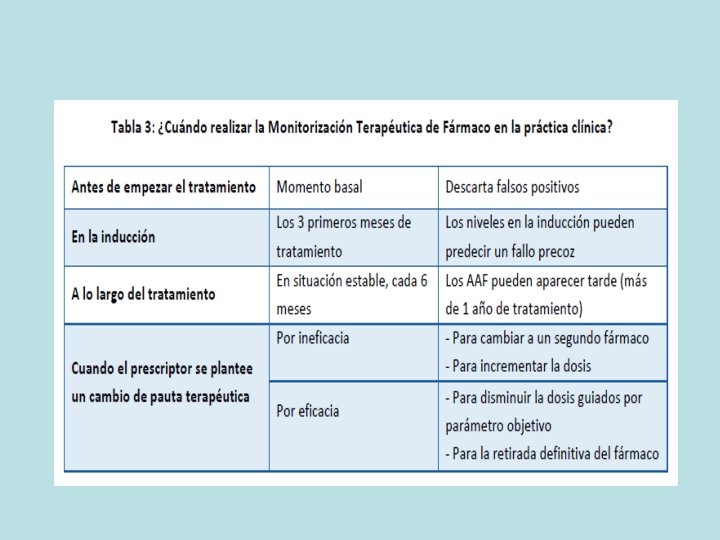


CONCLUSIONES • La medida de niveles es un dato objetivo, no cruento para el pac y proporciona una información más temprana q la variación de índices clínicos. • Relac directa entre fco y efecto biológico. • Monitorización niveles en valle de fco y AAF puede identificar la razón de fracaso de tto.

Gracias!
- Slides: 42