Molekulov fyzika Reln plyn Prof RNDr Emanuel Svoboda

Molekulová fyzika Reálný plyn Prof. RNDr. Emanuel Svoboda, CSc.

Reálný plyn Existence vzájemného silového působení mezi částicemi (tzv. van der Waalsovské síly) Odpudivá síla mezi částicemi (interakce překryvová) při dostatečně malých vzdálenostech mezi částicemi (plyny o velkých tlacích) Slabě se uplatňuje přitažlivé působení mezi obalem a jádrem

Typy přitažlivých van der Waal. sil 1. interakce mezi permanentními dipólovými momenty molekul , např. molekuly H 2 O, SO 2, NH 3, HCl, HBr 2. interakce mezi permanentními dipólovým momentem jedné molekuly (polární molekula) a indukovaným dipólovým momentem druhé (původně nepolární) molekuly – jedná se o polarizované molekuly; párová interakce. Např. plyn CO. 3. interakce mezi částicemi, které nemají dipólový moment – vzácné plyny (He, Xe), ale také např. H 2, N 2, CO 2; jde o tzv. disperzní interakci; v důsledku časově proměnného rozložení hustoty elektronů v atomu vznikne v okolí sousedních atomů proměnné elektrické pole, které indukuje tzv. mžikový dipólový moment. Výsledkem je přitažlivá síla - největší přispěvovatel k ∑F+

Souhrnně přitažlivé síly ZÁVĚR: Všechny mezimolekulové síly mají svůj původ v elektrických silách. Zdůvodnění průběhu grafů F(r) Neplatí stavová rovnice IP, především při vysokých tlacích a nízkých teplotách plynu; vnitřní energie reálného plynu je funkcí nejen teploty, ale i objemu!!!

Projev přitažlivých sil – příklady : vazba atomů C v grafitu kondenzace páry odporové síly pavouka drží příchytné chlupy – až půl milionu chloupků na konci nohou např. skákavka černá by nespadla, ani kdyby měla hmotnost 173 x větší než má umělá noha s příchytnými chloupky pavoučími o ploše s obsahem 1 m 2 by unesla 24 tun!
Gekoni, superizolepa Gekoni (trop. ještěři) – miliardy pružných rozvětvených submilimetrových stětiček – spatul - se přitahují van der W. silami s atomy podkladu S gekoní pokožkou na dlani by člověk mohl viset ze skleněného stropu superizolepa Gekon turecký žijící u nás

Odvození stavové rovnice van der Waalsovy Zvolíme 1 mol plynu N = {NA}, objem Vm Uvažujeme nejprve vliv odporových sil, tj. vlastní rozměr (objem) molekul Molekuly tvoří tuhé koule o průměru d Nákres – filosofie úvahy (převod na soustavu hmotných bodů) Další předpoklad: molekuly nelnou ke stěnám a odrážejí se od nich pružně Kolem každé molekuly opíšeme sféru molekulového působení o poloměru d, objem sféry označíme d Tedy: ke středu kterékoli molekuly se může jiná molekula přiblížit jen na vzdálenost d; vnitřek koule o poloměru d je pro ostatní molekuly nepřístupný objem Vm musíme zmenšit o součet objemů těchto koulí.

Výpočet skutečného objemu – jeho číselné hodnoty pro N = 1 je k disp. objem {Vm} pro N = 2 pro N = 3 pro N = k pro N = {NA} {Vm} - {Vo} {Vm} - 2{Vo} {Vm} – (k-1){Vo} {Vm} – ({NA} -1){Vo} Průměrný objem (jeho číselná hodnota) přístupný středu kterékoli molekuly z celkového počtu N = {NA} : OPRAVA

Korekce na molární objem Objem 1 molekuly b je 4 násobek vl. objemu všech molekul v 1 molu plynu První závěr: Uvažujeme-li odpudivé síly, pak pro 1 mol reálného plynu má stavová rovnice tvar Neboli částice RP můžeme nahradit hmotnými body, jestliže molární objem zmenšíme o hodnotu b

Význam vztahu pro b (kromě opravy na molární objem) Známe-li b, můžeme vypočítat průměr d molekuly Viz úloha 3 ve cvičení 7 Problém: Jak určit b? Probereme později

Oprava na vliv přitažlivých sil Při malých vzájemných vzdálenostech molekul (velký počet molekul, plyn má velkou teplotu) se uplatňují tzv. kohézní síly (pokud molekuly nejsou v přímém kontaktu) Je-li sféra vzájemného působení uvnitř plynu (daleko od stěny nádoby), je výslednice vzájemného silového působení nulová Je-li molekula blízko stěny, pak na každou molekulu působí výsledná síla kolmá na stěnu nádoby a mířící dovnitř nádoby – viz obrázek Výslednice zvaná kohezní síla (směřující dovnitř nádoby) vyvolává kohézní tlak - o tuto hodnotu je tlak plynu menší než by byl u IP
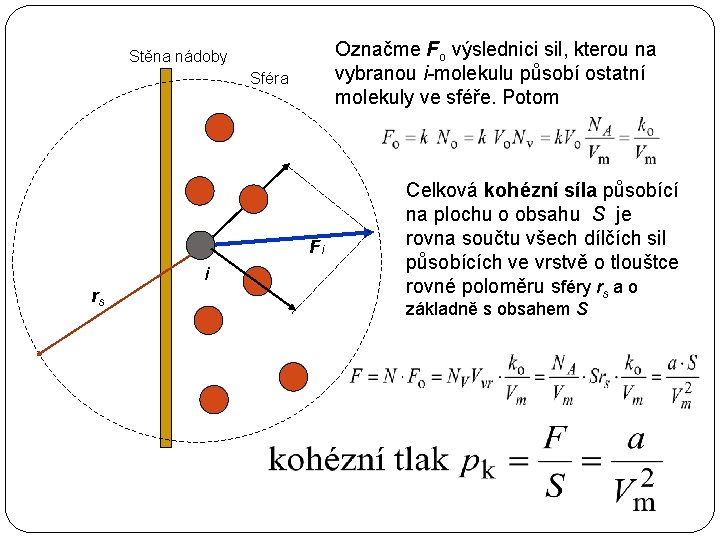
Označme Fo výslednici sil, kterou na vybranou i-molekulu působí ostatní molekuly ve sféře. Potom Stěna nádoby Sféra Fi i rs Celková kohézní síla působící na plochu o obsahu S je rovna součtu všech dílčích sil působících ve vrstvě o tlouštce rovné poloměru sféry rs a o základně s obsahem S

Oprava na kohésní tlak Započítáním obou změn – van der Waalsova rovnice pro reálný plyn (1873, Nobelova cena): Hodnoty a a b – viz st. materiál
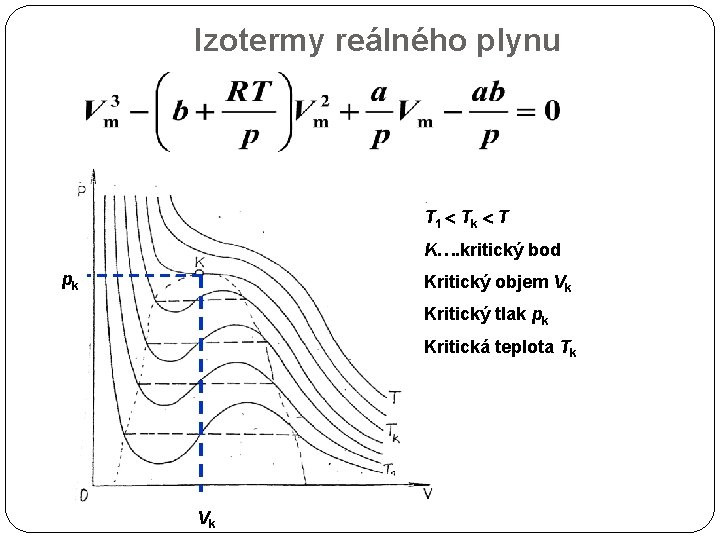
Izotermy reálného plynu T 1 Tk T K…. kritický bod pk Kritický objem Vk Kritický tlak pk Kritická teplota Tk Vk
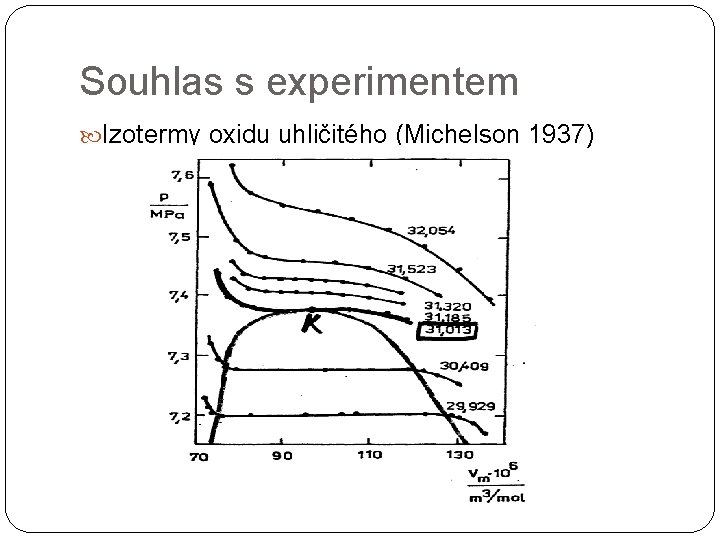
Souhlas s experimentem Izotermy oxidu uhličitého (Michelson 1937)
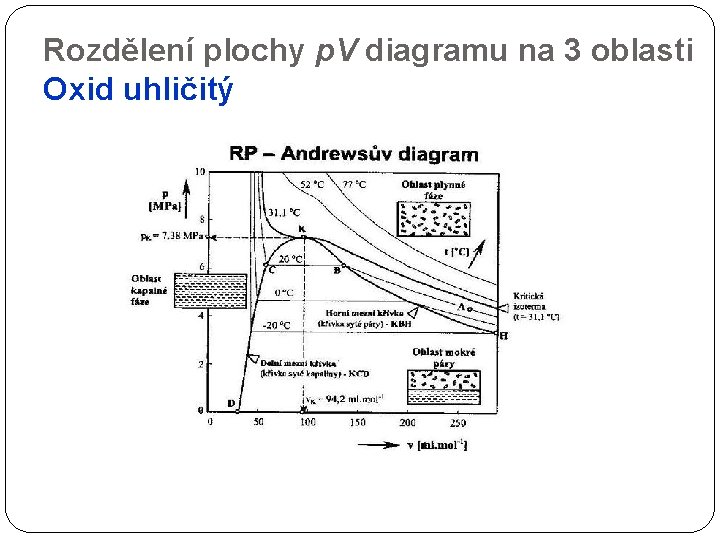
Rozdělení plochy p. V diagramu na 3 oblasti Oxid uhličitý

Souhlas experimentu s rovnicemi u IP a RP pro H 2 a N 2 Zvolíme počáteční hodnoty V = 1 m , 3 p = 0, 1 MPa T = 273 K (tím dáno n) Kdyby se reálný plyn řídil stav. rovnicí pro IP, musel by součin p. V být konstantní pro izoterm. děj – číselně 0, 1 nezávisle na p. Ale pro rostoucí tlak (grafy 1) velké odchylky, např. pro 100 MPa dvojnásobné. Použijeme-li van der Waalsovu rovnici, tak velmi dobrý souhlas (grafy 2) – odchylky pro vysoké tlaky 4, 5 % (N 2) a 9 % (H 2) Hledání lépe vyhovujících stavových rovnic Berthelotova 1900 Berthelot-franc. chemik a politik Redlich – Kwongova 1948 Redlich, Rakušan, přesídlil do USA ; fyz. chemik. Kwong, Číňan, emigrace do USA, chem. inženýr

Viriálová rovnice (viriální rozvoj, 1901) Pro stavovou rovnici IP pouze 1. koeficient Pro van der Waalsovský plyn B(T) = b – a/RT, C(T) = b 2 (když provedeme rozvoj výrazu (1 – b/Vm)– 1 podle b/Vm)

Binomický rozvoj

Výpočet koeficientů a a b z kritických veličin Pro 1 mol reálného plynu platí rovnice Pro tlak plynu pak vztah Pro inflexní bod K na izotermě Řešením dostaneme Např. vodní pára: a = 0, 552 J m 3 mol– 2; b = 30, 4 10– 6 m 3 mol– 1

Úloha 1 Uzavřená nádoba je naplněna sytou vodní párou teploty 20 o. C (bez přítomnosti vody). Určete přírůstek tlaku v nádobě, zvýšíme-li teplotu páry na 150 o. C. Předpokládejte, že nedochází k deformaci nádoby. Van der Waalsovy koeficienty pro vodu jsou a = 5, 55. 105 J·m 3·kmol– 2, b = 3, 04. 10– 2 m 3·kmol– 1. Hustota syté vodní páry při teplotě 20 °C je 17, 3 g·m– 3 (z tabulek).

Řešení úlohy 1 Z van der Waalsovy rovnice vyjádříme p a vypočteme p Zkouška jednotek: Početně: p 1, 04 k. Pa Kdybychom uvažovali, že se jedná o ideální plyn (zanedbali b), pak vyjde p 1 k. Pa.

Úloha 2 • Určete průměr molekuly metanu, víte- li, že hodnota van der Waalsovy konstanty pro tento plyn je b = 0, 038 m 3·kmol– 1.

Řešení úlohy 2 • K řešení použijeme vztah pro korekční člen b:

Úloha 3 • Použijte van der Waalsovu rovnici a vypočtěte teplotu, pro níž tlak kyslíku O 2, který má hustotu 100 kg m-3, je 8, 0 MPa. Vypočítanou hodnotu porovnejte s teplotou, která by vyšla při použití stavové rovnice ideálního plynu.
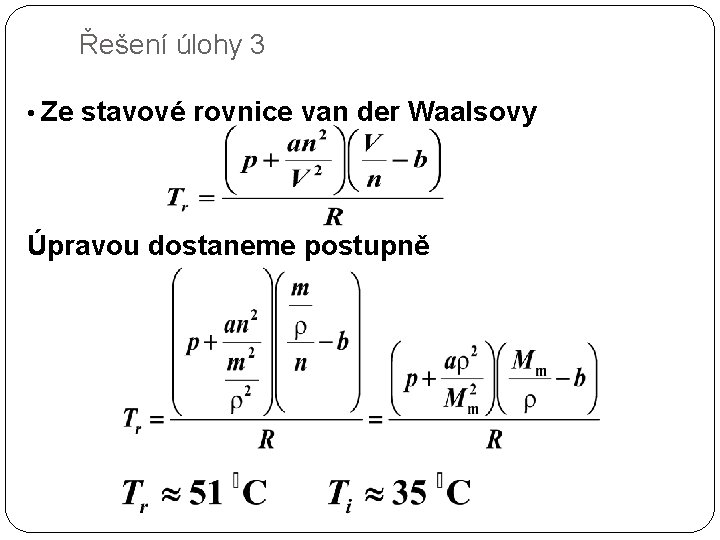
Řešení úlohy 3 • Ze stavové rovnice van der Waalsovy Úpravou dostaneme postupně
- Slides: 26