Molekulov fyzika 2 prezentace Teplota Plynov teplomr GayLussac






- Slides: 8

Molekulová fyzika 2. prezentace „Teplota“

Plynový teploměr Gay-Lussac: °C-1 (ideální plyn)

Součinitelé rozpínavosti a roztažnosti pro reálné plyny p=130 k. Pa: plyn vodík dusík vzduch helium neon p (103 K-1) 3, 659 3, 673 3, 658 3, 660 V (103 K-1) 3, 662 3, 674 3, 661 3, 662 p – součinitel roztažnosti V – součinitel rozpínavosti = 3, 6610 10 -3 K-1 (pro ideální plyn) extrapolace k nulovému tlaku (Bakule R. , Brož. J: Molekulová fyzika. Skriptum MFF UK, 1989 )

Teplota z mikroskopického hlediska M m – molární hmotnost R – univerzální plynová konstanta v – rychlost molekuly Teplota je pro daný druh plynu jednoznačně určena střední hodnotou kvadrátu rychlosti molekul. Ø Nemá smysl mluvit o teplotě jedné izolované molekuly, ale teplota je veličina, která charakterizuje intenzitu chaotického pohybu souboru molekul. Ø Počet molekul v souboru musí být dostatečně velký, abychom mohli aplikovat statistický přístup. Ø

Kinetická energie částic v jednom molu ideálního plynu 1 molekula 1 stupeň volnosti Na každý stupeň volnosti neuspořádaného postupného pohybu molekul plynu, který je ve stavu termodynamické rovnováhy, připadá stejně velká, na druhu plynu nezávislá, střední kinetická energie rovná k. BT/2. → EKVIPARTIČNÍ TEORÉM PRO JEDNOATOMOVÝ PLYN

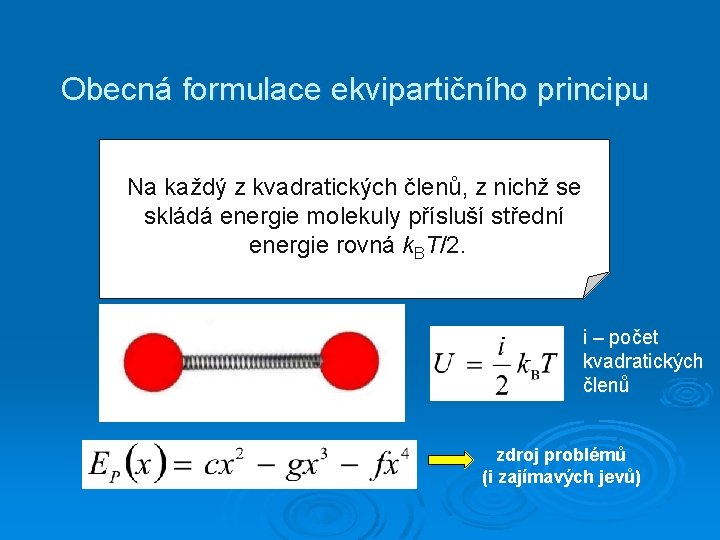
Obecná formulace ekvipartičního principu Na každý z kvadratických členů, z nichž se skládá energie molekuly přísluší střední energie rovná k. BT/2. i – počet kvadratických členů zdroj problémů (i zajímavých jevů)

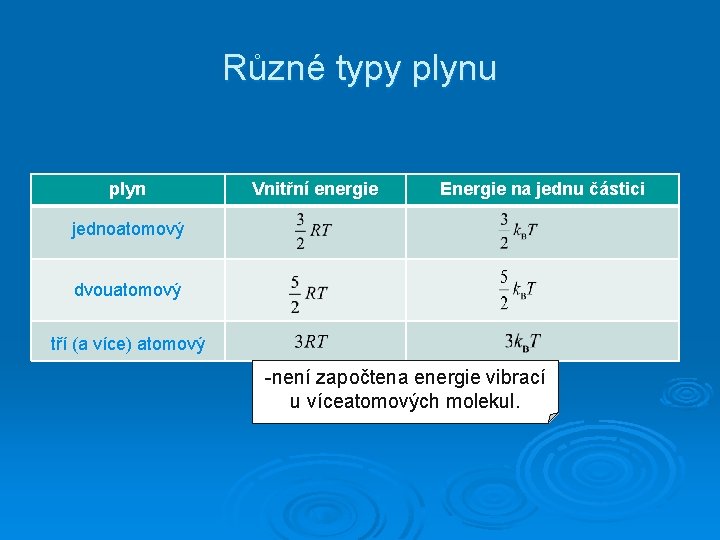
Různé typy plynu plyn Vnitřní energie Energie na jednu částici jednoatomový dvouatomový tří (a více) atomový -není započtena energie vibrací u víceatomových molekul.

Co na to experiment? Ø jednoatomový plyn → bez problémů ? Ø dvouatomové molekuly → Ø přidat Ep je problematické; vyžadovalo by to speciální charakter meziatomových sil Teplota a energie na sobě závisí, ale pro každou látku je tato závislost jiná. Ø Ekvipartiční teorém funguje jen při vysokých teplotách ( 2000 K) Ø