MOLEKLLER ARASI ETKLEMLER 1 Hazrlayan Feride BAHEC MOLEKLLER
MOLEKÜLLER ARASI ETKİLEŞİMLER 1 Hazırlayan: Feride BAHÇECİ
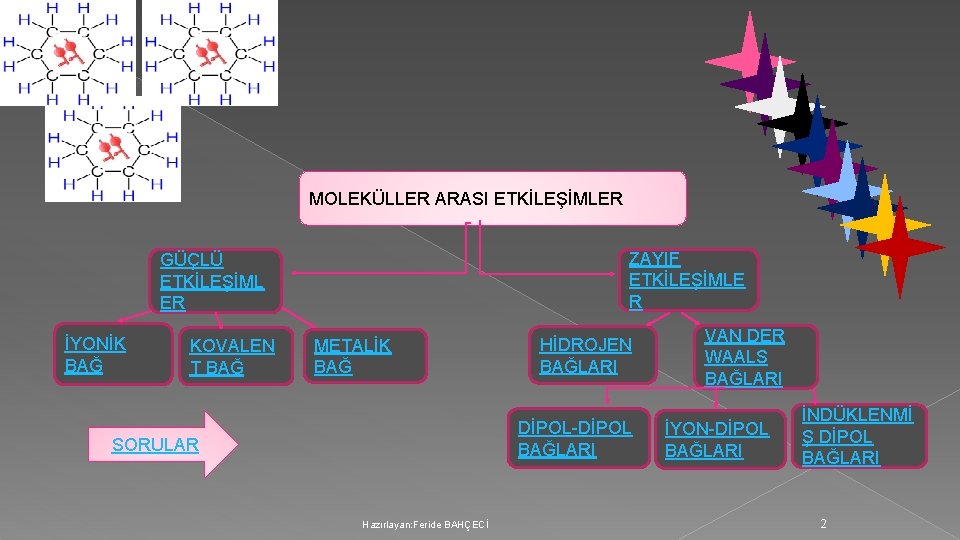
MOLEKÜLLER ARASI ETKİLEŞİMLER ZAYIF ETKİLEŞİMLE R GÜÇLÜ ETKİLEŞİML ER İYONİK BAĞ KOVALEN T BAĞ METALİK BAĞ HİDROJEN BAĞLARI DİPOL-DİPOL BAĞLARI SORULAR Hazırlayan: Feride BAHÇECİ VAN DER WAALS BAĞLARI İYON-DİPOL BAĞLARI İNDÜKLENMİ Ş DİPOL BAĞLARI 2

GÜÇLÜ ETKİLEŞİMLER � Kimyasal türler arasında oluşan güçlü etkileşimler üç tanedir. � 1. İyonik bağ � 2. Kovalent bağ � 3. Metalik bağ � Bu bağlar kimyasal türler arası etkileşimler içerisinde en güçlü olanlarıdır. 3

İYONİK BAĞ � � � Kimyasal türler arası etkileşimler içindeki ilk etkileşimdir. Elektronegatiflikleri çok farklı olan atomlar arasında elektron alış verişinin tam olduğu ve sonuçta iyonların oluştuğu varsayılır. Elektron kaybeden pozitif iyon, elektron alan ise negatif iyon olur. İyonik bağ ise pozitif ve negatif iyonların arasındaki elektrostatik çekme kuvvetidir. Na. Cl bileşiği iyonik bağ için iyi bir örnektir. Na atomu Na+ iyonuna dönüştüğünde oktete uymuştur. Cl atomu CI- iyonuna dönüştüğünde oktete uymuştur. İyonlar arasında iyonik bağlı Na+ CI- ya da Na. CI bileşiği oluşur. 4

İyonik Bağların Sağlamlığı � � � � İyonik bağlı bileşiklerde iyonik bağın sağlamlığı iyon yarıçaplarına ve iyon yüklerine göre yorumlanabilir. İyon yarıçapı arttıkça, elektrostatik çekim gücü azalır. İyon yükü arttıkça çekim gücü artar ve iyonik bağın kuvveti artar. Örneğin, Na. F, Na. CI, Na. Br ve Nal bileşiklerindeki iyonik bağların sağlamlığını karşılaştırmak için bileşiklerdeki iyonlar arası uzaklıklara bakılabilir. İyon yarıçapları I- > Br- > Cl- > F- şeklindedir. İyonların çekirdekleri arasındaki uzaklık azaldıkça iyonik bağ daha sağlam hale gelir. Böylece erime noktası yükselir. İyonlar arası uzaklık: Nal > Na. Br > Na. CI > Na. F şeklindedir. 5

İyonik bağın sağlamlığı: Na. F > Na. CI > Na. Br > Nal şeklindedir. Bileşiklerin erime noktaları: Na. F > Na. CI > Na. Br > Nal şeklindedir. Örneğin, Ca. O ve Ca. CI 2 bileşiklerindeki iyonik bağların sağlamlığını karşılaştırmak için iyonların yüklerine bakılabilir. � Coulomb kanununa göre yüklerin büyüklüğü arttıkça, elektrostatik çekim kuvveti artar. � Ca. O katısındaki anyonun yükü (O-2), Ca. CI 2'deki anyonun yükünden (Cl-) daha büyüktür. Dolayısıyla elektrostatik çekim kuvveti Ca. O katısında daha büyüktür. Bunun sonucu olarak iyonik bağ Ca. O'de daha sağlamdır, erime noktası da daha yüksektir. � � � 6

İyonik Bağlı Bileşiklerin Özellikleri � � � İyonik bağlı bileşikler zıt yüklü iyonların bir araya gelmesiyle oluşan elektrostatik çekim kuvveti olduğundan, erime ve kaynama noktaları yüksektir. İyonik bileşiklerin katı halleri sert ve kırılgandır. İyonik katı üzerine çekiçle vurulduğunda iyonik kristalin düzenli yapısı bozulur ve kırılma olayı gerçekleşir. Bu yüzden iyonik katılar çekiçle dövülerek şekillendirilemez. İyonik bağlı katılarda iyonlar hareket etmediği için elektrik akımını iletmezler. İyonik katılar suda çözündüğünde sulu çözeltilerine iyonlarını verirler, böylelikle oluşan çözelti elektrik akımını iletir. (Elektrolit çözelti oluşur. ) İyonik katılar sıvı hale dönüştüğünde elektrik akımını iletir. 7

KOVALENT BAĞ � Daha kararlı hale gelebilmek için iki atom arasında iki veya daha fazla elektronun ortaklaşa kullanılması ile oluşan kimyasal bağlara kovalent bağ denir. Oluşan bileşiklere ise kovalent bağlı bileşikler denir. Kovalent bağlı moleküllerin oluşması için kullanılan elementlerin ametal olması gerekir. H 2, O 2, CO 2, H 2 O, NH 3, CH 4, C 2 H 6 gibi moleküller kovalent bağlıdır. 8
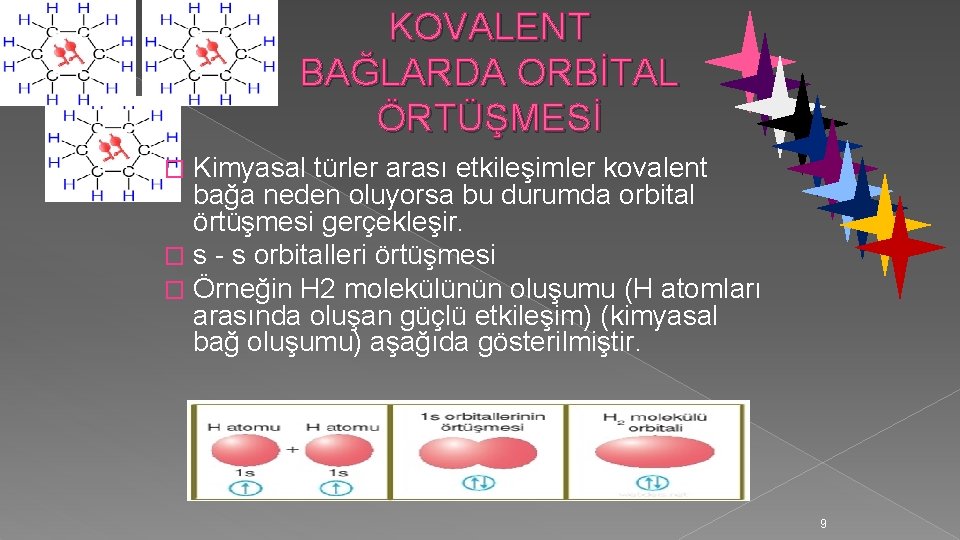
KOVALENT BAĞLARDA ORBİTAL ÖRTÜŞMESİ Kimyasal türler arası etkileşimler kovalent bağa neden oluyorsa bu durumda orbital örtüşmesi gerçekleşir. � s - s orbitalleri örtüşmesi � Örneğin H 2 molekülünün oluşumu (H atomları arasında oluşan güçlü etkileşim) (kimyasal bağ oluşumu) aşağıda gösterilmiştir. � 9

1 H: 1 s 1 elektron dizilimine göre iki hidrojen atomu birbirine yaklaştığında 1 s orbitalleri birbirinin içine geçmeye başlar. Bu olaya orbitallerin örtüşmesi denir. � Hidrojen atomundaki 1 s orbitallerinin örtüşmesi orbital şemaları ile gösterelim. � � Şekilde de hidrojen atomunda s örtüşmesi gösterilmiştir. Burada çekirdekler arasında negatif yüklü elektron yoğunluğu artışı olur ve çekim kuvveti artar. H atomları arasında kovalent bağ oluşur. � s - p ve p - p orbitalleri örtüşmesi � 10
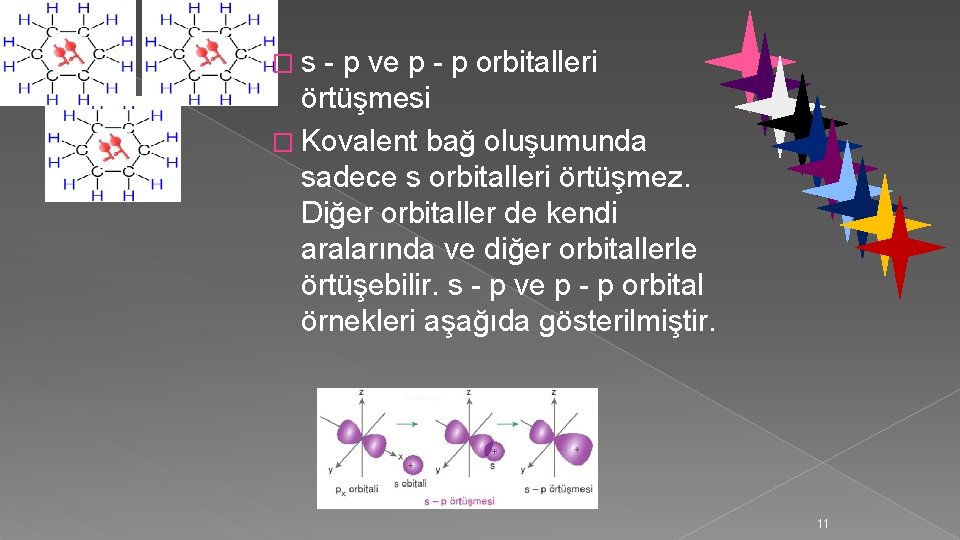
�s - p ve p - p orbitalleri örtüşmesi � Kovalent bağ oluşumunda sadece s orbitalleri örtüşmez. Diğer orbitaller de kendi aralarında ve diğer orbitallerle örtüşebilir. s - p ve p - p orbital örnekleri aşağıda gösterilmiştir. 11

Metalik Bağ Metal atomlarının gevşek bağlı değerlik elektronları vardır. Bu elektronlar diğer metal atomlarında bulunan eş enerjili boş değerlik orbitalleri arasında gezinir. Bu şekilde çok sayıda elektronların metal atomları arasında gezinmesiyle bir elektron denizi oluşur. Bu arada elektron kaybeden atomlar pozitif yüklü iyon haline gelir. � Pozitif yüklü metal iyonları ile elektron denizi arasında elektrostatik çekim kuvveti meydana gelir. Bu çekim kuvveti metalik bağ olarak adlandırılır. Metalik bağ atomlarının bir arada durmasını sağlar. � 12

Gevşek değerlik elektronlarının oluşturduğu elektron denizi ile metal katyonları arasında oluşan çekim metalik bağdır. Metal atomları metalik bağla bir araya gelerek kristal yapı oluşturur. � Metalik bağda ortamda hareket eden değerlik elektronları ve değerlik elektronlarını vermiş gibi olan metal katyonu vardır. Metalik bağda pozitif ve negatif yük sayısı birbirine eşittir. Metalik kristalin örgü yapısında değerlik elektronlarının serbestçe dolaşabilmesi metalik bağın iyonik ve kovalent bağlardan farklı olmasına sebep olur. Elementler içerisinde metallerin en önemli özelliklerinden birisi elektrik akımını ve ısıyı iyi iletebilmeleridir. Bununla birlikte metallere has başka özellikler de bulunur. � 13

Metallerin Bazı Özellikleri � Kimyasal türler arası etkileşimler sonucunda metallerin çeşitli özellikleri ortaya çıkar. Metallerin özelliklerine bu konu çerçevesinden bakabiliriz. � Tel ve Levha Haline Getirebilme � Metallerin Elektrik iletkenliği � Metalik Parlaklık � Metallerin Sertliği 14

Zayıf Etkileşimler � Kimyasal türler arası etkileşimler içinde daha güçsüz olanları zayıf etkileşimler olarak adlandırırız. Zayıf etkileşimler (fiziksel bağlar) maddelerin yoğun fazlarında (sıvı ve katı halde) etkilidir. Bu tür bağların kuvveti sıcaklığa bağlıdır. Sıcaklık değiştikçe tanecikler arasındaki etkileşimin kuvveti değişir, maddenin fiziksel hali değişir. Ancak maddenin kimyasal türü değişmez. Bundan dolayı bu tür değişimler fiziksel olaylardır. 15

DİPOL Kimyasal türlerde elektron yoğunluğunun fazla olduğu yer negatif kutup, elektron yoğunluğunun az olduğu yer pozitif kutup olarak adlandırılır. Bir kimyasal tür pozitif ve negatif kutup bulunduruyorsa yani elektron yük yoğunluğu eşit dağılmamış bir yapı içeriyorsa iki kutuplu anlamına gelen dipol terimi kullanılır. � Bazı türler kalıcı dipole sahipken, bazı türler geçici (anlık) dipol içerirler. � Kalıcı dipoller: HF, HCI, HBr gibi moleküllerdeki atomların elektronegatiflikleri farklıdır. Bu yüzden moleküller polar moleküllerdir. Bu moleküllerde atomların birinde negatif yük yoğunluğu diğerinde ise pozitif yük yoğunluğu bulunur. Bunlar kalıcı dipol karakter oluşturur. � Bu kutuplar bağ kopmadığı sürece korunur. Bu nedenle polar kovalent bağ yapmış iki atomlu moleküller kalıcı dipole sahiptir. Örneğin HCI, HF ve Hl gibi moleküller kalıcı dipole sahiptir. � 16

Geçici (İndüklenmiş) dipoller: Aynı atomlardan oluşan H 2, F 2, Cl 2, N 2 gibi moleküller ve He, Ne, Ar gibi soygazlarda elektron dağılımı eşittir. Böyle maddelere apolar denir. Bu türlerde kalıcı dipoller oluşmaz. � Ancak apolar yapılar polar yapı kazanabilir. Bunun için elektronların ait olduğu atomun veya molekülün bir bölgesine yığılması gerekir. Bu yığılma dışarıdan yapılan bir etkiyle oluşuyorsa ortaya çıkan dipole indüklenmiş dipol denir. � Apolar bir tanecikte ne kadar çok elektron varsa indüklenmiş dipolün polaritesi o kadar büyük olur. � Kimyasal türler arası etkileşimler zayıf etkileşimse Wan der Waals ya da hidrojen bağı vardır. � 17

Van Der Waals Bağları Kalıcı dipol ve indüklenmiş dipole sahip olan kimyasal türlerin kendi aralarında ve diğer türler ile yaptığı her türlü fiziksel bağ (hidrojen bağı hariç) Van der waals bağıdır. � Dipol - dipol Bağları: Polar moleküller arasında oluşan bağ türüdür. İki polar molekül birbirine yaklaşırken birinin pozitif kutbu ile diğerinin negatif kutbu arasında oluşan elektrostatik çekmelere dipol - dipol kuvvetleri denir. � Dipol - dipol bağlarında sadece çekme kuvvetleri yoktur, benzer yükler arasında itme kuvvetlerinde vardır. Bu da oluşan bağı zayıflatır, taneciklerin düzenli bir şekilde bir araya gelmelerini engeller. � Dipol - dipol kuvvetleri HCI, Hl gibi maddelerin yoğun fazlarında görülen ya da bu tür maddelerin birbiri içinde çözünmesi sırasında oluşan kuvvet türüdür. Bu nedenle polar yapıya sahip moleküller birbiri içinde çözünebilir. Örneğin etil alkolün (C 2 H 5 OH) su içerisinde çözünmesinde her iki molekülün de polar yapıya sahip olması önemli bir etkendir. � 18

� � � İyon - Dipol Bağları: Bir iyonun polar bir molekül ile etkileşmesi sırasında oluşan bağ türüdür. Katyonlar molekülün negatif kutbu ile anyonlar ile molekülün pozitif kutbu ile etkileşir. Yemek tuzunun (Na. CI) suda çözünmesi olayında tanecikler arasında oluşan etkileşim iyon - dipol bağıdır. Na. CI kristalleri suya atıldığında polar su moleküllerinin negatif kutbu Na+ katyonlarına pozitif kutbu Cl-iyonlarına yaklaşır ve iyonlar kristal örgüden koparak su içerisinde dağılırlar. İndüklenmiş (Geçici) Dipoller Arasındaki Bağlar (London Kuvvetleri): Polar olmayan He, Ne, H 2, O 2, CO 2 gibi tanecikler arasında çekim kuvvetleri oldukça zayıftır. Bu taneciklerin birbiri ile çarpışması sonucunda geçici dipoller oluşur. Geçici dipoller sayesinde N 2, CO 2, CH 4 gibi apolar moleküller sıvı hatta katı hale geçebilirler. İndüklenmiş dipol - indüklenmiş dipol kuvvetlerine London kuvvetleri de denir. Bu kuvvetler ilk kez Fritz London tarafından açıklanmıştır. 19

Dipol - İndüklenmiş Dipol Etkileşimi: Polar maddelerin dipolleri ile apolar maddelerin indüklenmiş dipolleri arasında anlık oluşan kuvvetlere dipol - indüklenmiş dipol etkileşimi denir. � Dipol - indüklenmiş dipol bağları dipol - dipol bağlarını koparacak kadar kuvvetli değildir. Bu nedenle polar maddeler ile apolar maddelerin birbiri içindeki çözünürlüğü yok denecek kadar azdır. Örneğin apolar l 2 molekülleri polar H 2 O da çözünmez, ancak apolar CCI 4 de iyi çözünür. � İndüklenmiş Dipol - İndüklenmiş Dipol Etkileşimi: Aynı veya farklı apolar taneciklerin geçici dipolleşmesi sonucu aralarında oluşan elektrostatik çekim kuvvetleri indüklenmiş dipol etkileşimidir. � Apolar maddeler birbiri içerisinde genellikle iyi çözünür. Örneğin apolar l 2 katısı apolar CCI 4 sıvısında çözünür. � 20

Hidrojen Bağları Hidrojen bağının oluşabilmesi için hidrojenin molekülde bulunması gerekir. � Hidrojen bağı Van der Waals bağları ile kıyaslandığında, hidrojen bağları yaklaşık olarak 10 kat daha güçlüdür. � Hidrojen bağı oluşturan maddeler birbiri içinde daha iyi çözünür. Örneğin etilalkol (C 2 H 5 OH) su molekülleriyle dipol - dipol bağlarının yanında hidrojen bağları da oluşturur. Bu yüzden etil alkol suda çok iyi çözünür. � Çok sayıda hidrojen bağı oluşturabilen bazı moleküllerin arasındaki fiziksel bağlar atomlar arası kovalent bağlardan daha kuvvetli olabilir. Örneğin glikoz bir kapta ısıtıldığında erimeye başlamadan önce molekül yapısı bozulur. Çünkü çok sayıda hidrojen bağı yapan şeker molekülleri arasındaki fiziksel bağ o kadar kuvvetlidir ki, bu bağlar kopmadan moleküldeki kovalent bağlar kopar. Bu nedenle ısıtılan şeker önce karamelleşir ısıtılmaya devam edildiğinde ise kömürleşir. � 21

Soru – 1 Aşağıdaki kimyasal bağlardan en kuvvetli olanı hangisidir? A) Polar Kovalent Bağ B) Wan der Vaals Kuvvetleri C) Dipol – Dipol Etkileşimi D) Hidrojen Bağı E) London Kuvvetleri 22

Soru – 2 Aşağıdaki bileşiklerden hangisi kovalent bağlıdır? A) KCl B) Mg. Cl 2 C) Al 2 O 3 D) Be. Cl 2 E) NO 3 23

Soru – 3 Aşağıdaki kimyasal etkileşimlerden hangisi apolar kovalent bağlıdır? A) NO 2 B) Na. Cl C) N 2 D) NO E) SO 2 24

Soru – 4 I. Elementlerin elektrik iletkenliği II. Elementlerin Isıl İletkenliği III. Elementlerin periyodik cetveldeki grup numarası IV. Elementlerin sertlik ve yumuşaklığı Yukarıda sıralanan maddelerden hangisi veya hangileri metalik bağlarla ilgilidir? A) Yalnız I B) I ve II C) I ve III D) I, II ve IV E) I, III ve IV 25

Soru – 5 O 2 gazında bulunan moleküller arası etkileşim türü aşağıdakilerden hangisidir? A) Apolar Kovalent B) London Kuvvetleri C) Polar Kovalent D) Dipol – Dipol Etkileşimi E) İyon Bağları 26

MÜKEMMEL DOĞRU CEVAP Diğer Soruya Geç 27

Üzgünüm Yanlış Cevap Soruya Geri Dön 28

SUNUM BİTTİ DİNLEDİĞİNİZ İÇİN TEŞEKKÜR EDERİM. . Hazırlayan: Feride BAHÇECİ 29
- Slides: 29