Molculas na Troposfera J sabemos que A Troposfera
Moléculas na Troposfera

Já sabemos que: A Troposfera, é a camada: üMais próxima do solo; üMais fina; üMais activa, no que diz respeito a acontecimentos visíveis (chuva, relâmpagos, furacões); üQue contém cerca de 80 % da massa total de ar e praticamente todo o vapor de água;

Constituição da Troposfera Espécies maioritárias Espécies vestigiais Azoto (N 2) Hidrogénio (H 2) Oxigénio (O 2) Metano (CH 4) Água (H 2 O) Amoníaco (NH 3) Dióxido de carbono (CO 2)

A ligação entre dois átomos de hidrogénio, forma uma molécula de hidrogénio. Ligação química (ligação covalente) A ligação covalente forma-se pela partilha de electrões de ambos os átomos nela envolvidos.

Modelo da ligação covalente A ligação covalente pode ser: Simples (ordem um) – partilha de dois electrões (um par); Dupla (ordem dois) – partilha de quatro electrões (dois pares); Tripla (ordem três) – partilha de seis electrões (três pares);

Notação de Lewis Uma estrutura de Lewis é constituída pelo símbolo de um elemento rodeado por um ponto por cada electrão de valência presente no átomo desse elemento. ou
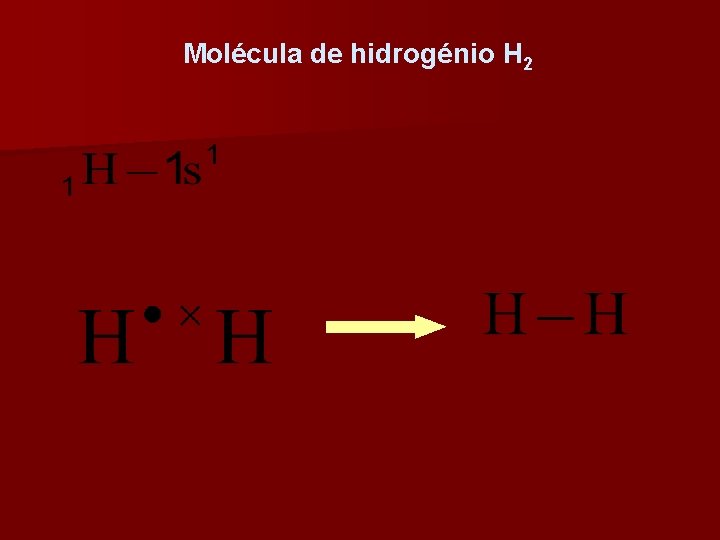
Molécula de hidrogénio H 2
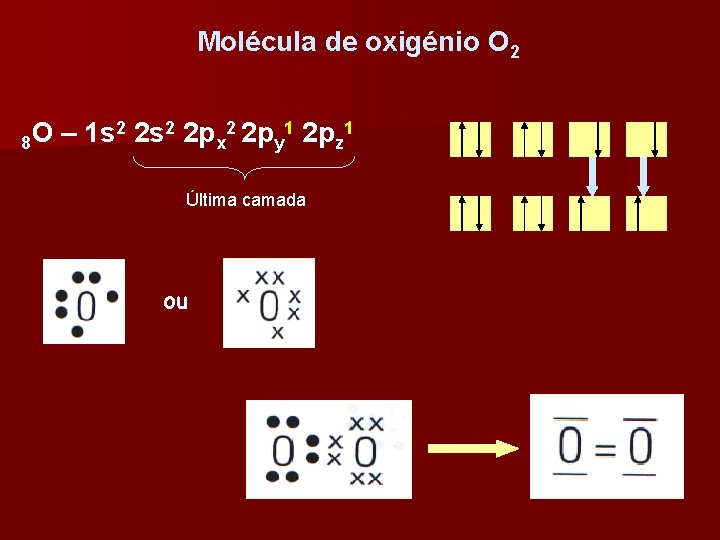
Molécula de oxigénio O 2 2 2 s 2 2 p 1 O – 1 s 8 x y z Última camada ou
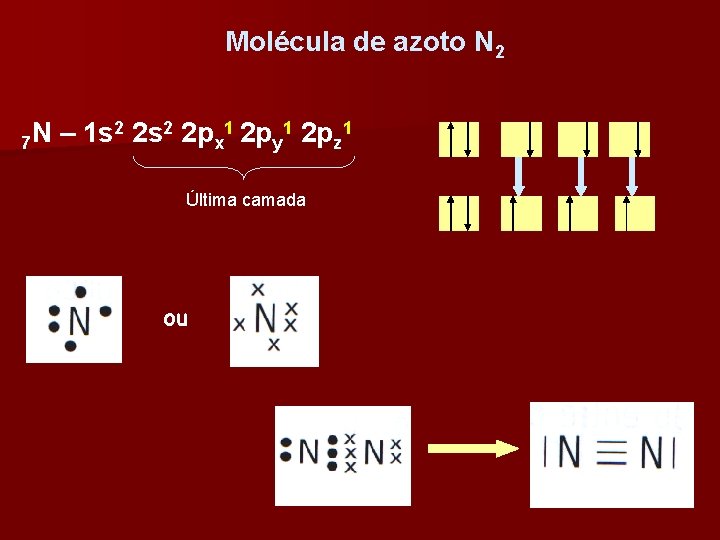
Molécula de azoto N 2 2 2 s 2 2 p 1 N – 1 s 7 x y z Última camada ou

Electrões ligantes e electrões não ligantes Numa ligação química os electrões do nível de valência podem ser: Ligantes - electrões que estabelecem a ligação, são partilhados pelos dois átomos. Não ligantes – electrões que não contribuem para a ligação.

Regra do Octeto Qualquer átomo, excepto o hidrogénio, tem tendência para formar ligações de forma a ficar rodeado por oito electrões de valência.

Gases Nobres Estes gases apresentam as orbitais do último nível completamente preenchidas. 2 2 s 2 2 p 6 Ne – 1 s 10
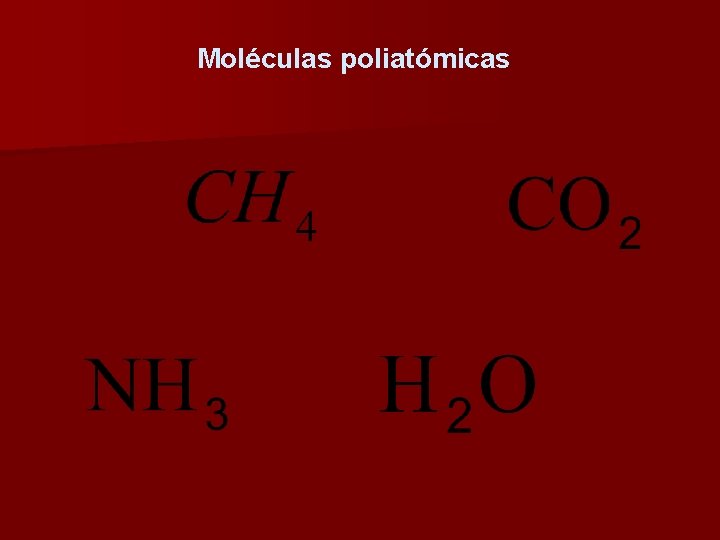
Moléculas poliatómicas
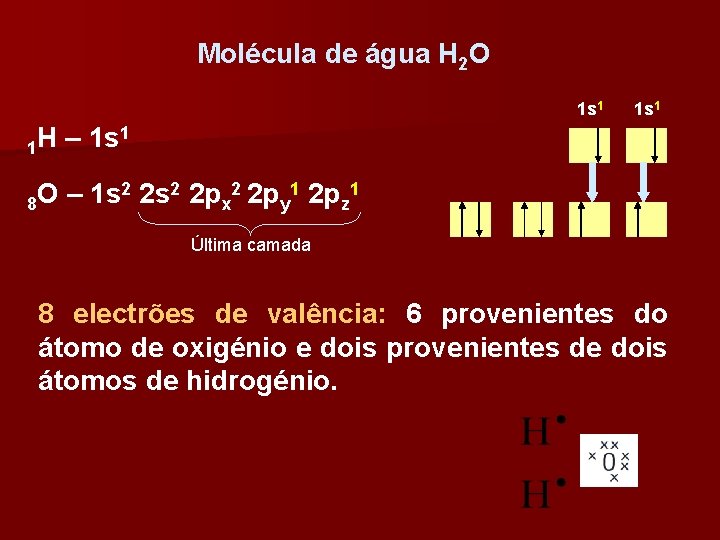
Molécula de água H 2 O 1 s 1 1 H – 1 s 1 2 2 s 2 2 p 1 O – 1 s 8 x y z Última camada 8 electrões de valência: 6 provenientes do átomo de oxigénio e dois provenientes de dois átomos de hidrogénio.
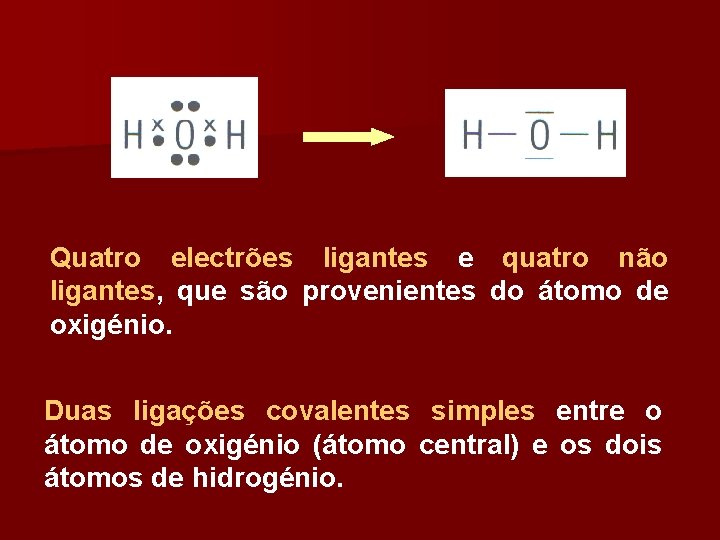
Quatro electrões ligantes e quatro não ligantes, que são provenientes do átomo de oxigénio. Duas ligações covalentes simples entre o átomo de oxigénio (átomo central) e os dois átomos de hidrogénio.
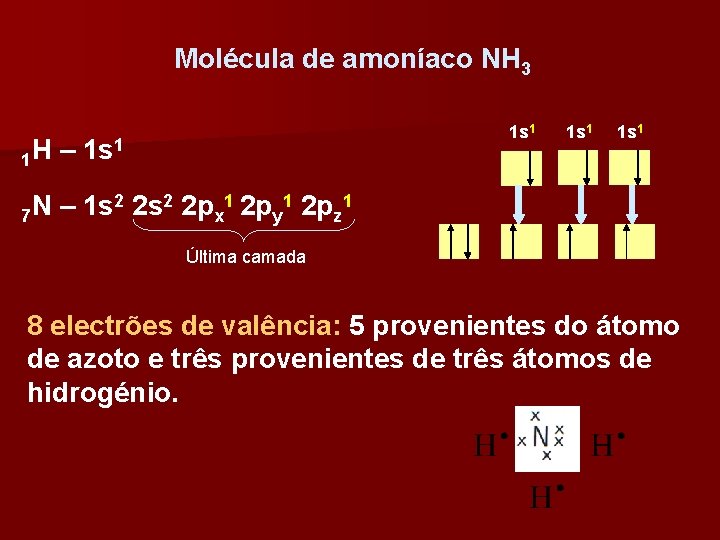
Molécula de amoníaco NH 3 1 s 1 1 H – 1 s 1 2 2 s 2 2 p 1 N – 1 s 7 x y z Última camada 8 electrões de valência: 5 provenientes do átomo de azoto e três provenientes de três átomos de hidrogénio.
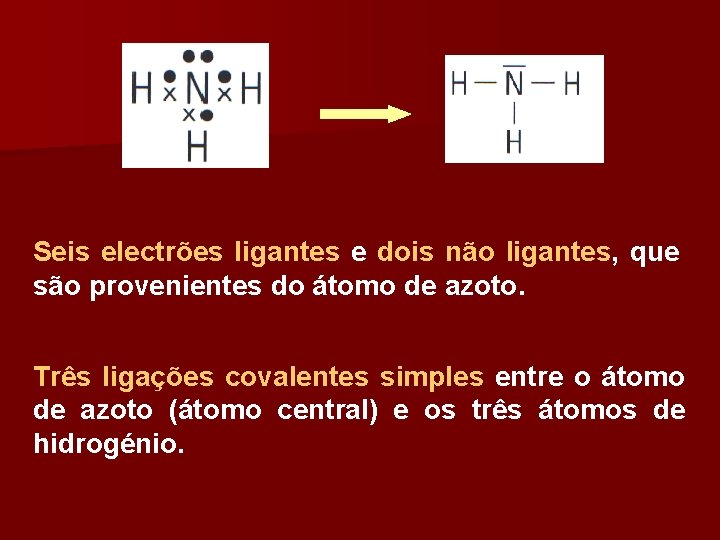
Seis electrões ligantes e dois não ligantes, que são provenientes do átomo de azoto. Três ligações covalentes simples entre o átomo de azoto (átomo central) e os três átomos de hidrogénio.
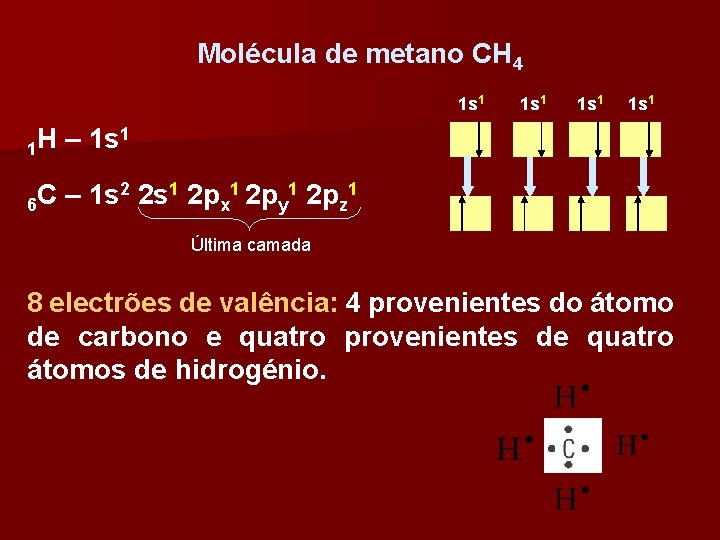
Molécula de metano CH 4 1 s 1 1 H – 1 s 1 2 2 s 1 2 p 1 C – 1 s 6 x y z Última camada 8 electrões de valência: 4 provenientes do átomo de carbono e quatro provenientes de quatro átomos de hidrogénio.
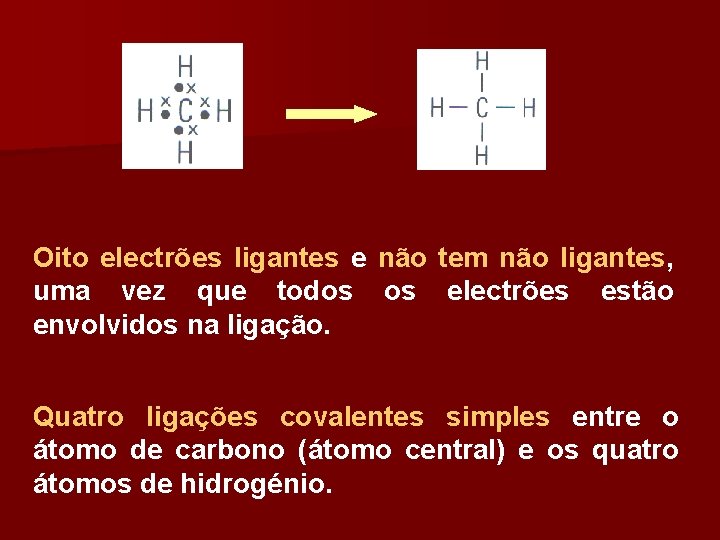
Oito electrões ligantes e não tem não ligantes, uma vez que todos os electrões estão envolvidos na ligação. Quatro ligações covalentes simples entre o átomo de carbono (átomo central) e os quatro átomos de hidrogénio.
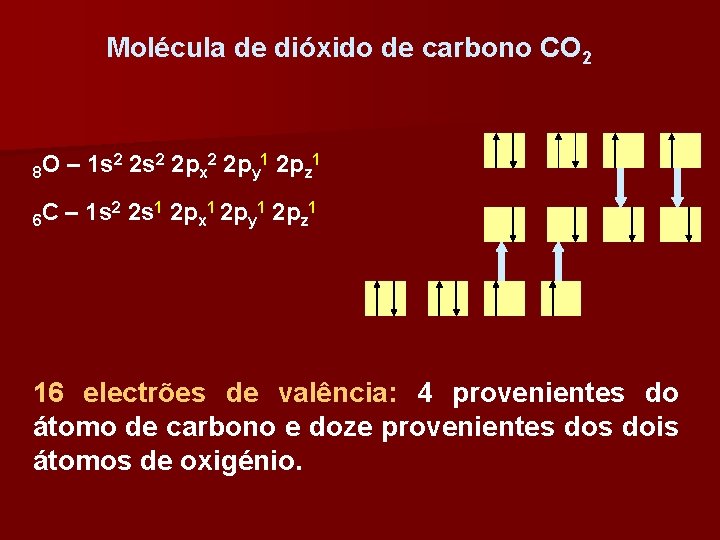
Molécula de dióxido de carbono CO 2 8 O – 1 s 2 2 px 2 2 py 1 2 pz 1 6 C – 1 s 2 2 s 1 2 px 1 2 py 1 2 pz 1 16 electrões de valência: 4 provenientes do átomo de carbono e doze provenientes dois átomos de oxigénio.
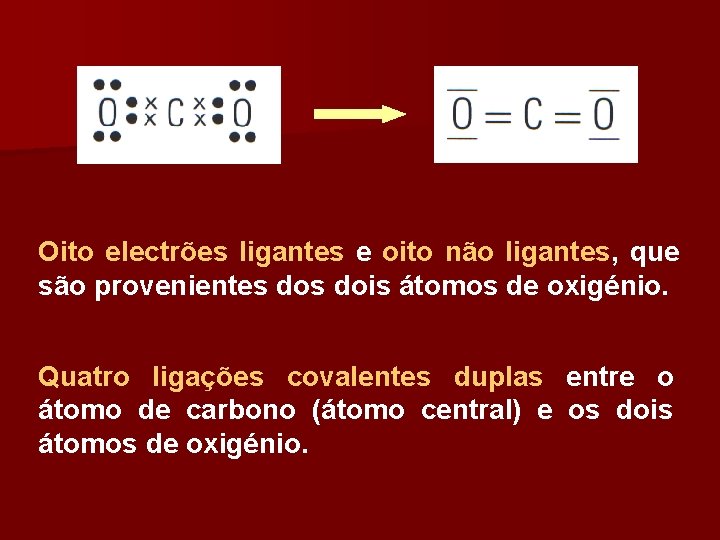
Oito electrões ligantes e oito não ligantes, que são provenientes dois átomos de oxigénio. Quatro ligações covalentes duplas entre o átomo de carbono (átomo central) e os dois átomos de oxigénio.
- Slides: 21