MODUL GINJAL DAN CAIRAN TUBUH PENGATURAN KESEIMBANGAN ASAMBASA
MODUL GINJAL DAN CAIRAN TUBUH PENGATURAN KESEIMBANGAN ASAM-BASA

Pokok Bahasan n n Pengaturan homeostasis Imbangan Asam Basa oleh tubuh Kelainan Imbangan Asam Basa: asidosis and alkalosis
![p. H n n n p. H = - log [H+] H+ adalah suatu p. H n n n p. H = - log [H+] H+ adalah suatu](http://slidetodoc.com/presentation_image_h2/4166b816844d2420a5366546febddd65/image-3.jpg)
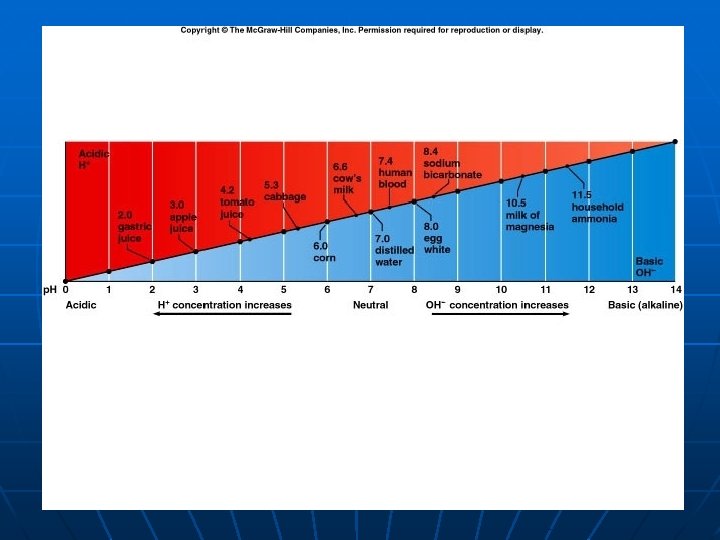
p. H n n n p. H = - log [H+] H+ adalah suatu proton Rentang: 0 - 14 Bila[H+] tinggi, larutan bersifat asam, p. H < 7 Bila [H+] rendah, larutan bersifat basa atau alkalis ; p. H > 7


n n n Asam adalah donor H+. Basa adalah akseptor H+, atau memberikan OH- pd larutan. Asam dan Basa disebut: • Kuat – bila terdisosiasi secara sempurna dalam larutan, contoh: n HCl, Na. OH • Lemah – hanya sebagian terdisosiasi dalam larutan, contoh: n Asam laktat, asam karbonat

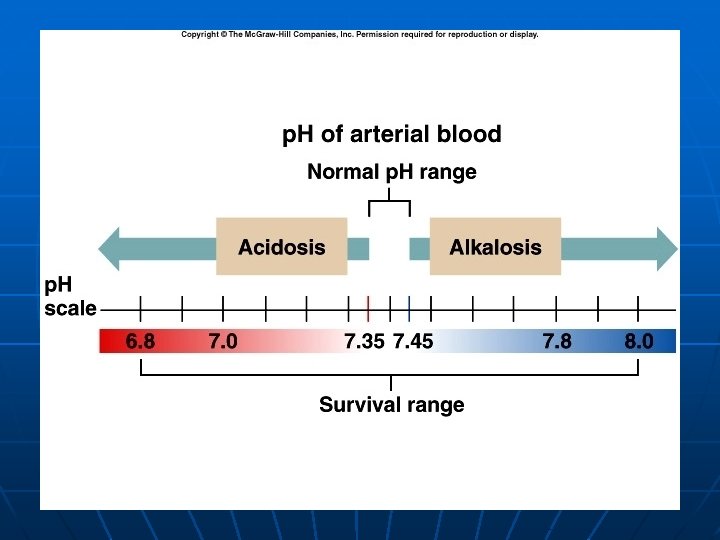
TUBUH dan p. H n n n Homeostasis p. H dikontrol secara ketat p. H cairan ekstraseluler = 7. 4 p. H darah= 7. 35 – 7. 45 < 6. 8 atau > 8. 0 menyebabkan kematian Asidosis (acidemia) < 7. 35 Alkalosis (alkalemia) > 7. 45
![IMBANGAN ASAM BASA Keadaan [H+] yg diserap selalu setara dg [H+] yg dilepaskan dlm IMBANGAN ASAM BASA Keadaan [H+] yg diserap selalu setara dg [H+] yg dilepaskan dlm](http://slidetodoc.com/presentation_image_h2/4166b816844d2420a5366546febddd65/image-9.jpg)
IMBANGAN ASAM BASA Keadaan [H+] yg diserap selalu setara dg [H+] yg dilepaskan dlm keadaan ini p. H cairan tubuh berada dlm rentang normal p. H darah 7, 35 – 7, 45 hrs dipertahankan dlm rentang normal, karena § Hasil metabolisme menyebabkan terbentuknya ASAM dan BASA (terutama asam) § Sebagian besar enzim sangat peka terhadap perubahan p. H

Tubuh menghasilkan lebih banyak asam dibanding basa n n n Asam didapat dalam makanan Metabolisme protein menghasilkan: sulfat & fosfat Metabolisme asam lemak menghasilkan benda keton Glikolilisis an aerob menghasilkan: laktat Glikolisis aerob menghasilkan CO 2 Metabolisme seluler menghasilkan CO 2

ASAM YG DIHASILKAN OLEH TUBUH Asam karbonat Asam sulfat Asam fosfat Asam laktat Asam sitrat Ion amonium Benda keton : - Asam asetoasetat - -hidroksi butirat - Aseton

ASAM YG DIHASILKAN TUBUH DIKELOMPOKKAN SBB: A. ASAM VOLATIL n n Asam yg dpt menguap : H 2 CO 3 Hampir semua CO 2 diubah mjd as. karbonat PCO 2 berhubungan terbalik dg p. H sehingga PCO 2 merupakan faktor penting dlm mempengaruhi p. H.

B. n ASAM FIXED asam yg tdk terpisahkan dg larutan : H 2 SO 4 H 2 PO 4 C. ASAM ORGANIK n asam hasil metabolisme anaerob : ASAM LAKTAT

SISTEM PENGATURAN IMBANGAN ASAM-BASA Imbangan asam-basa dipertahankan dg cara melakukan pengaturan imbangan ion hidrogen (H+) Dikoordinasi 3 sistem: PARU, GINJAL & BUFER

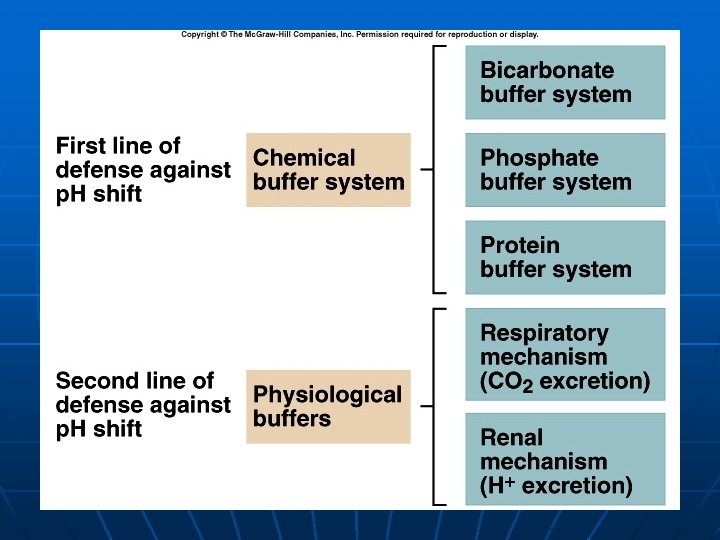
A. PENGATURAN JANGKA PANJANG: PROSES ELIMINASI BUKAN NEUTRALISASI, oleh 1. PARU 2. GINJAL mengatur imbangan asam-basa dg cara mengatur sekresi dan reabsorpsi H+ dan HCO 3 B. PENGATURAN JANGKA PENDEK diatur oleh sistem BUFER

Laju Perbaikan/Koreksi n n n Bufer beraksi hampir seketika (instan) beberapa detik Mekanisme respirasi (paru) perlu waktu beberapa menit sampai jam Mekanisme renal perlu waktu beberapa jam sampai hari

1. PARU Mekanisme paru dlm homeostasis p. H darah yi: mengatur Respiratory Rate A. Pd keadaan ASIDOSIS METABOLIK (p. H drh ) H 2 CO 3 dlm drh dpt dikurangi dg cara meningkatkan RR shg akan lbh banyak CO 2 yg keluar mll paru. Sebaliknya : B. Pd keadaan ALKALOSIS METABOLIK (p. H drh ) menurunkan RR , shg CO 2 ditahan dlm paru dg akibat p. H drh menurun.
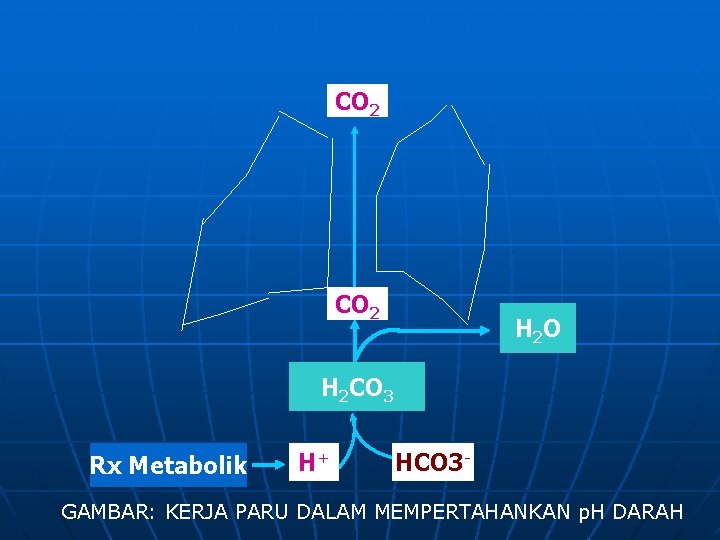
CO 2 H 2 O H 2 CO 3 Rx Metabolik H+ HCO 3 - GAMBAR: KERJA PARU DALAM MEMPERTAHANKAN p. H DARAH
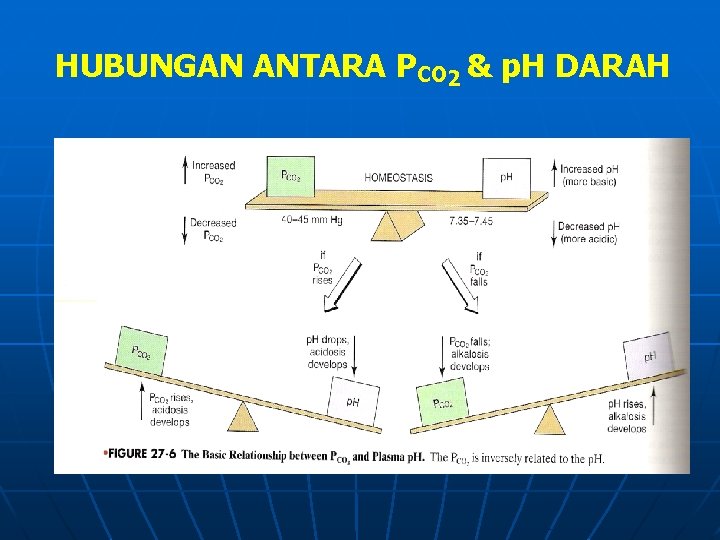
HUBUNGAN ANTARA PCO 2 & p. H DARAH

2. GINJAL q q q Regulator p. H yg efektif Bila ginjal gagal, homeostasis p. H gagal Mengatur sekresi, ekskresi dan reabsorpsi H+ Mengatur sekresi dan reabsorpsi HCO 3 Mekanisme pengaturan oleh ginjal dg cara: a. Produksi amonia b. Produksi bufer as. karbonat/bikarbonat c. Bufer fosfat (b & c dibahas pada sistim bufer)

a. AMONIA q q GINJAL: berfungsi sbg sumber utama amonia urin Amonia (NH 3) merupakan hasil deaminasi as. amino GLUTAMIN (H 5 N 2 O 3) C 5 H 10 N 2 O 3 Rx dikatalisis oleh: ENZ. GLUTAMINASE H+ hasil metabolisme berikatan dg amonia membentuk ion amonium NH 4+ dan diekskresikan bersama urin

MEKANISME GINJAL MENGEKSKRESIKAN PROTON (H+) H+ AMONIA berikatan dg H+ setelah berada di lumen tubulus distal, ttp dpt juga saat masih berada di dlm sel tubulus distal NH 3 ( AMONIA) NH 4+ (ION AMONIUM) URIN
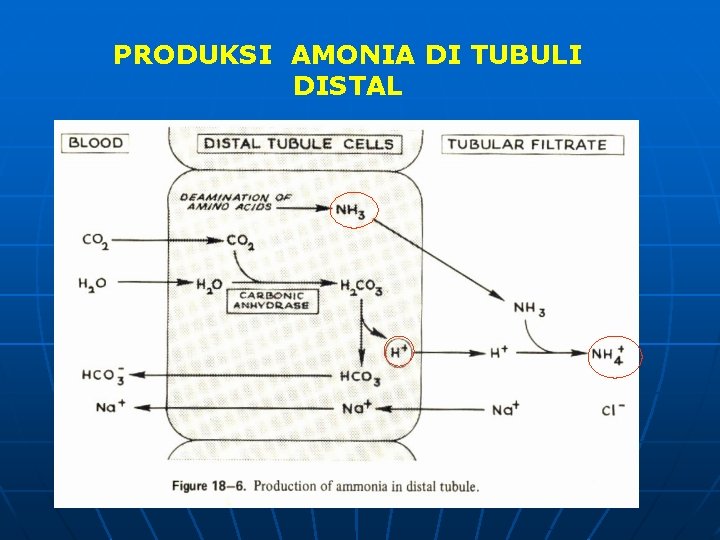
PRODUKSI AMONIA DI TUBULI DISTAL

MEKANISME GINJAL UTK MEMPERTAHANKAN KONSENTRASI BUFER HCO 3 Dengan dua cara, yi: A. HCO 3 - yg difiltrasi semuanya direabsorpsi di tubulus proksimalis. B. HCO 3 - dibtk lagi dlm tubulus distalis, utk menggantikan HCO 3 - yg dipakai oleh asam yg tdk menguap (HCL, H 3 PO 4, H 2 SO 4 dan as. organik) dlm drh hasil proses metabolisme.
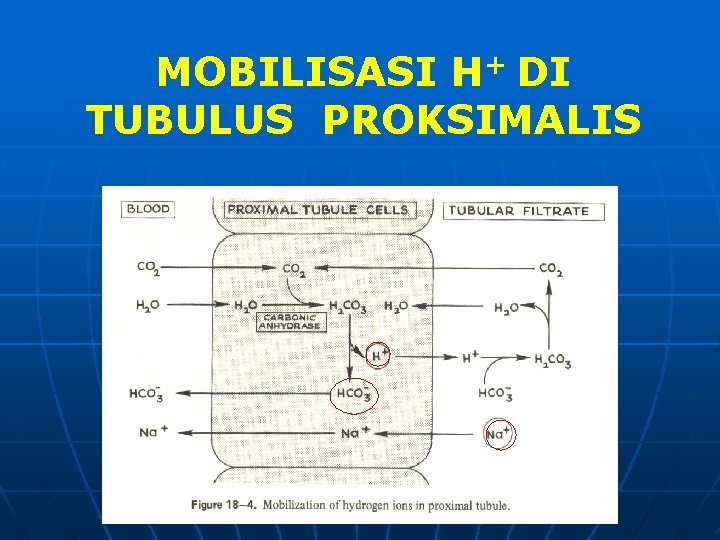
MOBILISASI H+ DI TUBULUS PROKSIMALIS
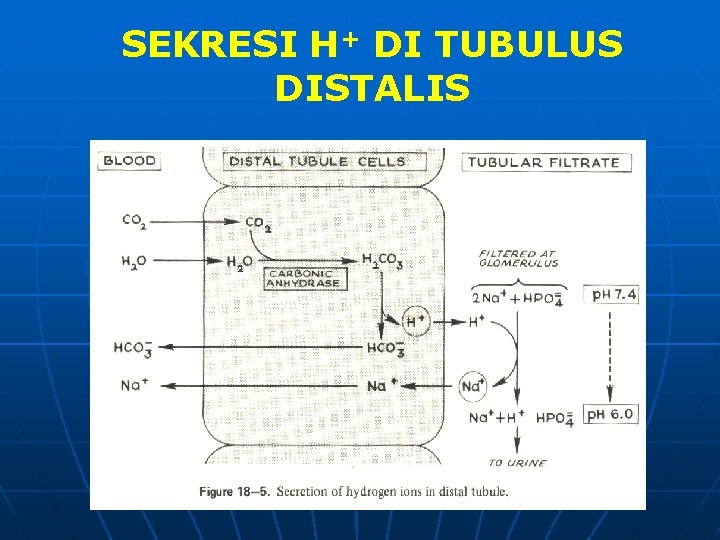
SEKRESI H+ DI TUBULUS DISTALIS

n Tjd proses yg sama dg tub proksimal. H+ dibtk dr CO 2 + H 2 O dan disekresi ke dlm lumen tubulus DITUKAR dg ion Na (Na+) n Proses pertukaran berlgs sp p. H 4, 5. Bila kead. ini tjd mk sekresi H+ TERHENTI ok selisih H+ filtrat dan sel tubulus terlalu tinggi. n Utk mencegah tercapainya p. H yg RENDAH & menjamin tersedianya HCO 3 - ada 2 mekanisme, yi:

a. Kerja BUFER FOSFAT (HPO 4 2 -) Semua HCO 3 - diserap kembali dan H+ yg disekresi + HPO 4 2 - H 2 PO 4 - dg akibat keasaman urin dan p. H urin b. Sekresi amonia oleh GINJAL. n Dlm kead normal, setiap hr : * 30 -50 m. Eq H+ dibuang/diekskresi dg cara bergabung dg amonia * 10 -30 m. Eq H+ sbg asam dititrasi oleh bufer fosfat

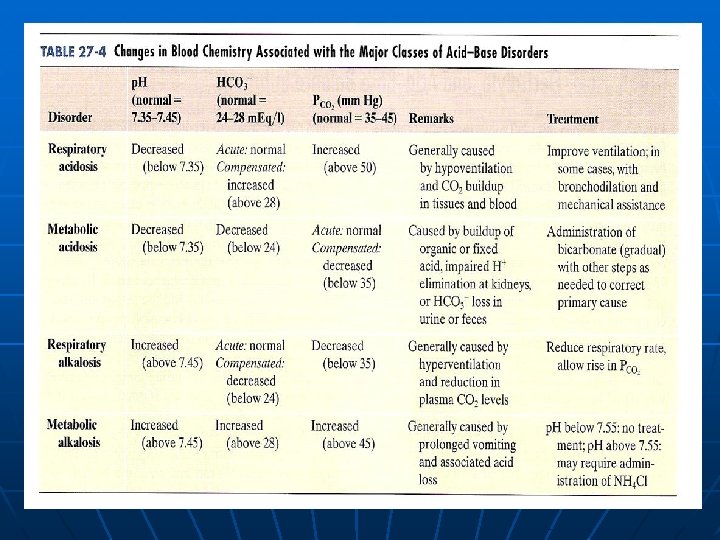
Ketidak Imbangan Asam Basa n n n p. H< 7. 35 asidosis p. H > 7. 45 alkalosis Respon tubuh untuk menanggulangi ketidak seimbangan asam basa disebut: KOMPENSASI Kompensasi Sempurna, bila p. H kembali ke rentang normal Kompensasi Partial, bila p. H diluar rentang normal

Kompensasi n n Bila penyebab metabolik, hiperventilasi at. hipoventilasi dapat membantu, disebut : Kompensasi Respiratorik Bila penyebab ok respiratorik, dapat diatasi oleh mekanisme renal: Kompensasi metabolik
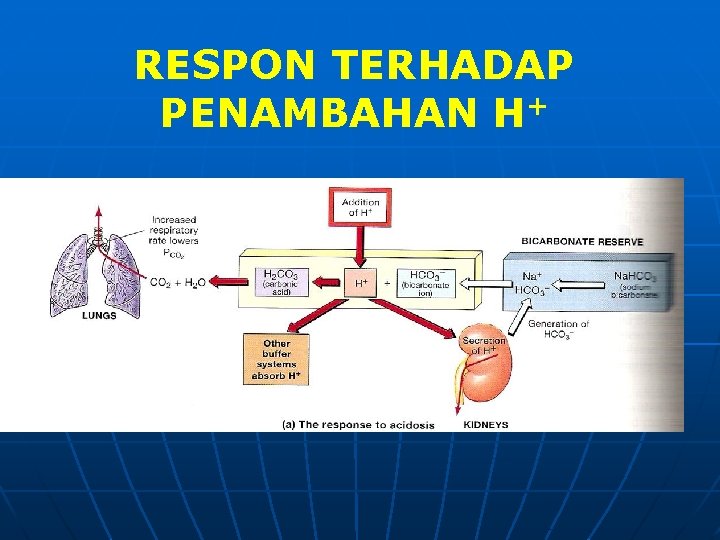
RESPON TERHADAP PENAMBAHAN H+
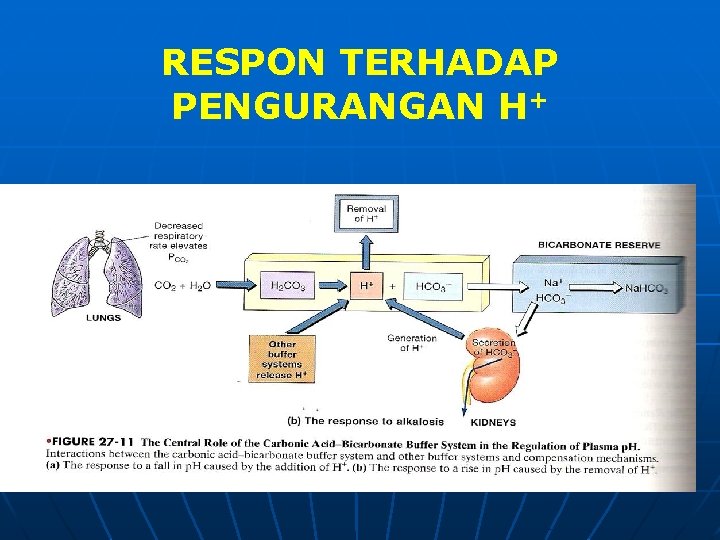
RESPON TERHADAP PENGURANGAN H+

KELAINAN – KELAINAN PENGATURAN ASAM – BASA OLEH GINJAL PERSAMAAN HENDERSON-HASSELBALCH DIPAKAI PD RATIO PASANGAN BUFER HCO 3 -/H 2 CO 3 , SBB: p. H = 6, 10 + log [HCO 3 -] 0, 0301 PCO 2 Perub PENYEBUT PCO 2 at adl KHAS pd kead ASIDOSIS/ ALKALOSIS “RESPIRATORIK” Perub PEMBILANG HCO 3 - at adl KHAS pd kead ASIDOSIS/ALKALOSIS “METABOLIK”

EFEK CO 2 TERHADAP p. H DARAH As karbonat dibentuk hsl kerja enzim karbonat anhidrase, yg akan berdisosiasi sbb: H 2 CO 3 H+ + HCO 3 - + B BHCO 3 - + H+ p. H darah 7, 4 ratio [HCO 3 -] / H 2 CO 3 = 20 : 1 Dari rumus : “HENDERSON HASELBALCH” Bila p. H darah 7, 4; p. Ka as. karbonat = 6, 1 maka : 7, 4 = 6, 10 + log garam (bikarbonat)/asam 1, 30 = log [HCO 3 -] / H 2 CO 3 antilog 1, 30 = 20

Ratio dipertahankan shg p. H darah tdk berubah dr : 7, 4 Perubahan ratio menyebabkan gangguan keseimbangan asam basa terjadi ASIDOSIS atau ALKALOSIS Perubahan ventilasi paru mempunyai pengaruh besar terhadap p. H darah

n Bila, PCO 2 krn prod di jar. perifer atau hipoventilasi [H 2 CO 3] ratio < 1, 30 ASIDOSIS RESPIRATORIK Sebaliknya n Bila PCO 2 menurun krn hiperventilasi [H 2 CO 3] menurun ratio > 1, 30 ALKALOSIS RESPIRATORIK

GANGGUAN METABOLIK 1. Plg umum ok produksi as. fixed & as. organik , contoh: a. ASIDOSIS LAKTAT, tbl ok hipoksia jaringan berkepanjangan metab. anaerob di jaringan b. KETOASIDOSIS, produksi benda keton akibat starvasi & diabetes melitus yg tak terkendali jaringan tdk dpt memanfaatkan glukosa dr sirkulasi shg mengandalkan metab. lipid & keton.

2. Relatif jarang, contoh: Jaringan tdk mampu ekskresi H+ melalui ginjal, contoh: glomerulonefritis. 3. Setelah kehilangan bikarbonat, contoh: DIARE KRONIK. Pd kead normal HCO 3 disekresi ke saluran cerna & direabsorpsi sblm defekasi diare menyebabkan HCO 3 - tdk direabsorpsi konsentrasi di dlm cairan ekstraseluler me .

PENYEBAB ASIDOSIS METABOLIK A. ANION YG TDK TERUKUR 1. Ketoasidosis diabetes 2. Payah ginjal azotemia 3. Asidosis laktat 4. Keracunan : SALISILAT, METIL ALKOHOL, PARALDEHID, ETILEN GLIKOL.

B. ANION YG TDK TERUKUR NORMAL (ASIDOSIS METABOLIK HIPERKLOREMIK) 1. Diare dan fistula yg bersekresi 2. Pemberian amonium klorida 3. Tubulus ginjal asidosis (proksimal & distal) 4. Uterosigmoidoskopi 5. Inhibitor karbonat anhidrase 6. Asidosis “expansion”

ANION GAP n n n konsep anion gap penting dlm diagnosis gangguan keseimbangan asam - basa Secara rutin lab klinik mengukur konsentrasi: Na+, K+, Cl- dan HCO 3 - plasma Normal : jumlah konsentrasi Na+ & K+ > jumlah konsentrasi Cl- & HCO 3 – A = { [Na+] + [K+ ] } - { [Cl-] + [HCO 3 - ] } Normal A= 12 - 16 m. Eq/L, bl [K+ ] tdk diukur nilai menjadi 8 - 12 m. Eq/L
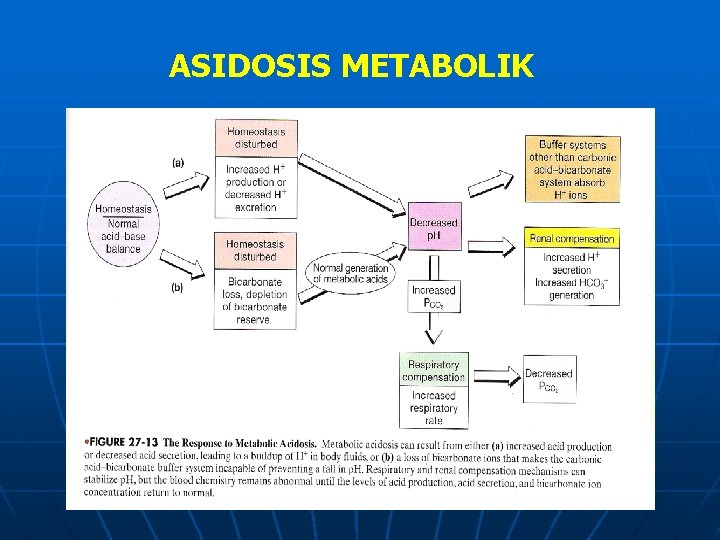
ASIDOSIS METABOLIK

PENYEBAB ALKALOSIS METABOLIK 1. Kehilangan asam (muntah-muntah, drainase lambung) 2. Pengobatan diuretika 3. Alkalosis posthiperkapnia 4. Sindroma kelebihan mineralo kortikoid: aldosteronism, sindr. Cushing, sindr. Bartter, tumor yg mengekskresi ACTH, keracunan licorice 5. Pemberian alkali yg berlbhan 6. Kekurangan kalium yg brt 7. Alkalosis kontraksi
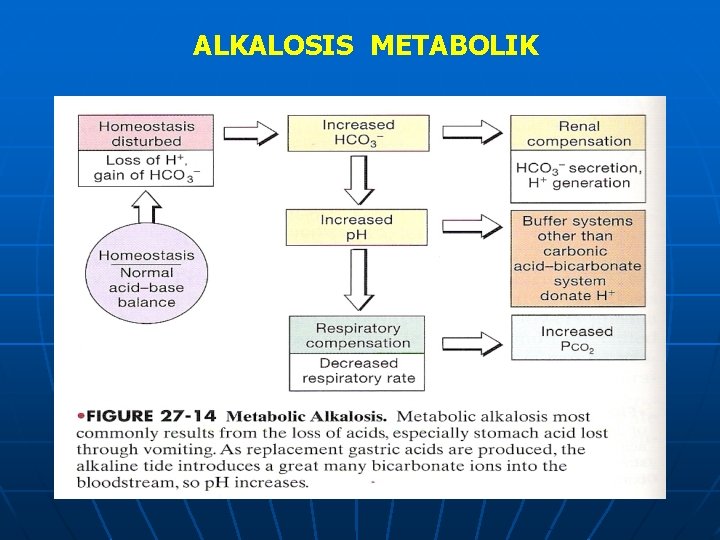
ALKALOSIS METABOLIK

GANGGUAN RESPIRATORIK ASIDOSIS RESPIRATORIK • Apabila terjadi gangguan ventilasi alveolar yang menyebabkan gangguan eliminasi CO 2, shg terjadi akumulasi CO 2 di alveoli mengakibatkan terjadinya peningkatan PCO 2 • Sistem bufer pada mulanya dapat mengatasi, namun pada akhirnya terjadi penurunan p. H. ALKALOSIS RESPIRATORIK Apabila terjadi hiperventilasi alveolar sehingga terjadi penurunan PCO 2 dan mengakibatkan peningkatan p. H.
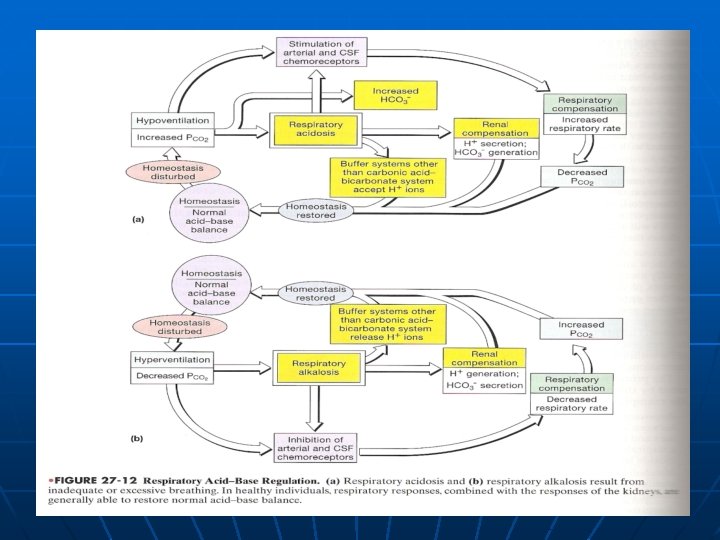

ETIOLOGI ASIDOSIS RESPIRATORIK 1. Inhibisi pusat pernapasan: n Obat Henti jantung n Central Sleep Apnea n Kelebihan O 2 pada hiperkapnia kronik 2. Penyakit neuromuskuler n Neurologis: poliomielitis, sindroma Guillain Barre n Muskuler: hipokalemia, muskuler distrophy

3. Obstruksi jalan nafas: n Asma bronkial n Penyakit Paru Obstruktif Kronik (PPOK) n Spasme laring n Aspirasi n Obstructive sleep apnea 4. Kelainan Restriktif: n Penyakit pleura: efusi pleura, empiema, pneumothoraks, fibrothoraks n Kelainan dinding dada: kifoskoliosis, obesitas n Kelainan restriktif paru: fibrosis pulmoner, pneumonia, edema paru 5. Mechanical underventilation 6. Overfeeding

ETIOLOGI ALKALOSIS RESPIRATORIK 1. Rangsangan hipoksemik - peny paru dg kelainan A-a gradien - peny jantung dg right to left shunt - peny jantung dg edema paru - anemi gravis 3. Stimulasi pusat pernapasan di medula - kelainan neorologis - psikogenik mis. panik, nyeri - gagal hati dg ensefalopati - kehamilan 4. Sepsis 5. Pengaruh obat: salisilat, hormon progesteron 6. Mechanical overventilation

- Slides: 52