Modul 2 Kimia Fisika IV REAKSI KOMPLEKS DAN




















- Slides: 22

Modul 2 Kimia Fisika IV REAKSI KOMPLEKS DAN MEKANISME REAKSI Dr. M. Masykuri, M. Si. Chemical Education Study Program Teacher Training and Educational Studies Sebelas Maret University (UNS) Website: http: //masykuri. staf. fkip. uns. ac. id, email: mmasykuri@yahoo. com Teacher Training and Educational Studies 10/19/2010 Sebelas Maret University 1 M. Masykuri_Physical Chemistry IV Sep, 2010 Solo, Sep 2010

Definisi Reaksi Sederhana: • Persamaan stokiometrinya menggambarkan apa yang sebenarnya berlangsung • Berlangsung 1 tahap (reaksi elementer) • Misal: H 2 + Br = HBr + H satu molekul H 2 bertumbukan dengan satu atom Br, dan terjadi pertukaran “partner” dengan pembentukan HBr dan H, maka reaksi tersebut adalah reaksi sederhana • Persamaan lajunya diberikan oleh Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Definisi Reaksi Kompleks (Rumit): • Tersusun atas beberapa reaksi sederhana. • Pada umumnya persamaan laju reaksi rumit tidak dapat diturunkan dari persamaan stoikiometrinya • Misal: CO + Cl 2 = COCl 2 ? Bagaimana persamaan lajunya? Tahapan reaksi? Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Definisi Reaksi Kompleks (Rumit): • Contoh Reaksi: CO + Cl 2 = COCl 2 • Persamaan lajunya diberikan oleh • Mekanisme yang melibatkan beberapa kesetimbangan seperti berikut : (i) Cl 2 == 2 Cl 2 (ii) Cl + CO == COCl (iii) COCl + Cl 2 COCl 2 + Cl Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Komponen Reaksi Kompleks Tiga macam komponen penyusun reaksi kompleks: 1. Reaksi Paralel 2. Reaksi Seri/Berurutan 3. Reaksi Berlawanan Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Reaksi Paralel • Suatu susunan reaksi disebut sebagai parallel bila satu pereaksi secara bersamaan dapat mengalami dua atau lebih reaksi yang berbeda, dengan produk yang berbeda pula. A→B A→C Or: A→B C Bagaimana penurunan persamaan lajunya? Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Reaksi Paralel Contoh Reaksi Paralel: A+B P 1 + … A+C P 2 + … • Persamaan lajunya diberikan oleh: Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Reaksi Seri/Berurutan • Suatu susunan reaksi disebut sebagai berurutan bila salah satu produk dari reaksi pertama mengalami reaksi lebih lanjut pada reaksi kedua. A→B→C • Sebagai contoh adalah dua reaksi pertama pada mekanisme dissosiasi etana, dengan kehadiran oksida nitrogen : C 2 H 6 + NO → C 2 H 5 → + HNO Teacher Training and Educational Studies Sebelas Maret University H + C 2 H 4 M. Masykuri_Physical Chemistry IV Sep, 2010

Reaksi Seri/Berurutan Contoh Reaksi Seri C 2 H 6 + NO C 2 H 5 + HNO C 2 H 5 H + C 2 H 4 • C 2 H 5 disebut zat antara, karena tidak terdapat dalam produk reaksi maupun dalam pereaksi. • Laju pembentukan C 2 H 5 diberikan oleh Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Reaksi Berlawanan • Suatu susunan reaksi disebut berlawanan bila produk reaksinya dapat bereaksi kembali menghasilkan reaksi awal. A→B B→A • Sebagai contoh adalah satu bagian dari mekanisma pembentukan HBr dari hidrogen dan brom Br + H 2 k 1 → HBr + H H + HBr k 2 → H 2 + Br Teacher Training and Educational Studies Sebelas Maret University q Ini bukan suatu reaksi kesetimbangan, karena lajunya tak harus sama pada kedua arah. q Penyusunan persamaan laju berdasar mekanisma M. Masykuri_Physical Chemistry IV Sep, 2010

Pendekatan Steady state • Zat antara/Intermediet (disingkat ZANTARA): Pada awal reaksi, konsentrasi zat antara nol yang kemudian bertambah; pada saat yang sama zat ini mengalami reaksi pula, yang mengurangi konsentrasinya • Pendekatan steady state/keadaan tunak: bila X adalah zat antara Orde reaksi terhadap A = p, diperoleh dari slope = tg Tetapan laju k, diperoleh dari intersep grafik Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Pendekatan Steady state Contoh: Reaksi yang secara stokiometri diberikan oleh A+B=C+D Kemungkinan mekanisma reaksi 1: melibatkan suatu zat antara X, adalah sebagai berikut, k 1 → A+B X k 2 → X+D C Bagaimana penurunan persamaan lajunya? Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Pendekatan Steady state 1 Mekanisma reaksi 1: k 1 → A+B X k 2 → X+D Laju reaksi pada pembentukan produk C, C Ungkapan bagi konsentrasi X diperoleh dari pendekatan steady state bagi X, yaitu: Maka persamaan laju secara keseluruhan menjadi, Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

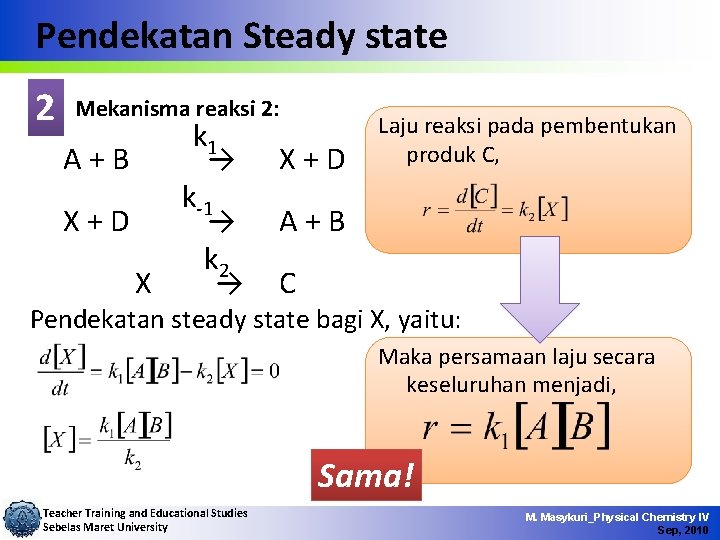
Pendekatan Steady state 2 Mekanisma reaksi 2: k 1 A+B → k-1 X+D → k 2 X → X+D Laju reaksi pada pembentukan produk C, A+B C Pendekatan steady state bagi X, yaitu: Maka persamaan laju secara keseluruhan menjadi, Sama! Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Pendekatan Kesetimbangan Bila pada mekanisma reaksi 2: k 1 A+B → k-1 X+D → k 2 X → X+D A+B Bila kedua tetapan laju dari reaksi berlawanan ini jauh lebih besar dari tetapan laju reaksi terakhir C maka reaksi terakhir tak berpengaruh pada pasangan reaksi berlawanan. Pasangan reaksi ini praktis mengalami suatu kesetimbangan. Sehingga: Disebut: Pendekatan Kesetimbangan Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Contoh-contoh Contoh 1. Reaksi pembentukan fosgen: CO + Cl 2 = COCl 2 • dengan persamaan laju, • Reaksi ini diterangkan melalui suatu mekanisme: Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Contoh-contoh • Dari dua reaksi kesetimbangan diperoleh ungkapan berikut Persamaan laju pembentukan fosgen menjadi, • yang menghasilkan ungkapan, Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Contoh-contoh Contoh 2. Reaksi penguraian nitrogen pentokside: 2 N 2 O 5 = 2 N 2 O 4 + O 2 • dengan persamaan laju, • Mekanismeyang diusulkan oleh Ogg: Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Contoh-contoh • Penerapan pendekatan steady state bagi NO 3 dan NO: • Sedangkan laju reaksi adalah : • Eliminasi konsentrasi NO dan NO 3 menghasilkan, Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Contoh-contoh Contoh 3. Reaksi penguraian OZON: 2 O 3 = 3 O 2 • FAKTA PENGAMATAN: Reaksi berbanding terbalik dengan konsentrasi oksigen dan pada keadaan oksigen berlebihan diamati berorde dua terhadap ozon • Mekanisme Benson dan Axworthy, dimana M adalah molekul sebarang atau permukaan Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Contoh-contoh • Laju reaksi, • Penerapan kaidah steady state bagi konsentrasi O menghasilkan, • Sehingga ungkapan laju reaksi, Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010

Sekian Teacher Training and Educational Studies Sebelas Maret University M. Masykuri_Physical Chemistry IV Sep, 2010