Modle de latome de Bohr The neon atom

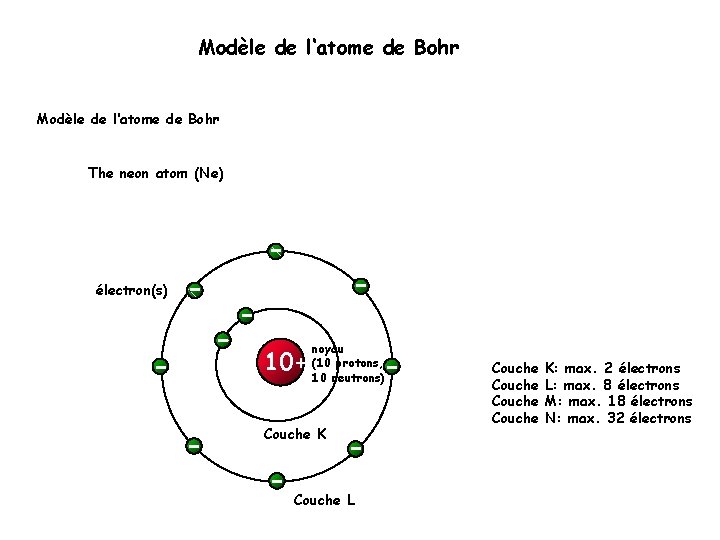
Modèle de l‘atome de Bohr The neon atom (Ne) électron(s) 10+ noyau (10 protons, 10 neutrons) Couche K Couche L Couche K: max. 2 électrons L: max. 8 électrons M: max. 18 électrons N: max. 32 électrons
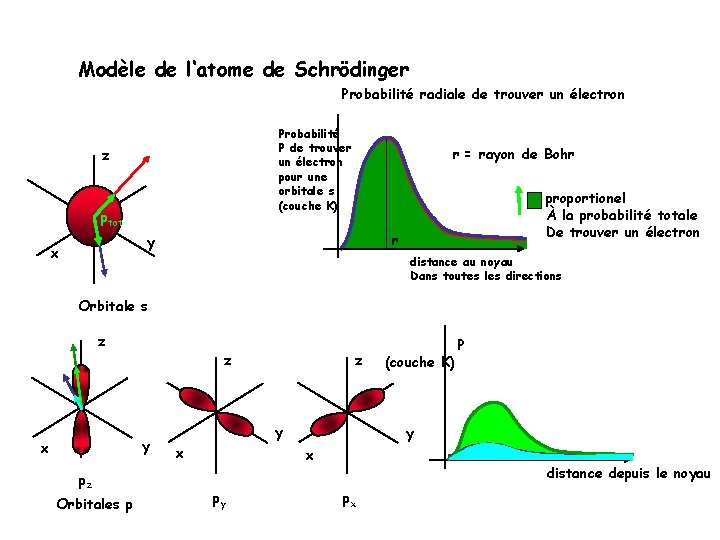
Modèle de l‘atome de Schrödinger Probabilité radiale de trouver un électron Probabilité P de trouver un électron pour une orbitale s (couche K) z ptot r = rayon de Bohr r y x proportionel À la probabilité totale De trouver un électron distance au noyau Dans toutes les directions Orbitale s z z y x pz Orbitales p z y x py (couche K) P distance depuis le noyau px
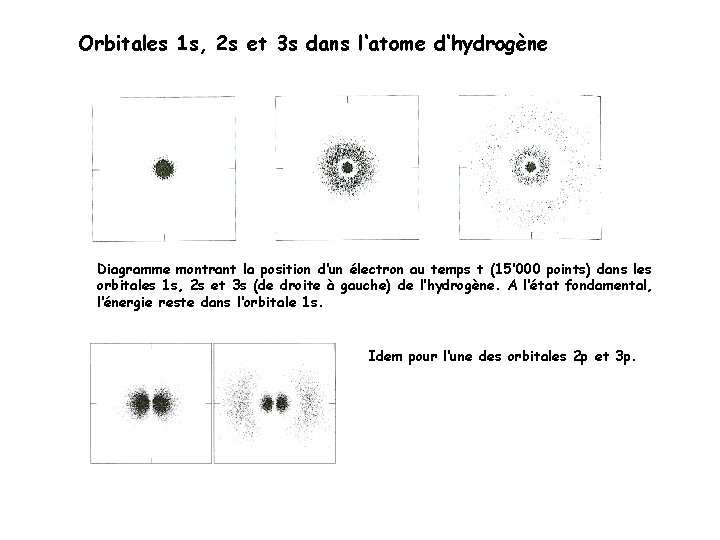
Orbitales 1 s, 2 s et 3 s dans l‘atome d‘hydrogène Diagramme montrant la position d‘un électron au temps t (15‘ 000 points) dans les orbitales 1 s, 2 s et 3 s (de droite à gauche) de l‘hydrogène. A l‘état fondamental, l‘énergie reste dans l‘orbitale 1 s. Idem pour l‘une des orbitales 2 p et 3 p.
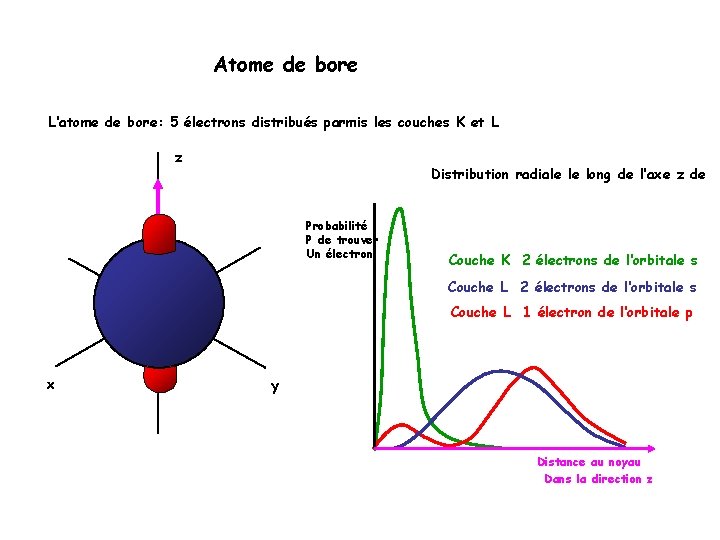
Atome de bore L‘atome de bore: 5 électrons distribués parmis les couches K et L z Distribution radiale le long de l‘axe z de Probabilité P de trouver Un électron Couche K 2 électrons de l‘orbitale s Couche L 1 électron de l‘orbitale p x y Distance au noyau Dans la direction z
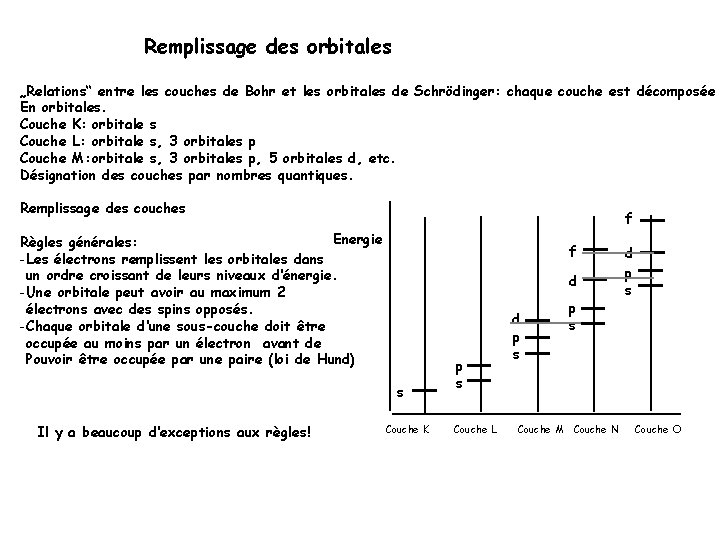
Remplissage des orbitales „Relations“ entre les couches de Bohr et les orbitales de Schrödinger: chaque couche est décomposée En orbitales. Couche K: orbitale s Couche L: orbitale s, 3 orbitales p Couche M: orbitale s, 3 orbitales p, 5 orbitales d, etc. Désignation des couches par nombres quantiques. Remplissage des couches f Energie Règles générales: -Les électrons remplissent les orbitales dans un ordre croissant de leurs niveaux d‘énergie. -Une orbitale peut avoir au maximum 2 électrons avec des spins opposés. -Chaque orbitale d‘une sous-couche doit être occupée au moins par un électron avant de Pouvoir être occupée par une paire (loi de Hund) f d s Il y a beaucoup d‘exceptions aux règles! Couche K p s Couche L d p s Couche M Couche N d p s Couche O
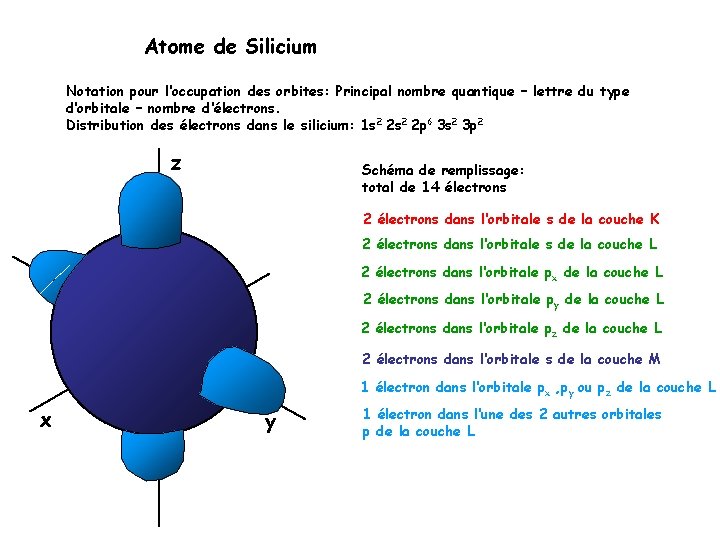
Atome de Silicium Notation pour l‘occupation des orbites: Principal nombre quantique – lettre du type d‘orbitale – nombre d‘électrons. Distribution des électrons dans le silicium: 1 s 2 2 p 6 3 s 2 3 p 2 z Schéma de remplissage: total de 14 électrons 2 électrons dans l‘orbitale s de la couche K 2 électrons dans l‘orbitale s de la couche L 2 électrons dans l‘orbitale px de la couche L 2 électrons dans l‘orbitale py de la couche L 2 électrons dans l‘orbitale pz de la couche L 2 électrons dans l‘orbitale s de la couche M 1 électron dans l‘orbitale px , py ou pz de la couche L x y 1 électron dans l‘une des 2 autres orbitales p de la couche L
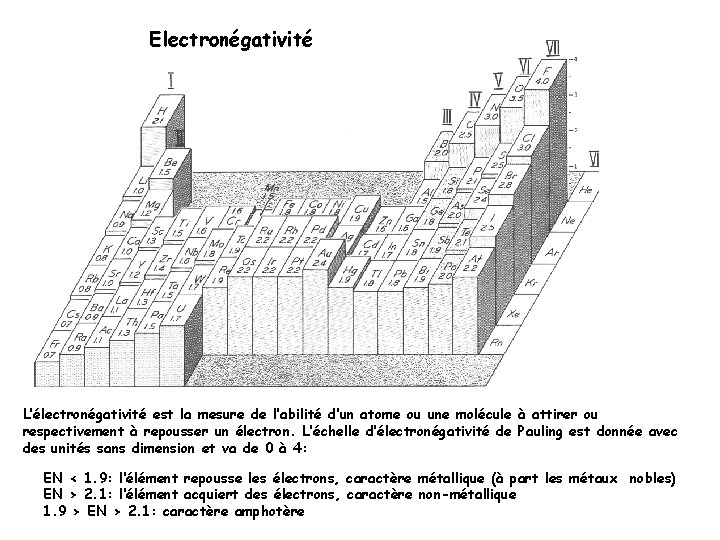
Electronégativité L’électronégativité est la mesure de l’abilité d’un atome ou une molécule à attirer ou respectivement à repousser un électron. L’échelle d’électronégativité de Pauling est donnée avec des unités sans dimension et va de 0 à 4: EN < 1. 9: l‘élément repousse les électrons, caractère métallique (à part les métaux nobles) EN > 2. 1: l‘élément acquiert des électrons, caractère non-métallique 1. 9 > EN > 2. 1: caractère amphotère

Liaisons covalentes I Liaisons covalentes: partage d‘électrons entre atomes = chevauchement d‘orbitales. Seulement entre des atomes avec basse �E (différence d‘électronégativité), la liaison covalente est parfaite seulement quand �E = 0 => entre des atomes semblables. Exemple: Configuration des électrons du fluor: 1 s 22 s 2 p 5 Orbitals 2 p du fluor rouge: occupée par 2 électrons bleu: occupée par 1 électron Orbitales chevauchantes: Chevauchement des 2 orbitales 2 p occupées par un électron seul (=partage des électrons seuls) orbitales moléculaires Orbitales hybrides avec symérie axiale: liaisons �� La directionnalité est la principale différence entre les liaisons covalentes et ioniques. La plupart des liaisons présentent des caractéristiques de plusieurs types. La contribution covalente est donnée par: CC(%)= 100 - (16 E + 3. 5 E 2)

Liaisons covalentes II L‘hybridation (recombination) des orbitales de différents types pour former des orbitales avec de nouvelles formes et orientations. Exemple d‘hybridation d‘orbitales s et p dans le diamant. Configuration électronique du carbone: 2 s 2 p 2 Le chevauchement des orbitales 2 sp 3 donne la structure cristalline du diamant: Orbitale 2 sp 3 hybride Hybridation 2 px 1 2 py 1 2 pz 0 1 s 2 2 s 2 1 s 2 2 sp 1 empty + 2 s 2 = 2 px 1 py 1 pz 0 2 sp 3 La liaison entre 2 atomes de carbones par le chevauchement de 2 orbitales 2 sp 3 hybridées.
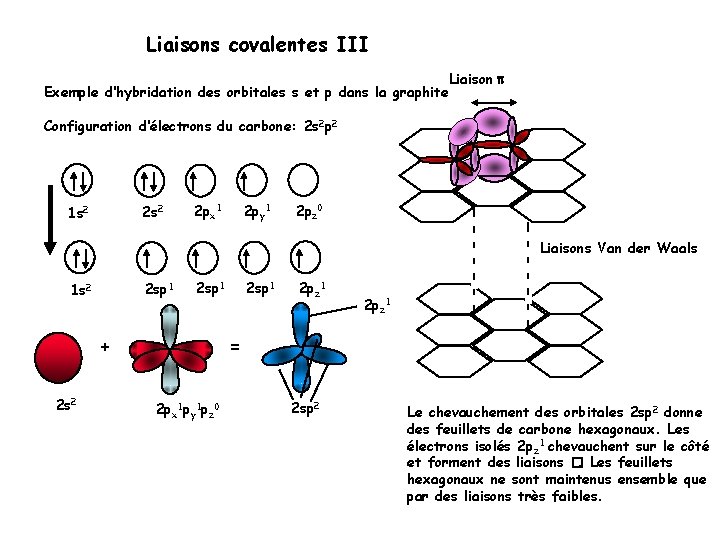
Liaisons covalentes III Exemple d‘hybridation des orbitales s et p dans la graphite Liaison Configuration d‘électrons du carbone: 2 s 2 p 2 2 s 2 1 s 2 2 px 1 2 py 1 2 pz 0 Liaisons Van der Waals 2 sp 1 1 s 2 2 sp 1 + 2 s 2 2 sp 1 2 pz 1 = 2 px 1 py 1 pz 0 2 sp 2 Le chevauchement des orbitales 2 sp 2 donne des feuillets de carbone hexagonaux. Les électrons isolés 2 pz 1 chevauchent sur le côté et forment des liaisons �. Les feuillets hexagonaux ne sont maintenus ensemble que par des liaisons très faibles.
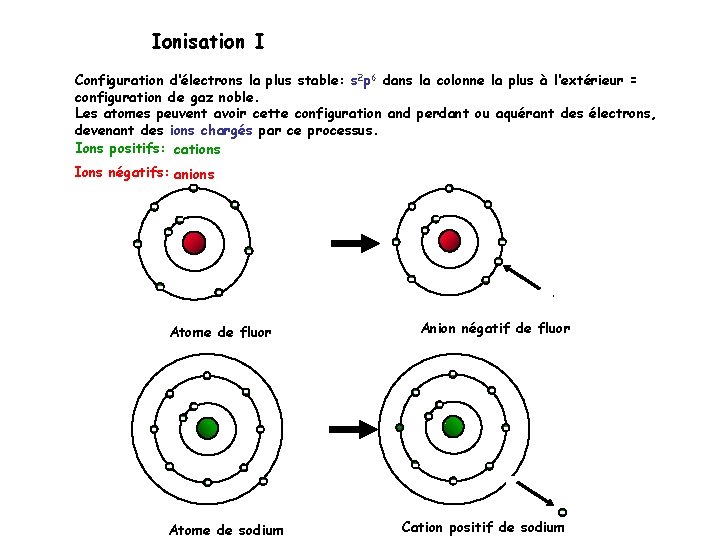
Ionisation I Configuration d‘électrons la plus stable: s 2 p 6 dans la colonne la plus à l‘extérieur = configuration de gaz noble. Les atomes peuvent avoir cette configuration and perdant ou aquérant des électrons, devenant des ions chargés par ce processus. Ions positifs: cations Ions négatifs: anions Atome de fluor Atome de sodium Anion négatif de fluor Cation positif de sodium

Ionisation II Tendance à la ionisation �potentiel de ionisation configuration électronique s 2 p 6: configuration la plus stable, configuration de “gaz noble” => haut potentiel de ionisation La tendance à donner un électron augmente quand: - aucun autre électron n‘a été ajouté ou soustrait auparavant - la couche de valence d‘un ion se rapproche d‘une configuration s 2 p 6 - l‘électron est dans une orbitale de faible énergie, loin du noyau Exemples: Elément Configuration d‘électron premier potentiel d‘ionisation Lithium Césium 1 s 22 s 1 1 s 22 s 2 p 63 s 2 p 6 d 104 s 2 p 6 d 10 5 s 2 p 66 s 1 5. 39 e. V 3. 89 e. V Néon Krypton 1 s 22 s 2 p 63 s 2 p 6 d 104 s 2 p 6 21. 56 e. V 14. 00 e. V Abilité à aquérir un électron de valence: affinité électronique. Affinités positive = Libération d‘énergie Exemple Chlore Affinité électronique 1 s 22 s 2 p 63 s 2 p 5 3. 61 e. V

Liaisons ioniques I - Grande différence d‘électronégativité �� E entre 2 atomes => transfert complet d‘électrons d‘un atome à l‘autre. - Charges des atomes opposées => attraction de Coulomb = liaison ionique avec gain d‘énergie cohésive. Caractéristiques énergétiques d‘une formation chlore sodium à partir des éléments gazeux. Na + 5. 14 e. V Énergie d‘ionisation Gaz e - + Gaz + + e Na+ - 5. 14 e. V - Gaz Cl Cl - + 3. 61 e. V Affinité électronique Gaz Na Na Bilan énergétique Gaz Cl Gaz - Na + Cl Cristal - +7. 90 e. V + 7. 9 e. V énergie cohésive Total: + 6. 37 e. V
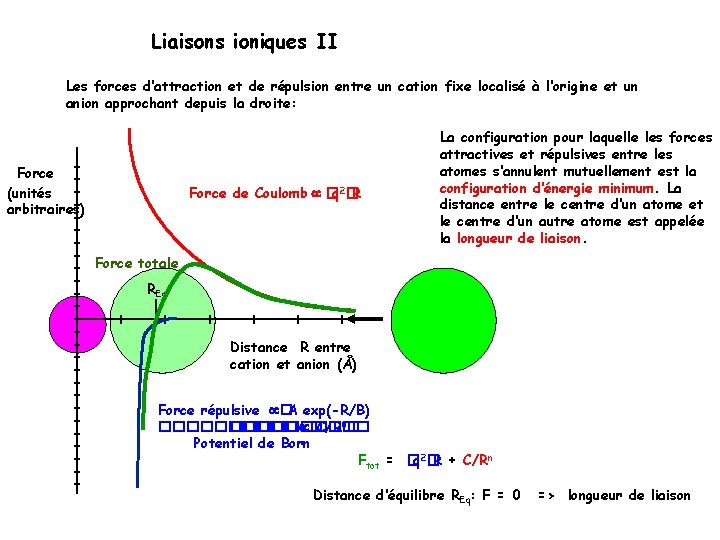
Liaisons ioniques II Les forces d‘attraction et de répulsion entre un cation fixe localisé à l‘origine et un anion approchant depuis la droite: Force (unités arbitraires) Force de Coulomb �q 2�R La configuration pour laquelle les forces attractives et répulsives entre les atomes s‘annulent mutuellement est la configuration d‘énergie minimum. La distance entre le centre d‘un atome et le centre d‘un autre atome est appelée la longueur de liaison. Force totale REq Distance R entre cation et anion (Å) Force répulsive � A exp(-R/B) ���������� �C/Rn� Potentiel de Born Ftot = �q 2�R + C/Rn Distance d‘équilibre REq: F = 0 => longueur de liaison
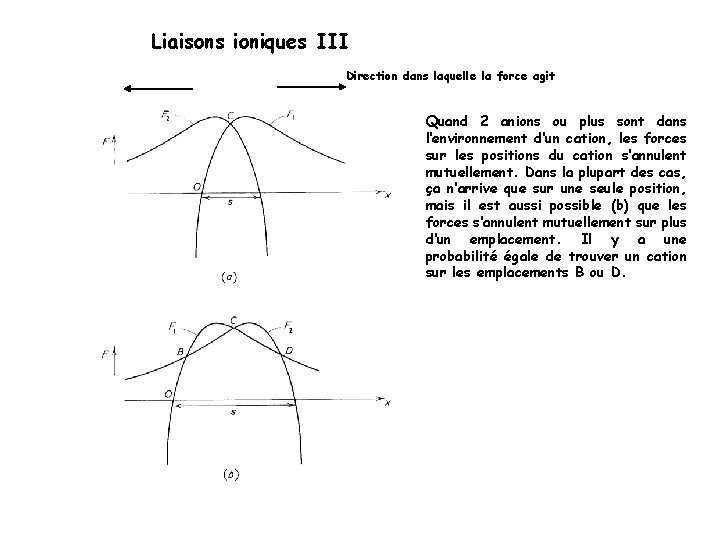
Liaisons ioniques III Direction dans laquelle la force agit Quand 2 anions ou plus sont dans l‘environnement d‘un cation, les forces sur les positions du cation s‘annulent mutuellement. Dans la plupart des cas, ça n‘arrive que sur une seule position, mais il est aussi possible (b) que les forces s‘annulent mutuellement sur plus d‘un emplacement. Il y a une probabilité égale de trouver un cation sur les emplacements B ou D.
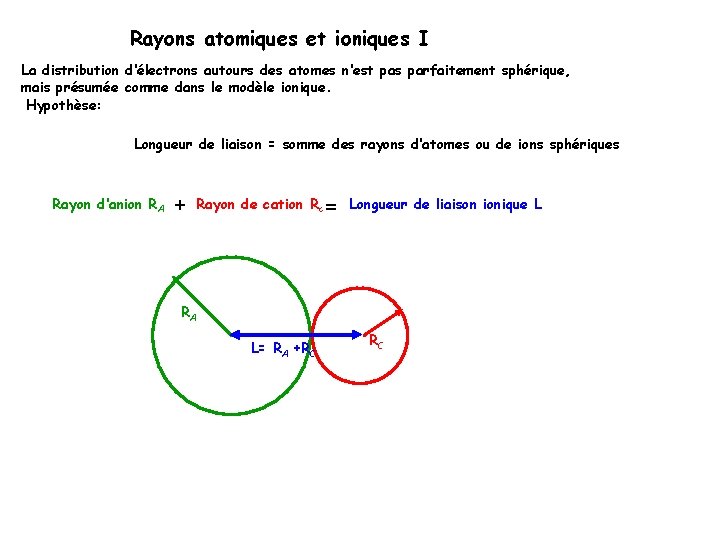
Rayons atomiques et ioniques I La distribution d‘électrons autours des atomes n‘est pas parfaitement sphérique, mais présumée comme dans le modèle ionique. Hypothèse: Longueur de liaison = somme des rayons d‘atomes ou de ions sphériques Rayon d‘anion RA + Rayon de cation Rc = Longueur de liaison ionique L RA L= RA +RC RC
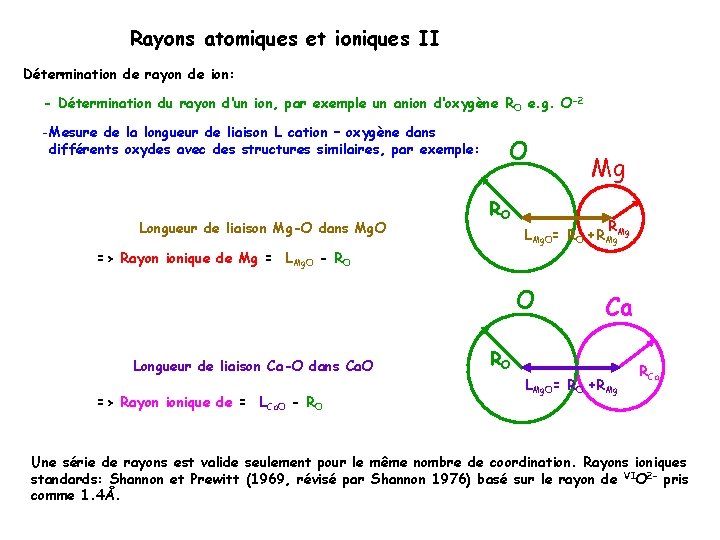
Rayons atomiques et ioniques II Détermination de rayon de ion: - Détermination du rayon d‘un ion, par exemple un anion d‘oxygène R O e. g. O-2 -Mesure de la longueur de liaison L cation – oxygène dans différents oxydes avec des structures similaires, par exemple: Longueur de liaison Mg-O dans Mg. O O RO Mg R LMg. O= RO +RMg. Mg => Rayon ionique de Mg = LMg. O - RO O Longueur de liaison Ca-O dans Ca. O => Rayon ionique de = LCa. O - RO Ca RO LMg. O= RO +RMg RCa Une série de rayons est valide seulement pour le même nombre de coordination. Rayons ioniques standards: Shannon et Prewitt (1969, révisé par Shannon 1976) basé sur le rayon de VIO 2 - pris comme 1. 4Å.
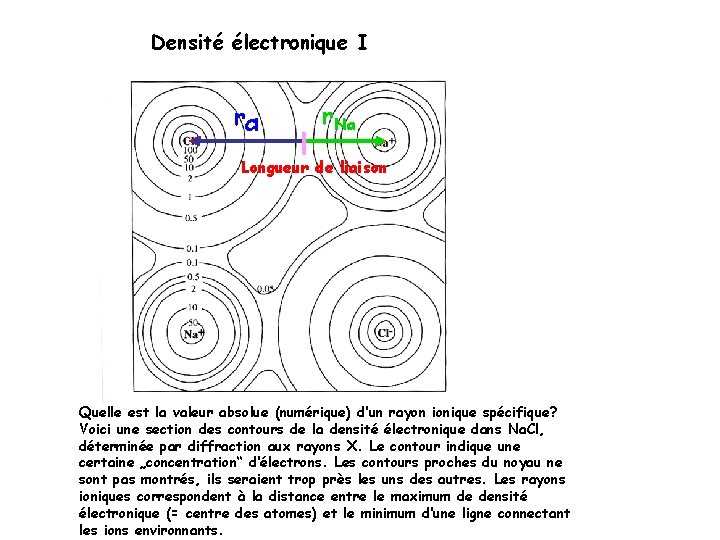
Densité électronique I r. Cl r. Na Longueur de liaison Quelle est la valeur absolue (numérique) d‘un rayon ionique spécifique? Voici une section des contours de la densité électronique dans Na. Cl, déterminée par diffraction aux rayons X. Le contour indique une certaine „concentration“ d‘électrons. Les contours proches du noyau ne sont pas montrés, ils seraient trop près les uns des autres. Les rayons ioniques correspondent à la distance entre le maximum de densité électronique (= centre des atomes) et le minimum d‘une ligne connectant les ions environnants.
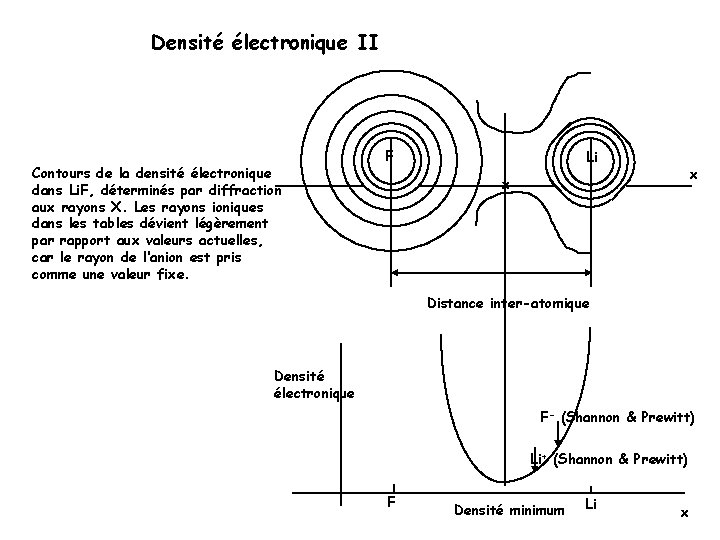
Densité électronique II Contours de la densité électronique dans Li. F, déterminés par diffraction aux rayons X. Les rayons ioniques dans les tables dévient légèrement par rapport aux valeurs actuelles, car le rayon de l‘anion est pris comme une valeur fixe. F Li x x Distance inter-atomique Densité électronique F- (Shannon & Prewitt) Li+ (Shannon & Prewitt) F Densité minimum Li x

Liaisons métalliques La liaison métallique est caractéristique entre les éléments situés ± sur la gauche dans le tableau périodique des éléments. Chaque atome perd ses électrons de valence. Les électrons libres de valence se déplace librement, formant un „gaz électronique“ entre les noyaux chargés positivement. Exemple schématique du sodium métallique: + + + + Électrons libres
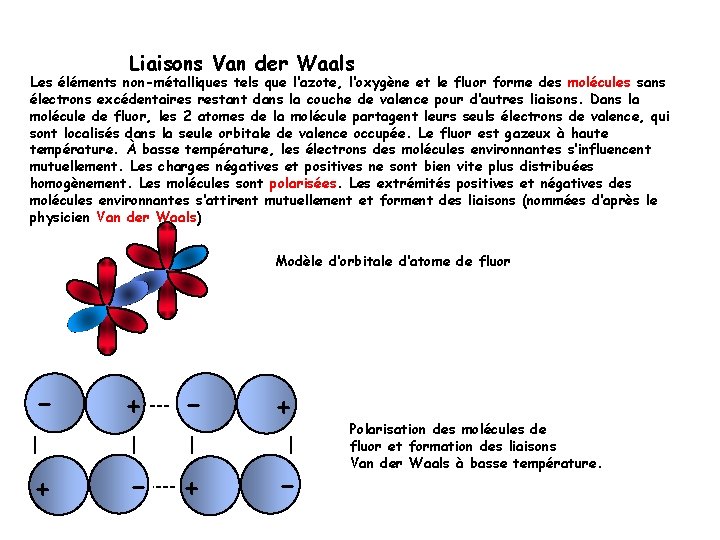
Liaisons Van der Waals Les éléments non-métalliques tels que l‘azote, l‘oxygène et le fluor forme des molécules sans électrons excédentaires restant dans la couche de valence pour d‘autres liaisons. Dans la molécule de fluor, les 2 atomes de la molécule partagent leurs seuls électrons de valence, qui sont localisés dans la seule orbitale de valence occupée. Le fluor est gazeux à haute température. À basse température, les électrons des molécules environnantes s‘influencent mutuellement. Les charges négatives et positives ne sont bien vite plus distribuées homogènement. Les molécules sont polarisées. Les extrémités positives et négatives des molécules environnantes s‘attirent mutuellement et forment des liaisons (nommées d‘après le physicien Van der Waals) Modèle d‘orbitale d‘atome de fluor - + + - Polarisation des molécules de fluor et formation des liaisons Van der Waals à basse température.
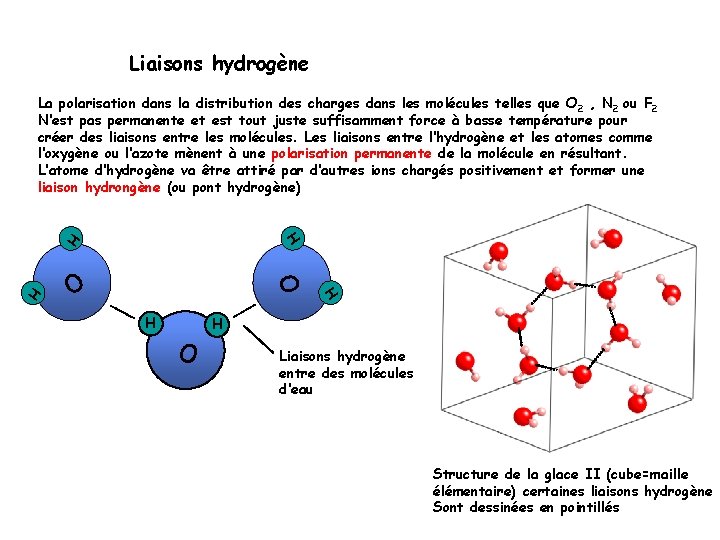
Liaisons hydrogène La polarisation dans la distribution des charges dans les molécules telles que O 2 , N 2 ou F 2 N‘est pas permanente et est tout juste suffisamment force à basse température pour créer des liaisons entre les molécules. Les liaisons entre l‘hydrogène et les atomes comme l‘oxygène ou l‘azote mènent à une polarisation permanente de la molécule en résultant. L‘atome d‘hydrogène va être attiré par d‘autres ions chargés positivement et former une liaison hydrongène (ou pont hydrogène) O H H H O Liaisons hydrogène entre des molécules d‘eau Structure de la glace II (cube=maille élémentaire) certaines liaisons hydrogène Sont dessinées en pointillés
- Slides: 23