Modifications physicochimiques des constituants alimentaires Les glucides Rappels












- Slides: 18

Modifications physicochimiques des constituants alimentaires

Les glucides / Rappels Leur formule brute s’écrit : Cn(H 2 O)n Il existe 2 grandes familles de glucides : n n T. S. B. les glucides simples (ou sucres) Les glucides complexes ou polyholosides 9. Modifications physicochimiques

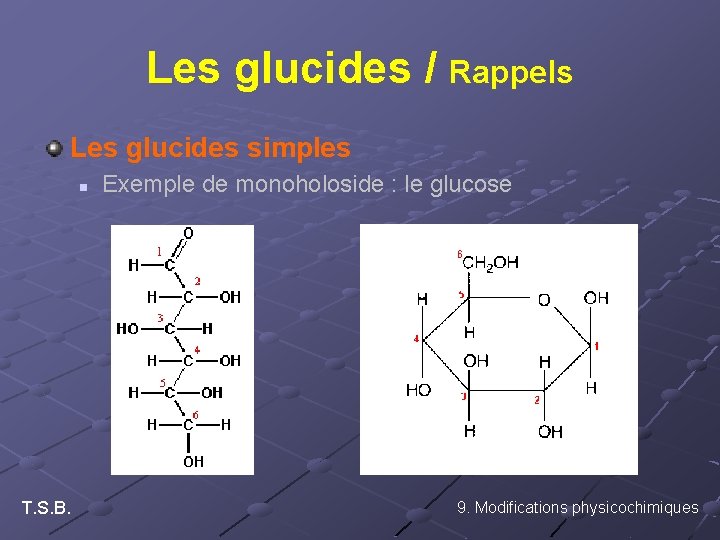
Les glucides / Rappels Les glucides simples n T. S. B. Exemple de monoholoside : le glucose 9. Modifications physicochimiques

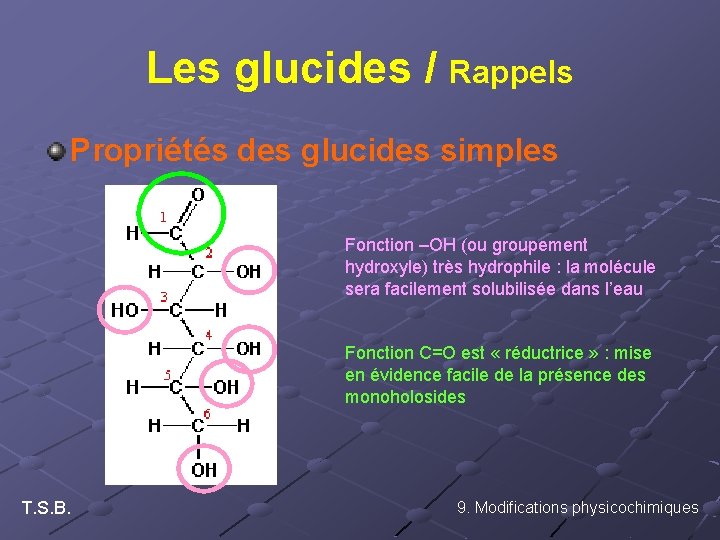
Les glucides / Rappels Propriétés des glucides simples Fonction –OH (ou groupement hydroxyle) très hydrophile : la molécule sera facilement solubilisée dans l’eau Fonction C=O est « réductrice » : mise en évidence facile de la présence des monoholosides T. S. B. 9. Modifications physicochimiques

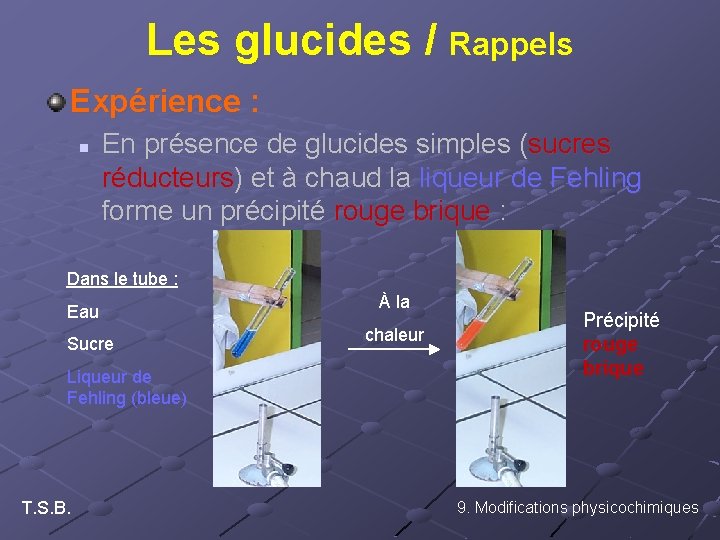
Les glucides / Rappels Expérience : n En présence de glucides simples (sucres réducteurs) et à chaud la liqueur de Fehling forme un précipité rouge brique : Dans le tube : Eau Sucre Liqueur de Fehling (bleue) T. S. B. À la chaleur Précipité rouge brique 9. Modifications physicochimiques

Les glucides / Rappels Autres glucides simples: n T. S. B. Le fructose Le galactose 9. Modifications physicochimiques

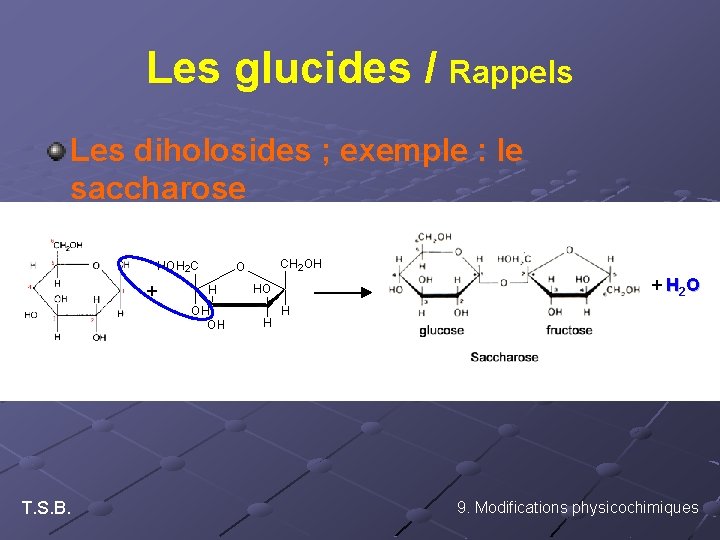
Les glucides / Rappels Les diholosides ; exemple : le saccharose + T. S. B. + H 2 O 9. Modifications physicochimiques

Les glucides / Rappels Autres diholosides : n n T. S. B. Le lactose : glucose + galactose (dans le lait) Le Maltose : glucose + glucose (n’existe pas à l’état brut dans les aliments) 9. Modifications physicochimiques

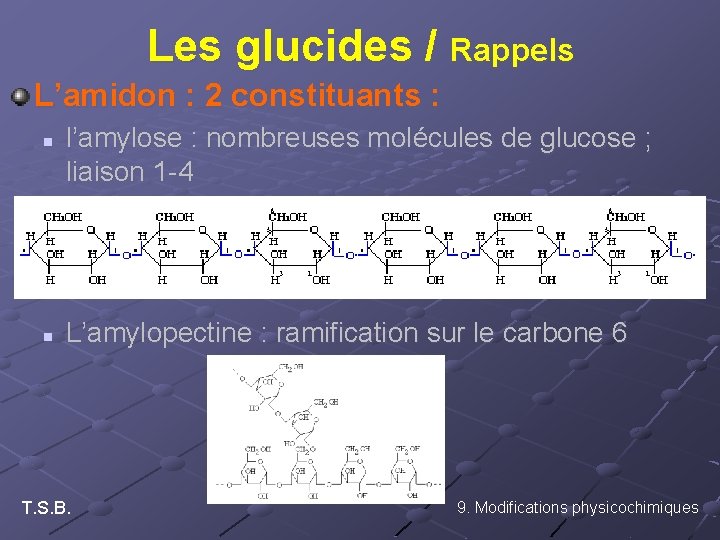
Les glucides / Rappels L’amidon : 2 constituants : n n l’amylose : nombreuses molécules de glucose ; liaison 1 -4 L’amylopectine : ramification sur le carbone 6 T. S. B. 9. Modifications physicochimiques

Les glucides / Rappels L’amidon : expérience n L’amidon est mis facilement en évidence : au contact d’eau iodée, il donne une couleur bleu foncée/violette Pomme de terre sur laquelle a été versée de l’eau iodée : T. S. B. 9. Modifications physicochimiques

Les glucides / Rappels Autres polyholosides : n Le glycogène T. S. B. n La cellulose n Les pectines 9. Modifications physicochimiques

Principales transformations Le pouvoir sucrant Fructose 1, 5 Saccharose 1 Glucose 0, 7 Maltose 0, 3 Lactose 0, 2 Polyholosides (ce ne sont pas des sucres !) T. S. B. 0 9. Modifications physicochimiques

Principales transformations Solubilité dans l’eau des glucides simples n n n T. S. B. Solubilisation importante grâce aux groupements hydroxyles Saturation : il n’y a plus de molécule d’eau disponible pour se lier aux molécules de saccharose Possibilité de repousser la saturation en chauffant l’eau 9. Modifications physicochimiques

Principales transformations Influence de la concentration n Le point d’ébullition augmente avec la concentration en sucre L’eau pure bout à T. S. B. 100°C Une solution sucrée à 10 % bout à 100, 2°C Une solution sucrée à 30 % bout à 101°C Une solution sucrée à 50 % bout à 102°C Une solution sucrée à 80 % bout à 106, 5°C Une solution sucrée à 90 % bout à 130°C 9. Modifications physicochimiques

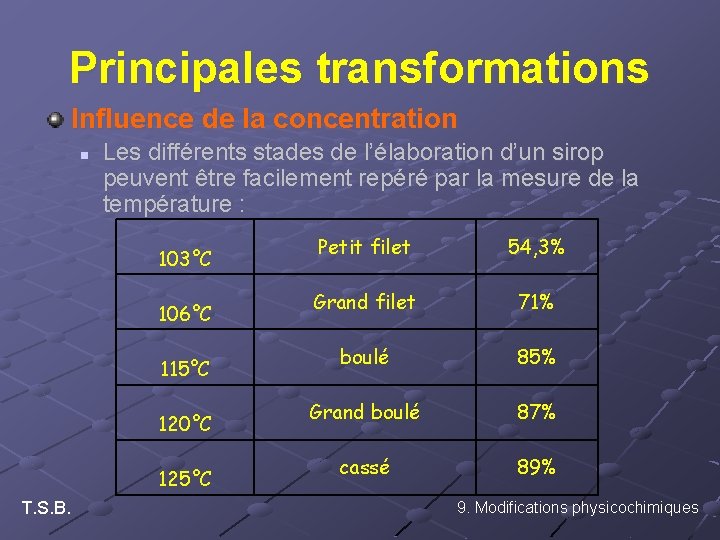
Principales transformations Influence de la concentration n Les différents stades de l’élaboration d’un sirop peuvent être facilement repéré par la mesure de la température : 103°C 106°C 115°C 120°C 125°C T. S. B. Petit filet 54, 3% Grand filet 71% boulé 85% Grand boulé 87% cassé 89% 9. Modifications physicochimiques

Principales transformations Solubilité des glucides complexes : n n Insoluble dans l’eau froide Chauffage d’une solution d’eau et d’amidon : vers 70°C : lait d’amidon. UTILISATION DE L’AMIDON COMME AGENT EPAISSISSANT T. S. B. 9. Modifications physicochimiques

Principales transformations Hydrolyse de l’amidon: n Expérience : un lait d’amidon est lentement chauffé en milieu acide. De temps en temps de petites quantités sont prélevées et testées à l’eau iodée et à la liqueur de Fehling. Qu’est ce qu’on recherche ? T. S. B. 9. Modifications physicochimiques

Principales transformations Hydrolyse de l’amidon: n Résultats : 1° prélèvement : donne une coloration bleue foncée ; les chaînes d’amidon sont intactes. 2° prélèvement : donne une coloration rosée ; les chaînes sont coupées en fragments irréguliers. Ce sont des dextrines 3° prélèvement : il n’y a plus de coloration à l’eau iodée : il n’y a plus d’amidon dans la solution. Par contre le test à la liqueur de fehling est positif Qu’est ce qu’on conclue ? T. S. B. 9. Modifications physicochimiques