Modern infektolgia Dr Krivn Gergely A leggyakoribb hallokok

Modern infektológia Dr Kriván Gergely
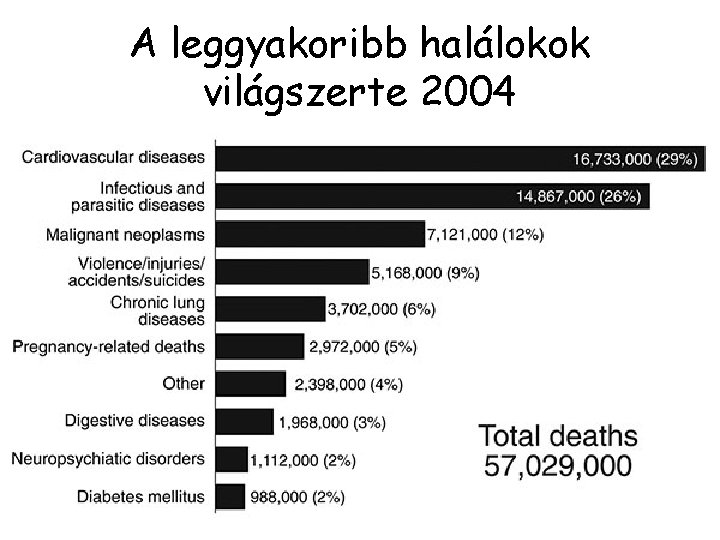
A leggyakoribb halálokok világszerte 2004
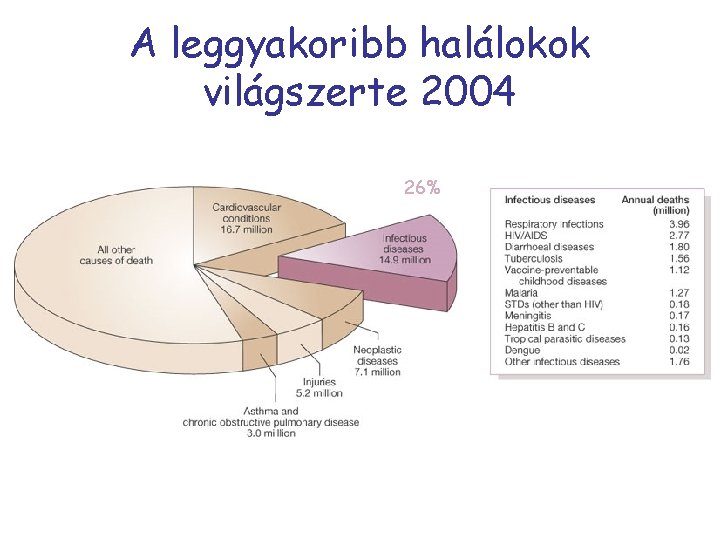
A leggyakoribb halálokok világszerte 2004 26%

Mit nevezünk infektológiának? • „Az infektológia az infekciós betegségekkel foglalkozó tudomány, olyan klinikai diszciplina, mely az infekciós betegségek kóroktanával, patomechanizmusával, klinikai lefolyásával, gyógyításával és a megelőzés lehetőségeivel foglalkozik. Kutatásának tárgya minden olyan betegség, melyet a szervezetben szaporodó mikroorganizmusok, vírusok, baktériumok, gombák, egy- és többsejtű paraziták okoznak, függetlenül attól, hogy a kórokozó támadása mely szervet vagy szervrendszert érint” Infektológia. Egyetemi tankönyv 2009 (szerk. Ludwig Endre, Szalka András)

A korszerű infektológia jellemzői • Rendkívül szerteágazó, multidisciplináris jellegű tudományág (~ immunológia, genetika) • Korszerű infektológia integratív tudomány: pl. belgyógyászat, mikrobiológia, kórélettan, gyógyszertan, immunológia, epidemiológia, vakcinológia, infekció-kontroll és antibiotikum politika stb. • Óriási fejlődés a diagnosztikában, terápiában – a szemléletben

Az infektológia változása • Korábban: ragályosan terjedő megbetegedések → az összes mikróba okozta megbetegedés • Egyre több betegség hátterében igazolódik infekciós eredet: gyomor és nyombélfekély, méhnyakrák, arthritisek, májtumorok stb. • Új, eddig ismeretlen kórokozók jelentek meg (SARS, H 5 N 1 - közlekedés, globalizáció), illetve korábban feledésbe merült infekciók élednek fel (migráció, szociális leszakadás). • Növekszik a csökkent érzékenységű vagy rezisztens kórokozók aránya. Költségnövekedés. Nosocomiális fertőzések – infekciókontroll, antibiotikum politika. • Immunkompromittált betegek növekvő száma – opportunista kórokozók, szokatlan fertőzések. • Új eljárások, módszerek megjelenése – speciális mikrobiológiai, gyógyszertani, farmakokinetikai ismeretek szükségesek.
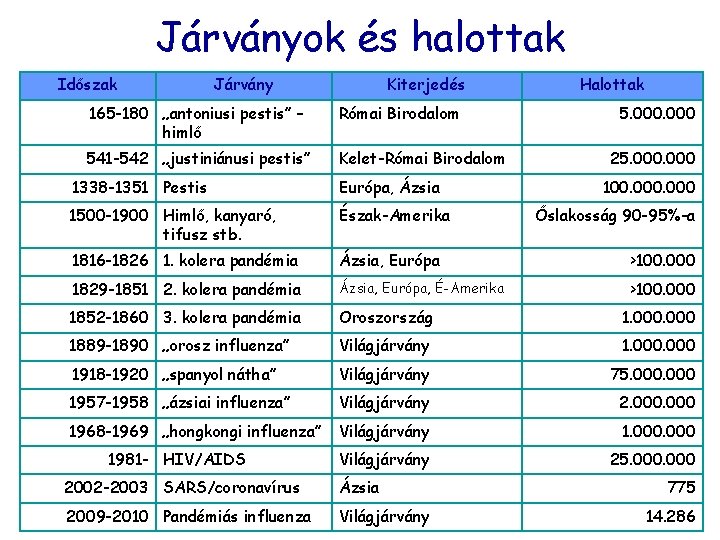
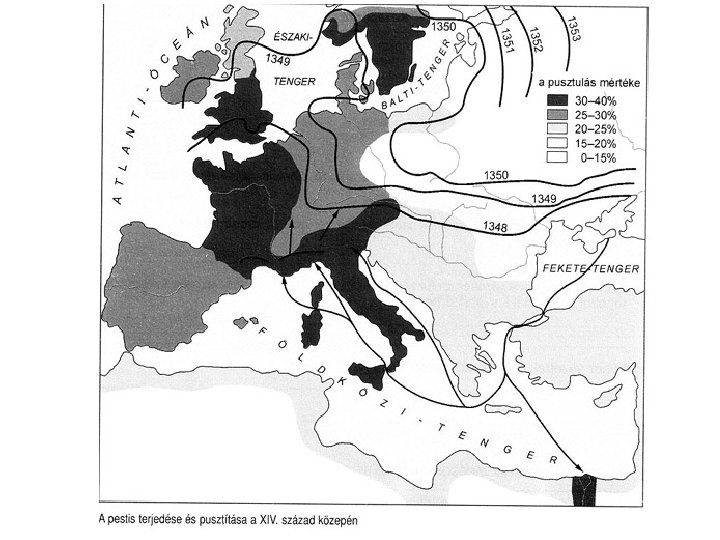
Járványok és halottak Időszak Járvány Kiterjedés 165 -180 „antoniusi pestis” – himlő Római Birodalom 541 -542 „justiniánusi pestis” Kelet-Római Birodalom Halottak 5. 000 25. 000 1338 -1351 Pestis Európa, Ázsia 1500 -1900 Himlő, kanyaró, tifusz stb. Észak-Amerika 1816 -1826 1. kolera pandémia Ázsia, Európa >100. 000 1829 -1851 2. kolera pandémia Ázsia, Európa, É-Amerika >100. 000 1852 -1860 3. kolera pandémia Oroszország 1. 000 1889 -1890 „orosz influenza” Világjárvány 1. 000 1918 -1920 „spanyol nátha” Világjárvány 75. 000 1957 -1958 „ázsiai influenza” Világjárvány 2. 000 1968 -1969 „hongkongi influenza” Világjárvány 1. 000 Világjárvány 25. 000 1981 - HIV/AIDS 2002 -2003 SARS/coronavírus Ázsia 2009 -2010 Pandémiás influenza Világjárvány 100. 000 Őslakosság 90 -95%-a 775 14. 286


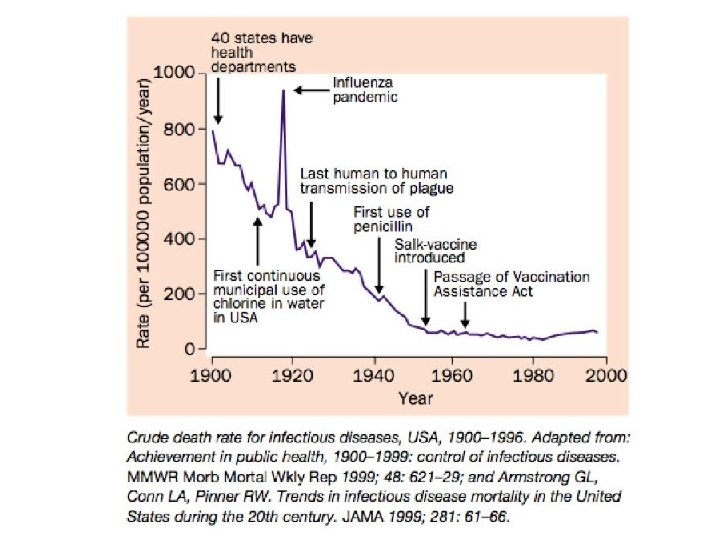
Járványok kialakulásának és terjedésének megakadályozása • Közegészségügyi viszonyok javulása • Infekció-kontroll • A patogének felfedezése • Az orvostudomány fejlődése (pl. infúziós kezelés) • Vakcináció • Antimikróbás szerek
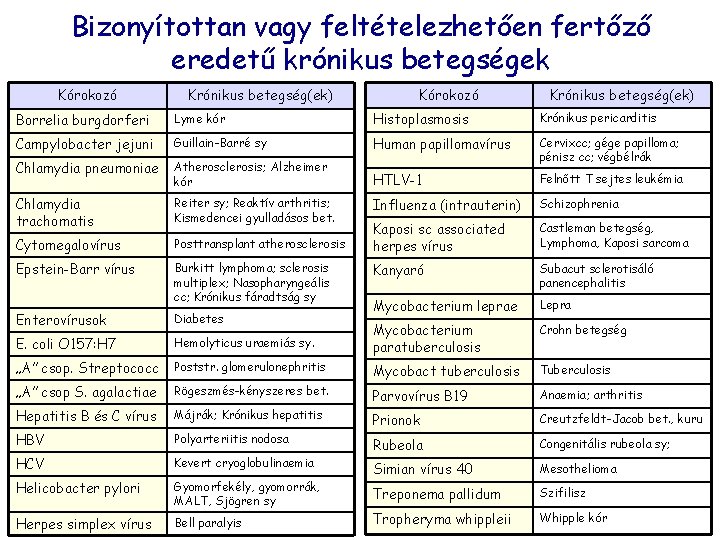
Bizonyítottan vagy feltételezhetően fertőző eredetű krónikus betegségek Kórokozó Krónikus betegség(ek) Borrelia burgdorferi Lyme kór Histoplasmosis Krónikus pericarditis Campylobacter jejuni Guillain-Barré sy Human papillomavírus Chlamydia pneumoniae Atherosclerosis; Alzheimer kór Cervixcc; gége papilloma; pénisz cc; végbélrák HTLV-1 Felnőtt T sejtes leukémia Chlamydia trachomatis Reiter sy; Reaktív arthritis; Kismedencei gyulladásos bet. Influenza (intrauterin) Schizophrenia Cytomegalovírus Posttransplant atherosclerosis Kaposi sc associated herpes vírus Castleman betegség, Lymphoma, Kaposi sarcoma Epstein-Barr vírus Burkitt lymphoma; sclerosis multiplex; Nasopharyngeális cc; Krónikus fáradtság sy Kanyaró Subacut sclerotisáló panencephalitis Enterovírusok Diabetes Mycobacterium leprae Lepra E. coli O 157: H 7 Hemolyticus uraemiás sy. Mycobacterium paratuberculosis Crohn betegség „A” csop. Streptococc Poststr. glomerulonephritis Mycobact tuberculosis Tuberculosis „A” csop S. agalactiae Rögeszmés-kényszeres bet. Parvovírus B 19 Anaemia; arthritis Hepatitis B és C vírus Májrák; Krónikus hepatitis Creutzfeldt-Jacob bet. , kuru HBV Prionok Polyarteriitis nodosa Congenitális rubeola sy; HCV Kevert cryoglobulinaemia Rubeola Mesothelioma Helicobacter pylori Gyomorfekély, gyomorrák, MALT, Sjögren sy Simian vírus 40 Treponema pallidum Szifilisz Herpes simplex vírus Bell paralyis Tropheryma whippleii Whipple kór
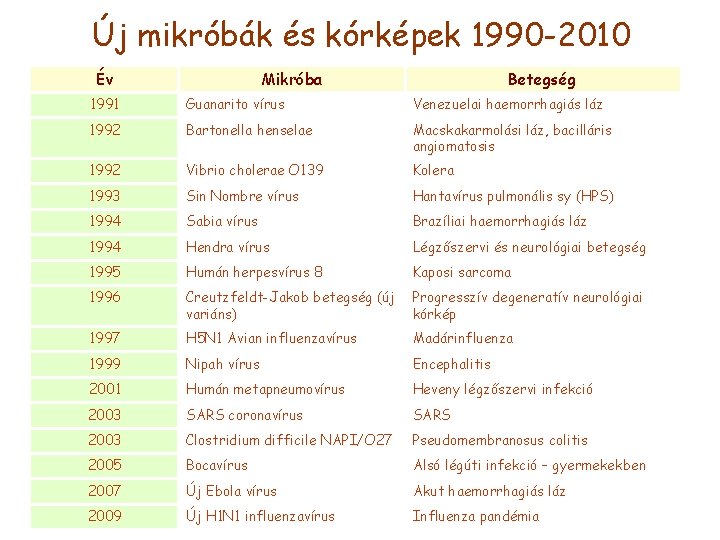
Új mikróbák és kórképek 1990 -2010 Év Mikróba Betegség 1991 Guanarito vírus Venezuelai haemorrhagiás láz 1992 Bartonella henselae Macskakarmolási láz, bacilláris angiomatosis 1992 Vibrio cholerae O 139 Kolera 1993 Sin Nombre vírus Hantavírus pulmonális sy (HPS) 1994 Sabia vírus Brazíliai haemorrhagiás láz 1994 Hendra vírus Légzőszervi és neurológiai betegség 1995 Humán herpesvírus 8 Kaposi sarcoma 1996 Creutzfeldt-Jakob betegség (új variáns) Progresszív degeneratív neurológiai kórkép 1997 H 5 N 1 Avian influenzavírus Madárinfluenza 1999 Nipah vírus Encephalitis 2001 Humán metapneumovírus Heveny légzőszervi infekció 2003 SARS coronavírus SARS 2003 Clostridium difficile NAPI/O 27 Pseudomembranosus colitis 2005 Bocavírus Alsó légúti infekció – gyermekekben 2007 Új Ebola vírus Akut haemorrhagiás láz 2009 Új H 1 N 1 influenzavírus Influenza pandémia
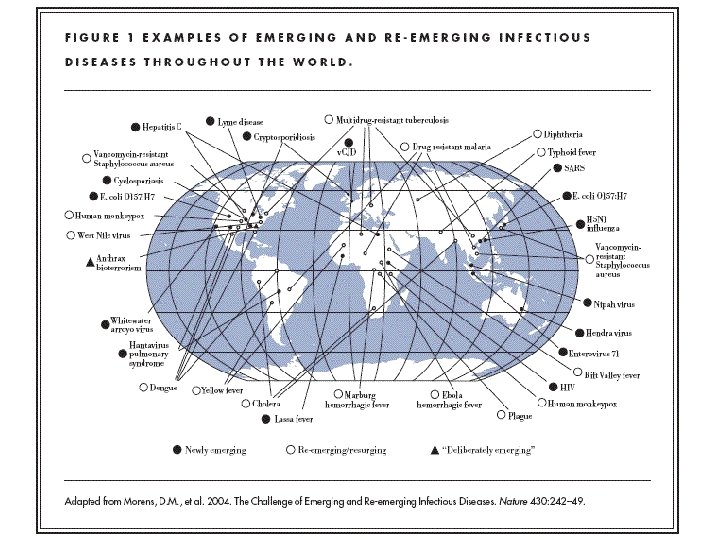

Egyes fertőző betegségek újranövekedésének okai • A kórokozók genetikai változásai: gyógyszer rezisztencia kialakulása, virulencia növekedés • Társadalmi mozgalmak, szegénység, migráció, turizmus: kórokozók és a vektorok mozgása nő • Népesség növekedés: új területek meghódítása – korábban nem ismert, újabb kórokozókkal ill. kórokozókat hordozó állatfajokkal való találkozás • Éghajlati változások • Védőoltások elhanyagolása
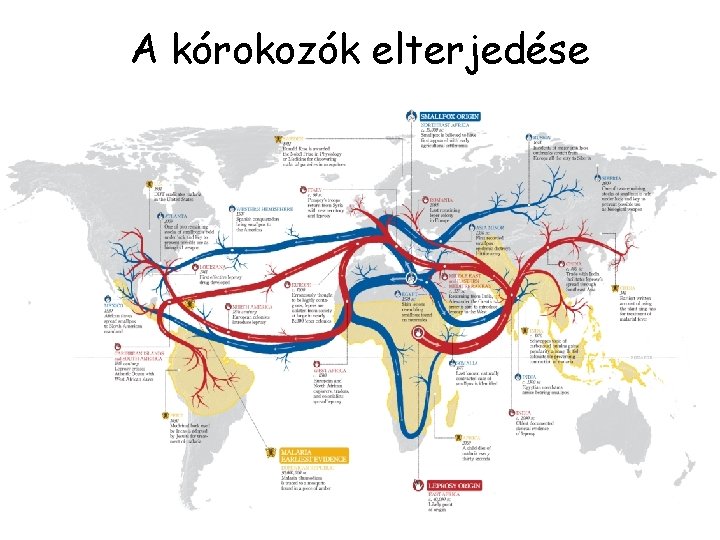
A kórokozók elterjedése
Globális keveredés Növekvő populáció-sűrűség Csökkent utazási idő

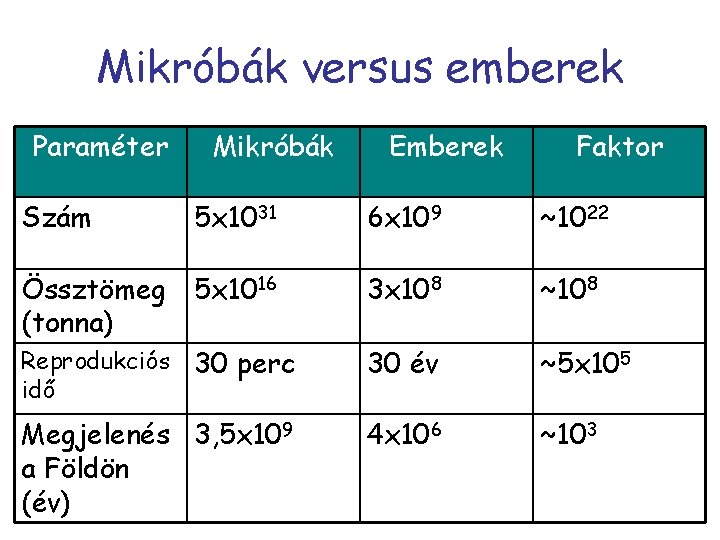
Mikróbák versus emberek Paraméter Mikróbák Emberek Faktor Szám 5 x 1031 6 x 109 ~1022 Össztömeg (tonna) 5 x 1016 3 x 108 ~108 Reprodukciós idő 30 perc 30 év ~5 x 105 Megjelenés 3, 5 x 109 a Földön (év) 4 x 106 ~103

• • • “It is time to close the book on infectious diseases, and declare the war against pestilence won” „Eljött az ideje annak, hogy becsukjuk a fertőző betegségek tankönyvét, és kijelentsük a győzelmünket a fertőzések elleni háborúban” “Warning flags are still flying in the communicable disease field. . While we are engaged in taking on new duties. . . we cannot and must not lose sight of our traditional program responsibilities” 65 th Annual Meeting of the Association of State and Territorial Health Officers in 1967 „A figyelmeztető jelek továbbra láthatók a fertőző betegségek területén… Az új feladatok következetes megoldásakor nem szabad figyelmen kívül hagynunk a korábbi problémákból adódó kötelezettségeinket sem” William H. Stewart (1921 -2008)

A rezisztencia definíciói • Multidrug rezisztens (MDR) baktériumok: – – – – – MRSA (methicillin rezisztens S aureus) VRE (vancomycin rezisztens enterococcusok) Pseudomonas aeruginosa Acinetobacter baumannii Enterobacter species ESBL – termelő Klebsiella sp és E. coli Stenotrophomonas maltophilia Mycobacterium tuberculosis DRSP (drug rezisztens S. pneumoniae) • Multirezisztens baktériumok: • Pánrezisztens baktériumok: • XDR (extrém drug rezisztens) baktériumok: – Egyidejűleg 3 különböző osztályba tartozó hatóanyaggal szemben rezisztens (cephalosporinok. , fluorokinolonok, aminoglikozidok) – Antipseudomonas hatású cephalosporin és carbapenem, pip/tazo, ciprofloxacin és levofloxacin rezisztens G- baktériumok – Antipseudomonas hatású cephalosporin és carbapenem, pip/tazo, ciprofloxacin és levofloxacin, aminoglikozid, tigecyclin, polymyxin rezisztens G- baktériumok
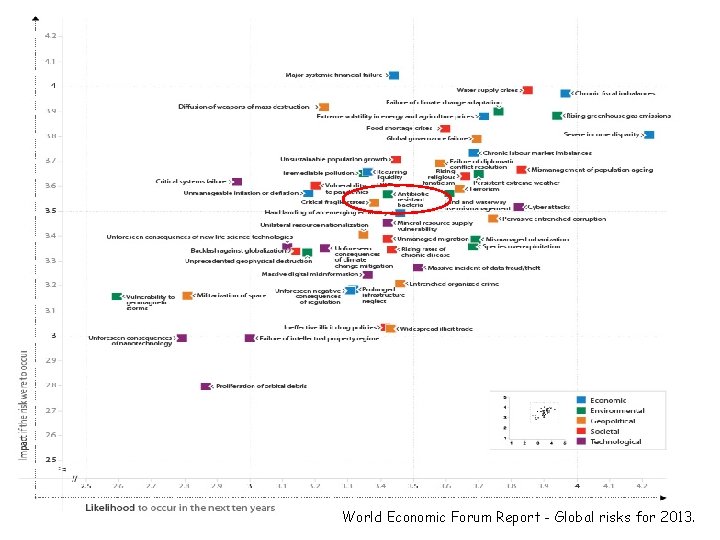
World Economic Forum Report - Global risks for 2013.

ESKAPE patogének Patogén Probléma E Enterococcus faecium A vancomycin rezisztens enterococcusok száma nő (↑USA) S Staphylococcus aureus (MRSA) 1. 2. 3. Egyre gyakrabban izolálják Megjelentek a CA-MRSA törzsek vancomycin érzékenysége csökken (MIC ↑) K Klebsiella pneumoniae E. Coli 1. 2. Egyre több ESBL termelőt izolálnak Megjelentek a területen is az ESBL-termelő klebsiellák és colik Már vannak carbapenemáz termelő Klebsiella pneumoniae izolátumok A Acinetobacter baumannii 1. 2. Egyre növekvő carbapenem rezisztencia Növekszik a súlyos fertőzések száma P Pseudomonas aeruginosa 1. 2. Az infekciók száma egyre nő Emelkedik a carbapenem-, fluorokinolon-, aminoglikozid rezisztens izolátumok előfordulása E Enterobacter species 1. 2. Egyre gyakrabban izolálják különböző infekciókban Nő az ESBL-, carbapenemáz-, cefalosporináz termelő törzsek gyakorisága 3. Szalka A: LAM 2011
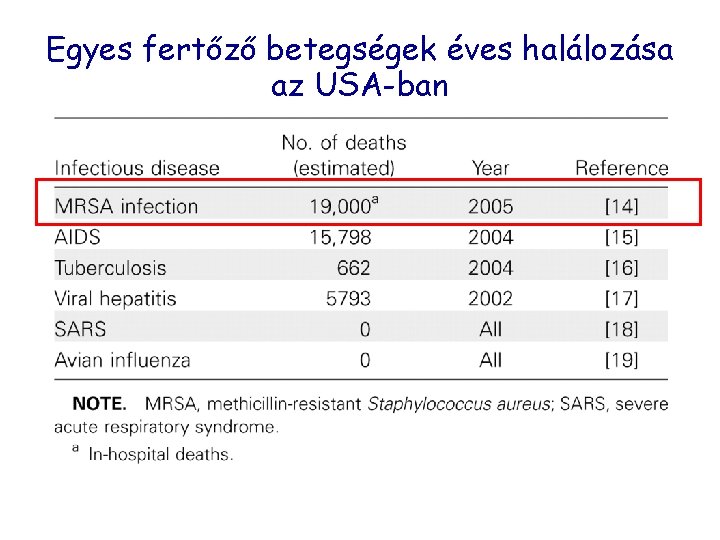
Egyes fertőző betegségek éves halálozása az USA-ban Boucher H W , Corey G R: Clin Infect Dis. 2008; 46: S 344 -S 349

Az MRSA jelentősége • A rezisztens S aureus fertőzések kezelése nehezebb • Késlekedés a megfelelő kezelésben • Költségnövekedés (MRSA MSSA véráram infekció) – Kórházi tartózkodás és kezelési költség 3 X nő • Halálozás?

Study on European Practices of Infections (bacteriaemia) with S aureus (SEPIA) Anti-MRSA kezelés első vonalban: O (%) A másodvonalbeli anti-MRSA kezelésig eltelt idő (nap) A harmadvonalbeli anti-MRSA kezelésig eltelt idő (nap) Bacteriaemia (n=152) SSTI* (n=132) FN/FUO** (n=190) Endocarditis (n=90) Iv. katéter (n=31) Összesen (n=605) 45 49 58 49 44 49 6 10 13 5 5 6 6 17 5 15 6 8 Bizonyított MRSA fertőzésben szenvedő betegek retrospektív elemzése az EU-ban *Bőr és lágyrész fertőzések, **Lázas neutropenia és ismeretlen eredetű láz Az MRSA betegek csaknem 50%-a nem kapott megfelelő első vonalbeli kezelést! Ammerlaan H. és mtsai: CID 49: 997 -1004, 2009.

Az MRSA jelentősége • A rezisztens S aureus fertőzések kezelése nehezebb • Késlekedés a megfelelő kezelésben • Költségnövekedés (MRSA MSSA véráram infekció) – Kórházi tartózkodás és kezelési költség 3 X nő • Halálozás?
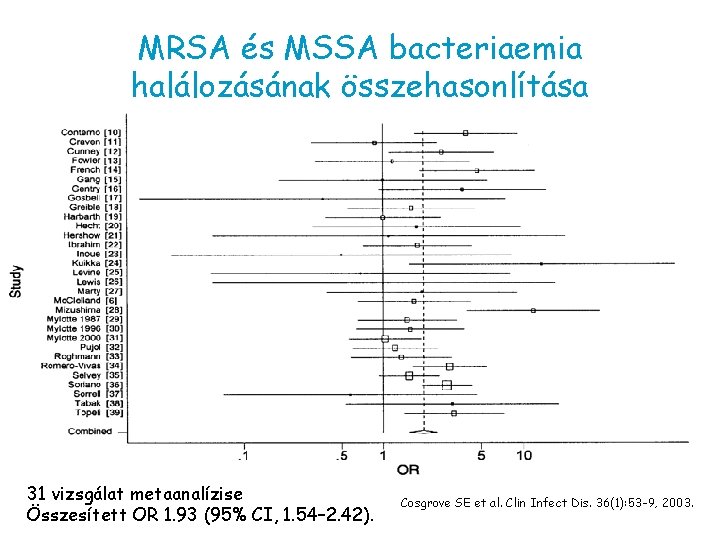
MRSA és MSSA bacteriaemia halálozásának összehasonlítása 31 vizsgálat metaanalízise Összesített OR 1. 93 (95% CI, 1. 54– 2. 42). Cosgrove SE et al. Clin Infect Dis. 36(1): 53 -9, 2003.
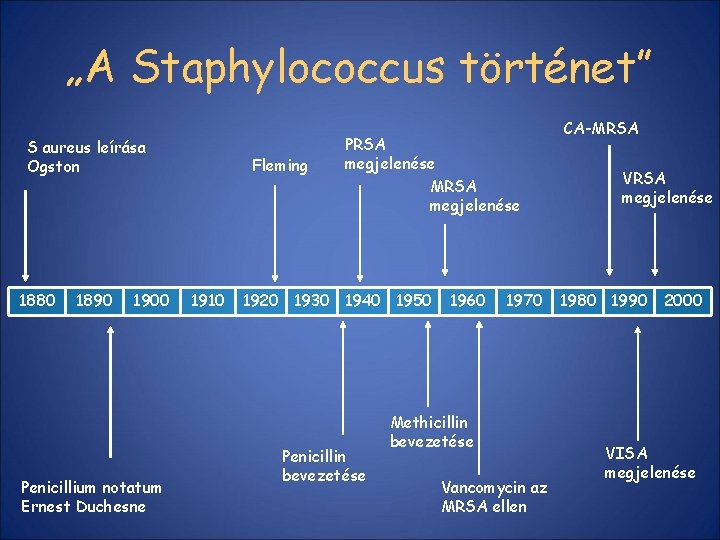
„A Staphylococcus történet” S aureus leírása Ogston 1880 1890 1900 Penicillium notatum Ernest Duchesne Fleming 1910 PRSA megjelenése MRSA megjelenése 1920 1930 1940 1950 Penicillin bevezetése 1960 1970 Methicillin bevezetése Vancomycin az MRSA ellen CA-MRSA VRSA megjelenése 1980 1990 2000 VISA megjelenése

VISA - Vancomycin intermediate S aureus (MIC 4 -8 ug/ml) METHICILLIN REZISZTENS S AUREUS VRSA – Vancomycin resistant S aureus (MIC ≥ 16 ug/ml)

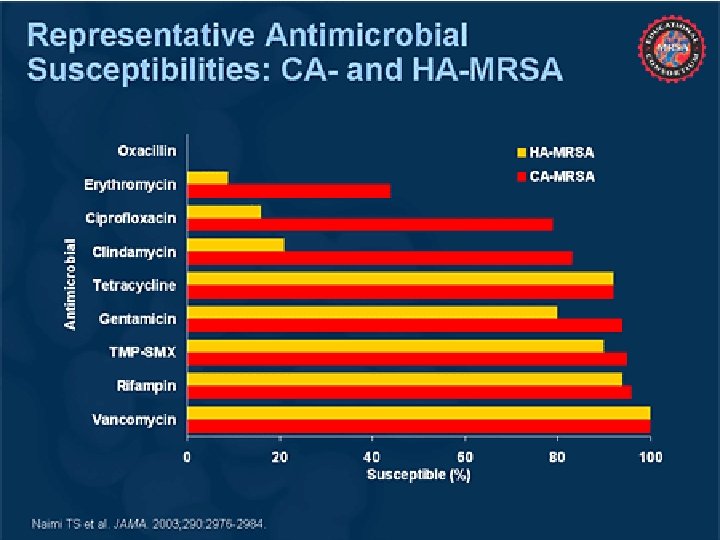
A CA-MRSA és a HA-MRSA jellemzői CA-MRSA HA-MRSA Kockázati csoport Gyermekek, sportolók, rabok, katonák, egyes etnikai csoportok, iv. drog, homoszexuálisok Ápolási otthonok lakói, dializáltak, diabetes, elhúzódó kórházi tartózkodás, ITO, iv eszközök SCCmec típus IV I, II és III AB rezisztencia Csak ß-laktám rezisztencia, Rendszerint TMP-SMX, clindamycin érzékeny Multirezisztens, Rendszerint TMP-SMX érzékeny Panton-Valentine (PVL) toxin Gyakori Ritka Társuló klinikai tünetek SSTI, posztinfluenzás necrotizáló pneumonia Nosocomiális pneumonia, katéterrel összefüggő UTI, véráram fertőzések, SSTI (Staphylococcus Chromosomális Cazett) SSTI: bőr- és lágyrészinfekció; UTI: húgyúti fertőzés
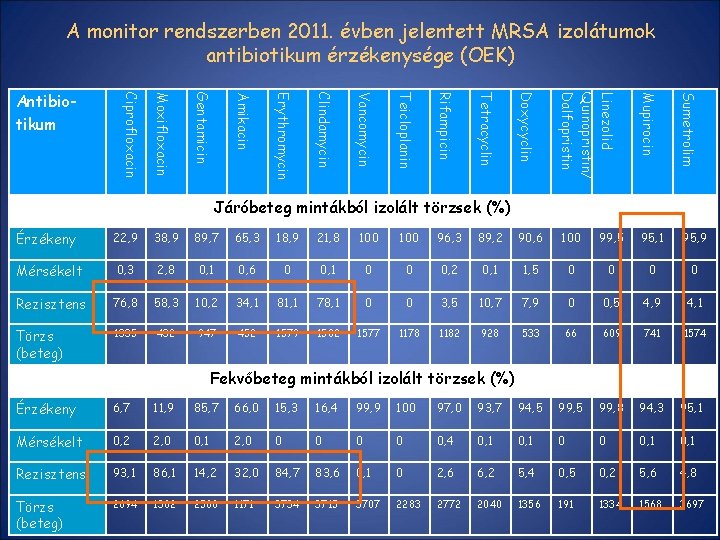
A monitor rendszerben 2011. évben jelentett MRSA izolátumok antibiotikum érzékenysége (OEK) Mupirocin Sumetrolim Linezolid Quinopristin/ Dalfopristin Doxycyclin Tetracyclin Rifampicin Teicloplanin Vancomycin Clindamycin Erythromycin Amikacin Gentamicin Moxifloxacin Ciprofloxacin Antibiotikum Érzékeny 22, 9 38, 9 89, 7 65, 3 18, 9 21, 8 100 96, 3 89, 2 90, 6 100 99, 5 95, 1 95, 9 Mérsékelt 0, 3 2, 8 0, 1 0, 6 0 0, 1 0 0 0, 2 0, 1 1, 5 0 0 Rezisztens 76, 8 58, 3 10, 2 34, 1 81, 1 78, 1 0 0 3, 5 10, 7 7, 9 0 0, 5 4, 9 4, 1 Törzs (beteg) 1335 432 947 452 1579 1582 1577 1178 1182 928 533 66 609 741 1574 Járóbeteg mintákból izolált törzsek (%) Fekvőbeteg mintákból izolált törzsek (%) Érzékeny 6, 7 11, 9 85, 7 66, 0 15, 3 16, 4 99, 9 100 97, 0 93, 7 94, 5 99, 8 94, 3 95, 1 Mérsékelt 0, 2 2, 0 0, 1 2, 0 0 0, 4 0, 1 0 0 0, 1 Rezisztens 93, 1 86, 1 14, 2 32, 0 84, 7 83, 6 0, 1 0 2, 6 6, 2 5, 4 0, 5 0, 2 5, 6 4, 8 Törzs (beteg) 2694 1382 2580 1171 3734 3715 3707 2283 2772 2040 1356 191 1334 1568 3697
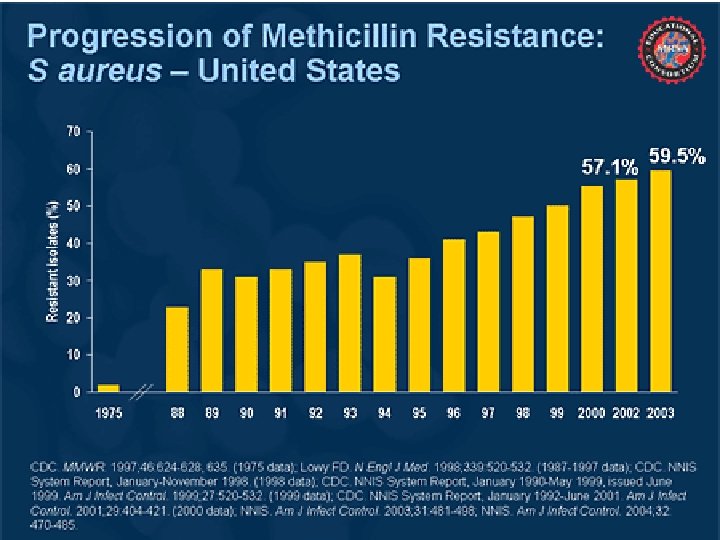
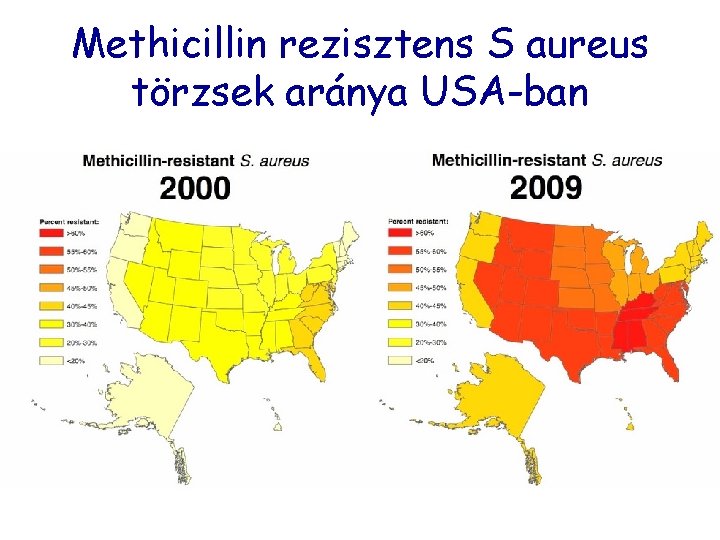
Methicillin rezisztens S aureus törzsek aránya USA-ban
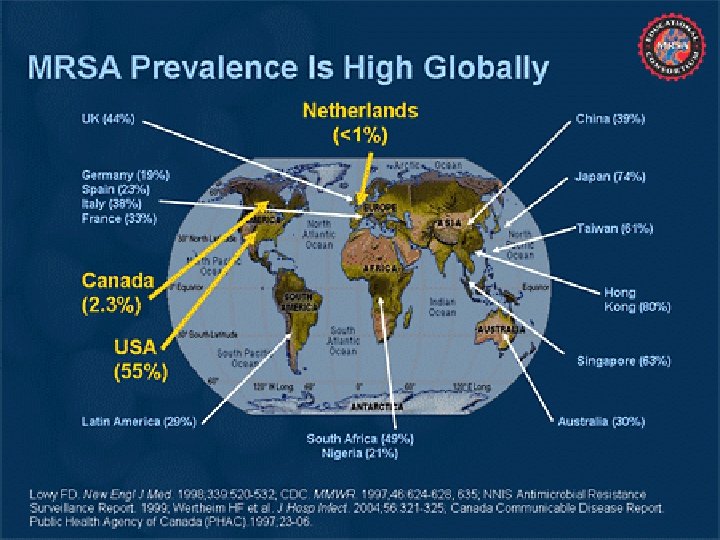
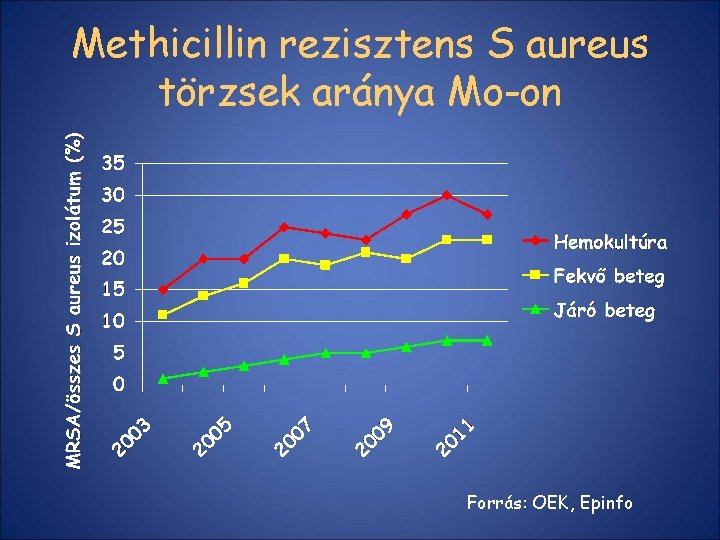
Methicillin rezisztens S aureus törzsek aránya Mo-on Forrás: OEK, Epinfo
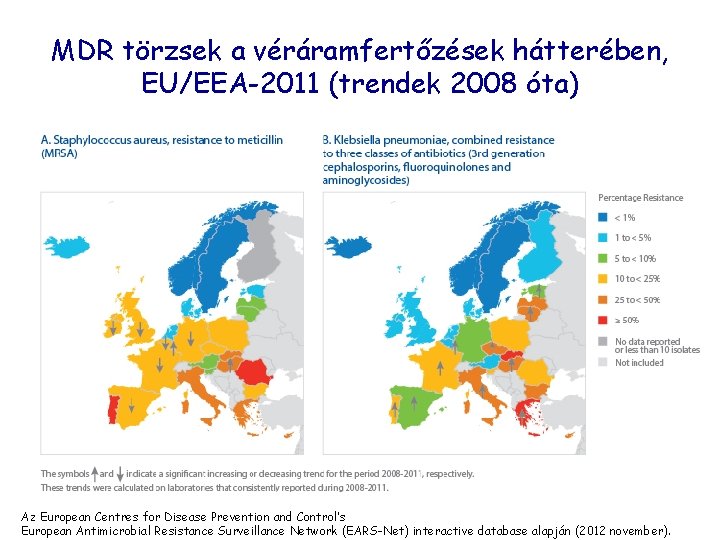
MDR törzsek a véráramfertőzések hátterében, EU/EEA-2011 (trendek 2008 óta) Az European Centres for Disease Prevention and Control’s European Antimicrobial Resistance Surveillance Network (EARS-Net) interactive database alapján (2012 november).
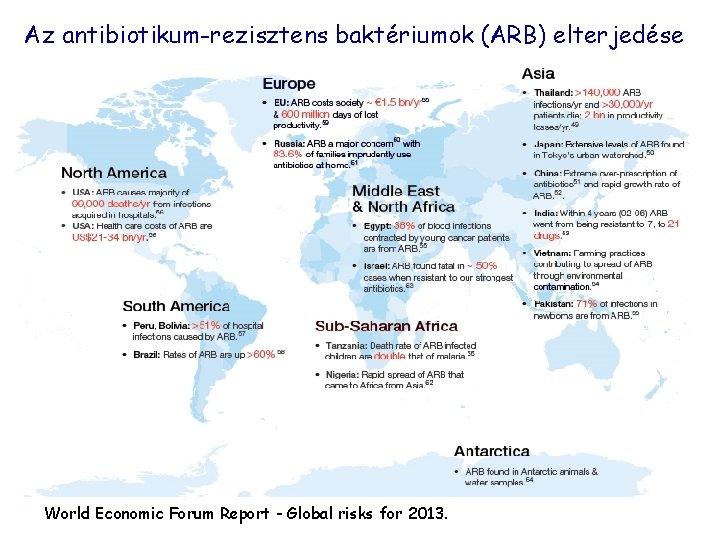
Az antibiotikum-rezisztens baktériumok (ARB) elterjedése World Economic Forum Report - Global risks for 2013.

Immunkompromittált betegek számát növeli: • Malignus hematológiai és daganatos betegségek agresszív kezelése • Vérképző őssejt-átültetés • Szolid szervtranszplantáció • Biológiai terápiák elterjedése • Autoimmun betegségek agresszív kezelése • HIV/AIDS • Növekvő életkor
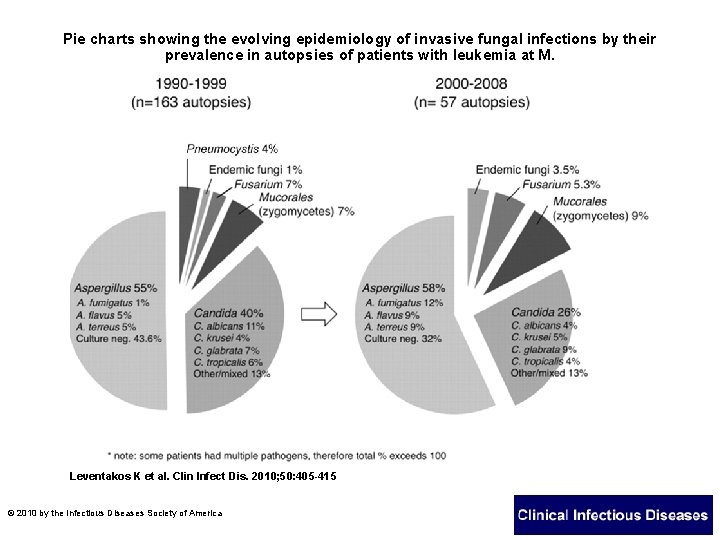
Pie charts showing the evolving epidemiology of invasive fungal infections by their prevalence in autopsies of patients with leukemia at M. Leventakos K et al. Clin Infect Dis. 2010; 50: 405 -415 © 2010 by the Infectious Diseases Society of America
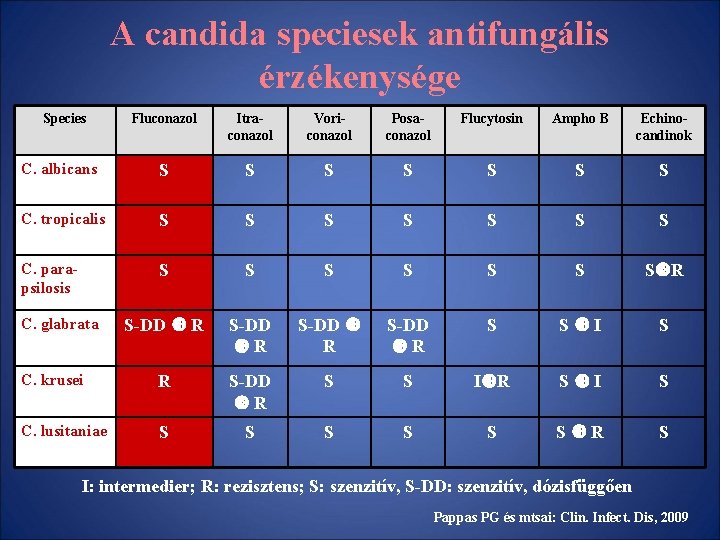
A candida speciesek antifungális érzékenysége Species Fluconazol Itraconazol Voriconazol Posaconazol Flucytosin Ampho B Echinocandinok C. albicans S S S S C. tropicalis S S S S C. parapsilosis S S S S R S-DD R S S I S C. krusei R S-DD R S S I R S I S C. lusitaniae S S S R S C. glabrata I: intermedier; R: rezisztens; S: szenzitív, S-DD: szenzitív, dózisfüggően Pappas PG és mtsai: Clin. Infect. Dis, 2009

Az egyes antibiotikum osztályok felfedezésének dátuma Nincs újabb osztály 1987 óta World Economic Forum Report - Global risks for 2013. Carlet, J. et al. Ready for a World Without Antibiotics? The Pensieres Antibiotic Resistance Call to Action. In Antimicrobial Resistance and Infection Control, 2012, 1: 11.

Érvek az antibiotikum fejlesztés ellen • Az antibiotikum kezelések tartama általában rövid krónikus betegségek (cardiovasculáris, neuropszichiátriai, reumatológiai stb. ) • Egy szer kifejlesztése: 10 év, 1 milliárd USD • A multi-, pánrezisztens kórokozók elleni szerek tartalék (rezerv) szerek • A törzskönyvezés nehézségei

IDSA kezdeményezés • „Antibiotic Availability Task Force (AATF)” 2004 • USA-EU: Trans. Atlantic Task Force on Antibiotic Resistance (TATFAR) 2009

Az antimikróbás rezisztencia terjedésének és kontrolljának lehetőségei Tényezők Szempontok Beavatkozás A kórokozók ökológiája Evolúció Túlélőképesség Virulencia Kommenzális flóra Laboratóriumi kimutatás és identifikálás Evolúció befolyásolása Mikrobiális génexpresszió gátlása Antitestek, biológiai válasz módosítók Probiotikumok Korszerűbb gyorsdiagnosztikai tesztek Antibiotikum felírási gyakorlat Antimikróbás szerek alkalmazási gyakorlata Eltérő gyógyszerfelírási gyakorlat Képzés és szaktudás Multimodális megközelítés Populációs jellemzők Migráció, utazás és globalizáció Betegösszetétel, immunkompetencia megváltozása Gyógyszerszedési szokások és tévhitek Transzmissziós, infekciós ráta Szűrés és jobb surveillance Immunizáció; a krónikus betegségek jobb kontrollja Felvilágosító kampányok Egészségpolitika Gyógyszerpromóció szabályozása Technológiai fejlődés Finanszírozási változások Törvényalkotás, ellenőrzés Új prevenciós és kezelési lehetőségek Politika és egészségpolitika Segítség a döntéshozatalban Oktatás és felvilágosítás Kézhigiéne, óvintézkedések
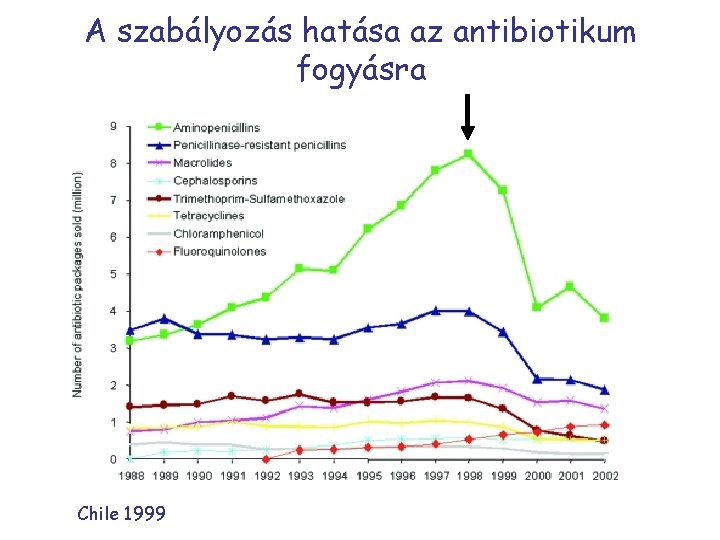
A szabályozás hatása az antibiotikum fogyásra Chile 1999
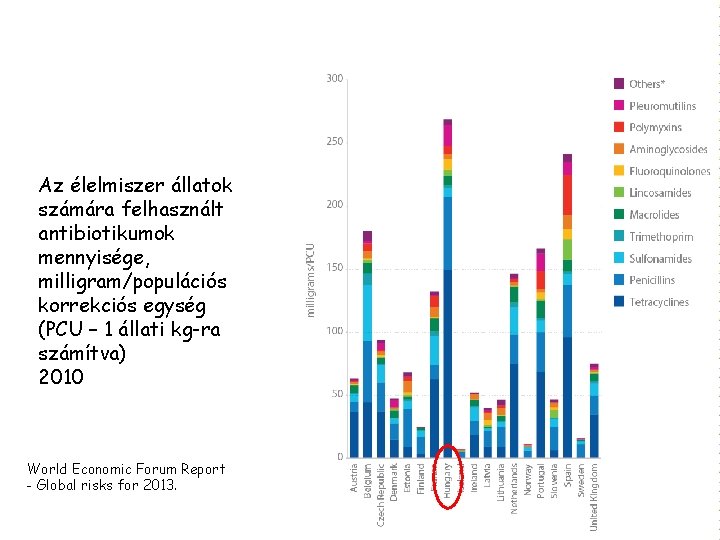
Az élelmiszer állatok számára felhasznált antibiotikumok mennyisége, milligram/populációs korrekciós egység (PCU – 1 állati kg-ra számítva) 2010 World Economic Forum Report - Global risks for 2013.


A hatékony vakcina - aktiválja az antigén bemutató sejteket → citokin felszabadulás, antigén prezentáció - a T és B sejtek stimulálása révén memóriasejtek keletkeznek - számos olyan epitópot tartalmaz, melyekre a T sejtek specifikusak → patogén variációk, MHC polimorfizmusokból adódó immunválasz különbségek áthidalhatók - az antigén sokáig perzisztál → memória B sejtek kialakulása hatékonyabb

Diagnosztika • Mikrobiológiai laboratóriumok: – FISH, DNS alapú identifikálási rendszerek (szekvenálás, kvantitatív PCR, DNS microarray) – Tömegspektrometria (MALDI-TOF) – Flow-cytometria • Képalkotó diagnosztika • Laboratóriumi – Akut fázis fehérjék • Gyorstesztek
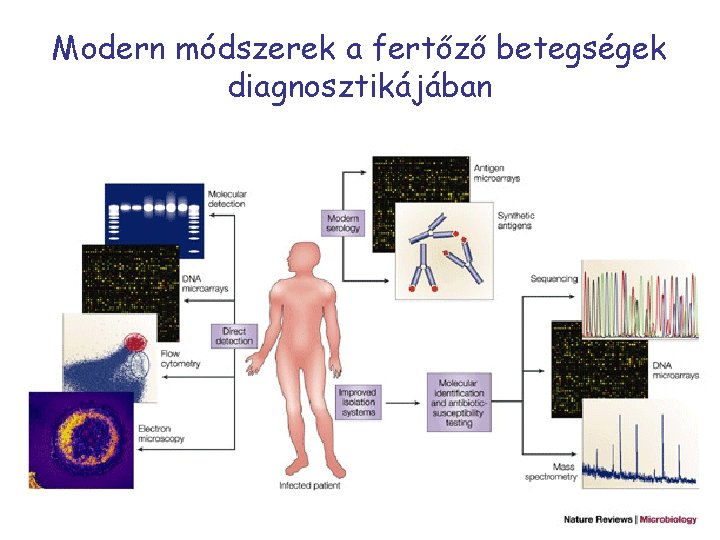
Modern módszerek a fertőző betegségek diagnosztikájában
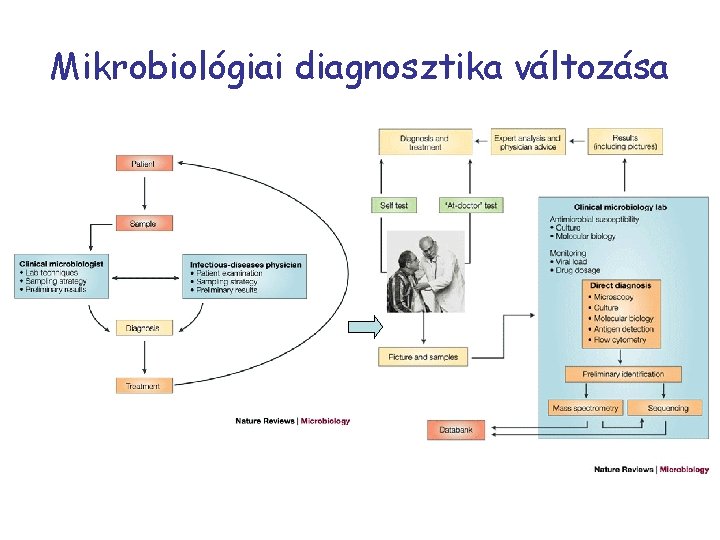
Mikrobiológiai diagnosztika változása

Biomarkerek • Objektíven mérhetők • Szenzitíven és specifikusan jellemzik a patológiás folyamatot • Jól monitorizálják a terápiás választ • Diagnózis • Rizikóbecslés • Betegség vezetése

A biomarkerekkel szembeni elvárások • Az antibiotikummal kezelendő bakteriális infekciók, szepszis korai felismerése, elkülönítése – Vírusfertőzéstől – Nem infekciós gyulladástól (pl. trauma, pancreatitis, vasculitisek, megerőltető fizikai terhelés, pszichiátriai betegségek, stressz) • Az antibiotikum kezelés időben való elkezdése – Az infekció kimenetelének javítása • A felesleges, helytelen antibiotikum használat csökkentése – Rezisztencia, költség, mellékhatások csökkentése

Akut fázis proteinek (AFP) • Szérum koncentrációváltozás gyulladásos állapotokban: > 25% • Citokinek (IL-6, IL-1ß, TNFα, IFNγ) hatására: ↑ • Pozitív AFP: CRP, se amyloid A, ferritin, fibrinogén, alfa-1 antitripszin, haptoglobin, IL-1 receptor antagonista, hepcidin stb. • Negatív AFP: albumin, transzferrin, transztiretin
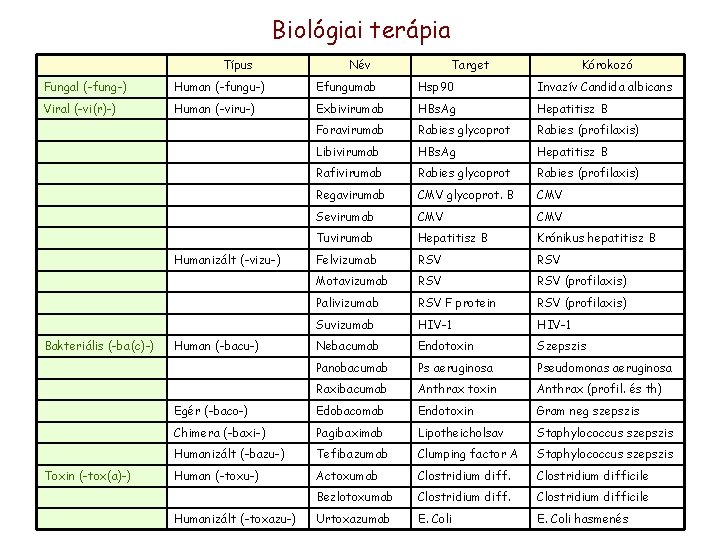
Biológiai terápia Típus Név Target Kórokozó Fungal (-fung-) Human (-fungu-) Efungumab Hsp 90 Invazív Candida albicans Viral (-vi(r)-) Human (-viru-) Exbivirumab HBs. Ag Hepatitisz B Foravirumab Rabies glycoprot Rabies (profilaxis) Libivirumab HBs. Ag Hepatitisz B Rafivirumab Rabies glycoprot Rabies (profilaxis) Regavirumab CMV glycoprot. B CMV Sevirumab CMV Tuvirumab Hepatitisz B Krónikus hepatitisz B Felvizumab RSV Motavizumab RSV (profilaxis) Palivizumab RSV F protein RSV (profilaxis) Suvizumab HIV-1 Nebacumab Endotoxin Szepszis Panobacumab Ps aeruginosa Pseudomonas aeruginosa Raxibacumab Anthrax toxin Anthrax (profil. és th) Egér (-baco-) Edobacomab Endotoxin Gram neg szepszis Chimera (-baxi-) Pagibaximab Lipotheicholsav Staphylococcus szepszis Humanizált (-bazu-) Tefibazumab Clumping factor A Staphylococcus szepszis Human (-toxu-) Actoxumab Clostridium difficile Bezlotoxumab Clostridium difficile Urtoxazumab E. Coli hasmenés Humanizált (-vizu-) Bakteriális (-ba(c)-) Toxin (-tox(a)-) Human (-bacu-) Humanizált (-toxazu-)

Antibiotikum politika • Cél: – hatásos antibiotikum kezelés: gyógyszerválasztás, dózis, spektrumszűkítés, kezelés tartama – antibiotikum használat mérséklése – rezisztencia késleltetése • Eszköz: – képzés, irányelvek, kombinációs kezelés, dózis optimalizáció, orális kezelés… • Stratégia: – antibiotikum, infekció kontroll, gyógyszerterápiás bizottság – helyzetértékelés, tervezés, kivitelezés, ellenőrzés, értékelés

A korszerű infektológia jellemzői • Rendkívül szerteágazó, multidisciplináris jellegű tudományág (~ immunológia, genetika) • Korszerű infektológia integratív tudomány: pl. belgyógyászat, mikrobiológia, kórélettan, gyógyszertan, immunológia, epidemiológia, vakcinológia, infekció-kontroll és antibiotikum politika stb. • Óriási fejlődés a diagnosztikában, terápiában – a szemléletben
- Slides: 61