MODELO ATOMICO DE THOMSON CAMI ALVAREZ FRANCO MACHIN












- Slides: 16

MODELO ATOMICO DE THOMSON CAMI ALVAREZ FRANCO MACHIN RODRIGO MONTERO MANUEL CIAVAGLIA GUZMAN PORLEY

SU VIDA… Thomson nació en 1856 en Cheetham Hill, un distrito de Mánchester en Inglaterra, y tenía ascendencia escocesa. En 1870 estudió ingeniería en el Owens Collage, hoy parte de la Universidad de Mánchester, y se trasladó al Trinity Collage de Cambridge en 1876. En 1880, obtuvo su licenciatura en Matemáticas (Segunda Wrangler y segundo premio Smith) y MA (obteniendo el Premio Adams) en 1883. En 1884 se convirtió en profesor de Física en Cavendish. Uno de sus alumnos fue Ernest Rutherford, quien más tarde sería su sucesor en el puesto.

EL… Fecha de nacimiento: 18 de diciembre de 1856, Mánchester, Reino Unido Fecha de la muerte: 30 de agosto de 1940, Cambridge, Reino Unido

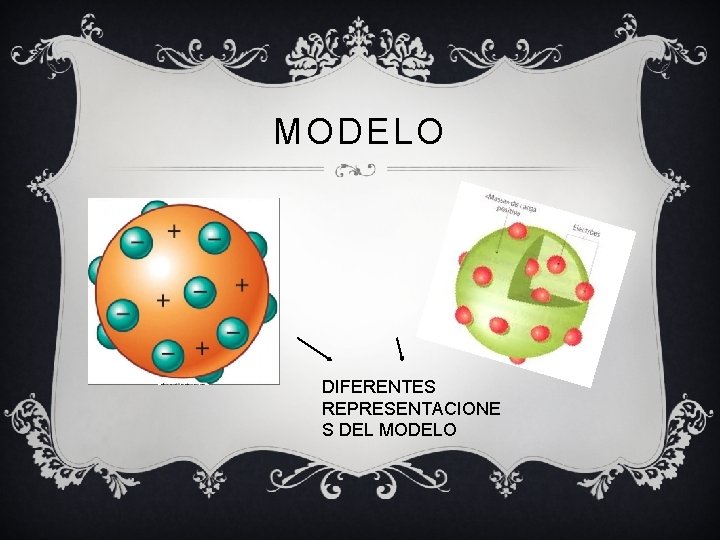
SU MODELO v El modelo atómico de Thomson es una teoría sobre la estructura atómica propuesta en 1904 por Joseph John Thomson, quien descubrió el electrón 1 en 1898, mucho antes del descubrimiento del protón y del neutrón. En dicho modelo, el átomo está compuesto por electrones de carga negativa en un átomo positivo, como un pudin de pasas. Postulaba que los electrones se distribuían uniformemente en el interior del átomo suspendidos en una nube de carga positiva. El átomo se consideraba como una esfera con carga positiva con electrones repartidos como pequeños gránulos. La herramienta principal con la que contó Thomson para su modelo atómico fue la electricidad.

MODELO DIFERENTES REPRESENTACIONE S DEL MODELO

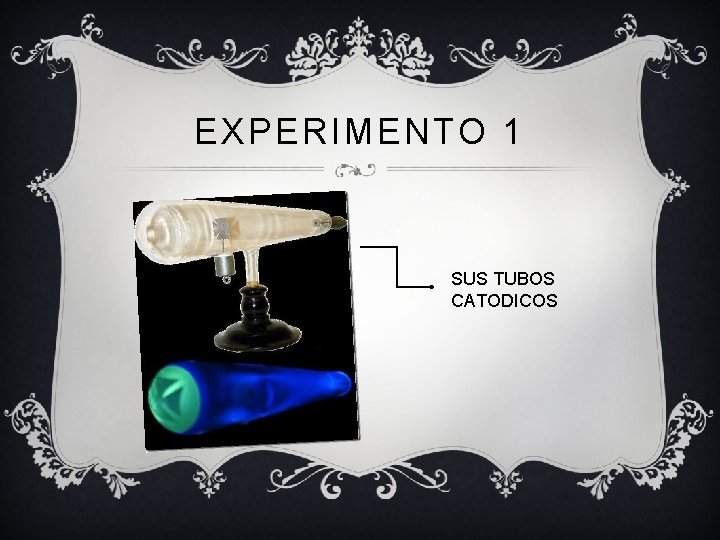
EXPERIMENTO 1 v Thomson investigó si podrían ser separadas las cargas negativas de los rayos catódicos y utiliza un medio el del magnetismo. v Para este experimento construyo un tubo de rayos catódicos el cual al final del tubo termina en dos cilindros con ranuras, las ranuras fueron conectadas a su vez a un electrómetro. v Con este método Thomson descubre que cuando los rayos son desviados magnéticamente de tal forma que no puedan entrar en las hendiduras, el electrómetro marca al registrar poca carga. v Esto llevo a Thomson a la conclusión que la carga negativa es inseparable de los rayos.

EXPERIMENTO 1 SUS TUBOS CATODICOS

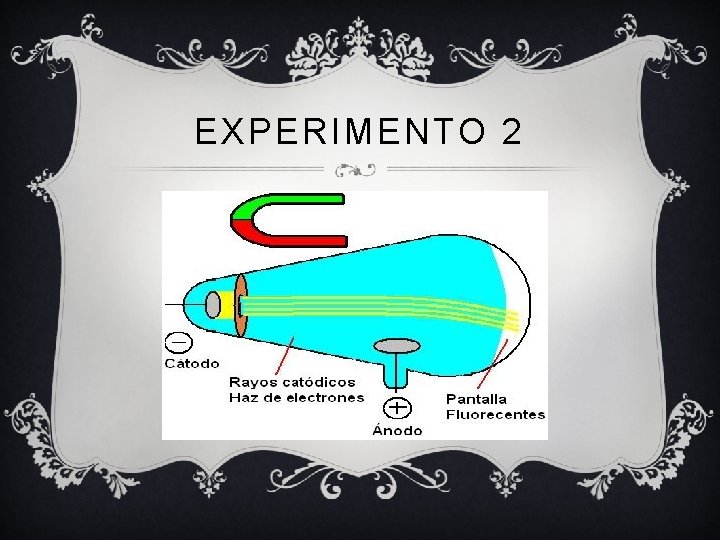
EXPERIMENTO 2 v Para este segundo experimento, JJ Thomson construye un tubo de rayos catódicos, logrando un vacío casi perfecto, en uno de sus extremos lo recubre con pintura fosforescente. v La intención del este experimento era investigar si estos rayos podían ser desviados con un campo eléctrico, se conocía que en anteriores experimentos no se habían observado este fenómeno (esto es muy característico de las partículas con carga). v Con la creación de este tubo en el que en uno de sus extremos estaba recubierto con pintura fosforescente, Thomson descubre que muchos rayos si se podían doblar con la influencia de un campo magnetizado.

EXPERIMENTO 2

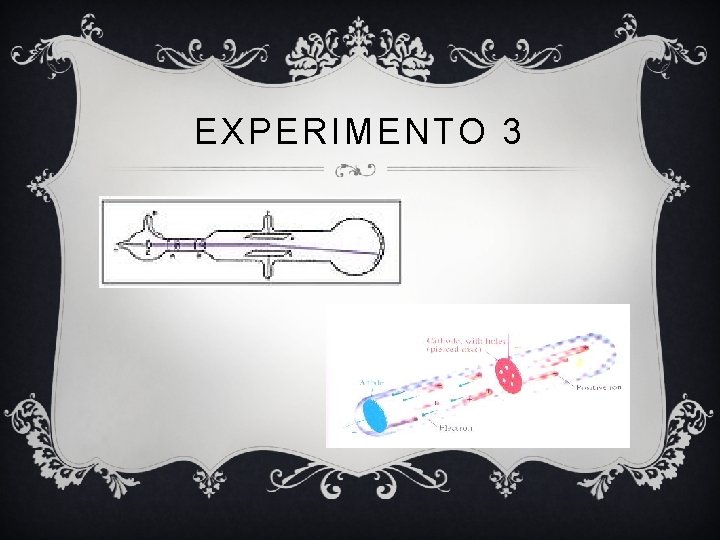
EXPERIMENTO 3 v Para el tercer experimento, Thomson fundamento la relación que hay entre la masa de los rayos catódicos y la carga, para esto mide la cantidad que se desvía por un campo magnético y cuanta cantidad de carga de energía contenida. v La relación masa/carga que encuentra es de un millar de veces superior a la que contiene el ion de Hidrógeno, esto indica que bien las partículas deben ser más livianas o con mucha más carga. v Aquí Thomson toma una posición audaz: Thomson, a los rayos catódicos que estaban cargados por partículas les llamó “corpúsculos” dichos corpúsculos se originaban dentro de los átomos de los electrodos, a lo que esto significaba, que los átomos deben ser divisibles, imagina “un mar” totalmente repleto de cargas positivas en estos corpúsculos en el átomo, es por esto que se le llama y conoce con el nombre de budín de pasas al modelo de Thomson.

v El premio novel de física lo obtiene en 1906, gracias al trabajo que realizo sobre la conducción de la electricidad a través de los gases. v La forma de su explicación de que el átomo esta formado por un núcleo unido y compacto y que en su exterior la denomina como corteza, deja mucha puertas abiertas tanto para Ernest Rutherford o Niels Bohr, quienes continúan con esta investigación dando luz y planteando otras teorías para los átomos y las partes diferenciadas

EXPERIMENTO 3

EJERCICIOS PAGINA 1 v 1) _ _ _ _ v 1) El átomo está compuesto por electrones de carga negativa en un átomo positivo. . . v 2) _ _ _ _ v Demostró que dentro de los átomos hay unas partículas diminutas, con carga eléctrica negativa. . . v 3) _ _ _ _

EJERCIOS PAGINA 2 v 3) Afirma que la materia está compuesta por pequeñas partículas llamadas átomos. . v 4) _ _ _ v 4) Partícula muy pequeña que no se puede dividir. . .

HAZ LA SOPA DE LETRA…

PAGINA DE LA CUAL SE EXTRAJERON LA INFORMACION v http: //es. wikipedia. org/wiki/Joseph_John_Thomson v http: //quimicalibre. com/modelo-atomico-de-thomson/ v www. google. com v http: //www. educaplay. com/es/recursoseducativos/560905/ modelos_atomicos. htm