MODELO ATOMICO DE BORH CONTINUACIN CAPITULO No 4

MODELO ATOMICO DE BORH CONTINUACIÓN CAPITULO No 4

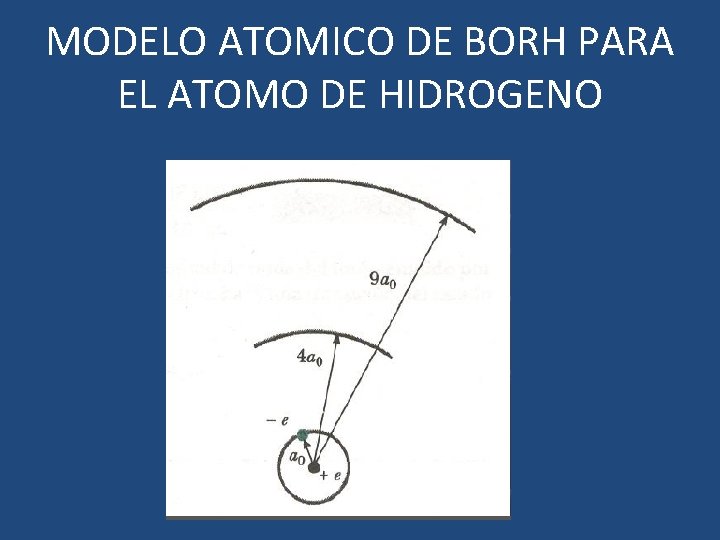
MODELO ATOMICO DE BORH PARA EL ATOMO DE HIDROGENO

En 1913 Niels Bohr, quien trabajaba con Rutherford, tuvo la oportunidad de leer la teoría de la radiación del cuerpo negro de Planck. Consideró que la frecuencia de oscilación de un electrón es similar a la frecuencia del oscilador de Planck. Por lo tanto aplicando esto formuló los siguientes postulados:

POSTULADOS DE BORH PRIMER POSTULADO El átomo de Hidrogeno está constituido por un núcleo con carga +Ze y un electrón ligado a él mediante fuerza electrostática SEGUNDO POSTULADO Existe para el átomo un conjunto discreto de estados energéticos donde el electrón gira alrededor del núcleo en orbitas circulares, sin emitir energía radiante. (estados estacionarios

TERCER POSTULADO Son solo posibles las orbitas en las cuales el electrón tiene una momento angular que es múltiplo de (hache barra) constante de Planck dividida por 2π Así el electrón solo puede ubicarse en ciertas orbitas cuyos radios están determinados por la condición del tercer postulado
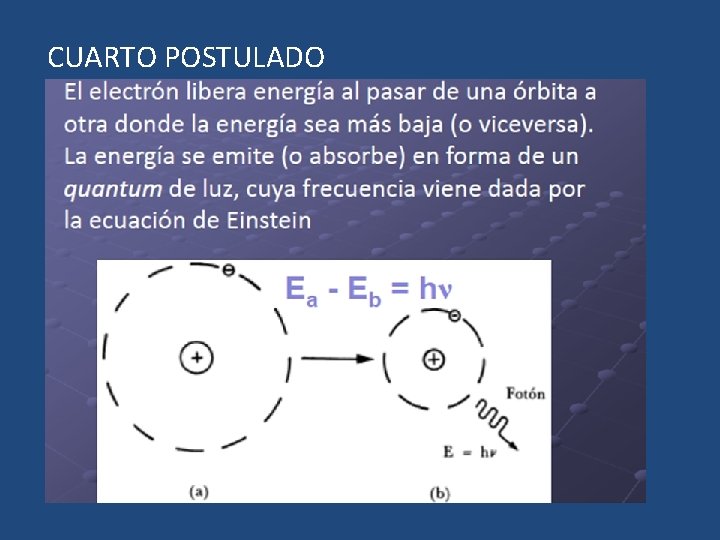
CUARTO POSTULADO
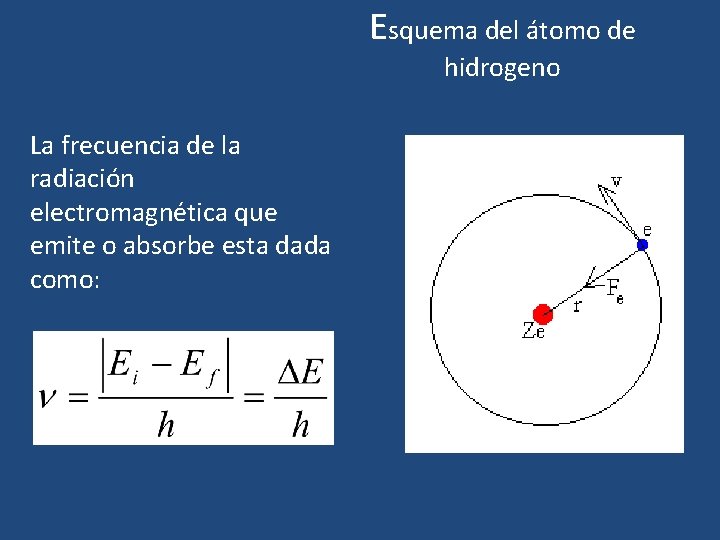
Esquema del átomo de hidrogeno La frecuencia de la radiación electromagnética que emite o absorbe esta dada como:

Consideremos un electrón que gira alrededor de un núcleo +Ze, el electrón se encuentra en la n-sima orbita permitida de radio rn y la orbita es estable cuando la fuerza centrípeta es igual a la fuerza eléctrica. Esto es: De la ecuación del tercer postulado y la inmediatamente anterior s e obtienen la velocidad y el radio de las orbitas permitidas por el electrón

Donde a 0 se denomina radio de Bohr (radio de la primera orbita n= 1) y su valor es de 0, 53 A° para el átomo de Hidrogeno. La energía total del electrón es igual a la suma de su energía cinética y su energía potencial eléctrica; entonces: Reemplazando en esta ecuación la velocidad y el radio hallados anteriormente se obtiene:

La ecuación anterior nos permite conocer la energía del electrón en todas sus orbitas permitidas, ya que el núcleo se ha considerado en reposo, la energía anterior es la energía de cualquiera de los estados permitidos para el átomo. Adicionalmente nos damos cuenta que la energía está cuantizada siendo n el número cuántico correspondiente. El signo negativo nos indica que el electrón está ligado al núcleo. Cuando el número cuántico n es infinito la energía total del electrón es nula. A partir de ese momento los electrones son libres de moverse con cualquier energía. Cuando el número cuántico es igual a la unidad, el átomo se encuentra en su estado base de energía denominado estado base o fundamental
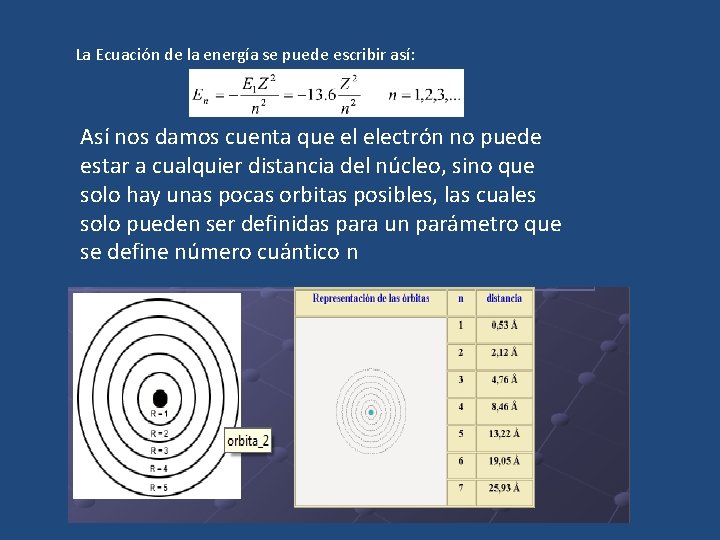
La Ecuación de la energía se puede escribir así: Así nos damos cuenta que el electrón no puede estar a cualquier distancia del núcleo, sino que solo hay unas pocas orbitas posibles, las cuales solo pueden ser definidas para un parámetro que se define número cuántico n
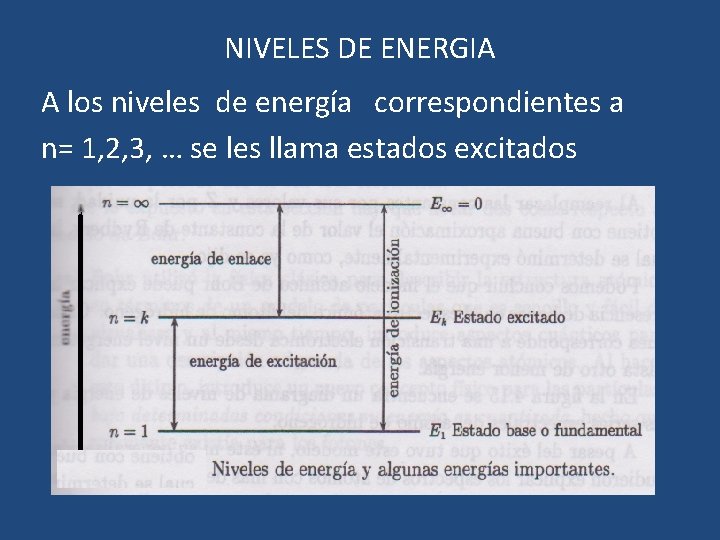
NIVELES DE ENERGIA A los niveles de energía correspondientes a n= 1, 2, 3, … se les llama estados excitados

• La diferencia de energía entre un estado excitado con n=α y el estado base, Eα- E 1 es la energía que debo suministrar al átomo para desprender de él, un electrón. Esta energía se llama energía de ionización. • Si el electrón se encuentra en K, estado excitado la energía que debe suministrarse es Eα- Ek , se denomina energía de enlace. Finalmente la diferencia de energía entre el estado base y un excitado es Ek- E 1, se denomina energía de excitación

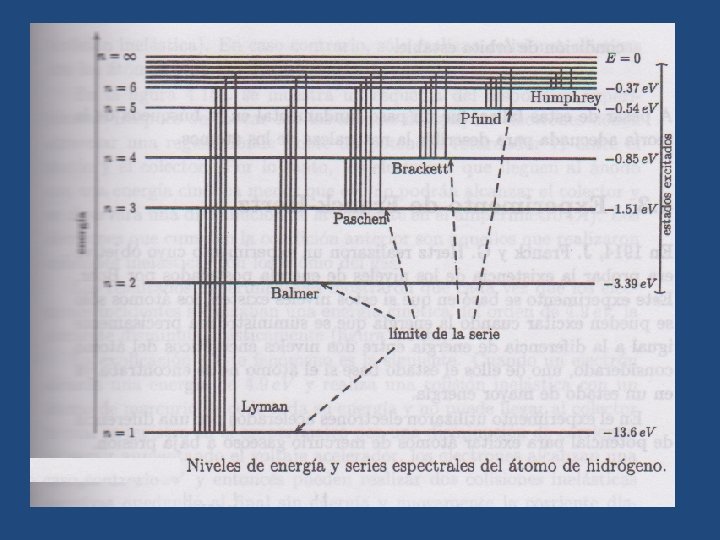
Se puede hallar la frecuencia con la cual el electrón salta de una orbita mayor a otra menor, de acuerdo a los postulados de Bohr Si expresamos la frecuencia en función de la longitud de onda la relación anterior se transforma en:

De la ecuación anterior se puede reemplazar el valor de las constantes y el valor de Z por la unidad y se obtendrá el valor de la constante de Rydberg, que se había obtenido experimentalmente en la espectroscopia. Podemos concluir que Bohr explica la presencia de líneas en el espectro atómico del átomo de Hidrogeno, cada línea corresponde a una transición electrónica desde un nivel de energía hasta otro de menor energía Simulador: http: //www. portaleso. com/portaleso/trabajos/fisicayquimi/lamateria/modelo s_atomicos_sin_ejerc. . swf http: //Www. deciencias. net/simulaciones/quimica/atomo/modelobohr. htm

Siendo RH igual a: Y teniendo en cuenta que Z=1 Obtenemos la ecuación a demostrar


Problema No 4 • Un haz de electrones incide sobre una muestra de hidrogeno gaseoso ¿A qué diferencia de potencial se deben acelerar los electrones para que los átomos de hidrogeno al regresar a su estado base emitan durante el proceso la primera línea de la serie Balmer? Solución: la formula de Balmer es:


Ejercicio No 7 •
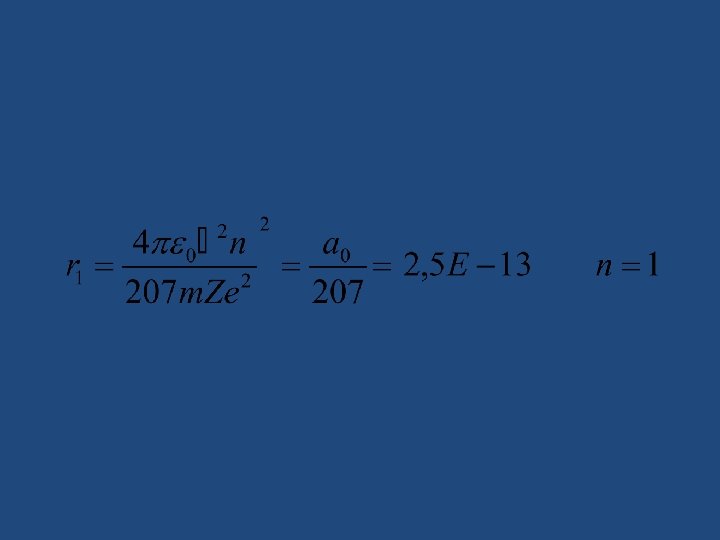

PREGUNTAS DEL MODELO DEL ATOMO DE BORH • ¿CUALES SON LOS POSTULADOS DEL MODELO DEL ATOMO DE BORH? • ¿QUÉ FENOMENOS LOGRA EXPLICAR? • ¿QUÉ REQUISITOS DEBE TENER UN ELECTRON PARA SALTAR O BAJAR A OTROS NIVELES DE ENERGIA? • ¿CUALES FUERON LOS GRANDES ACIERTOS DE ESTE MODELO? • ¿CUALES FUERON LAS FALENCIAS O MEJOR LO QUE NO LOGRO EXPLICAR ESTE MODELO?
- Slides: 24