Modelo Atmico de Bohr El espectro de un

Modelo Atómico de Bohr El espectro de un elemento es un diagrama de frecuencias específicas de la luz que los atómos del mismo pueden emitir o absorber. Éste se puede observar mediante un prisma o una retícula de difracción, mostrándose líneas brillantes para ciertos colores determinados, correspondientes a las frecuencias de luz que emiten los átomos de dicho elemento. Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr Desde antes de los estudios realizados por Thomson, Rutherford y Bohr, con relación a la estructura átomica, ya se sabía que cada elemento tenía un espectro característico. Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr En 1884 J. Balmer encontró una fórmula empírica mediante la cual se podían expresar las frecuencias de las catorce líneas de hidrógeno entonces conocidas, puestas más tarde por J. R. Rydberg en función de las longitudes de onda. Donde RH es la constante de Rydberg con valor aproximado de 10967757. 6 ± 1. 2 [m-1] Fís. Edgar Raymundo López Téllez
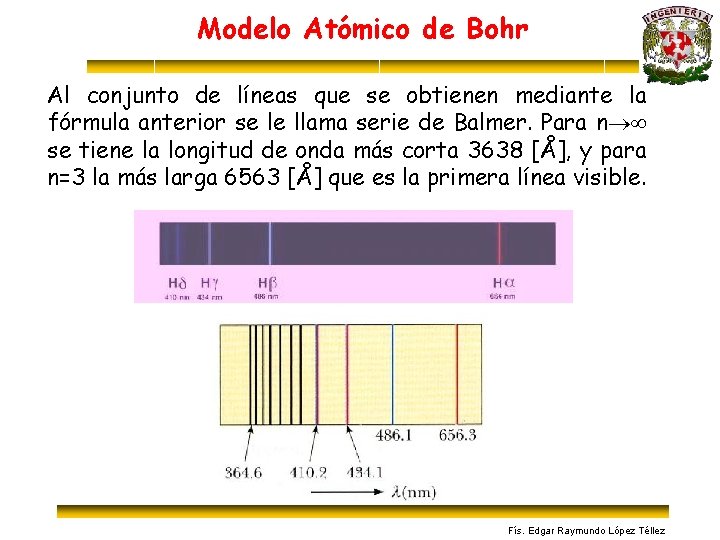
Modelo Atómico de Bohr Al conjunto de líneas que se obtienen mediante la fórmula anterior se le llama serie de Balmer. Para n se tiene la longitud de onda más corta 3638 [Å], y para n=3 la más larga 6563 [Å] que es la primera línea visible. Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr Balmer dedujo la siguiente fórmula general Con m tomando valores fijos y n m + 1, lo que genera la las series conocidas: m=1 n 2 En el ultravioleta Serie de Lyman m=3 n 4 En el cercano infrarrojo Serie de Pashen m=4 n 5 En el infrarrojo Serie de Brackett m=5 n 6 En el lejano infrarrojo Serie de Pfund Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr El problema de la estructura de los átomos se manifestó al comparar la estabilidad de los átomos y los espectros atómicos discretos con las predicciones de la mecánica y la electrodinámica clásicas, ya que según éstas, un electrón en el átomo describiría una espiral colapsándose con el núcleo en un tiempo del orden de un cienmillonésimo de segundo y emitiendo radiación con un espectro continuo de frecuencias. Fís. Edgar Raymundo López Téllez
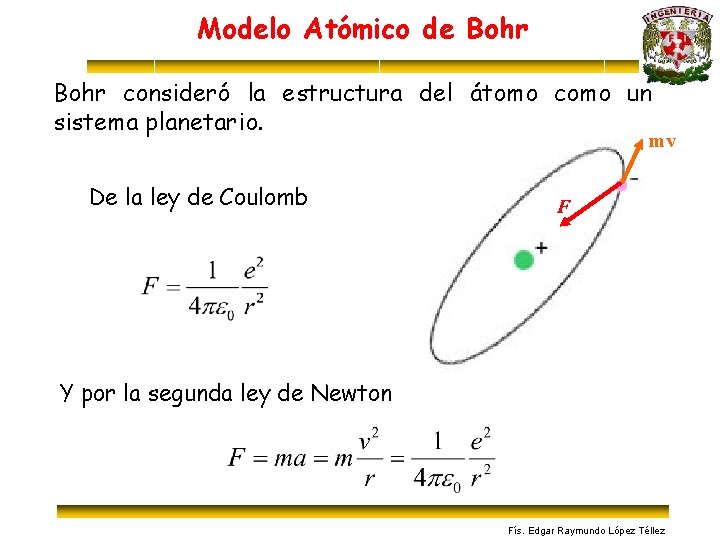
Modelo Atómico de Bohr consideró la estructura del átomo como un sistema planetario. mv De la ley de Coulomb F Y por la segunda ley de Newton Fís. Edgar Raymundo López Téllez
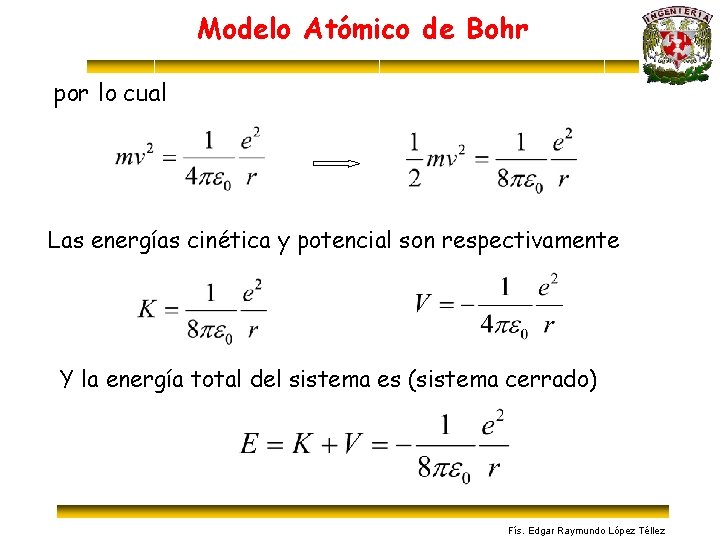
Modelo Atómico de Bohr por lo cual Las energías cinética y potencial son respectivamente Y la energía total del sistema es (sistema cerrado) Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr Dicha energía es la mínima para sacar al electrón del átomo. Experimentalmente se tiene que la energía de ionización es aproximadamente 13. 6 [e. V], teniendo entonces un valor para el radio del átomo de hidrógeno de (radio de Bohr) Teniendo para la frecuencia Y así Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr Los resultados concuerdan con los experimentos, pero entonces se debería dar una radiación electromagnética de forma continua. El electrón tiene un aceleración, así la frecuencia de radiación emitida debería ser igual a la frecuencia de revolución y la energía total del átomo debería disminuir, y la frecuencia de rotación debería aumentar, lo cual provocaría un colapso del electrón hacia el núcleo. Entonces Bohr concluyó que las leyes clásicas no eran aplicables a los fenómenos atómicos. Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr Para corregir las fallas del modelo planetario, Bohr introdujo dos suposiciones: Postulado de estados estacionarios: Se considera que los átomos existen en estados con energía bien definida y que la emisión u absorción de radiación están asociados con transiciones entre dos de esos estados estacionarios. Postulado o relación de frecuencias: La frecuencia de emisión o absorción es igual a la diferencia de las energías de los estados estacionarios involucrados dividida entre la constante de Planck, es decir, Fís. Edgar Raymundo López Téllez
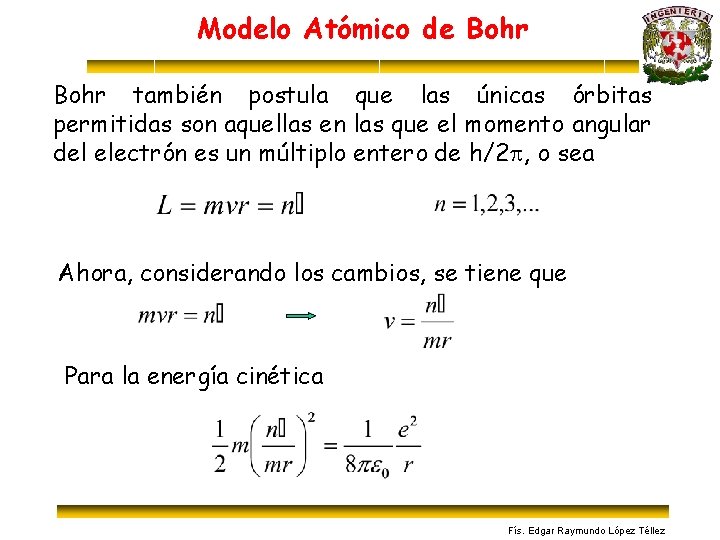
Modelo Atómico de Bohr también postula que las únicas órbitas permitidas son aquellas en las que el momento angular del electrón es un múltiplo entero de h/2 p, o sea Ahora, considerando los cambios, se tiene que Para la energía cinética Fís. Edgar Raymundo López Téllez
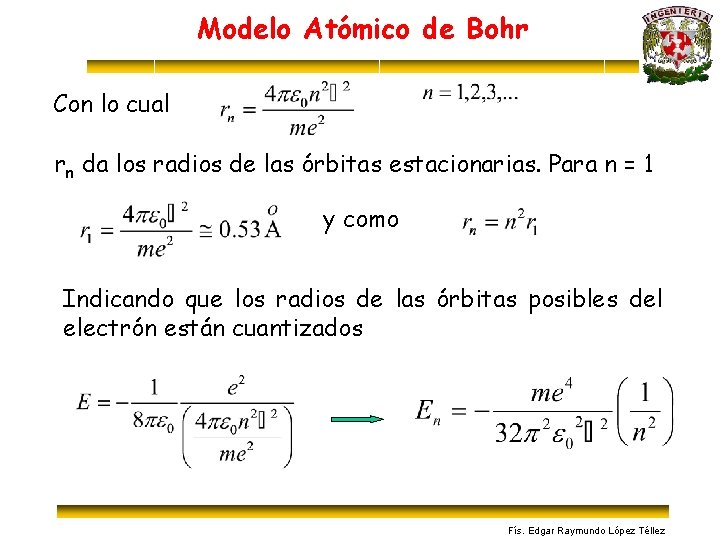
Modelo Atómico de Bohr Con lo cual rn da los radios de las órbitas estacionarias. Para n = 1 y como Indicando que los radios de las órbitas posibles del electrón están cuantizados Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr Para el átomo de hidrógeno Así la energía del estado base es Fís. Edgar Raymundo López Téllez
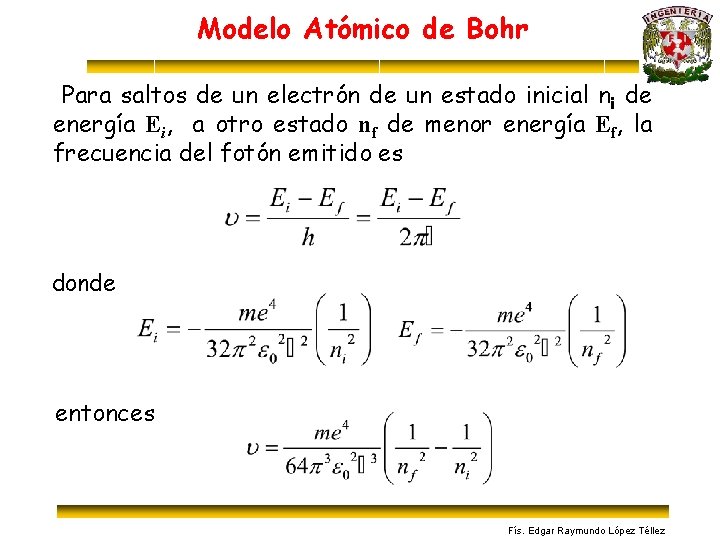
Modelo Atómico de Bohr Para saltos de un electrón de un estado inicial ni de energía Ei, a otro estado nf de menor energía Ef, la frecuencia del fotón emitido es donde entonces Fís. Edgar Raymundo López Téllez
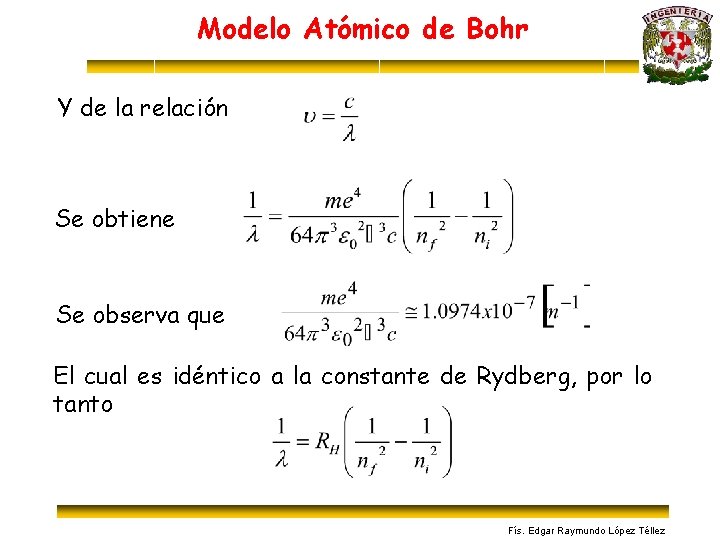
Modelo Atómico de Bohr Y de la relación Se obtiene Se observa que El cual es idéntico a la constante de Rydberg, por lo tanto Fís. Edgar Raymundo López Téllez
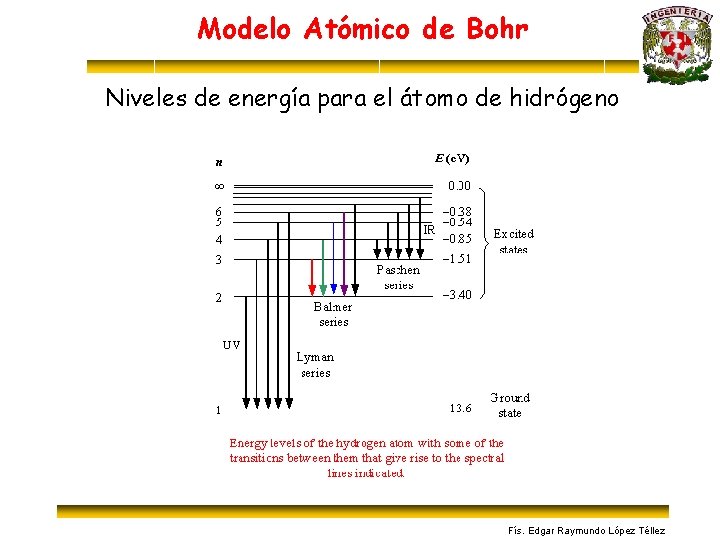
Modelo Atómico de Bohr Niveles de energía para el átomo de hidrógeno Fís. Edgar Raymundo López Téllez

Modelo Atómico de Bohr En resumen se tiene que - Se definen los radios atómicos - Se definen las energías de los estados estacionarios - Se reproduce la serie de Balmer incluyendo el valor numérico de la constante de Rydberg. Fís. Edgar Raymundo López Téllez
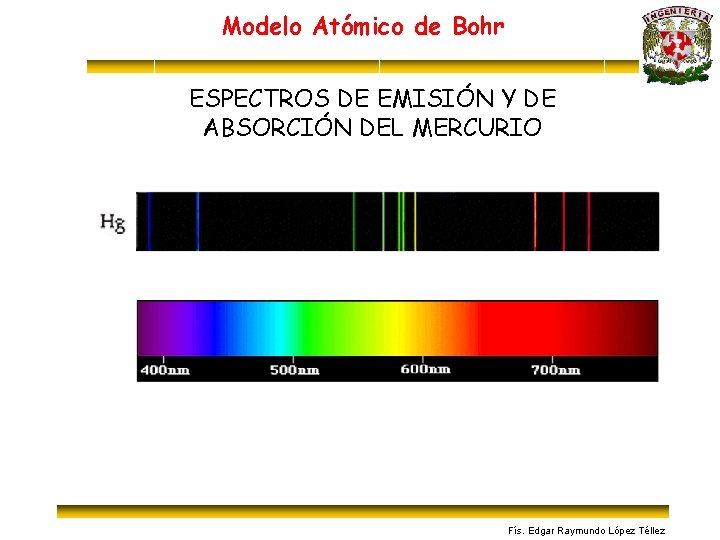
Modelo Atómico de Bohr ESPECTROS DE EMISIÓN Y DE ABSORCIÓN DEL MERCURIO Fís. Edgar Raymundo López Téllez
- Slides: 19