Mningites bactriennes en zone tropicale Docteur SAVINIMUREAU Hlne

Méningites bactériennes en zone tropicale Docteur SAVINI-MUREAU Hélène Service de pathologie infectieuse et tropicale HIA Laveran
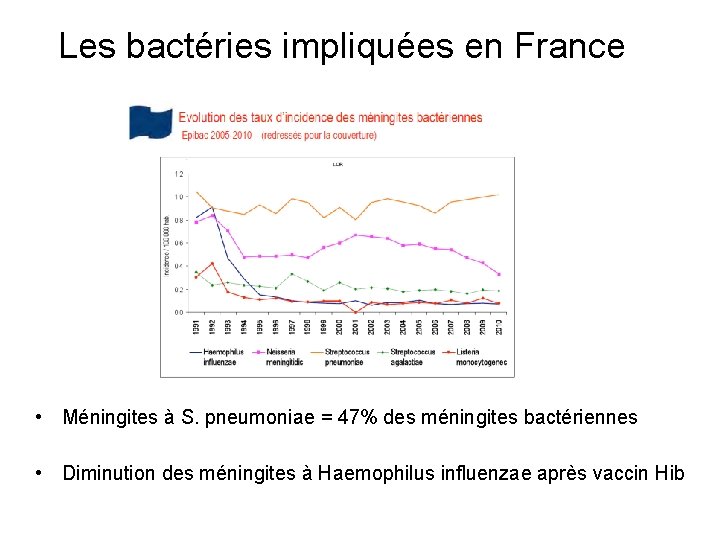
Les bactéries impliquées en France 1500 cas par an • Méningites à S. pneumoniae = 47% des méningites bactériennes • Diminution des méningites à Haemophilus influenzae après vaccin Hib INVS
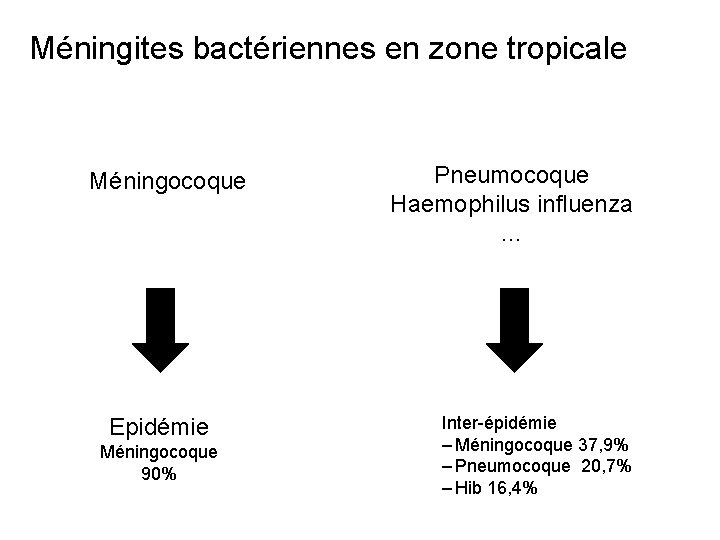
Méningites bactériennes en zone tropicale Méningocoque Epidémie Méningocoque 90% Pneumocoque Haemophilus influenza … Inter-épidémie – Méningocoque 37, 9% – Pneumocoque 20, 7% – Hib 16, 4%
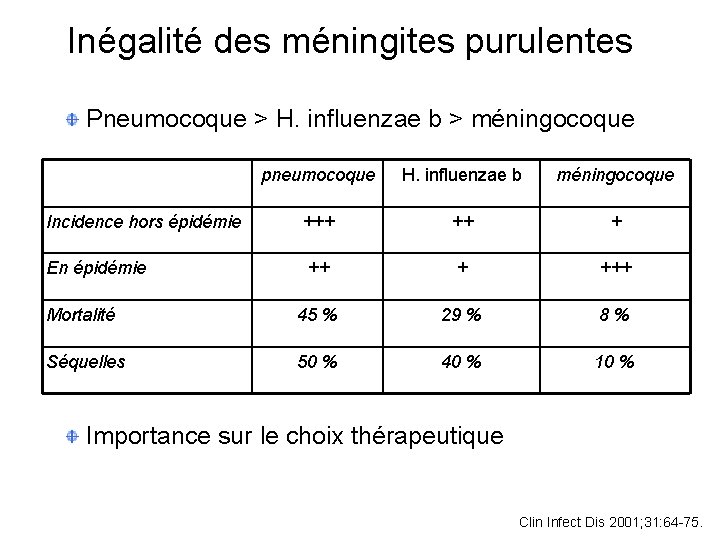
Inégalité des méningites purulentes Pneumocoque > H. influenzae b > méningocoque pneumocoque H. influenzae b méningocoque Incidence hors épidémie +++ ++ + En épidémie ++ + +++ Mortalité 45 % 29 % 8% Séquelles 50 % 40 % 10 % Importance sur le choix thérapeutique Clin Infect Dis 2001; 31: 64 -75.
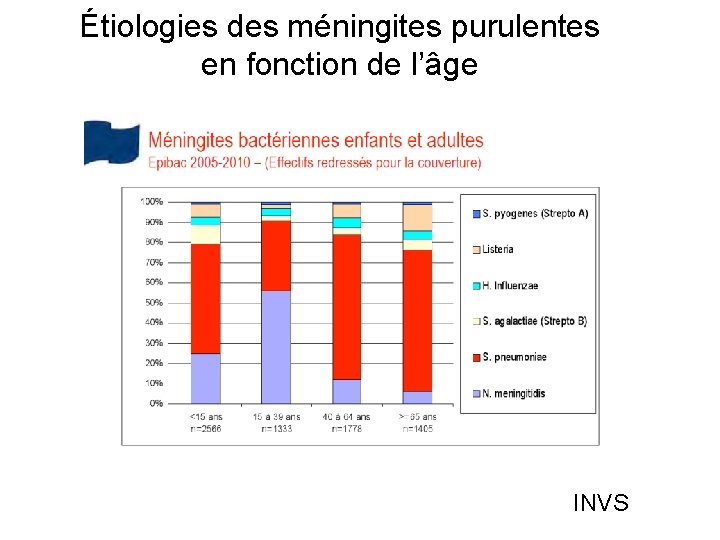
Étiologies des méningites purulentes en fonction de l’âge INVS

Méningites à méningocoque
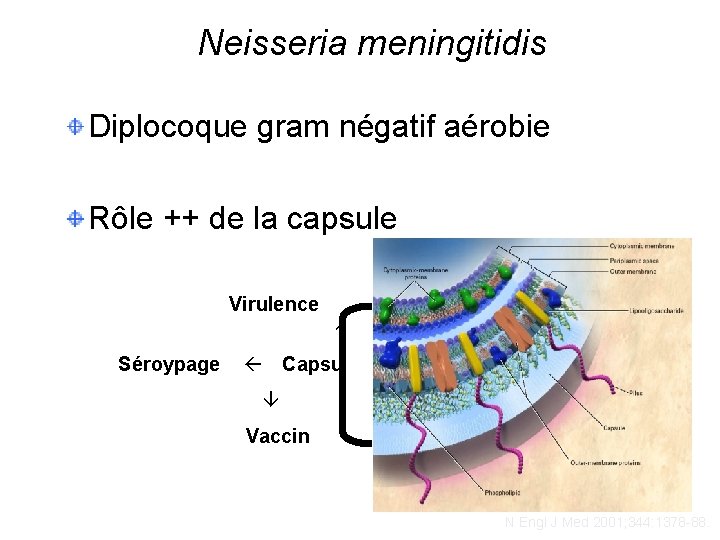
Neisseria meningitidis Diplocoque gram négatif aérobie Rôle ++ de la capsule Virulence Séroypage Capsule Vaccin N Engl J Med 2001; 344: 1378 -88.

Cycle Réservoir humain – Pharynx Transmission interhumaine – Baiser > gouttelettes Dissémination interhumaine – Promiscuité (cas intra–familial RR x 400 -800) – Épidémies
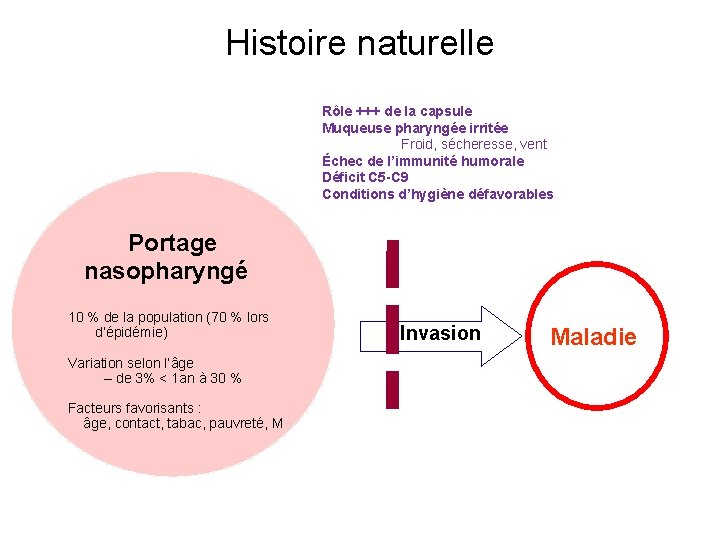
Histoire naturelle Rôle +++ de la capsule Muqueuse pharyngée irritée Froid, sécheresse, vent Échec de l’immunité humorale Déficit C 5 -C 9 Conditions d’hygiène défavorables Portage nasopharyngé 10 % de la population (70 % lors d’épidémie) Variation selon l’âge – de 3% < 1 an à 30 % Facteurs favorisants : âge, contact, tabac, pauvreté, M Invasion Maladie

Nosologie Infection invasive à méningocoque = méningococcie = Méningite à méningocoque = méningite cérébrospinale. MCS) Bactériémie à méningocoque = méningococcémie
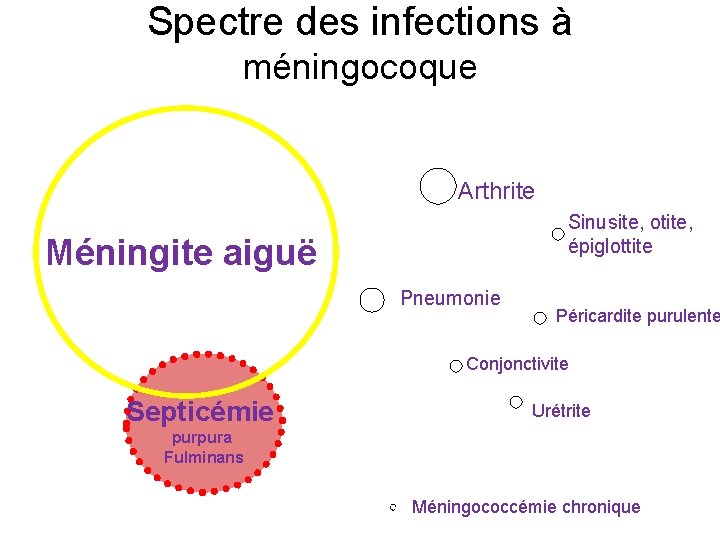
Spectre des infections à méningocoque Arthrite Sinusite, otite, épiglottite Méningite aiguë Pneumonie Péricardite purulente Conjonctivite Septicémie Urétrite purpura Fulminans Méningococcémie chronique

Arguments en faveur du méningocoque Début brutal, syndrome méningé franc Examen ORL normal Signes de localisation rares Purpura Arthralgies Hyperleucocytose sanguine

Points positifs du méningocoque • Agent pathogène fragile • Sensibilité aux antibiotiques conservée • Bonne réponse aux antibiotiques • Même en quelques jours • Existence d’antibiotiques pertinents pour la MCS • Forte puissance bactéricide sur N. m. dans le LCR • Administration IM

Protocole en France • Purpura fulminans (au moins une lésion > 3 mm) • En urgence avant PL, faire en IVL ou en IM • ceftriaxone : 50 mg/kg enfant, 1 -2 g adulte, • ou amoxicilline : 25 mg/kg enfant, 1 g adulte, puis … • Méningite à méningocoque • Ceftriaxone : 75 mg/kg/j (1 ou 2 IV/j) • Ou cefotaxime : : 200 mg/kg/j en 4 perfusions IV • Durée : > 4 jours • • Alternatives • Corticothérapie Pénicilline G (400000 UI/kg/j), amoxicilline, chloramphénicol

Évolution Le plus souvent favorable sous traitement Séquelles : 10 % (hypoacousie, paralysie, déficit intellectuel) Mortalité 10 -15 % souvent précoce ( avant ou rapidement après l ’admission ou par purpura fulminans)
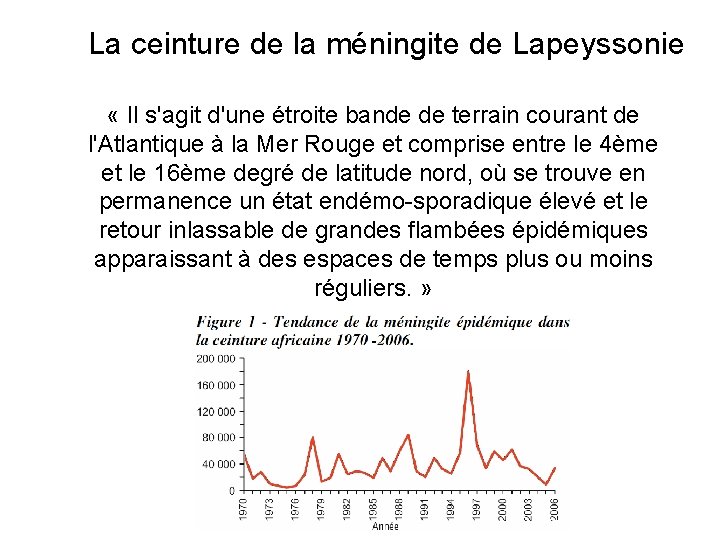
La ceinture de la méningite de Lapeyssonie « Il s'agit d'une étroite bande de terrain courant de l'Atlantique à la Mer Rouge et comprise entre le 4ème et le 16ème degré de latitude nord, où se trouve en permanence un état endémo-sporadique élevé et le retour inlassable de grandes flambées épidémiques apparaissant à des espaces de temps plus ou moins réguliers. » INVS international. 2007
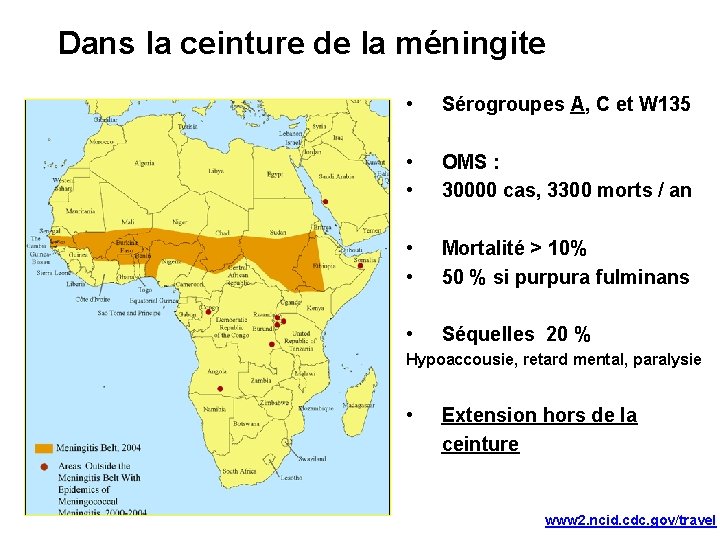
Dans la ceinture de la méningite • Sérogroupes A, C et W 135 • • OMS : 30000 cas, 3300 morts / an • • Mortalité > 10% 50 % si purpura fulminans • Séquelles 20 % Hypoaccousie, retard mental, paralysie • Extension hors de la ceinture www 2. ncid. cdc. gov/travel
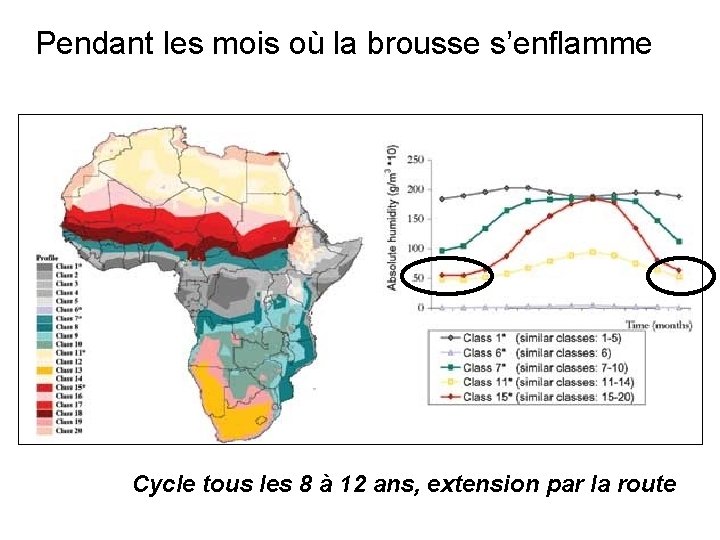
Pendant les mois où la brousse s’enflamme Cycle tous les 8 à 12 ans, extension par la route
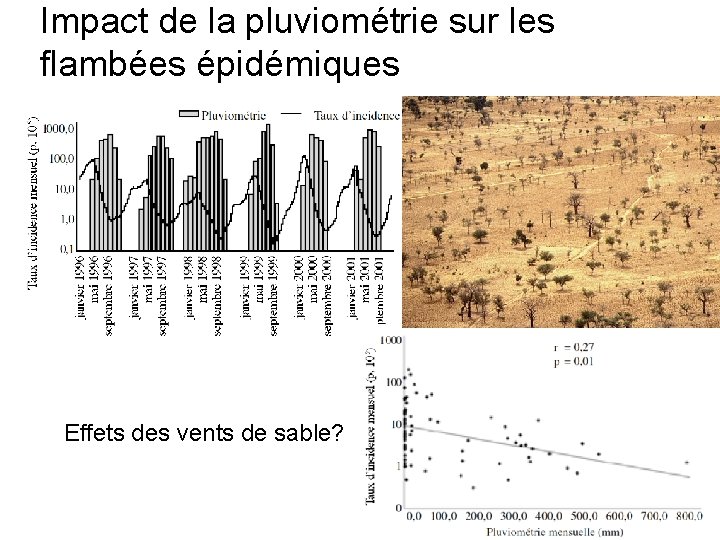
Impact de la pluviométrie sur les flambées épidémiques Effets des vents de sable? Jackou-Boulama et al. Méd Trop. 2005
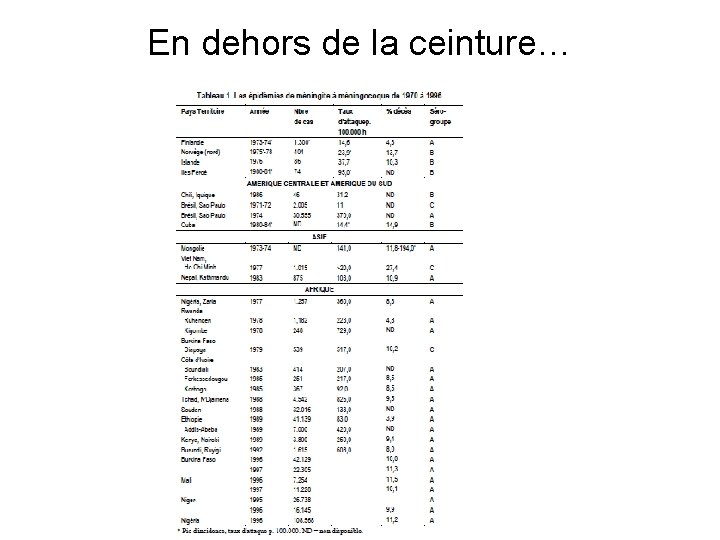
En dehors de la ceinture…

Méningites non-méningocciques

Pneumocoque : Streptococcus pneumoniae CG+ : diplocoque (courte chainette possible) – Plusieurs sérotypes Réservoir humain Sphère respiratoire – Influence climatique – Portage foyer ou passage hématogène Résistance en hausse – Pénicilline, macrolides

Arguments en faveur du pneumocoque Terrain favorisant – alcoolisme chronique, antécédent de traumatisme crânien, chirurgie de la base du crâne, asplénie (drépanocytose), infection VIH, myélome Début brutal, syndrome méningé franc Présence de signes neurologiques graves – coma, convulsions Purpura possible Présence d’un foyer associé : otite, sinusite, pneumopathie Hyperleucocytose sanguine, LCR franc

Méningite à pneumocoque, évolution Souvent favorables sous traitement – Mais séquelles dans 20 à 30 % des cas : surdité, hydrocéphalie, comitialité Mortalité : 20 à 30 % – Personnes âgées, polypathologiques et/ou immuno déficientes

Méningite à pneumocoque, traitement Première intention : C 3 G – Ceftriaxone : 100 mg/kg/j en 1 -2 perfusions IV – Ou Cefotaxime : 300 mg/kg/j en 4 perfusions IV Nouvelle évaluation à 48 heures sur les données de la clinique et de la PL. Seconde intention : – Evolution favorable • si souche AMX-S passage à l’amoxicilline : 200 mg/kg/j en 4 perfusions IV • sinon poursuite du traitement initial – Echec : recherche de foyer (drainage ? ) +/- vancomycine Durée du traitement : 10 à 14 jours (prolongée en cas de réponse lente et/ou de souche de sensibilité diminuée)

Haemophilus influenzae < 5 ans ou porte d’entrée ORL Tableau clinique franc Leucocytose élevée LCR : – Polynucléose – Possible présence de BG- au direct, culture+ le lendemain – Possible résistance à l’amoxicilline

Méningite à H. influenzae, traitement Première intention : C 3 G – Ceftriaxone : 75 mg/kg/j en 1 -2 perfusions IV – Ou Cefotaxime : 200 mg/kg/j en 4 perfusions IV Nouvelle évaluation à 48 heures sur les données de la clinique et de la PL. Seconde intention : – Evolution favorable • poursuite du traitement initial Echec : recherche de foyer (drainage ? ) Durée du traitement : 7 jours (prolongée si réponse lente)

Méningite à Listeria monocytogenes BG+ Bactérie de l’environnement Contamination digestive alimentaire – crudités, laitages non pasteurisés, charcuterie Développement chez les ID – ge avancé, corticoïdes, chimiothérapie, femme enceinte, alcoolisme Envahissement du SNC par voie hématogène atteinte prédominante du tronc cérébral avec ouverture dans les méninges d’un ou deux abcès.

Méningite à L. monocytogenes Adulte de tout âge – Terrain favorisant Installation progressive Atteinte de la base du crâne – Troubles de la consience – Rhombencéphalite : atteinte des NC LCR : purulent ou clair Ploynucleose, formule panachée, lymphocytaire – Hypoglycorachie – Direct souvent négatif Pronostic réservé selon le terrain et la gravité neurologique

Méningite à listéria, traitement Céphalosporine inactive +++ Amoxicilline : 300 mg/kg/j en 4 perfusions IV x 21 j + gentamicine 3 -5 mg/kg/j x 7 j – possibilité d’utiliser le cotrimoxazole IV à la place de l’aminoside

Méningite tuberculeuse Contexte épidémiologique +/- terrain ID (VIH) Installation lente / Tableau fruste – Ralentissement, confusion Méningite lymphocytaire hypoglycorachique – Hyperprotéinorachie <1 g/L – Examen direct négatif, même au Ziehl Cultures tardives Enquête étiologique : cher le BK ailleurs VIH + ou pas ? • Traitement RHEZ
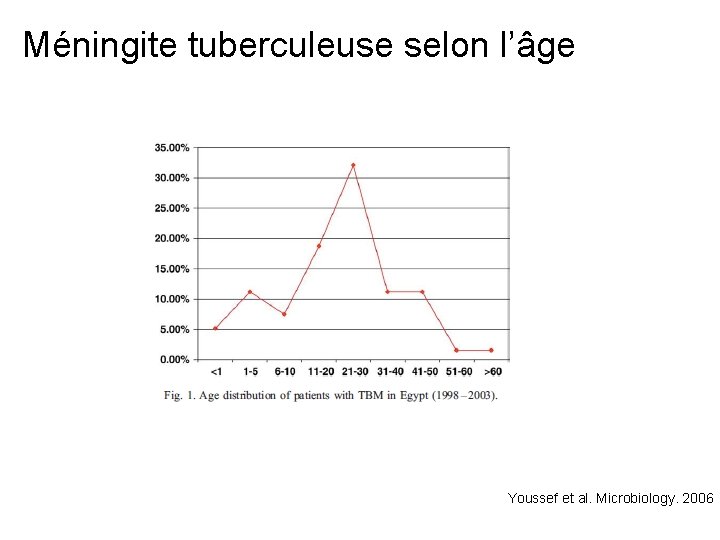
Méningite tuberculeuse selon l’âge Youssef et al. Microbiology. 2006

Méningite tuberculeuse Youssef et al. Microbiology. 2006

Sur le terrain…

Contexte africain de la MCS Les malades – Épidémies : incidence jusqu’à 1000 cas/100. 000 hab. – Enfants +++ Incidence et morbi-mortalité élevées Un plateau technique réduit – Place essentielle de la clinique – Soignant expérimenté + aiguilles + désinfectant + tube + lame + colorants + microscope + technicien compétent ? – Antibiotiques disponibles ? – Possibilité d’admission ? de suivi ? Prise en charge diagnostique et thérapeutique nécessairement adaptée à la réalité du terrain

Prise en charge individuelle : 4 temps Analyse de la situation clinique Confirmation de la méningite à N. meningitidis et élimination des diagnostics différentiels Traitement antibiotique Suivi

Évoquer la méningite Syndrome méningé – Céphalée + photophobie + vomissement + raideur + fièvre – Avéré ou résolutif – Inconstant en dessous de l’âge < 2 ans Symptômes de valeur équivalente – Fièvre avec confusion, délire ou convulsion – Bombement de la fontanelle, hypotonie, refus de manger – Purpura fulminans

Evoquer la méningite : atypies cliniques - liés à la bactérie en cause - liés au terrain : nouveau-né, nourrisson, sujet âgé, immunodéprimé, drépanocytaire - liés à un traitement antibiotique incomplet avant le diagnostic : méningite décapitée

Critères cliniques de gravité Terrain – Enfant < 5 ans Signes neurologiques – Coma, déficit S ou M, convulsions itératives Autres signes – Choc – Hémorragie cutanée ou muqueuse : purpura
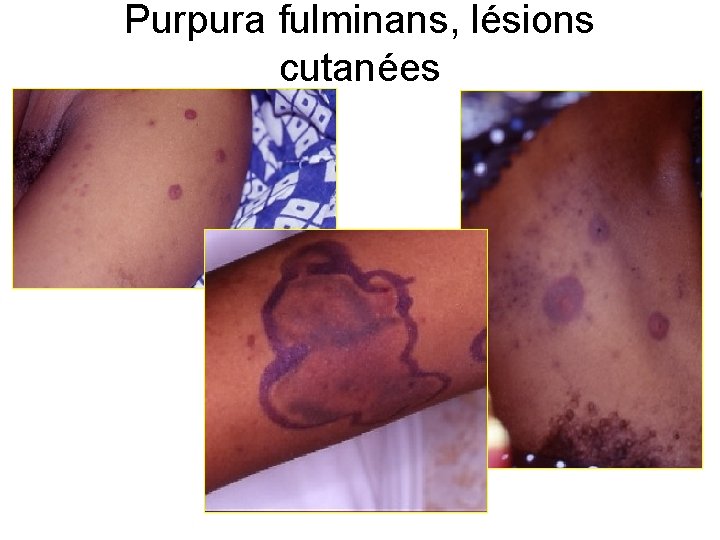
Purpura fulminans, lésions cutanées
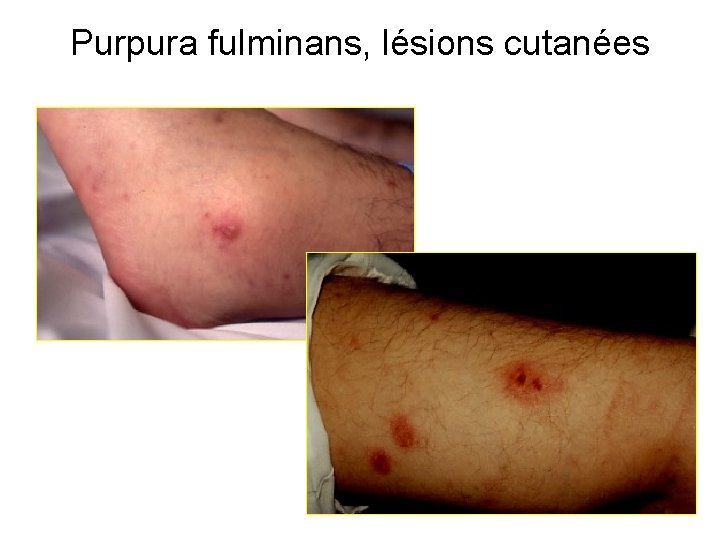
Purpura fulminans, lésions cutanées
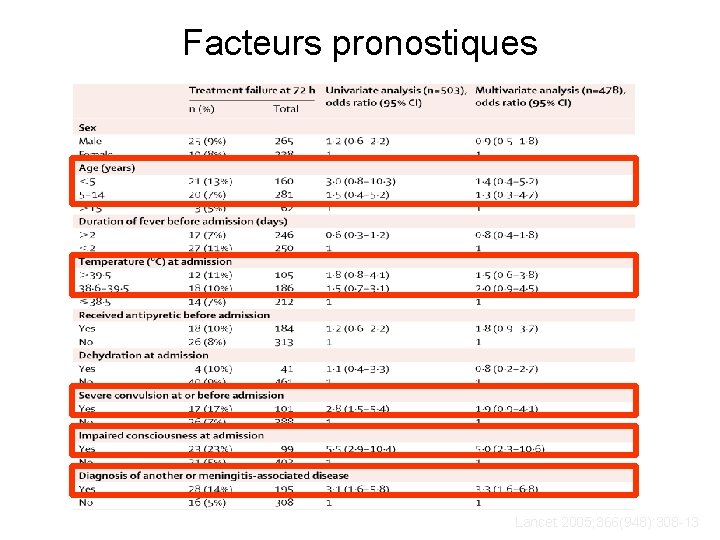
Facteurs pronostiques Lancet 2005; 366(948): 308 -13

Présomption de la bactérie Données épidémiologiques – – Saison, région Situation vaccinale collective Épidémie en cours ? Souches circulantes ? Cas dans l’entourage proche Données cliniques individuelles – – Purpura fulminans, choc… Statut vaccinal individuel Age ++ Foyer ORL, pulmonaire pneumocoque ou H. influenzae
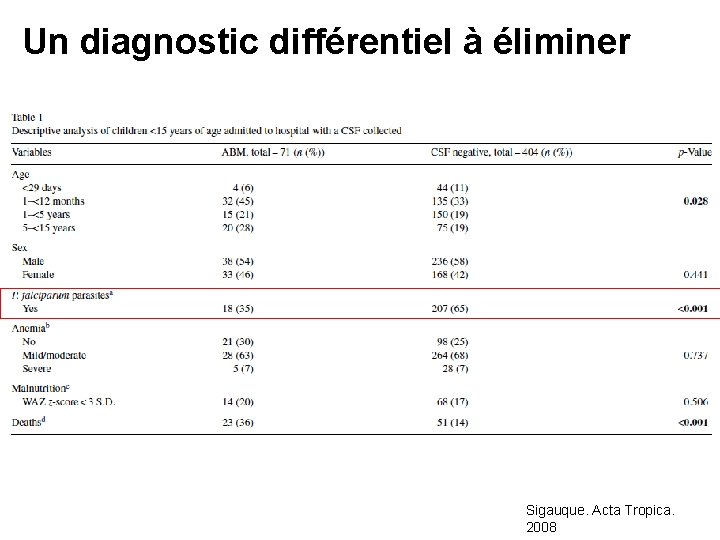
Un diagnostic différentiel à éliminer Sigauque. Acta Tropica. 2008

Méningite / Neuropaludisme : Un diagnostic difficile • Symptomatologie proche • Epidémiologie proche • Fond de parasitémie faible • Pléiocytose possible au cours d’un neuropaludisme • Association
Ponction lombaire, acte majeur Indication : toute suspicion Contre-indications : hémorragies hors épidémie ? Matériel – Alcool iodé ou polyvidone iodée > 3’ – Aiguilles spinales de 20 G à 22 G, IM pour l’enfant – Deux tube stériles Réalisation Pas de FO (Se et Sp médiocres) Position couchée si enfant, déficit ou coma, choc Enfants +++ : aiguille fine, contention efficace, geste prudent (qq mm)
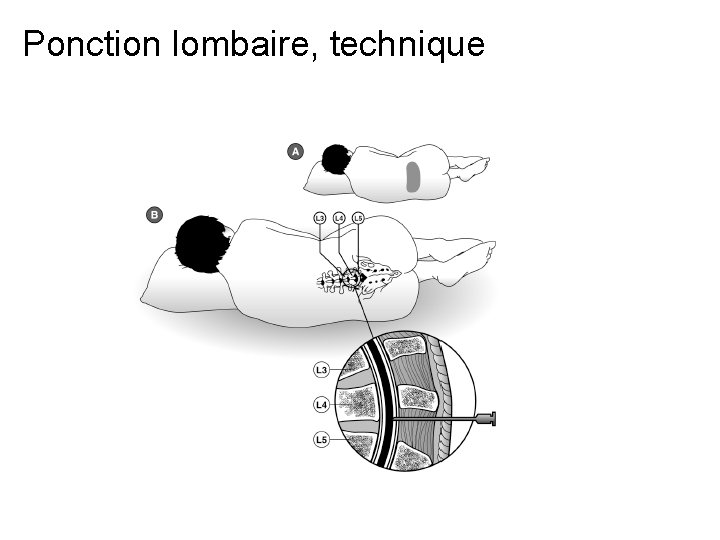
Ponction lombaire, technique

Analyse du LCR, certitude Examen macroscopique immédiat – Sur fond blanc – Purulent qd > 500 GB/mm 3 ; moiré entre 100 -500 ; clair qd < 100, hémorragique. Transport et exploitation immédiats – Centrifugation – Coloration de Gram (ou bleu) Cytologie, identification bactérienne – Techniques complémentaires ? – Ag solubles ? PCR ? Antibiogramme ?

Analyse du LCR • liquide clair : formule lymphocytaire (en règle méningite virale), formule panachée (méningite tuberculeuse) • liquide trouble, voire puriforme : méningite purulente d’origine bactérienne • liquide hémorragique : hémorragie méningée En cas de fièvre craindre un processus septique et mettre en culture.
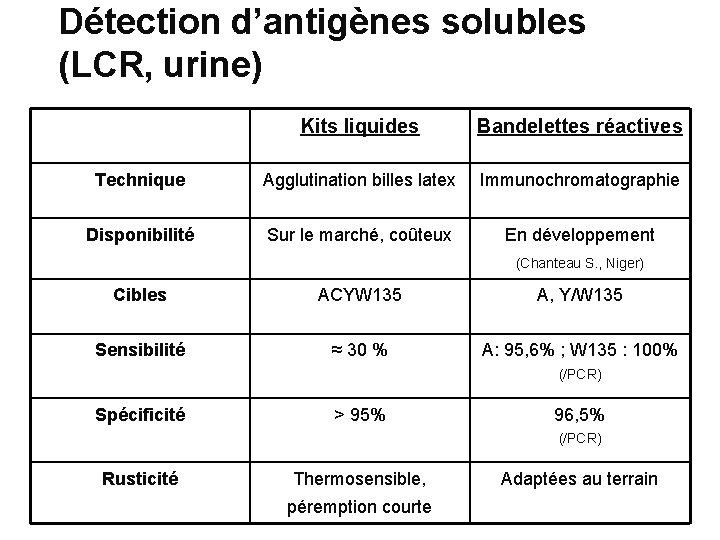
Détection d’antigènes solubles (LCR, urine) Kits liquides Bandelettes réactives Technique Agglutination billes latex Immunochromatographie Disponibilité Sur le marché, coûteux En développement (Chanteau S. , Niger) Cibles ACYW 135 A, Y/W 135 Sensibilité ≈ 30 % A: 95, 6% ; W 135 : 100% (/PCR) Spécificité > 95% 96, 5% (/PCR) Rusticité Thermosensible, péremption courte Adaptées au terrain

Étude bactériologique du LCR Laboratoires sentinelles (type CHU) – Culture initiale et souchier – Transport secondaire sécurisé CNR OMS (IMTSSA) Étude de la sensibilité aux antibiotiques – Sensibilité limitée de la culture – CMI sur milieu solide : E-test Identification phénotypique et génotypique – Suivi épidémiologique – Sérogroupe, complexe ST

Antibiogramme, peu disponible en routine Collection IMTSSA

Hémocultures non disponibles en routine. .

Principes de l’antibiothérapie de la MCS Urgente Parentérale Active sur toutes les souches de N. meningitidis – Peu de résistances (chrom. : gène pen. A PBP 2) Pénétration suffisante dans le LCR

Contraintes africaines Mortalité infantile du méningocoque – Virulence intrinsèque – Terrain – Prise en charge tardive Poussées épidémiques – Diffusion des cas dans toute une région, souvent rurale – Afflux massif de malades aux centres de santé – Désorganisation et surcharge d’un réseau de soins précaire Stock antibiotique limité – Coût majeur ++
![Antibiotiques et méningite, PK-PD Posologie LCR/sg [C] LCR (mg/l) Pouvoir bactéricid e Pénicilline G Antibiotiques et méningite, PK-PD Posologie LCR/sg [C] LCR (mg/l) Pouvoir bactéricid e Pénicilline G](http://slidetodoc.com/presentation_image_h2/db49081ccac4ab03025b98d281bff831/image-56.jpg)
Antibiotiques et méningite, PK-PD Posologie LCR/sg [C] LCR (mg/l) Pouvoir bactéricid e Pénicilline G 250. 000 UI/kg/j 5 -15 % 0, 8 1 -10 Amoxicilline 200 mg/kg/j 5 -15 % 1, 3 -6, 4 1 -10 20 mg/kg/j ND 0, 05 -0, 8 ND 50 -150 mg/j 5 -15 % 3, 5 -7, 9 >10 Vancomycine 40 mg/kg/j <5% 0, 9 1 -10 Gentamicine 3 -4, 5 mg/kg/j 0 -0, 9 ND Ciprofloxacine 200 mg/12 h > 20 % 0, 1 -0, 6 > 10 Chloramphénicol 25 -35 mg/kg/j > 20 % 16 -30 > 10 Ac. clavulanique Ceftriaxone Méd Mal Infect 1996; 26: 1032 -43

Recommandations nationales en France Purpura fulminans (au moins une lésion > 3 mm) –En urgence avant PL, faire en IVL ou en IM – ceftriaxone : 50 mg/kg enfant, 1 -2 g adulte, ou amoxicilline : 25 mg/kg enfant, 1 g adulte, puis … Méningite purulente sans agent pathogène –Ceftriaxone : 70 -100 mg/kg/j (1 ou 2 IV/j) ou cefotaxime Méningite à méningocoque confirmée –Ceftriaxone : 70 -100 mg/kg/j (1 ou 2 IV/j) ou cefotaxime –Durée : > 4 jours • Corticothérapie non systématique (Hi)

Stratégie de la dose unique en épidémie Objectifs à atteindre – Efficacité antibiotique : [C]LCR > CMI – Économiques : coût réduit de la prise en charge – Logistiques (schéma simple, malades du bout de la piste) Essais thérapeutiques non randomisés Résultats satisfaisants avec deux molécules = progrès Mais limites si pneumocoque ou H. influenzae b
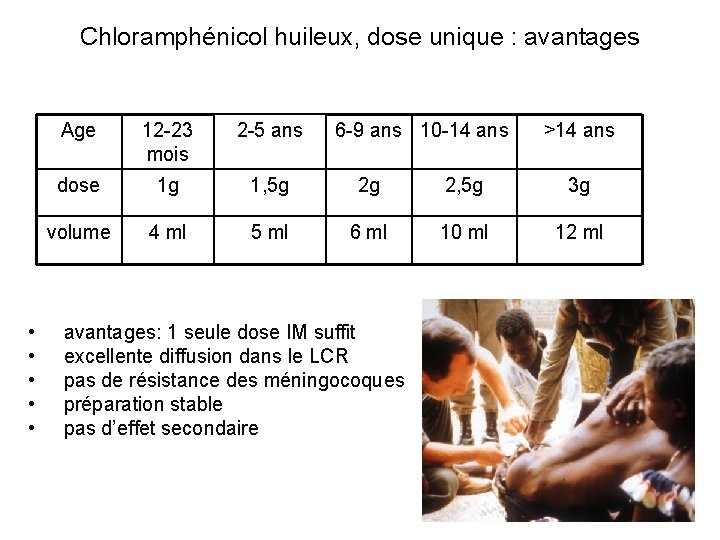
Chloramphénicol huileux, dose unique : avantages • • • Age 12 -23 mois 2 -5 ans 6 -9 ans 10 -14 ans dose 1 g 1, 5 g 2 g 2, 5 g 3 g volume 4 ml 5 ml 6 ml 10 ml 12 ml avantages: 1 seule dose IM suffit excellente diffusion dans le LCR pas de résistance des méningocoques préparation stable pas d’effet secondaire • CI grossesse allaitement <2 mois >14 ans
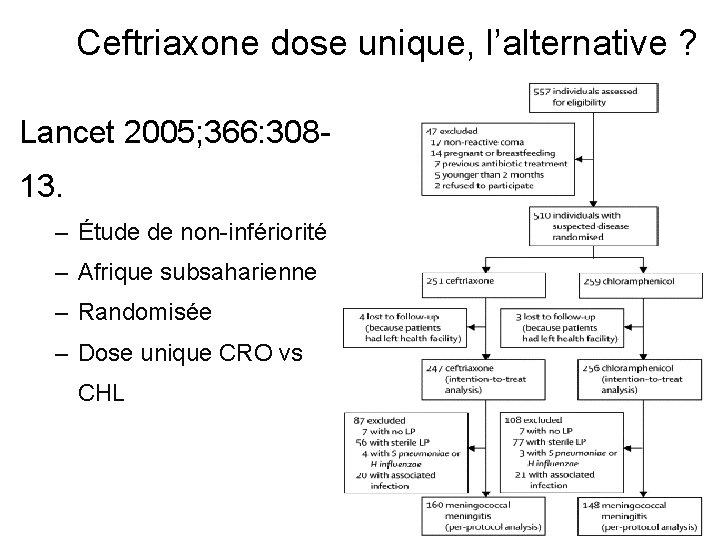
Ceftriaxone dose unique, l’alternative ? Lancet 2005; 366: 30813. – Étude de non-infériorité – Afrique subsaharienne – Randomisée – Dose unique CRO vs CHL
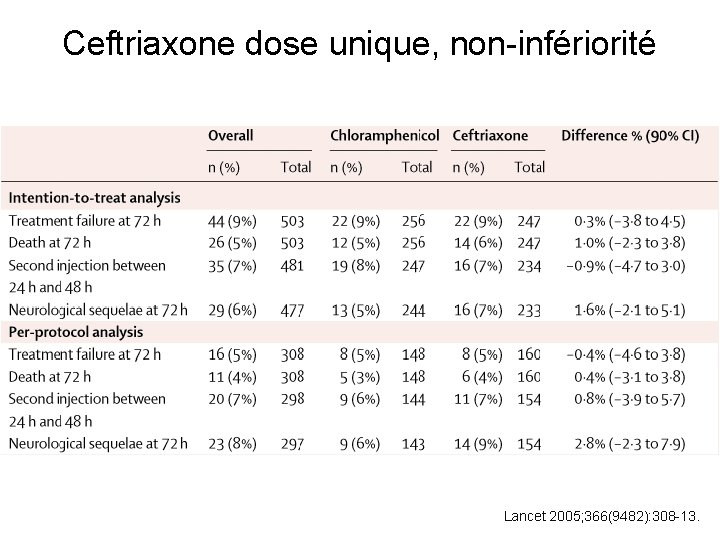
Ceftriaxone dose unique, non-infériorité Lancet 2005; 366(9482): 308 -13.
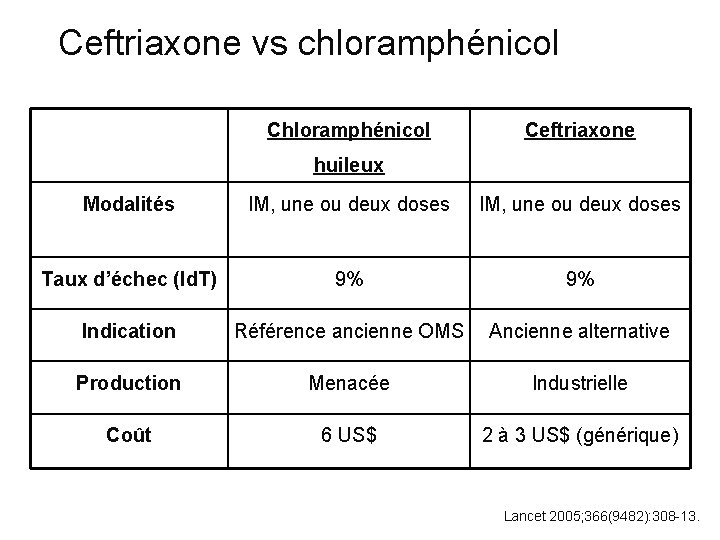
Ceftriaxone vs chloramphénicol Ceftriaxone huileux Modalités IM, une ou deux doses Taux d’échec (Id. T) 9% 9% Indication Référence ancienne OMS Ancienne alternative Production Menacée Industrielle Coût 6 US$ 2 à 3 US$ (générique) Lancet 2005; 366(9482): 308 -13.
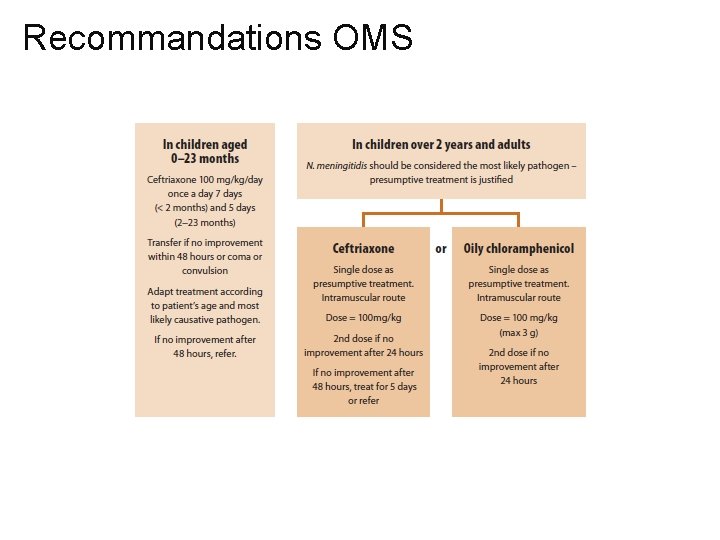
Recommandations OMS, 2010

Ceftriaxone dose unique Une crainte : l’antibiorésistance Non mise en évidence Prévention : Généraliser la vaccination Education pour réduire l’automédication Optimiser le diagnostic bactériologique

Ne pas oublier les co-morbidités +++ Déshydratation, dénutrition Paludisme – FS-GE, traitement systématique Pneumopathie d’inhalation …

Suivi clinique Efficacité clinique – Régression des signes généraux – Régression du syndrome méningé – Arrêt des convulsions Complications à recher – Fièvre : paludisme associé ? autre foyer ? veinite ? – Céphalée, vomissement, raideur : syndrome post-PL ? méningite iatrogène ? Manifestations tardives : atteintes osseuses • Pas de PL de contrôle

Prise en charge d’une épidémie : 4 temps

Prise en charge d’une épidémie : 4 temps Surveillance épidémiologique Alerte Confirmation - identification Intervention 1. Mise à disposition de stock de traitement 2. Campagne de vaccination 3. Information

Surveillance épidémiologique Avant l’épidémie… Objectif : identifier les premiers cas, identifier le sérotype EPR Comitte : « epidemic prepardness and response » Mise en place du système de surveillance en inter-épidémie Information, formation et dotation des personnels de santé Préparation d’une éventuelle campagne de vaccination Information du public

Surveillance épidémiologique et alerte Relevé hebdomadaire des déclarations cliniques – Sous-déclaration = moindre sensibilité – Seuils pour différencier épidémie et pic saisonnier Alerte épidémique : 5 cas/sem/100. 000 hab. – 2 cas/sem si pop. < 30. 000 hab. – Se>Sp enquête pour confirmer les cas et pour préparer la logistique des interventions Epidémie déclarée : 10 à 15 cas/sem/100. 000 hab. – Sp interventions déclenchées Lancet 2001; 358: 287 -293.

Risque épidémique +++ –pas d’épidémie depuis 3 ans –couverture vaccinale < 80% –Seuil d ’alerte tôt dans la saison épidémique –forte densité de population, ville

Identification - Confirmation • Au moins 10 échantillons positifs de Neisseria meningitidis, soit 20 à 30 LCR au début pour argumenter le choix du vaccin • Après le début de la campagne de vaccination, pas de confirmation de tous les malades • Contrôler tout changement du profil des souches: analyse de 5 LCR par semaine

Mise en place des traitements Rapide Appropriée Protocole de soin Accessible Gestion de stock Peu coûteuse OMS, 2010

Campagne de vaccination Meilleure efficacité que la vaccination de routine ? Efficacité collective au-delà de 4 semaines – 2 à 9 semaines de mise en route – 1 à 2 semaines de campagne 3 à 8% de cas évités en moins/semaine de retard Lancet 2001; 358: 287 -293.

Vaccins disponibles Plusieurs valences, B non disponible Aucune contre-indication Vaccins polysacchariques : A+C, A+C+Y+W 135 – Protection courte, inefficacité chez le petit enfant Vaccin conjugué A ou C – Efficacité dès le 2ème mois

Informations et implications des autorités locales INDISPENSABLES…
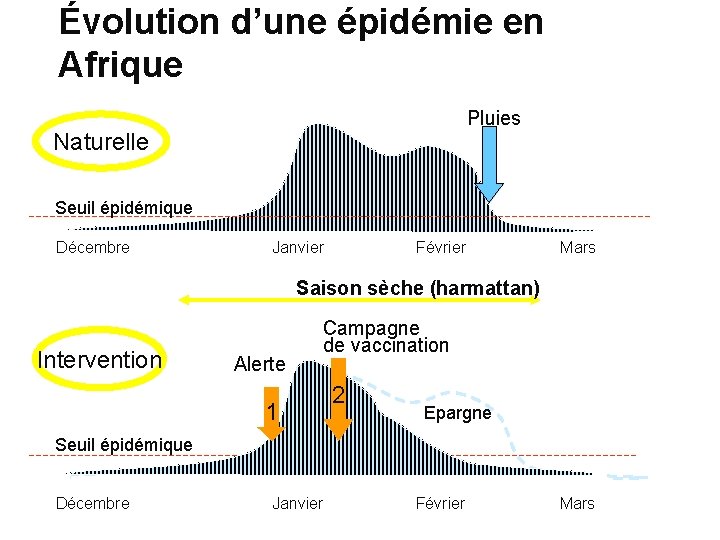
Évolution d’une épidémie en Afrique Pluies Naturelle Seuil épidémique Décembre Janvier Février Mars Saison sèche (harmattan) Intervention Alerte Campagne de vaccination 1 2 Epargne Seuil épidémique Décembre Janvier Février Mars
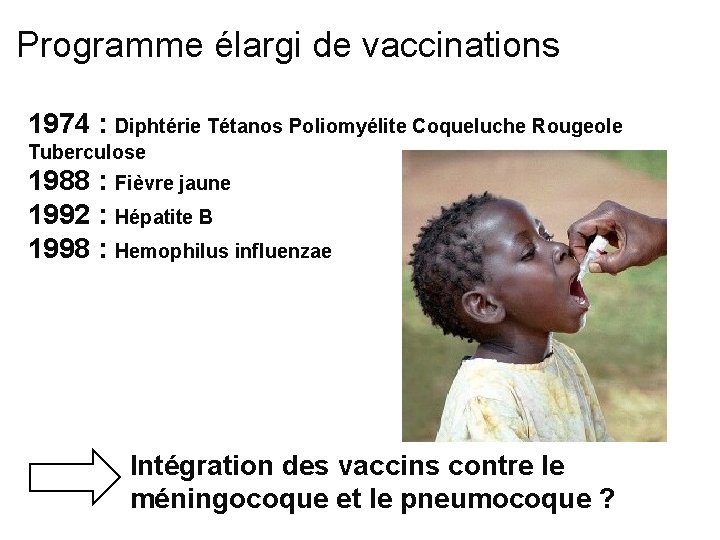
Programme élargi de vaccinations 1974 : Diphtérie Tétanos Poliomyélite Coqueluche Rougeole Tuberculose 1988 : Fièvre jaune 1992 : Hépatite B 1998 : Hemophilus influenzae Intégration des vaccins contre le méningocoque et le pneumocoque ?

Vers une vaccination systématique? Pneumocoque 23 valences non autorisé chez <2 ans 7 valences prioritaires dans les pays où la mortalité des enfants de moins de 5 ans est supérieure à 50/1000 (VIH et drépanocytaires) Limites : sérotype 5 non couvert (Mali) Méningocoque Vaccins A+C, A+C+W 135 non immunogènes Vaccin anti- C monovalent conjugué à partir de 2 mois Vaccin anti –A monovalent conjugué présélectionné par l'OMS
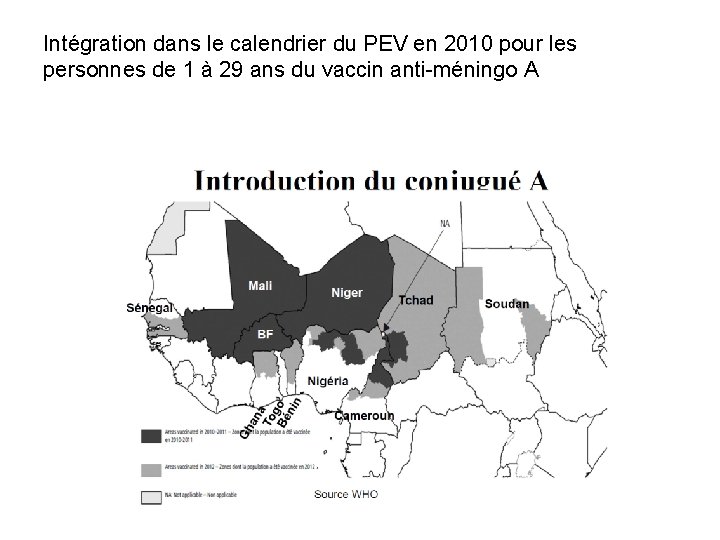
Intégration dans le calendrier du PEV en 2010 pour les personnes de 1 à 29 ans du vaccin anti-méningo A
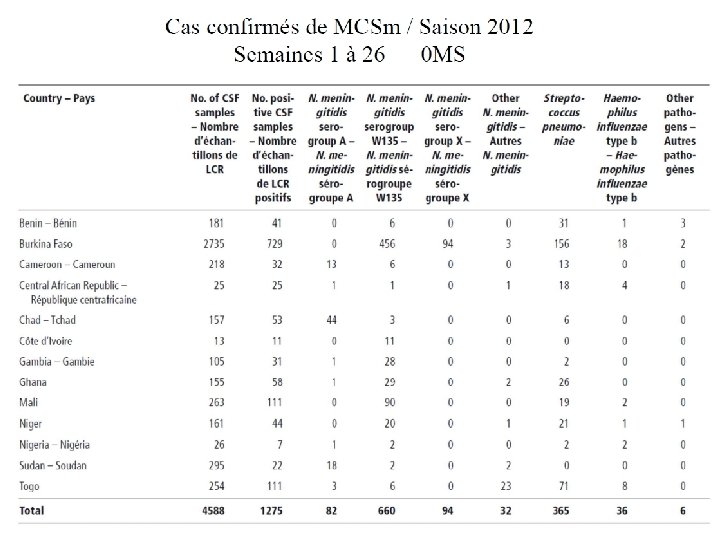
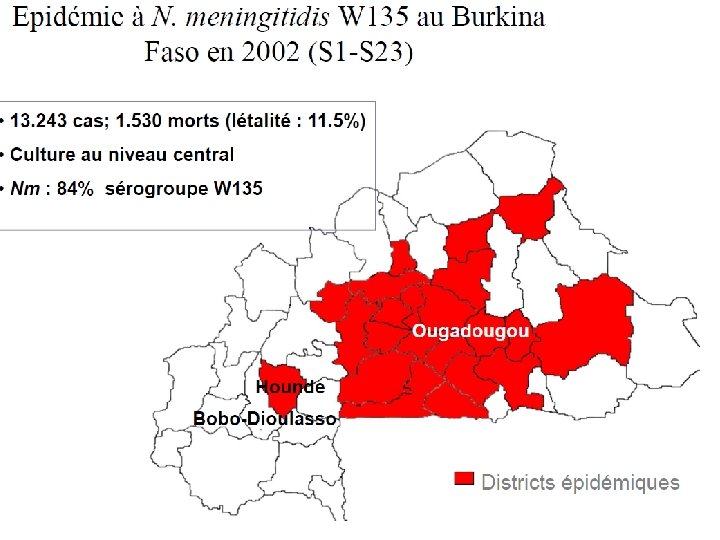

Vers une vaccination pentavalente ?

Merci de votre attention

Pour en savoir plus … Lutte contre les épidémies de méningite à méningocoque : guide pratique OMS. WHO/EMC/BAC/98. 3 Rosenstein NE, Perkins BA, Stephens DS et al. Meningococcal disease. N Engl J Med 2001; 344(18): 1378 -88. Lewis R, Nathan N, Diarra L, Belanger F, Paquet C. Timely detection of meningococcal meningitis epidemics in Africa. Lancet 2001; 358(9278): 287 -93. Nathan N, Borel T, Djibo A et al. Ceftriaxone as effective as long-acting chloramphenicol in short-course treatment of meningococcal meningitis during epidemics: a randomised non-inferiority study. Lancet 2005; 366(9482): 308 -13. Pilly E. Maladies infectieuses et tropicales 2011. CMIT.
- Slides: 85