Minrio O minrio de zinco normalmente usado tanto















- Slides: 32


Minério O minério de zinco normalmente usado tanto em pirometalúrgica quanto em hidrometalurgia é o sulfeto Zn. S, blenda ou esfalerita, normalmente concentrado por flotação. Esfalerita No Brasil o minério silicatado de Vazante MG com base na Calamina é particularmente importante por uma fração significativa da produção de zinco ser resultante deste tipo de minério.

Minério Sulfetado A hidrometalurgia tradicional trata dos minérios sulfetados. Esfalerita Zn. S

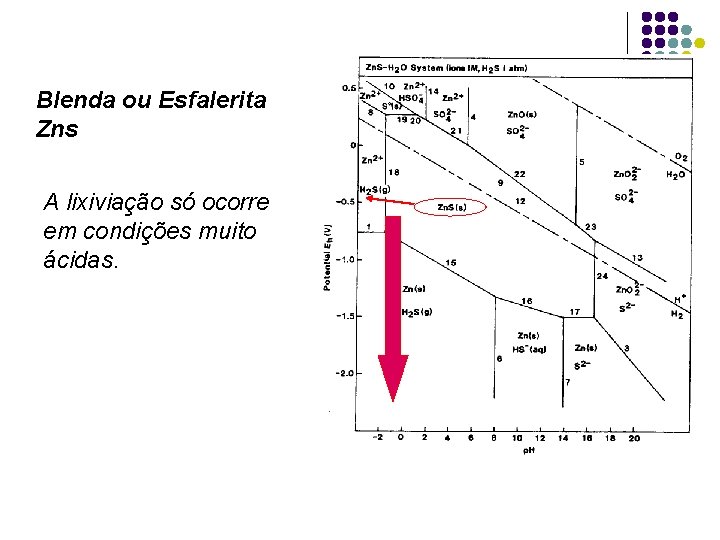
Blenda ou Esfalerita Zns A lixiviação só ocorre em condições muito ácidas.

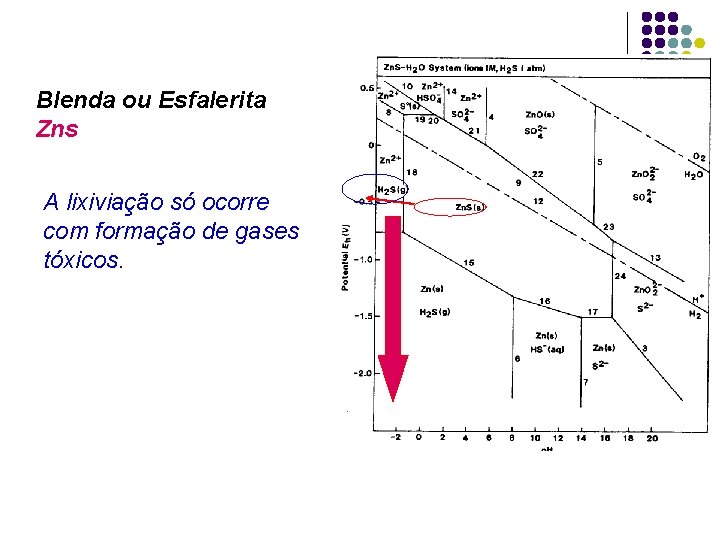
Blenda ou Esfalerita Zns A lixiviação só ocorre com formação de gases tóxicos.

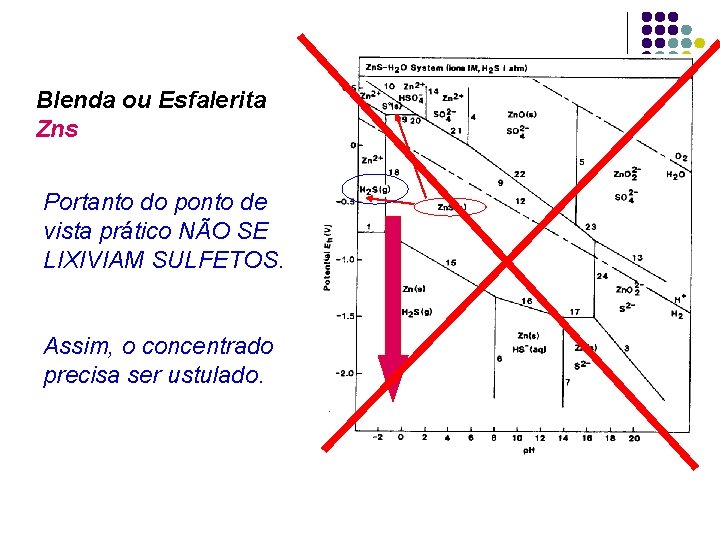
Blenda ou Esfalerita Zns Portanto do ponto de vista prático NÃO SE LIXIVIAM SULFETOS. Assim, o concentrado precisa ser ustulado.

Ustulação Passagem do Zn. S para Zn. O. No caso de pirometalurgia faz-se uma ustulação sinterizante para se condicionar o material para o processo de redução, todavia em hidrometalurgia não se deseja aglomerar. Normalmente são usados fornos de leito fluidizado operando entre 650 -900 C dependendo do concentrado e do processo. A ustulação a altas temperaturas pode levar à formação de ferritas de zinco: Fe 2 O 3 +Zn. O = Zn. O. Fe 2 O 3

Ustulação Passagem do Zn. S para Zn. O

Ustulação A ustulação a altas temperaturas pode levar à formação de ferritas de zinco: Fe 2 O 3 +Zn. O = Zn. O. Fe 2 O 3 As ferritas são mais difíceis de lixiviar do que o Zn. O. Assim, ou terão perdas de zinco ou então o processo deverá trabalhar em condições mais severas de lixiviação.

Lixiviação com p. H final entre 2 e 4, 5

Lixiviação A redução do p. H faz com que aumente a velocidade de lixiviação, na prática se trabalha com p. H próximo de 2

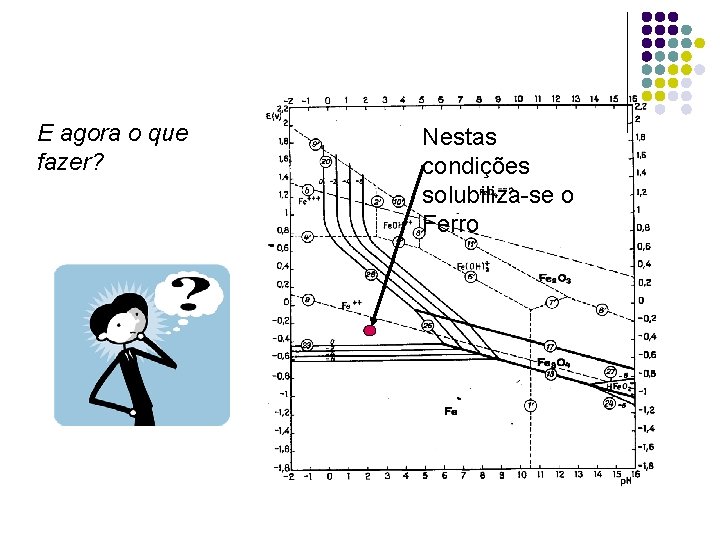
Nestas condições solubiliza-se o Ferro também

O ferro é o principal contaminante e se estiver na forma de íon ferroso posteriormente acabará formando um precipitado muito difícil de filtrar, o qual inviabiliza o processo. Nestas condições solubiliza-se o Ferro

E agora o que fazer? Nestas condições solubiliza-se o Ferro

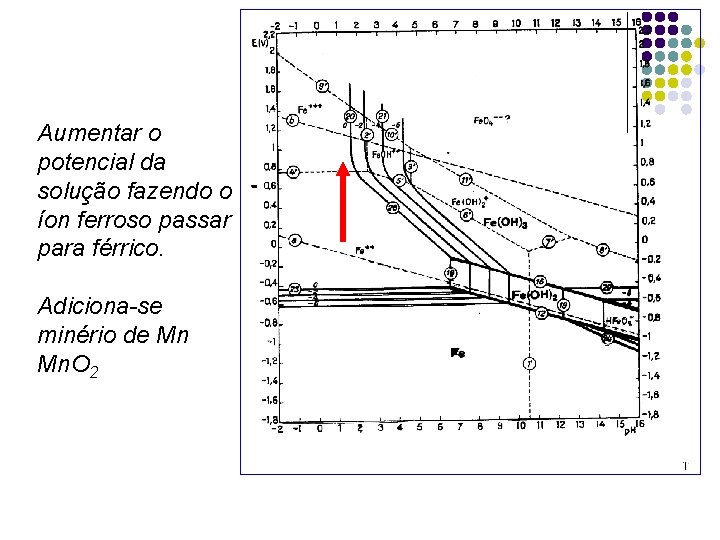
Aumentar o potencial da solução fazendo o íon ferroso passar para férrico. Adiciona-se minério de Mn Mn. O 2

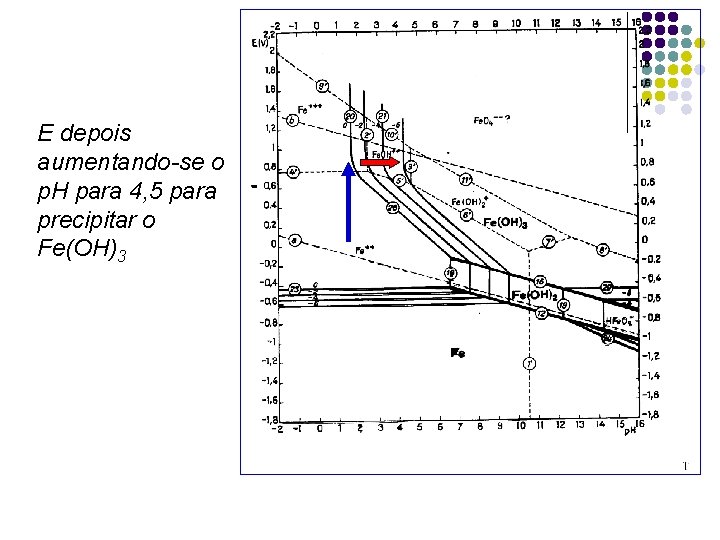
E depois aumentando-se o p. H para 4, 5 para precipitar o Fe(OH)3

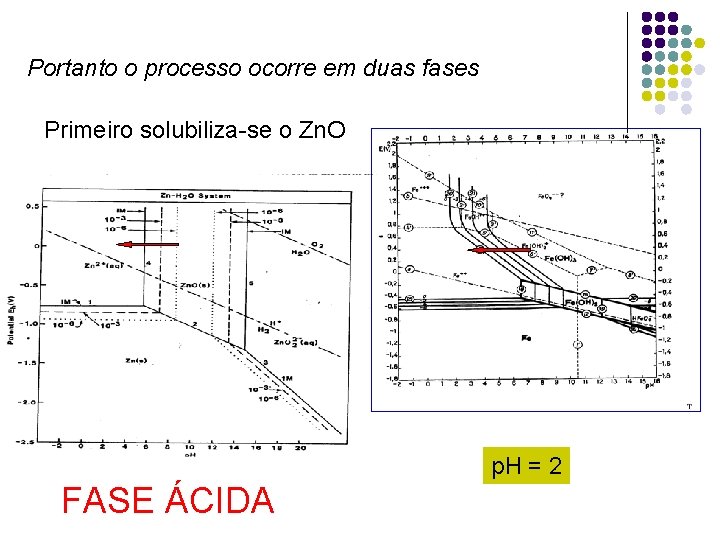
Portanto o processo ocorre em duas fases Primeiro solubiliza-se o Zn. O p. H = 2 FASE ÁCIDA

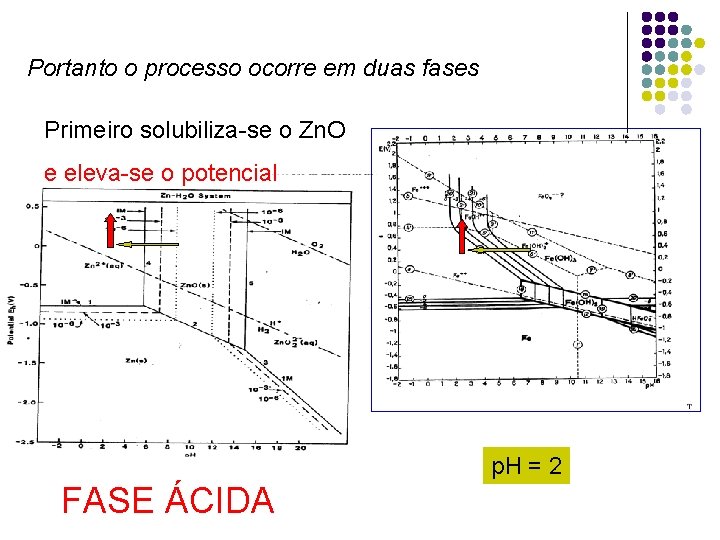
Portanto o processo ocorre em duas fases Primeiro solubiliza-se o Zn. O e eleva-se o potencial p. H = 2 FASE ÁCIDA

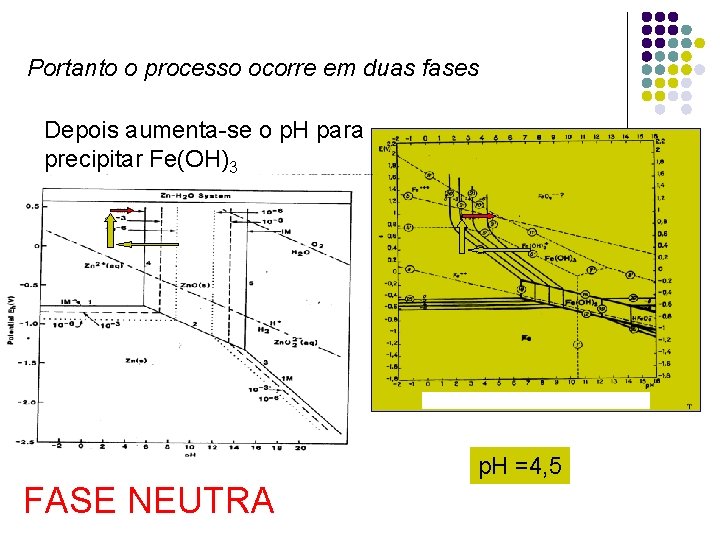
Portanto o processo ocorre em duas fases Depois aumenta-se o p. H para precipitar Fe(OH)3 p. H =4, 5 FASE NEUTRA

Portanto o processo ocorre em duas fases: Todavia o principal motivo para se aumentar o p. H é o seguinte: Ezn/zn 2+ = -0, 76 E H/H= = -0, 059 p. H – 0, 79 Portanto, aumentando-se o p. H aumenta-se a diferença entre o potencial de eletrodo do zinco e o do hidrogênio evitando a formação de H 2 na eletrólise. FASE NEUTRA p. H =4, 5

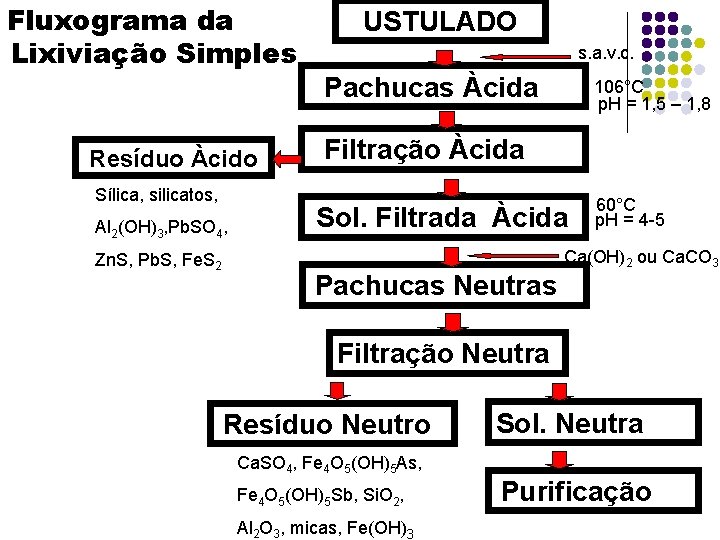
Fluxograma da Lixiviação Simples Resíduo Àcido Sílica, silicatos, Al 2(OH)3, Pb. SO 4, Zn. S, Pb. S, Fe. S 2 USTULADO s. a. v. c. Pachucas Àcida 106°C p. H = 1, 5 – 1, 8 Filtração Àcida Sol. Filtrada Àcida 60°C p. H = 4 -5 Ca(OH)2 ou Ca. CO 3 Pachucas Neutras Filtração Neutra Resíduo Neutro Ca. SO 4, Fe 4 O 5(OH)5 As, Fe 4 O 5(OH)5 Sb, Si. O 2, Al 2 O 3, micas, Fe(OH)3 Sol. Neutra Purificação

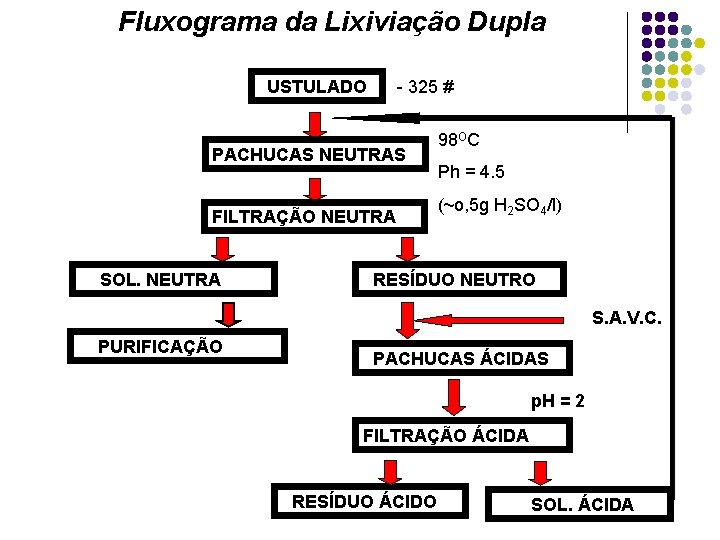
Fluxograma da Lixiviação Dupla USTULADO - 325 # PACHUCAS NEUTRAS FILTRAÇÃO NEUTRA SOL. NEUTRA 98 OC Ph = 4. 5 (~o, 5 g H 2 SO 4/l) RESÍDUO NEUTRO S. A. V. C. PURIFICAÇÃO PACHUCAS ÁCIDAS p. H = 2 FILTRAÇÃO ÁCIDA RESÍDUO ÁCIDO SOL. ÁCIDA

Reações da Lixiviação Fase Àcida: 1) Zn. O + H SO (s. a. v. c. ) Zn. SO (s. a. ) +H O (u) 2 4 4 2 2) Fe. O(u) + H SO (s. a. v. c. ) Fe. SO (s. a. ) + H O 2 4 4 2 3) Fe O (u) +3 H SO (s. a. v. c. ) Fe (SO ) (s. a) + H O 2 3 2 43 2 4) Zn. SO (u) + H O Zn. SO (s. a. ) + H O 2 4 4 2 5) As O (u) + 3 H O 2 As. O H (s. a. ) 2 3 3 6) Sb O (u) + 3 H O 2 sb. O H (s. a. ) 2 3 3 7) 2 Fe. SO (s. a. ) + 2 H SO + Mn. O Fe (SO ) (s. a. ) + 4 2 43 2 Mn. SO (s. a. )+ H O 4 2

Fase Neutra Lixiviação Simples Lixiviação Dupla

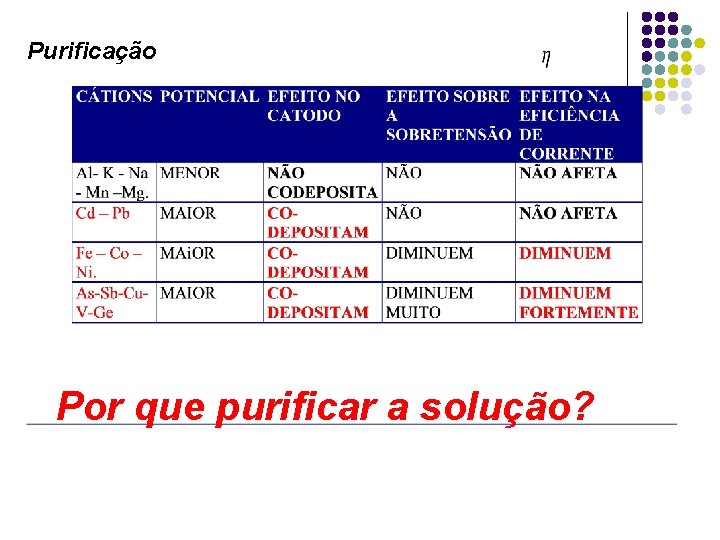
Purificação Por que purificar a solução?

Purificação Eliminação das Impurezas que prejudicam o processo de redução eletrolítica. As, Sb, Co, Cu, Ni, Cd, Ge, Te, In. Baseia-se na reação das impurezas formando compostos estáveis que precipitam, para condições de temperatura e p. H bem definidas. Cuº Refino com Zn em pó. precipitação: Cu 2+ + Zn = Cu + Zn 2+ Cd 2+ + Zn = Cd + Zn 2+ Znº

Purificação Refino com Zn em pó. precipitação: Cu 2+ + Zn = Cu + Zn 2+ Cd 2+ + Zn = Cd + Zn 2+ A precipitação pode ser seletiva: Cu 2+ + Cd = Cu + Cd 2+ Portanto o cobre tende a ser removido primeiro e assim por diante.

Purificação Elevando-se a temperatura diminui-se o teor de O 2 dissolvido e aumenta-se a velocidade das reações de precipitação. dissolução: M + 2 H+ +1/2 O 2 = M 2+ + H 2 O

Adições de Tartarato de antimônio e potássio ou trióxido de antimônio ou arsênico favorecem a precipitação de compostos estáveis do cobalto, níquel e cobre. É necessário ter-se cobre em solução (150 a 400 ppm), para favorecer a dissolução do aditivo.

Fatores que influem na sobretensão -Impurezas -Temperatura -Densidade de Corrente • O aumento da densidade de corrente causa aumento na sobretensão. • O aumento da temperatura causa diminuição na sobretensão. • Influência das impurezas. Impurezas Anódicas Relacionadas ao aumento da corrosão no anôdo de Pb e afetando a deposição de O 2. Cl - F - NO 3 - Cl. O 3 -2

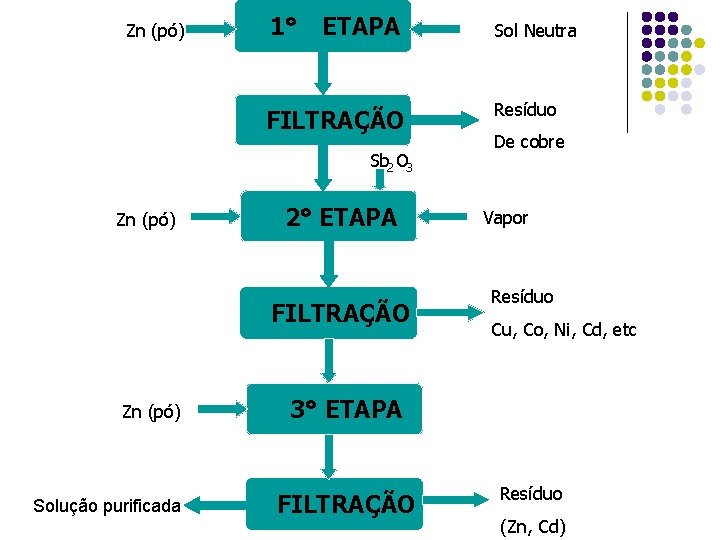
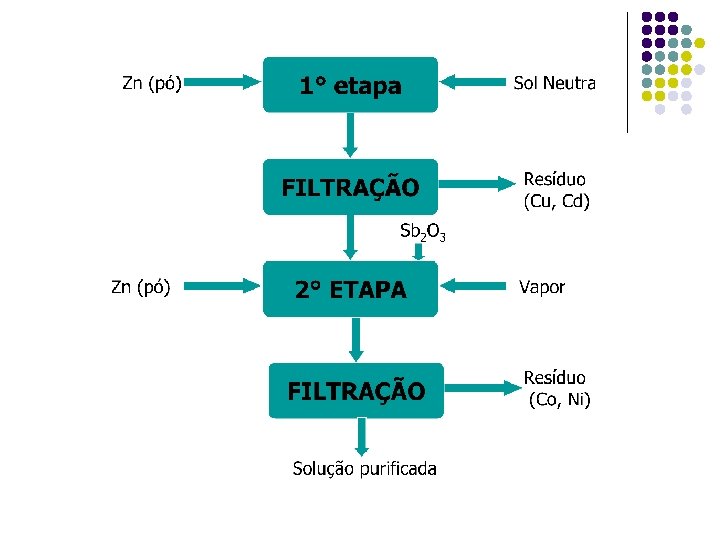
Zn (pó) 1° - ETAPA Sol Neutra FILTRAÇÃO Resíduo Sb 2 O 3 Zn (pó) 2° ETAPA FILTRAÇÃO Zn (pó) Solução purificada De cobre Vapor Resíduo Cu, Co, Ni, Cd, etc 3° ETAPA FILTRAÇÃO Resíduo (Zn, Cd)
