Mikronalalitikai kurzus szubsztrtknyvtr Szerin proteinzok specificits vizsglata kompetitv

Mikronalalitikai kurzus szubsztrátkönyvtár Szerin proteinázok specificitás vizsgálata kompetitív oligopeptid szubsztrát rendszer fordított fázisú HPLC analízisével.
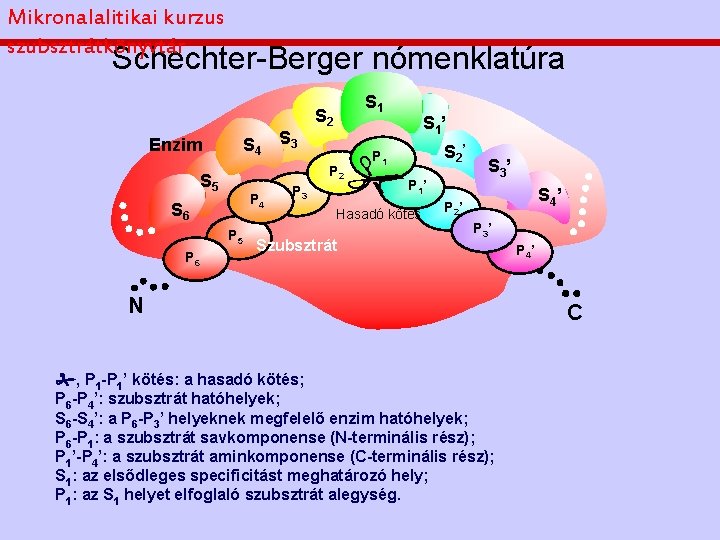
Mikronalalitikai kurzus szubsztrátkönyvtár Schechter-Berger nómenklatúra Enzim S 4 S 2 P 2 S 5 P 4 S 6 P 5 P 6 S 3 S 1 P 3 S 1’ S 2’ P 1’ Hasadó kötés Szubsztrát S 3’ S 4’ P 2’ P 3’ N , P 1 -P 1’ kötés: a hasadó kötés; P 6 -P 4’: szubsztrát hatóhelyek; S 6 -S 4’: a P 6 -P 3’ helyeknek megfelelő enzim hatóhelyek; P 6 -P 1: a szubsztrát savkomponense (N-terminális rész); P 1’-P 4’: a szubsztrát aminkomponense (C-terminális rész); S 1: az elsődleges specificitást meghatározó hely; P 1: az S 1 helyet elfoglaló szubsztrát alegység. P 4’ C
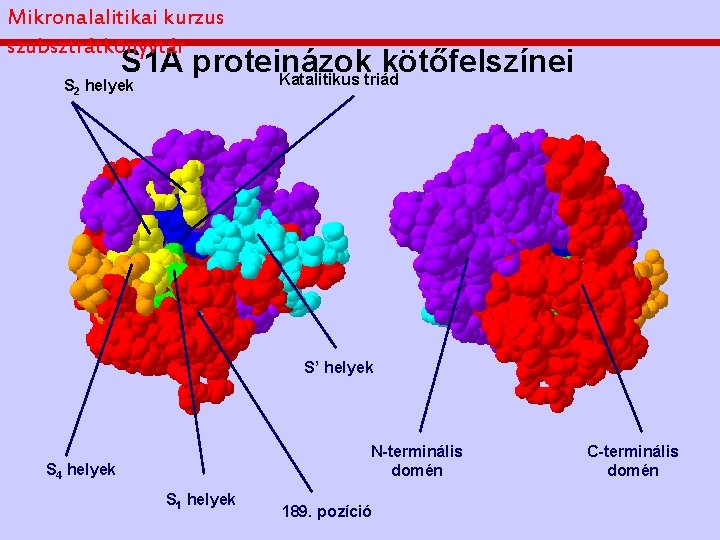
Mikronalalitikai kurzus szubsztrátkönyvtár S 1 A proteinázok kötőfelszínei Katalitikus triád S 2 helyek S’ helyek N-terminális domén S 4 helyek S 1 helyek 189. pozíció C-terminális domén
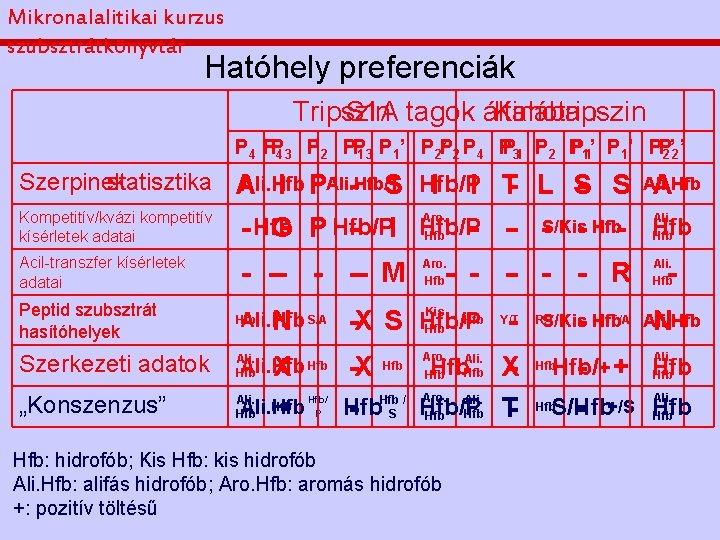
Mikronalalitikai kurzus szubsztrátkönyvtár Hatóhely preferenciák Tripszin S 1 A tagok általában Kimotripszin P 4 PP 4 3 P 2 PP 1 3 P 1’ P 2 P ’ 2 P 4 PP 31 P 2 P P 11’ PP 2’ 2’ Szerpinek Szerpin statisztika A Ali. Hfb I PAli. Hfb/T - S Hfb/P I I T- L S- S Ali. Hfb A Kompetitív/kvázi kompetitív kísérletek adatai Acil-transzfer kísérletek adatai Aro. - Hfb G P Hfb/P - I Hfb/P Hfb -- -S/Kis- Hfb- - -- M Aro. Hfb Ali. Hfb N S/A Kis Hfb Y/T -X S Hfb/P - R/T S/Kis Ali. Hfb X Hfb Aro. Hfb -X Hfb / Aro. Ali. Hfb - S Hfb/P Hfb T Hfb Peptid szubsztrát hasítóhelyek Hfb Szerkezeti adatok Ali. Hfb „Konszenzus” Ali. Hfb Hfb/ P Hfb - - - R Ali. Hfb X- Hfb: hidrofób; Kis Hfb: kis hidrofób Ali. Hfb: alifás hidrofób; Aro. Hfb: aromás hidrofób +: pozitív töltésű Ali. Hfb Ali. Hfb - - Hfb. T/A Ali. Hfb N Ali. Hfb/+ - + Hfb Ali. S/Hfb - +/S Hfb Hfb

Mikronalalitikai kurzus szubsztrátkönyvtár Optimális közös peptidgerinc tervezése. Megfontolások Alapkövetelmények: 1. S–P és S’–P’ kölcsönhatások kialakítása 2. Kompetitív reakcióelrendezés

Mikronalalitikai kurzus szubsztrátkönyvtár Optimális közös peptidgerinc tervezése. Megfontolások S–P és S’–P’ kölcsönhatások kialakítása A P’ kölcsönhatások hiánya miatt a kromogén szubsztrátok nem jöhetnek szóba. ↓ Az S 1 A enzim-szubsztrát kölcsönhatásokban általában szükséges és elégséges P 4–P 2’ távolságot átfogó oligopeptid szubsztrát Kompetitív reakcióelrendezés ↓ Olyan oligopeptidek keveréke, melyek azonos aminosavakat hordozó „gerinccel” rendelkeznek, és csak a hasítóhelyen (P 1 pozíció) tartalmazzák a vizsgálandó specificitásoknak megfelelő aminosav oldalláncokat

Mikronalalitikai kurzus szubsztrátkönyvtár Optimális közös peptidgerinc tervezése. Megfontolások Analitikai módszer: 1. Optikai detektálás 2. Egyéb módszerek (HPLC, fehérjeszekvenálás, MS)

Mikronalalitikai kurzus szubsztrátkönyvtár Optimális közös peptidgerinc tervezése. Megfontolások Optikai detektálás Egy lépéses egyszerű jelöléses vagy IFQ detektáláshoz egyelőre nem áll rendelkezésre kellő számú különböző csoport. ↓ Azonos jelölőcsoportot, vagy IFQ csoport párt tartalmazó szubsztrátok Az enzimatikus hasítás csak a komponensek elválasztása után lenne követhető. Egyéb módszerek Fehérjeszekvenálás: a reakcióelegy „pool” szekvenálása több analitikai buktatót is rejt. ↓ Megelőző analitikai HPLC Egyéb módszerek HPLC: a jelölt oligopeptidek alkalmazásához képest csökkent érzékenység ↓ A reakcióidő növelése

Mikronalalitikai kurzus szubsztrátkönyvtár Optimális közös peptidgerinc tervezése. Megfontolások • P 1 pozícióban a két archetípust, a tripszin és kimotripszin specificitást reprezentáló oldalláncok: Arg, Lys, Trp, Phe, Tyr és Leu • P 1 pozícióban a HPLC elválasztás belső standardjaként az egyik komponens tartalmazzon inert aminosavat: Pro-t • A közös szekvencia egyformán elfogadható vagy elfogadhatatlan mindkét archetípus és várhatóan a belőlük származtatható mutánsok, általában S 1 A proteinázok számára. • P 1’ pozícióban nem tartalmazhatnak a szerin proteináz hidrolízisben kedvezőtlen, „tiltott” aminosavakat: prolint, savas oldalláncot. • A közös szekvencia aminosavai nem szolgálhatnak jó hasítási helyként szerin proteinázok számára. • Az oligopeptideknek oldhatóaknak kell lenniük fiziológiás körülmények között, §nem tartalmazhatnak az oldódást gátló hidrofób „magot” §lehetőleg tartalmazzanak az oldódást megkönnyítő hidrofil oldalláncokat. • A peptidszekvenciákban ne legyenek olyan savas vagy bázikus „magok”, melyek a p. H helyi megváltoztatása révén befolyásolhatják az enzimreakció lefolyását. • Kerülendő olyan aminosavak beépítése, melyek problémát okozhatnak a szintézis vagy a tisztítási lépések során.

Mikronalalitikai kurzus szubsztrátkönyvtár Optimális közös peptidgerinc tervezése A közös P 4 -P 2’ mag tervezése • P 1 pozíció: Arg, Lys, Trp, Phe, Tyr, Leu és Pro • P 2 pozíció: hatóhely preferenciák konszenzusa alapján, illeszkedve a klasszikus kromogén szubsztrátokhoz: Pro • P 3 pozíció: hatóhely preferenciák konszenzusa alapján, illeszkedve a klasszikus kromogén szubsztrátokhoz: kis hidrofób: Ala • P 4 pozíció: hatóhely preferenciák konszenzusa alapján, illeszkedve a klasszikus kromogén szubsztrátokhoz: kis hidrofób: Ala • P 1’ pozíció: hatóhely preferenciák konszenzusa alapján, átlagosan elfogadott: Ser • P 2’ pozíció: hatóhely preferenciák konszenzusa alapján kis hidrofób: Ala

Mikronalalitikai kurzus szubsztrátkönyvtár Retenciós idő becslés A peptidkeverék komponensek retenciós időinek becslésére a következő képletet használtuk Tr= B+AS Dini Ahol Tr a retenciós idő, Di: i aminosav oldallánc hozzájárulása a peptid retenciójához, ni: i aminosav száma a peptidben, A és B: a kromatográfiás rendszerre az oszlop, holttérfogatok, gradiens, és az eluensek által meghatározott állandók. Aminosav D Gly 4, 0 Ser 1, 1 Ala 2, 4 Thr 7, 4 Val 7, 4 His 7, 8 Ile Leu Phe Tyr Trp Met 27, 4 26, 4 31, 4 21, 0 35, 8 14, 5 Arg Lys Asp Glu Asn Gln -3, 1 -0, 1 0, 0 2, 7 7, 9 3, 2 Pro 7, 9

Mikronalalitikai kurzus szubsztrátkönyvtár Optimális közös peptidgerinc tervezése. A komponensek RP-HPLC elválasztásának hangolása. Retenciós idő hangoló tagok bevitele Analitikai célú bővítés A magszekvencia retenciós viszonyai Rekker retenciós idő (TRr) lépés ha X peptid N HAAPXSADIQI HAAPXSADI HAAPXSA 5. 4. 3. 2. T HAAPXSADIQIDI 1. C SADIQIDI SADIQI SADI SA 88, 7 61, 4 30, 8 3, 5 K R P Y L F W 18, 4 9, 6 21, 5 12, 7 29, 4 20, 6 42, 5 33, 7 47, 9 39, 1 52, 9 44, 1 57, 3 48, 5 107, 1 79, 8 49, 2 21, 9 13, 1 110, 2 82, 9 52, 3 25, 0 16, 1 118, 1 90, 8 60, 2 32, 9 24, 1 131, 2 104 73, 3 46, 0 37, 2 136, 6 109, 3 78, 7 51, 4 42, 6 141, 6 114 83, 7 56, 4 47, 6 146 119 88, 1 60, 8 52

Mikronalalitikai kurzus szubsztrátkönyvtár RP-HPLC körülmények beállítása Lehetséges adattartományok: • A teljes szeparációs tartományt kihasználva adatgyűjtést végzünk az N-, és C-terminális peptidek és az intakt szubsztrátok retenciós tartományában. • Az adatgyűjtést csak az N-, és C-terminális peptidek retenciós tartományában végezzük. • Csak a C-terminális és az intakt peptidek retenciós tartományában gyűjtünk adatokat. A gradiens elúció sarokpontjai: Elválasztási körülmények • Oszlop: Aquapore OD 300 (2, 1 x 220 mm) • Áramlási sebesség: 300 ml/perc • Injektálási térfogat: 5 ml • Detektálás: 220 nm, 0, 05 Full Scale Ekvilibrálás Injektálás Elválasztás Mosás Idő [perc] Összetétel [%B] -12 -0 23 -23 0 -5 23 -23 5 -31 23 - 35 31 -35 100 -100
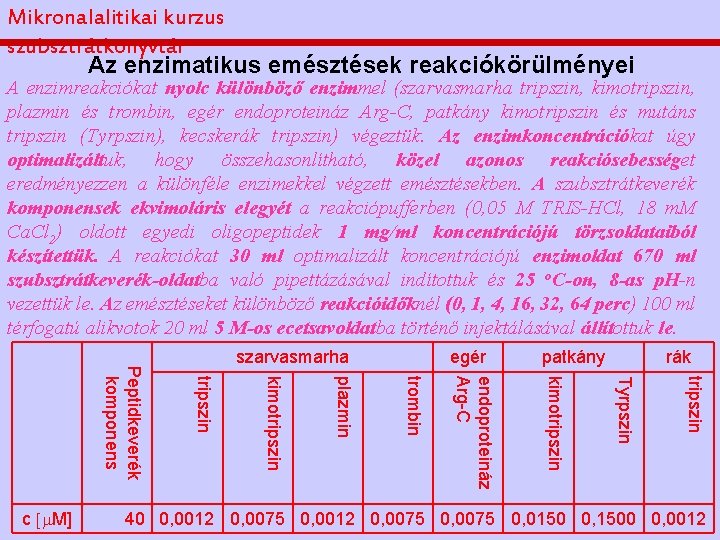
Mikronalalitikai kurzus szubsztrátkönyvtár Az enzimatikus emésztések reakciókörülményei A enzimreakciókat nyolc különböző enzimmel (szarvasmarha tripszin, kimotripszin, plazmin és trombin, egér endoproteináz Arg-C, patkány kimotripszin és mutáns tripszin (Tyrpszin), kecskerák tripszin) végeztük. Az enzimkoncentrációkat úgy optimalizáltuk, hogy összehasonlítható, közel azonos reakciósebességet eredményezzen a különféle enzimekkel végzett emésztésekben. A szubsztrátkeverék komponensek ekvimoláris elegyét a reakciópufferben (0, 05 M TRIS-HCl, 18 m. M Ca. Cl 2) oldott egyedi oligopeptidek 1 mg/ml koncentrációjú törzsoldataiból készítettük. A reakciókat 30 ml optimalizált koncentrációjú enzimoldat 670 ml szubsztrátkeverék-oldatba való pipettázásával indítottuk és 25 o. C-on, 8 -as p. H-n vezettük le. Az emésztéseket különböző reakcióidőknél (0, 1, 4, 16, 32, 64 perc) 100 ml térfogatú alikvotok 20 ml 5 M-os ecetsavoldatba történő injektálásával állítottuk le. kimotripszin rák tripszin patkány Tyrpszin egér endoproteináz Arg-C trombin plazmin kimotripszin Peptidkeverék komponens c [m. M] szarvasmarha 40 0, 0012 0, 0075 0, 0150 0, 1500 0, 0012
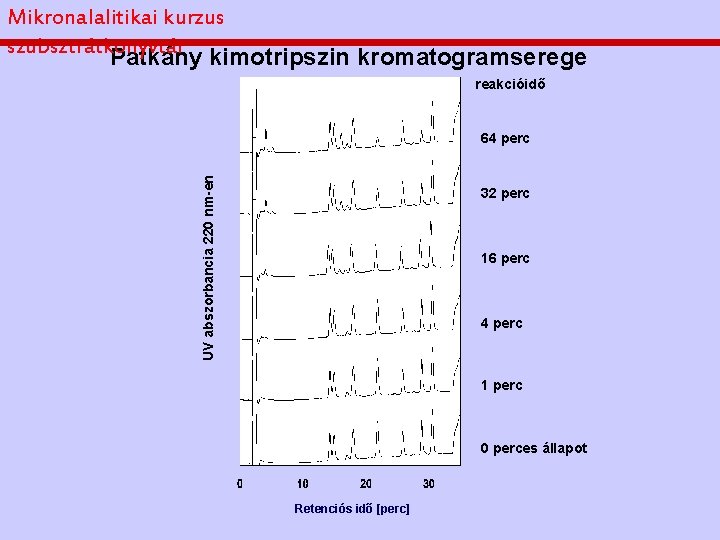
Mikronalalitikai kurzus szubsztrátkönyvtár Patkány kimotripszin kromatogramserege reakcióidő UV abszorbancia 220 nm-en 64 perc 32 perc 16 perc 4 perc 1 perc 0 perces állapot Retenciós idő [perc]
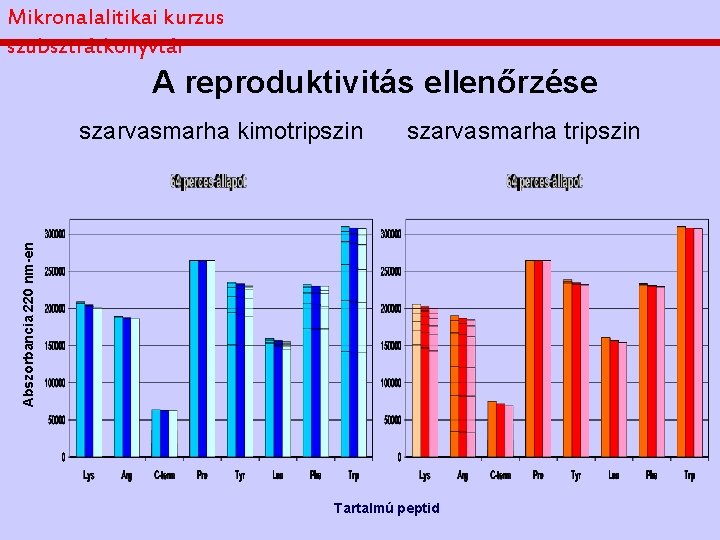
Mikronalalitikai kurzus szubsztrátkönyvtár A reproduktivitás ellenőrzése szarvasmarha tripszin Abszorbancia 220 nm-en szarvasmarha kimotripszin Tartalmú peptid
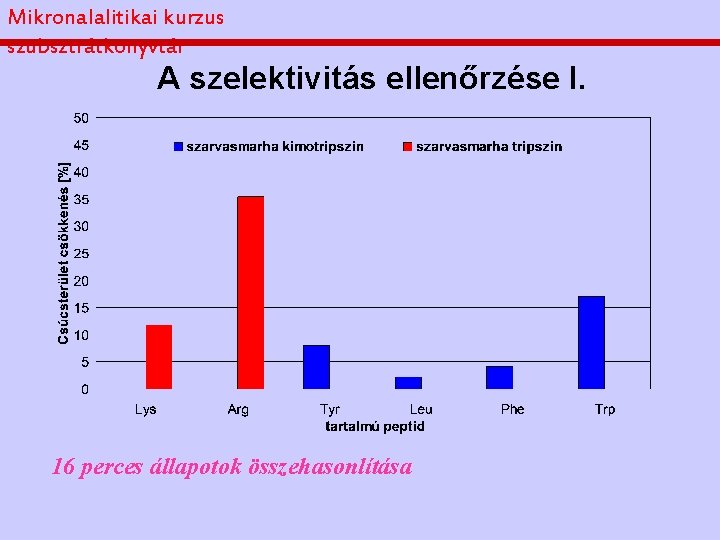
Mikronalalitikai kurzus szubsztrátkönyvtár A szelektivitás ellenőrzése I. 16 perces állapotok összehasonlítása

Mikronalalitikai kurzus szubsztrátkönyvtár A szelektivitás ellenőrzése II. 16 perces állapotok összehasonlítása Phe tartalmú peptid fogyására normalizált diagram
![Csúcsterület csökkenés [%] Szerin proteinázok tesztelése 16 perces állapotok összehasonlítása Csúcsterület csökkenés [%] Szerin proteinázok tesztelése 16 perces állapotok összehasonlítása](http://slidetodoc.com/presentation_image_h2/a9e3d6036f5c4d7b44bfa78a76664dbc/image-19.jpg)
Csúcsterület csökkenés [%] Szerin proteinázok tesztelése 16 perces állapotok összehasonlítása
- Slides: 19

















