Mikrobiom GI czowieka Prof dr hab Adam Jaworski

Mikrobiom GI człowieka Prof. dr hab. Adam Jaworski, UŁ i Społeczna Akademia Nauk „Najcenniejszym przymiotem Natury jest Jej Rozmaitość” Aleksander Świętochowski Żyjemy w epoce bakterii , tak było na początku , teraz , zawsze i na wieki.

Żyjemy w świecie trapionym przez nowe plagi Pomimo ogromnych postępów w medycynie, ochronie zdrowia i terapii chorób ludzie cierpią na nowe tajemnicze przypadłości zwane „ 10 plagami współczesności” : otyłość, cukrzycę, astmę, alergie wziewne i pokarmowe, refluks, rak przełyku, celiakię, chorobę Leśnikowskiego - Crona, wrzodziejące zapalenie jelita grubego, autyzm, egzemę. Otyłość - na świecie żyje 1, 5 mld ludzi z nadwagą, w tym otyłych o, 5 mld. Cukrzyca typu I (dziecięca insulino-zależna ), o podłożu autoimmunologicznym w krajach bogatych podwaja się co 20 lat. Wzrost zachorowalności na astmę; w USA 25 mln ludzi cierpi na astmę. Alergie pokarmowe, nietolerancje i alergie na białka obecne w żywności. Egzema (przewlekłe zapalenie skóry) dotyka ponad 15 % dzieci w USA. Autyzm, choroba o nieznanych przyczynach, zawiązana podobnie, jak wyżej wymienione „plagi współczesności, z dysfunkcja układu odpornościowego. Pytanie, czy dla tych 10 „plag współczesności” istnieje 10 odmiennych przyczyn, czy też jedna przyczyna leży u podstaw i napędza ich ekspansję w ludzkiej populacji ?

„Współczesne plagi” Należy postawić pytanie, czy istnieje 10 odmiennych przyczyn dla wymienionych 10 współczesnych plag? A może jedna, ale jaka? Profesor Martin Blaser, światowej klasy uczony, lekarz, lider badań nad mikroflorą człowieka, w swojej znakomitej książce „Utracone Mikroby” stawia tezę, że każda z tych chorób może mieć inne, oddzielne przyczyny, ale może istnieć tylko jeden czynnik będący siłą napędową dla wszystkich 10 plag? W książce pisze „Wierzę, że czynnikiem tym jest niekorzystna zmiana składu naszego mikrobiomu, rezydujących w nas mikrobów w czasie najintensywniejszego rozwoju organizmu, w pierwszych miesiącach życia każdego człowieka.

Antybiotyki a otyłość Płacimy z różnych powodów ogromna cenę za zanikanie bioróżnorodności mikrobiomu człowieka, który ewoluował z nami na przestrzeni milionów lat. Jednym z powodów jest nadużywanie antybiotyków, sulfonamidów, leków oraz innych medycznych i niemedycznych środków , jak antyseptyków. Utrata bioróżnorodności zmienia kierunek naszego rozwoju; ma ogromny wpływ na metabolizm, układ odpornościowy, a nawet zdolności poznawcze. Badania przeprowadzone na myszach dowiodły jednoznacznie, że u myszy karmionych we wczesnym dzieciństwie antybiotykami następuje zmiana składu mikrobioty jelita grubego, nadprodukcja SCAFs. co w konsekwencji prowadzi do szybszego wzrostu tkanek, masy ciała, odkładania tłuszczu i otyłości. Martin Baser, 2018 W latach 1991 -2 oo 6 w Wielkiej Brytani badaniom ankietowym poddano 14 500 kobiet. Jedno pytań brzmiało: „Czy Twoje dziecko dostawało w dzieciństwie (po 6, 15, 24 miesiącach życia) antybiotyki” ? Do wieku 2 lat trzy czwarte dzieci miło kontakt z antybiotykami. Analiza statystyczna ujawniła, że w grupie dzieci, którym podawano antybiotyki w pierwszych 6 miesiącach życia, otyłość pojawiała się znacznie częściej.

Przeciwzapalne działanie SCAFs Badania przeprowadzone na modelu myszy w 2015 roku przez Veena Taneja w Mayo Clinic na Florydzie wskazują, że SCAFs mogą hamować rozwój chorób autoimmunizacyjnych. W jelicie grubym wegetarian zidentyfikowano bardzo obfitą populację bakterii Prevotella, która bardzo hamująco wpływa na rozwój stwardnienia rozsianego i reumatoidalnego u modelowych myszy. Badaczka twierdzi, że w Indiach, gdzie wegetariańska dieta jest powszechna, znacznie mniej ludzi cierpi na artretyzm i reumatoidalne zapalenie stawów niż w USA. Trwają prace nad identyfikacją w przewodzie pokarmowym bakterii, producentów SCAFs, które podawanie doustnie będę wspomagać leczenie RSZ i stwardnienia rozsianego.

Aktywność fizyczna promuje syntezę SCAFs W trakcie regularnych ćwiczeń fizycznych wzrasta w jelitach poziom krótko-łańcuchowych kwasów tłuszczowych (SCFA), produktów bakteryjnej fermentacji (mleczanu, octanu, propionianu, maślanu), które mają działanie przeciwzapalne, a być może także przeciwnowotworowe. Kwasy te są także źródłem energii dla komórek nabłonkowych okrężnicy, obniżają p. H, zwiększają wchłanianie wapnia, żelaza oraz magnezu. Badania na myszach i ludziach dowiodły, że regularne ćwiczenia fizyczne, niezależnie od diety, promują rozwój w jelicie grubym populacji bakterii bardzo korzystnych dla zdrowia człowieka, produkujących duże ilości SCAFAs, w tym zwlaszcza maślanu. Prof. Jefrey Woods, University of Illionis, USA, „Gut Microbes”, 2017
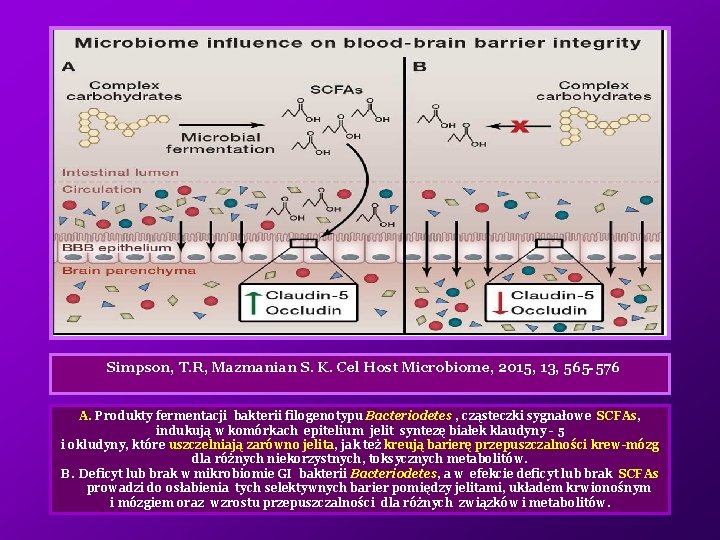
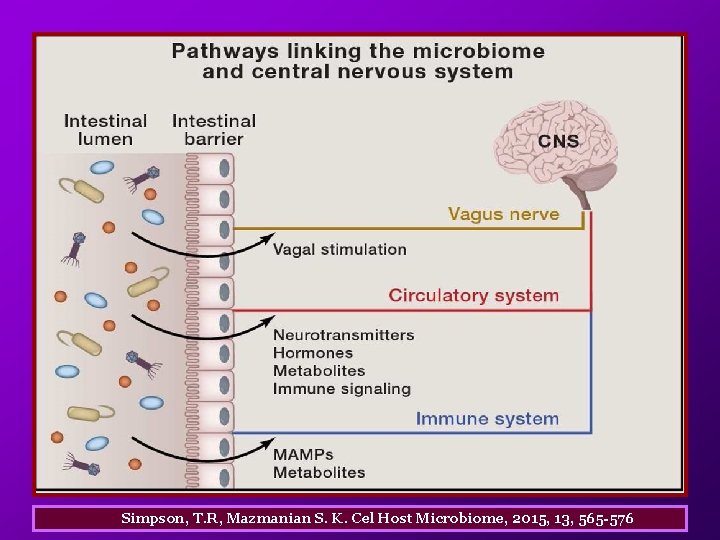
Simpson, T. R, Mazmanian S. K. Cel Host Microbiome, 2015, 13, 565 -576 A. Produkty fermentacji bakterii filogenotypu Bacteriodetes , cząsteczki sygnałowe SCFAs, indukują w komórkach epitelium jelit syntezę białek klaudyny - 5 i okludyny, które uszczelniają zarówno jelita, jak też kreują barierę przepuszczalności krew-mózg dla różnych niekorzystnych, toksycznych metabolitów. B. Deficyt lub brak w mikrobiomie GI bakterii Bacteriodetes, a w efekcie deficyt lub brak SCFAs prowadzi do osłabienia tych selektywnych barier pomiędzy jelitami, układem krwionośnym i mózgiem oraz wzrostu przepuszczalności dla różnych związków i metabolitów.
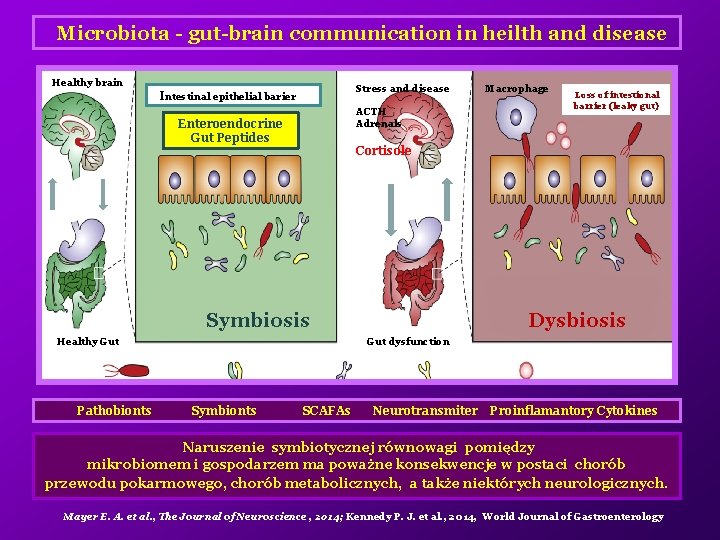
Microbiota - gut-brain communication in heilth and disease Healthy brain Stress and disease Intestinal epithelial barier ACTH Adrenals Enteroendocrine Gut Peptides Loss of intestional barrier (leaky gut) Cortisole Symbiosis Healthy Gut Pathobionts Macrophage Dysbiosis Gut dysfunction Symbionts SCAFAs Neurotransmiter Proinflamantory Cytokines Naruszenie symbiotycznej równowagi pomiędzy mikrobiomem i gospodarzem ma poważne konsekwencje w postaci chorób przewodu pokarmowego, chorób metabolicznych, a także niektórych neurologicznych. Mayer E. A. et al. , The Journal of Neuroscience , 2014; Kennedy P. J. et al. , 2014, World Journal of Gastroenterology
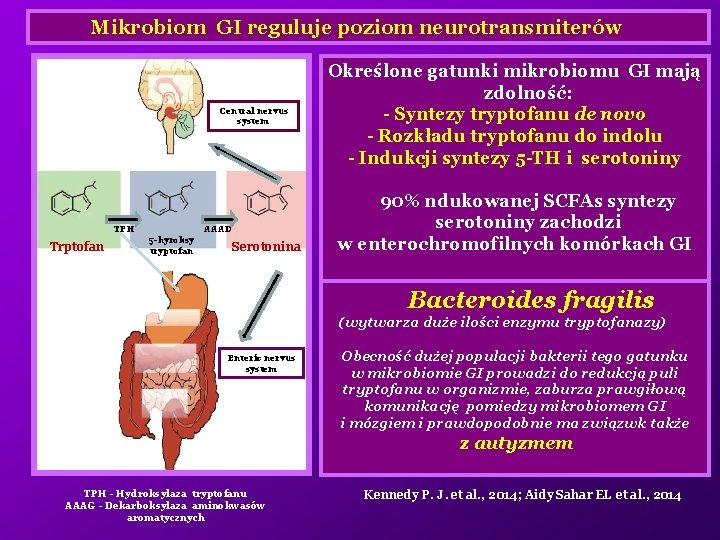
Mikrobiom GI reguluje poziom neurotransmiterów Central nervus system TPH Trptofan AAAD 5 -hyroksy tryptofan Serotonina Określone gatunki mikrobiomu GI mają zdolność: - Syntezy tryptofanu de novo - Rozkładu tryptofanu do indolu - Indukcji syntezy 5 -TH i serotoniny 90% ndukowanej SCFAs syntezy serotoniny zachodzi w enterochromofilnych komórkach GI Bacteroides fragilis (wytwarza duże ilości enzymu tryptofanazy) Enteric nervus system Obecność dużej populacji bakterii tego gatunku w mikrobiomie GI prowadzi do redukcją puli tryptofanu w organizmie, zaburza prawgiłową komunikację pomiedzy mikrobiomem GI i mózgiem i prawdopodobnie ma związwk także z autyzmem TPH - Hydroksylaza tryptofanu AAAG - Dekarboksylaza aminokwasów aromatycznych Kennedy P. J. et al. , 2014; Aidy Sahar EL et al. , 2014

Autyzm Schorzenie zostało po raz pierwszy opisane w 1943, jako bardzo rzadko spotykane. Dzisiaj 1 na około 90 dzieci cierpi na autyzm lub zaburzenia ze spektrum autyzmu. Liczba zachorowań od lat 60 -tych ubiegłego wieku wzrosła czterokrotnie. Istnieje wiele teorii próbujących wytłumaczyć wzrost zachorowalności na autyzm: toksyny w pożywieniu i powietrzu, kontakt z chemikaliami i pestycydami, szczepionki ( najmniej prawdipodobne) Obecnie specjaliści sugerują: odpowiedzialne mogą być mikroby jelitowe (niekorzystne zmiany ich struktury ), które na wczesnych etapach zakłócają rozwój mózgu.

Mikrobiom GI reguluje poziom neurotrasmiterów Systematycznie narasta wiedza na temat roli mikrobiomu GI w regulacji poziomu także innych ważnych neurotransmiterów: dopaminy, serotoniny, norepinefryny, kwasu γ-aminomasłowego (GABA), acetylocholiny. Dowiedziono, że bakterie Clostridium sporogenes i Ruminococcus gnavus produkują w przewodzie pokarmowym człowieka (w wyniku dekarboksylacji tryptofanu) tryptaminę, silny inhibitor 5 -HT. System ten spełnia funkcje regulacji samopoczucia i apetytu. Prawdopodobnie tryptamina może penetrować przez barierę krew mózg i bezpośrednio oddziaływać na centralny układ nerwowy. Innym przykładem jest tyramina, produkt dekarboksylacji tyrozyny przez bakterie Lactobacillus brevis i Enterococcus sp. , która również może modulować niektóre funkcje neurologiczne. Wiadomo, że wiele bakterii fermentacji mlekowej ma zdolność syntezy cząsteczek sygnałowych 5 -TH i GABA. Simpson T. , Mazmanian S. K. , 2015; Gershon M. D. , 2013; Lyte M. , 2013, 2014; Wiliams et al. . 2014

Komunikacja pomiędzy mikrobiomem GI a mózgiem Intensywna komunikacja pomiędzy jelitami i mózgiem zachodzi za pomocą cząsteczek sygnałowych oraz najdłuższego nerwu czaszkowego, jakim jest nerw błędny. Zaobserwowano, że gryzonie pozbawione flory bakteryjnej zachowują się tak, jakby nie znały poczucia strachu przed niebezpieczeństwem, a w hipokampie mózgu zwierząt ujawniono poważne zmiany, zaburzające reakcję na zagrożenie i stres. Stany zapalne jelit człowieka, będące skutkiem „chorego” mokrobiomu” mogą manifestować się stanami przygnębienia, a nawet depresji, w wyniku wydzielania cytokin prozapalnych mających działanie depresyjne. Około 30% pacjentów z zaburzeniami funkcji jelit cierpi na depresje i lęki. Borre Y. A. , Advances in Experimental Biology, 2014; Mayer E. A. et al. , The Journal of Neuroscience , 2014 Kennedy P. J. World Journal of Gastroenetology, 2014
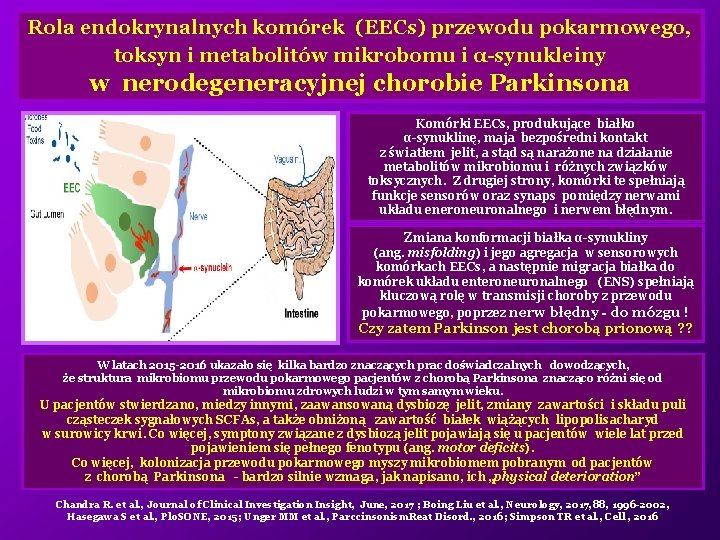
Rola endokrynalnych komórek (EECs) przewodu pokarmowego, toksyn i metabolitów mikrobomu i α-synukleiny w nerodegeneracyjnej chorobie Parkinsona Komórki EECs, produkujące białko α-synuklinę, maja bezpośredni kontakt z światłem jelit, a stąd są narażone na działanie metabolitów mikrobiomu i różnych związków toksycznych. Z drugiej strony, komórki te spełniają funkcje sensorów oraz synaps pomiędzy nerwami układu eneroneuronalnego i nerwem błędnym. Zmiana konformacji białka α-synukliny (ang. misfolding) i jego agregacja w sensorowych komórkach EECs, a następnie migracja białka do komórek układu enteroneuronalnego (ENS) spełniają kluczową rolę w transmisji choroby z przewodu pokarmowego, poprzez nerw błędny - do mózgu ! Czy zatem Parkinson jest chorobą prionową ? ? W latach 2015 -2016 ukazało się kilka bardzo znaczących prac doświadczalnych dowodzących, że struktura mikrobiomu przewodu pokarmowego pacjentów z chorobą Parkinsona znacząco różni się od mikrobiomu zdrowych ludzi w tym samym wieku. U pacjentów stwierdzano, miedzy innymi, zaawansowaną dysbiozę jelit, zmiany zawartości i składu puli cząsteczek sygnałowych SCFAs, a także obniżoną zawartość białek wiążących lipopolisacharyd w surowicy krwi. Co więcej, symptony związane z dysbiozą jelit pojawiają się u pacjentów wiele lat przed pojawieniem się pełnego fenotypu (ang. motor deficits). Co więcej, kolonizacja przewodu pokarmowego myszy mikrobiomem pobranym od pacjentów z chorobą Parkinsona - bardzo silnie wzmaga, jak napisano, ich „physical deterioration” Chandra R. et al. , Journal of Clinical Investigation Insight, June, 2017 ; Boing Liu et al. , Neurology, 2017, 88, 1996 -2002, Hasegawa S et al. , Plo. SONE, 2015; Unger MM et al. , Parccinsonism. Reat Disord. , 2016; Simpson TR et al. , Cell , 2016

Czy zabieg (ang. Vagotomy) zmniejsza ryzyko choroby Parkinsona, czy może spowalnia proces nasilania się objawów choroby ? W praktyce klinicznej stosuje dwa rodzaje przerwania przekaźnictwa sygnałów pomiędzy mózgiem i przewodem pokarmowym przez nerw błędny: całkowite przerwanie przekaźnictwa (ang. truncal vagatomy) dotyczy wielu organów (żołądka, wątroby, pęcherza moczowego, trzustki, jelita cienkiego oraz proksymalnej części jelita grubego. Zaś selektywna vegatomia dotyczy tylko żołądka. Stąd, formułowano hipotezę, że strategia chirurgiczna, vagatomy, może obniżyć ryzyko choroby Parkinsona, skoro wadliwie pofałdowana α-synukleina, podobnie jak inne białka prionowe , podlegają transmisji z jelit do mózgu poprzez najdłuższy nerw czaszkowy - nerw błędny. Wyniki opublikowanych w ostatnich latach prac doświadczalnych są obiecujące, aczkolwiek kontrowersyjne, a postawione wnioski końcowe należy traktować jako wstępne, zachęcające obserwacje. I tak, w 2015 roku donoszono, że „bilateral vagatomy” obniża ryzyko choroby Parkinsona, jednak wyniki innej pracy, z maja 2017 roku, dla 4. 93 o pacjentów w Szwecji, wskazują, że jedynie „truncal vagotomy”, przeprowadzona 5 lat przed postawieniem diagnozy, statystycznie znacząco obniżyła ryzyko choroby Parkinsona.
Simpson, T. R, Mazmanian S. K. Cel Host Microbiome, 2015, 13, 565 -576

Podsumowanie - przez jelita do mózgu Mikrobiom GI, czyli wszystkie bakterie, wirusy i grzyby zasiedlające przewód pokarmowy człowieka, stał się w ostatnich latach obiektem bardzo intensywnych badań. NIH i inne rządowe instytucje USA wydały już ponad 21 mln dolarów, a Europa 14 mln dolarów - na projekty badawcze, których celem jest rozpoznanie zależności między rozwojem i funkcjonowaniem mózgu i mikrobiomem, w tym pomiędzy chorobami psychicznymi i składem zasiedlających nas drobnoustrojów. Mikrobiom oddziałuje zarówno na nasze zdrowie fizyczne jak i psychiczne, na rozwój mózgu w dzieciństwie; ma także istotny wpływ na choroby takie jak depresje, stany lękowe, a także na niektóre choroby neurodegeneracjne.

„If you have alternation in the brain, you will almost certainly have altered output to the gut because the two organs are that closely connected. Conversely, feedback signals from the gut to the brain go well beyond obvious hungry-versus-full massage; abnormalities in the digestive system can directly shape both cognitive and emotional state”. Dr Emeran Mayer, University of California, Los Angeles.

„Antybiotykowa zima” Winą za ograniczenie bioróżnorodności mikrobiomu profesor Martin Blazer obarcza nadmierne dążenie do nadmiernej czystości, porody „cesarskim cieciem”, wiele współczesnych praktyk medycznych, a przede wszystkim: Nadmierne stosowanie od ponad 50 lat antybiotyków i innych leków w medycynie i w produkcji żywności. Pisze, że zmierzamy w kierunku sytuacji, którą nazywa „antybiotykową zimą” Pisze to w nawiązaniu do książki Tachel Carson „Cicha Wiosna”, w której autorka ostrzega, że ptaki mogą wyginąć z powodu nadużywania pestycydów, Profesor Blazer pisze: „My możemy podążać tą samą drogą”

„Tajemnica zdrowia człowieka tkwi w bardzo dużej części nie w materiale genetycznym, lecz w regulacji jego aktywności”. (Nessa Carey, Epigenetics-Revolution, 2012) „Genom człowieka jest jak scenariusz, ale w zależności od reżysera, aktorów i ich zamysłów nawet identyczny scenariusz może być bardzo różnie realizowany, a składniki diety oraz populacje mikrobioty czowieka są ważnymi regulatorami aktywności genów od poczęcia aż do śmierci”. (Adam Jaworski, 2017)

All disease begins in the gut”. „ Hipokrates „Człowiek jest tym, co je”. Lidwig Foeurbach
- Slides: 20