Mikrobioloki preparati Mikrobioloki preparati mikrobioloke preparate pravimo u
Mikrobiološki preparati

Mikrobiološki preparati - mikrobiološke preparate pravimo u cilju posmatranja MO (morfologija, struktura, oblik, raspored ćelija, pokretljivost…) Preparat može da bude: 1. Nativni preparat - posmatranje živih MO 2. Fiksirani preparat

Nativni preparat • • • posmatranje živih MO (pokretljivost) nedostatak-slaba vidljivost, mogućnost infekcije, jednokratna upotreba procedura pripreme: 1. 2. 3. na predmetnicu se stavlja uzorak (u slučaju tečne kulture stavlja se kap suspenzije, u slučaju čvrste podloge u kap fiziološkog rastvora unosi se materijal iz kulture) pokrovnica mikroskopiranje
Nativni preparat

Fiksirani preparat • • prednosti-višekratna upotreba, ne postoji mogućnost infekcije, posmatranje strukture, oblika i morfologije, ćelije lakše uočljive procedura pripreme: 1. 2. 3. 4. 5. nanošenje suspezije na predmetnicu i pravljenje razmaza sušenje na vazduhu fiksiranje (provlačenjem kroz plamen) kako bi ubili MO i fiksirali ih za predmetnicu bojenje preparata mikroskopiranje
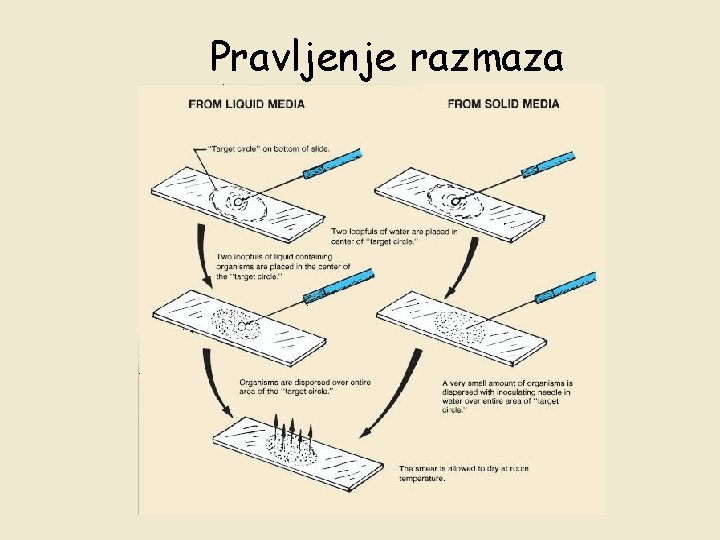
Pravljenje razmaza
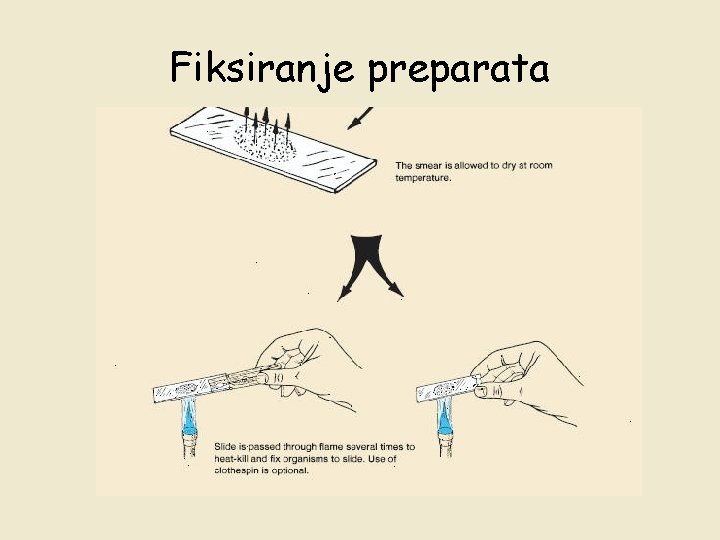
Fiksiranje preparata

Bojenje preparata 1. Prosto bojenje - koristi se 1 boja -uocavanje oblika i rasporeda celija -boje koje se primenjuju: kristal violet, safranin, metilensko plavo… 2. Slozeno bojenje - koristi se 2 ili vise boje -uocavanje morfologije i strukture celije -tipovi slozenog bojenja: bojenje po Gramm-u, bojenje acido-alkohol rezistentnih bakterija , bojenje kapsula, bojenje endospora, bojenje nukleinskih kiselina, bojenje flagela

Mikrobiološke boje • • 1. 2. 3. organska jedinjenja koja boje odredjene ćelijske strukture Prema poreklu dele se na: prirodne: šafranin (šafran), lakmus (lisajevi) veštačke (anilinske boje) soli koje prilikom pravljenja vodenih rastvora disosuju: bazno – katjonske boje (kristal violet, šafranin…) kiselo – anjonske boje, negativno bojenje (eozin) neutralno-neutralno crveno

Mikrobiološke boje • Svaka boja mora da sadrži dve grupe: 1. hromoformnu (nosilac karaktera boje, NO 2) 2. auksohromnu (el. disocija, OH¯, NH 2)

Prosto bojenje • 1. 2. 3. 4. Procedura: Pravljenje razmaza Sušenje (na vazduhu) Fiksiranje Bojenje -kristal violetom (na predmetnicu staviti filter hartiju i na nju naneti boju, nakon 1 -2 min ukloniti filter hartiju, preparat isprati vodom, osušiti filter hartijom, mikroskopiranje) -šafraninom-postupak je identičan, filter hartiju nije neophodno stavljati na preparat pre bojenja
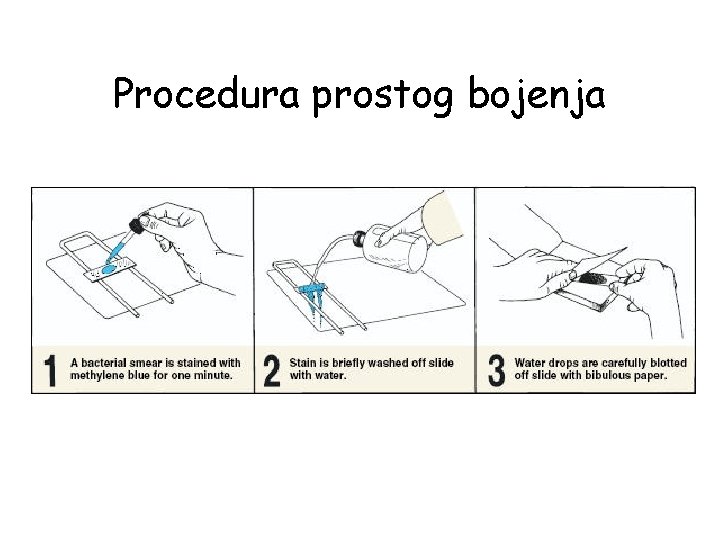
Procedura prostog bojenja
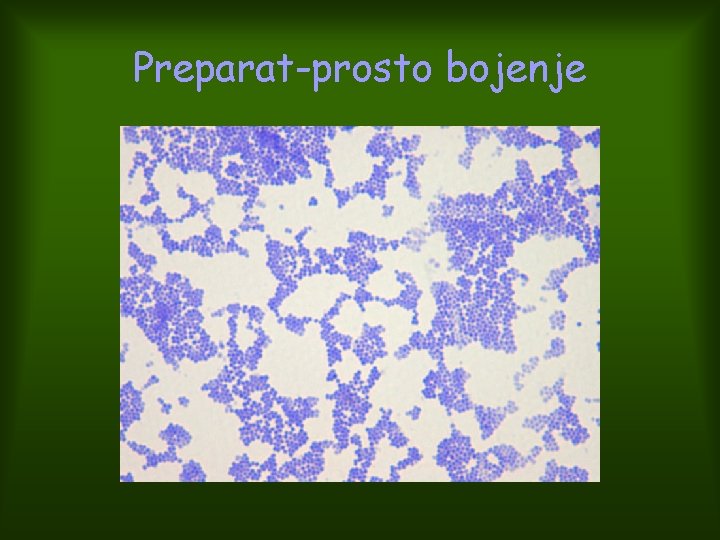
Preparat-prosto bojenje

Složeno bojenje-bojenje po Gramm-u • 1884. danski histolog Christian Gram razvio metod bojenja u cilju diferencijacije bakterijskih ćelija i nukleusa eukariotskih ćelija • diferencijalna slika (identifikacija Gr+ i Gr- bakterija) • na osnovu razlike u gradji cel. zida Gr+ bakterije boje se ljubičasto, dok se Gr- bakterije boje crveno • metoda se zasniva na sukcesivnoj primeni – – kristal violeta (osnovna boja) lugola (učvršćivač) – rastvor I u KI etanola (obezbojivač) 70% ili 95% šafranin (suprotna boja)

Procedura bojenja po Gramm-u • 1. 2. 3. 4. 5. 6. 7. Nakon pravljenja razmaza, sušenja na vazduhu i fiksiranja pristupa se proceduri bojenja preparata bojenje kristal violetom 1 -2 min (neophodno je staviti na preparat filter hartiju) lugol 1 -2 min ispiranje vodom ispiranje etanolom 5 -10 sec ispiranje vodom bojenje šafraninom 1 -2 min ispiranje vodom, susenje filter hartijom, mikroskopiranje
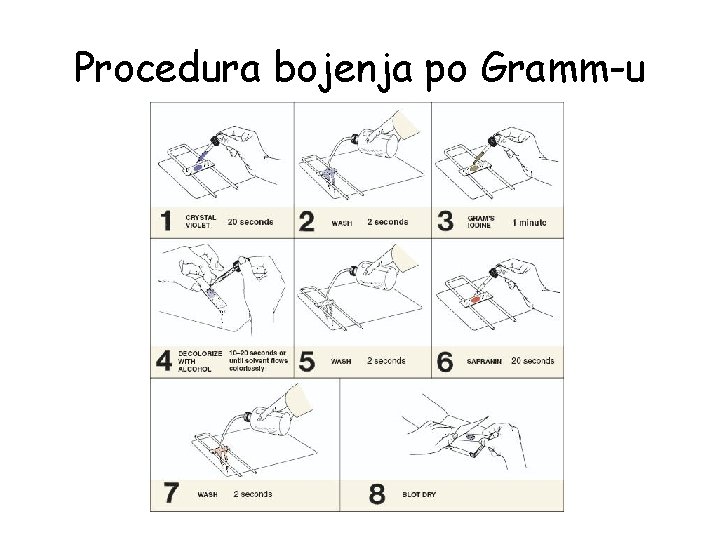
Procedura bojenja po Gramm-u
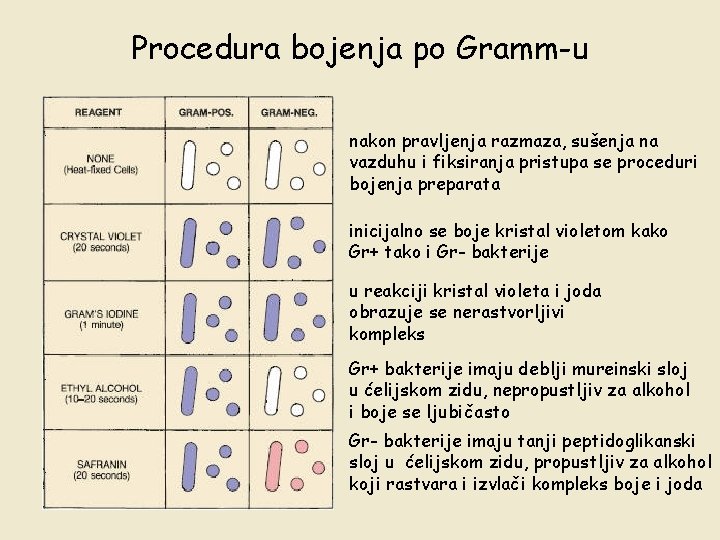
Procedura bojenja po Gramm-u nakon pravljenja razmaza, sušenja na vazduhu i fiksiranja pristupa se proceduri bojenja preparata inicijalno se boje kristal violetom kako Gr+ tako i Gr- bakterije u reakciji kristal violeta i joda obrazuje se nerastvorljivi kompleks Gr+ bakterije imaju deblji mureinski sloj u ćelijskom zidu, nepropustljiv za alkohol i boje se ljubičasto Gr- bakterije imaju tanji peptidoglikanski sloj u ćelijskom zidu, propustljiv za alkohol koji rastvara i izvlači kompleks boje i joda
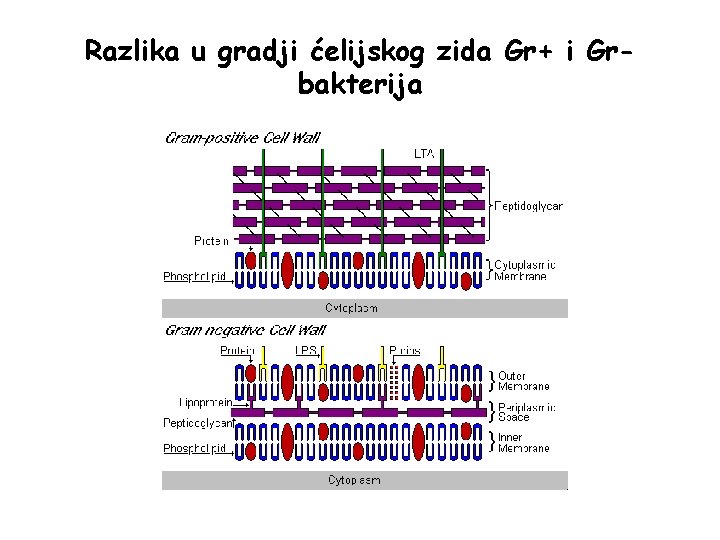
Razlika u gradji ćelijskog zida Gr+ i Grbakterija
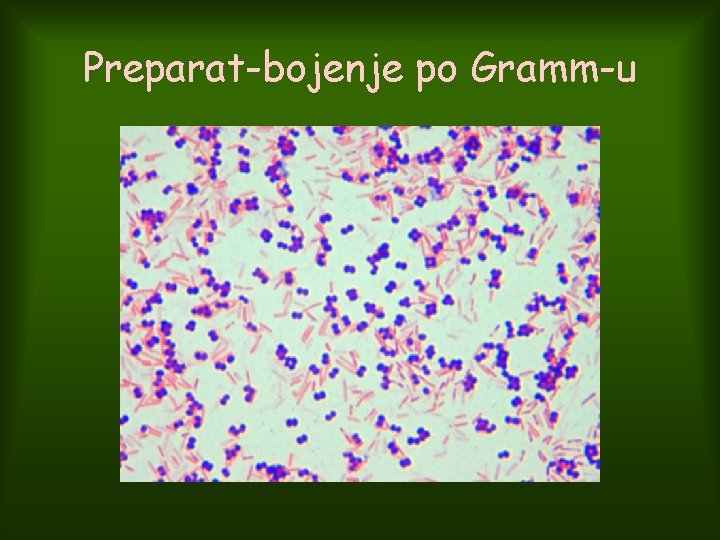
Preparat-bojenje po Gramm-u

Sporulacija • neke bakterije tokom rasta, procesom sporogeneze formiraju endospore • rezultat nepovoljnih uslova životne sredine, najčešće u uslovima limitiranosti nutrijentima (C, N najznacajniji) • karakteristike spora: odsustvo metaboličke aktivnosti, rezistentnost prema fizičkim i hemijskim činiocima (t°, UV, boje, hemijska jedinjenja, suša…) zbog prisustva egzosporijuma (proteinski omotač) • u povoljnim uslovima procesom germinacije formira vegetativnu ćeliju • jedna bakterijska celija najčešće formira samo 1 sporu • strukture koje služe za preživljavanje, a ne za razmnožavanje

Sporulacija • • rezistentnost na toplotu pripisuje se dehidriranom stanju i kalcijum dipikolinatu gradja spore: jezgro, zid, korteks, omotač, egzosporijum proces sporulacije odvija se u najmanje 7 faza tipovi sporulacije: 1. bacilarni-spora manjeg dijametra od ćelije (terminalno, subterminalno ili centralno postavljena) 2. klostridijalni-spora većeg dijametra od ćelije (centralno ili subterminalno postavljena) 3. plektridijalni-spora većeg dijametra od ćelije (terminalno postavljena)
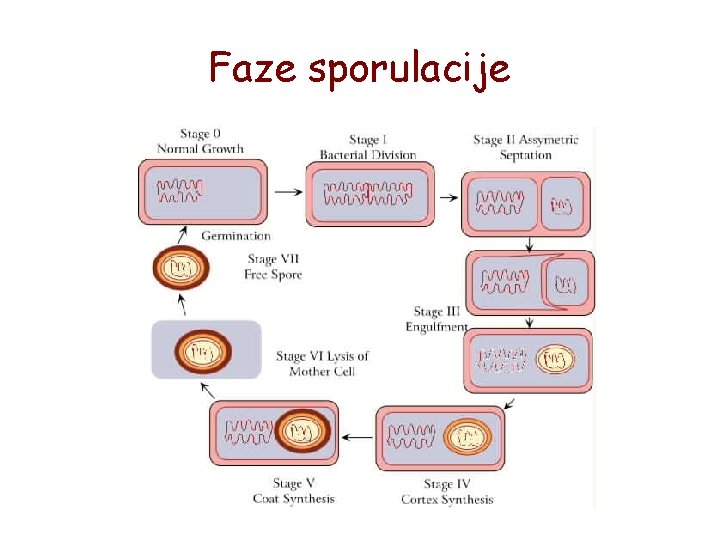
Faze sporulacije
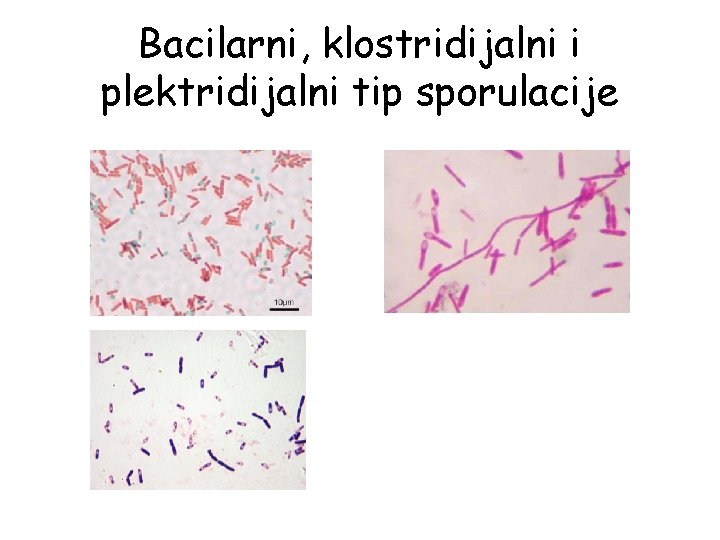
Bacilarni, klostridijalni i plektridijalni tip sporulacije

Bojenje endospora po Schaeffer. Fulton-u • zbog specifičnih fizičkih i hemijskih karakteristika spore teško usvajaju mikrobiološke boje (uočavaju se kao bezbojne intracelularne tvorevine kod prostog i bojenja po Gramm-u) • zagrevanjem preparata zid spore postaje propustljiv za boju, nepropustljivost zida omogućava da prilikom obezbojavanja alkohol ne prodire u sporu i ona ostaje obojena za razliku od drugih vegetativnih oblika bakterija

Bojenje endospora po Schaeffer. Fulton-u • • 1. 2. 3. 4. 5. • Nakon pravljenja razmaza, sušenja na vazduhu i fiksiranja, pristupa se bojenju preparata Procedura bojenja: Bojenje malahitno zelenom bojom (5%) 2 min, neophodno je koristiti filter hartiju Zagrevanje predmetnice na plamenu 3 -5 min (boja treba da isparava, ali ne da ključa), kada ispari veći deo boje doda se nova količina Ukloniti filter hartiju i ispirati vodom Bojenje safraninom 3 -5 min Ispiranje vodom, sušenje filter hartijom, mikroskopiranje Spore se boje zeleno, a vegetativne ćelije crveno
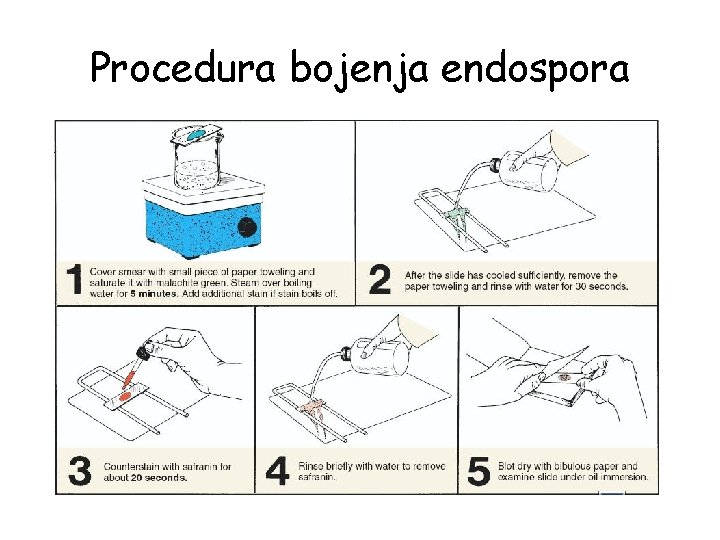
Procedura bojenja endospora

Bojenje acido-alkohol rezistentnih bakterija po Ziehl-Neelsen-u • bakterije koje na svojoj površini imaju voštane materije mogu se lako izdvojiti od drugih bakterija u razmazu • one primaju boju, ali se boja ne može isprati pod dejsvom alkohola i kiselina (acido-alkohol rezistentne) • bakterije bez voštanih materija na površini gube boju tokom ispiranja • acido-alkohol rezistentne bakterije na preparatima imaju crvenu boju, dok sve ostale imaju plavu boju • Acido-alkohol rezistentne bakterije: rod Mycobacterium, rod Nocardia

Procedura bojenja acido-alkohol rezistentnih bakterija 1. 2. 3. 4. 5. 6. 7. na fiksirani razmaz stavlja se filter hartija preko koje se naliva boja karbol fuksin predmetnica se blago zagreva iznad plamena tako da boja isparava, ali da ne ključa (topi se voštana ovojnica i omogućava prodiranje boje), kada veći deo boje ispari dodaje se nova količina, postupak se ponavlja u toku 5 min ispiranje vodom obezbojavanje smešom etilena i kiseline (HCl ili H 2 SO 4) 20 -30 sec ispiranje vodom bojenje metilensko plavim 1 -3 min ispiranje vodom, susenje u filter hartiji, mikroskopiranje
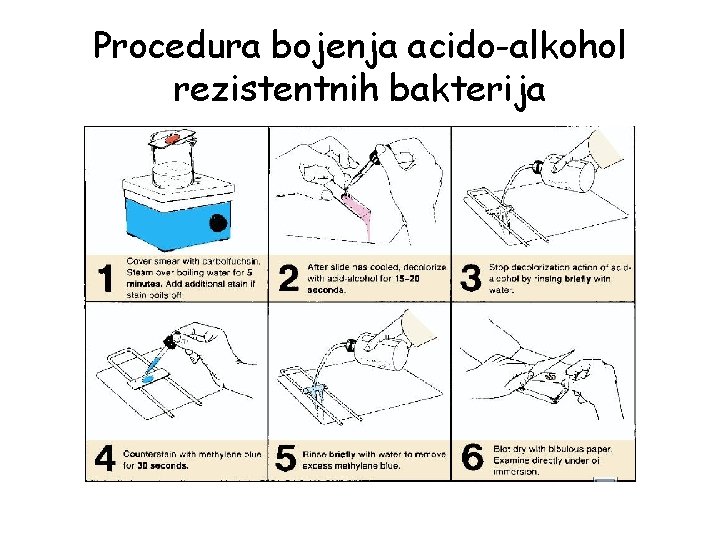
Procedura bojenja acido-alkohol rezistentnih bakterija

Negativno bojenje • podrazumeva upotrebu 1 kisele boje • boji se pozadina oko ćelija kako bi se lakše uočile veličina, oblik i organizacija celije • ćelije ostaju ne obojene • bakteriološki razmaz se ne fiksira toplotom (tačnija predstava oblika i veličine ćelije) • primenjuje se prilikom bojenja spirila i spiroheta, koje običnim postupkom prostog bojenja teže primaju boje

Procedura negativnog bojenja 1. 2. 3. 4. 5. na predmetnicu se stavlja kap nigrozina (tuša) bakterijske ćelije se prebacuju u kap nigrozina (ili tuša) drugom predmetnicom pravi se razmaz, prevlačeći je preko predmetnice sa uzorkom pod uglom od 45°, druga predmetnica se koristi kako bi se napravio tanak film ćelija razmaz se susi na vazduhu mikroskopiranje
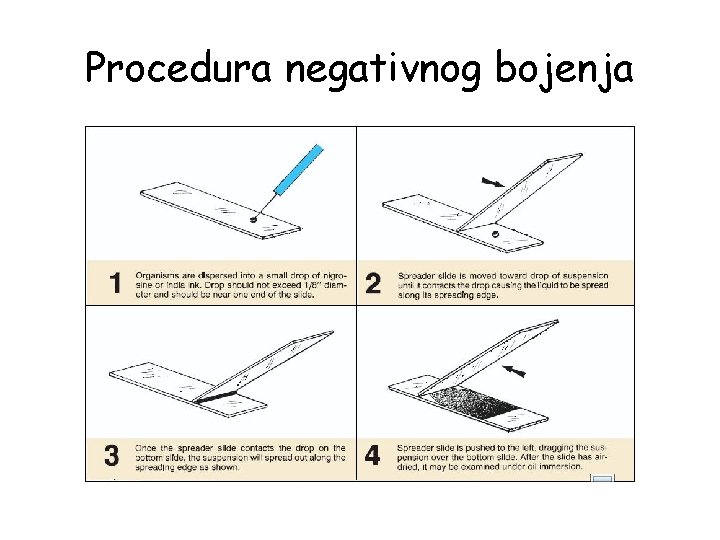
Procedura negativnog bojenja
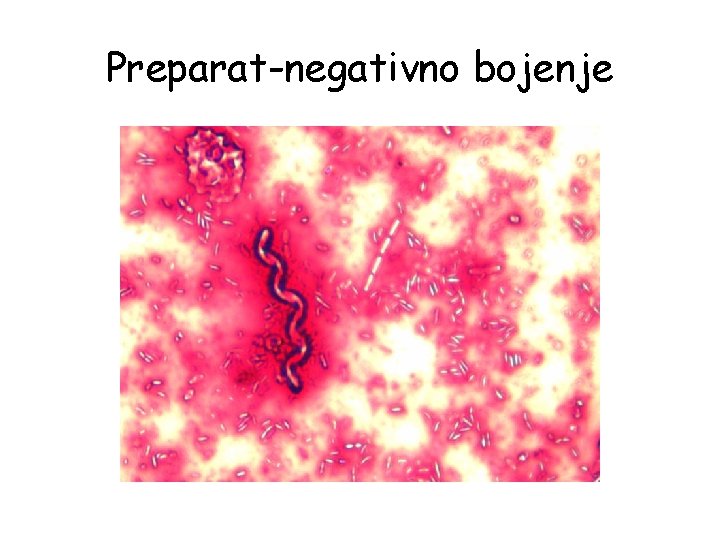
Preparat-negativno bojenje

Bojenje kapsula • neke bakterije tokom rasta formiraju kapsulu (glikokaliks) oko ćelije • štiti bakterijsku ćeliju od fizičkih i hemijskih faktora sredine, fagocitoze i predstavlja pomoćnu strukturu prilikom pripajanja ćelije za površinu u njihovoj sredini • kapsula-polisaharidna, redje polipeptidna struktura, faktor patogenosti, uočava se primenom kombinovane tehnike negativnog i prostog bojenja • tehnikom negativnog bojenja boji se pozadina primenom kisele boje (nigrozin, tus, eozin), dok se tehnikom prostog bojenja boje ćelije • razmaz se ne fiksira da se ne bi uništila kapsula, pa se ne preporucuje ispiranje vodom ili se to čini krajnje pažljivo da se bakterije ne speru

Bojenje kapsula • da bi se izbegli ovi problemi bakterije se nakon negativnog bojenja mogu fiksirati sa nekoliko kapi metil alkohola • pored ove metode koristi se i metoda bojenja razmaza kristal violetom (1%) 2 min, nakon čega se boja spira 20%-im rastvorom Cu 2 SO 4, obojeni razmaz se ne ispira vodom, suši se filter hartijom i mikroskopira, bakterije su obojene tamno ljubičasto, a kapsule plavičasto
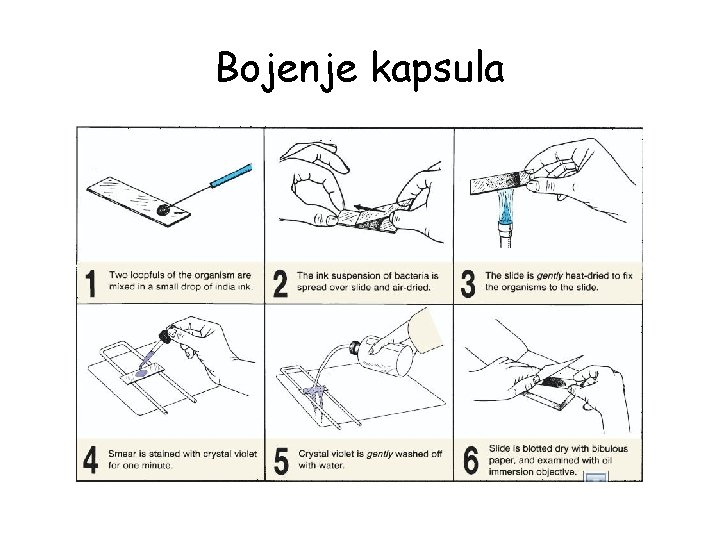
Bojenje kapsula
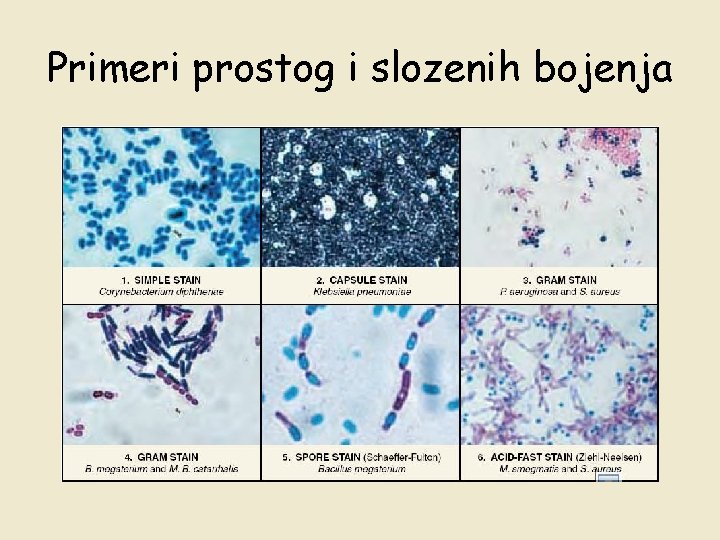
Primeri prostog i slozenih bojenja
- Slides: 38