mija 8 klase dens cilvka dzv 6 2










- Slides: 17

Ķīmija 8. klase Ūdens cilvēka dzīvē 6. 2. Šķīdumi. Aprēķina uzdevumi. 1

Kas notiks ar cukuru, ja to iebērs ūdenī? Kas notiks ar eļļu, ja to ielies ūdenī? Cukurs nogrims trauka dibenā, izšķīdīs. Eļļa nostāsies ūdens virspusē. 2

Šķīdumi ir viendabīgi maisījumi, kas sastāv no šķīdinātāja un izšķīdušās vielas. Šķīduma sasalšanas temperatūra ir zemāka nekā šķīdinātājam. Šķīduma viršanas temperatūra ir augstāka nekā šķīdinātājam. 3 http: //www. tutorbene. com/Images/inner-page/product_image-2. jpg

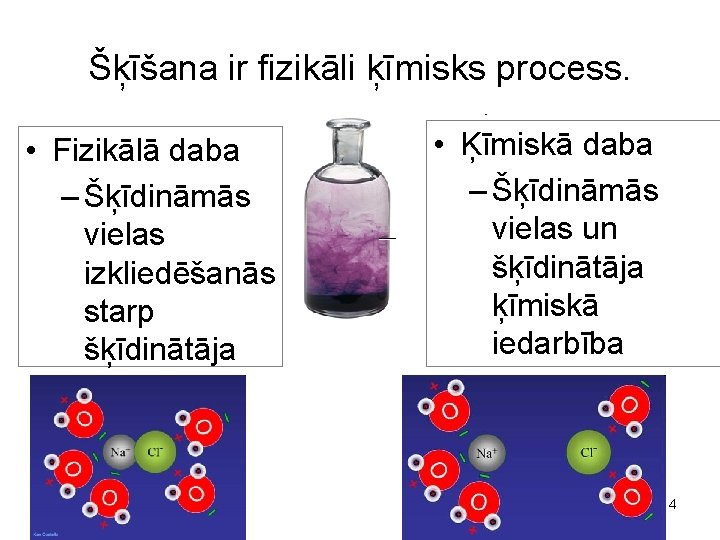
Šķīšana ir fizikāli ķīmisks process. • Fizikālā daba – Šķīdināmās vielas izkliedēšanās starp šķīdinātāja daļiņām • Ķīmiskā daba – Šķīdināmās vielas un šķīdinātāja ķīmiskā iedarbība 4

Šķīdība ir vielu spēja šķīst un veidot šķīdumus • Šķīstošas vielas • Mazšķīstošas vielas • Praktiski nešķīstošas vielas • Šķīdību izsaka ar vielas masu gramos, kas spēj izšķīst 100 g šķīdinātāja 5

Šķīdumi • Piesātināti – Viela dotajos apstākļos vairs nešķīst • Nepiesātināti – Viela dotajos apstākļos vēl var izšķīst Šķīdības atkarību no temperatūras, spiediena attēlo ar šķīdības līknēm. 6

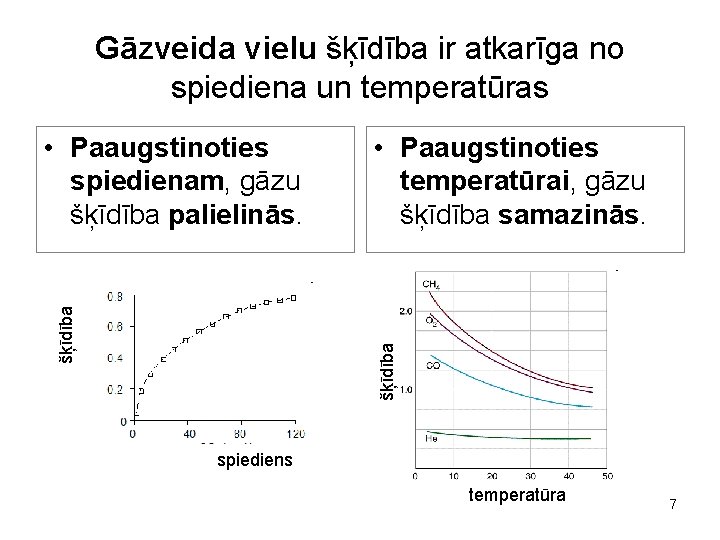
Gāzveida vielu šķīdība ir atkarīga no spiediena un temperatūras • Paaugstinoties temperatūrai, gāzu šķīdība samazinās. šķīdība • Paaugstinoties spiedienam, gāzu šķīdība palielinās. spiediens temperatūra 7

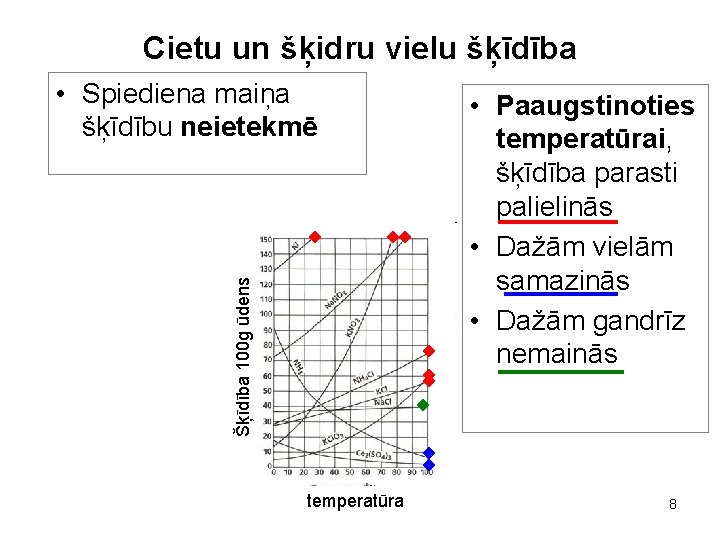
Cietu un šķidru vielu šķīdība Šķīdība 100 g ūdens • Spiediena maiņa šķīdību neietekmē temperatūra • Paaugstinoties temperatūrai, šķīdība parasti palielinās • Dažām vielām samazinās • Dažām gandrīz nemainās 8

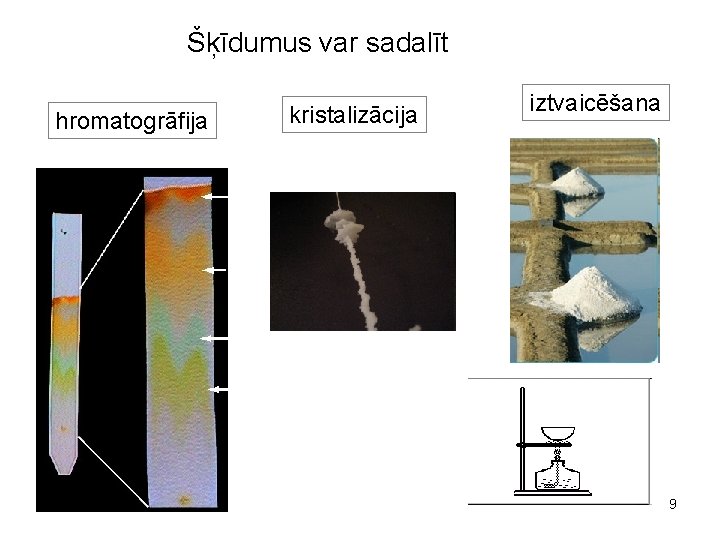
Šķīdumus var sadalīt hromatogrāfija kristalizācija iztvaicēšana 9

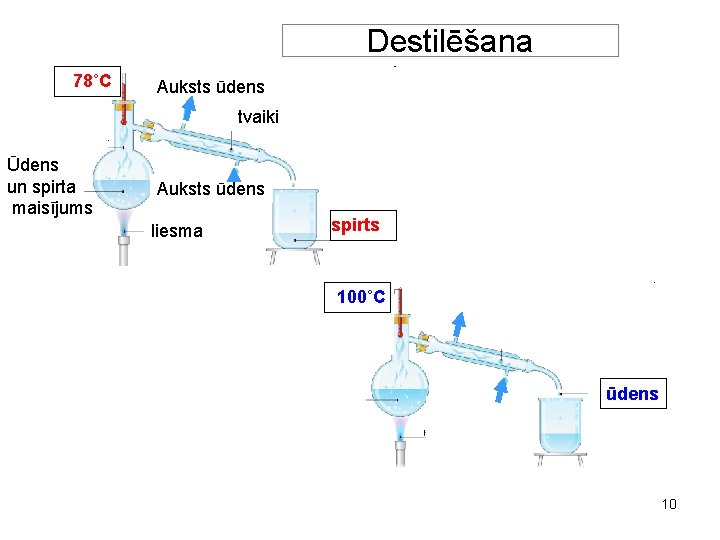
Destilēšana 78˚C Auksts ūdens tvaiki Ūdens un spirta maisījums Auksts ūdens liesma spirts 100˚C ūdens 10

Vielu šķīdības atkarība no temperatūras Vielas Šķīdība (g/100 g ūdens) 10˚C 50 ˚C KCl. O 3 6 20 Na. Cl 38 39 KCl 30 40 NH 4 Cl 32 50 KNO 3 22 80 11

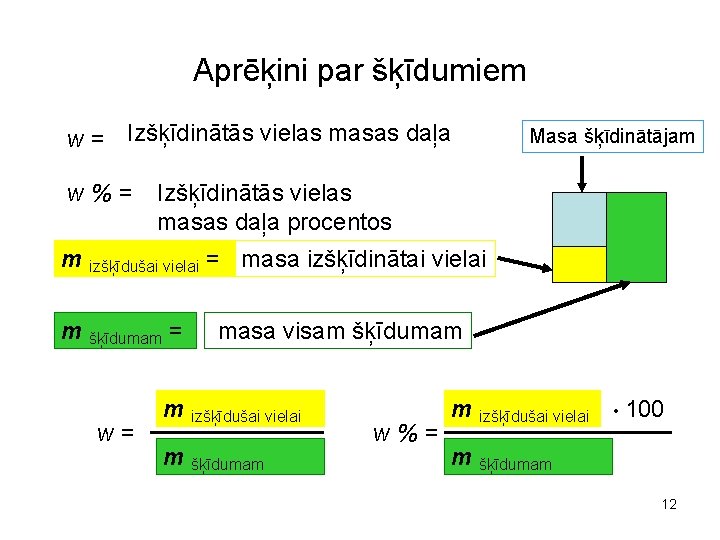
Aprēķini par šķīdumiem w = Izšķīdinātās vielas masas daļa w%= Masa šķīdinātājam Izšķīdinātās vielas masas daļa procentos m izšķīdušai vielai = masa izšķīdinātai vielai m šķīdumam = w= masa visam šķīdumam m izšķīdušai vielai m šķīdumam w%= m izšķīdušai vielai • 100 m šķīdumam 12

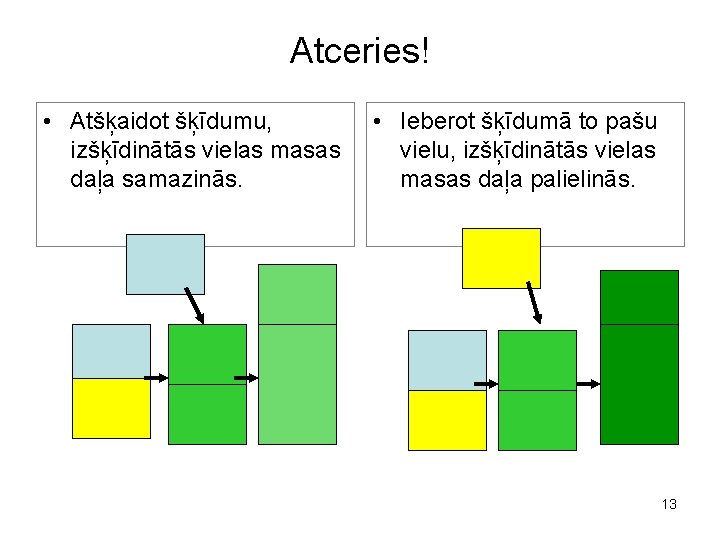
Atceries! • Atšķaidot šķīdumu, izšķīdinātās vielas masas daļa samazinās. • Ieberot šķīdumā to pašu vielu, izšķīdinātās vielas masas daļa palielinās. 13

Ja ūdenī šķīdina kādu vielu, tad iegūtā šķīduma blīvums kļūst vai nu mazāks, vai lielāks par ūdens blīvumu. m = ρ • V m = masa ρ = blīvums V = tilpums Šķīduma blīvuma noteikšanai izmanto areometru. 14

Cik gramu Na. Cl un cik gramu ūdens jāņem, lai pagatavotu 280 g nātrija hlorīda 5% šķīdumu? Dots w%= 5 mšķīd. = 280 g Jāaprēķina m(Na. Cl) =? m(H 2 O) =? w% = m izšķīdušai vielai • 100 m šķīdumam m izšķīdušai vielai = w% • m šķīdumam m(Na. Cl) = 5 • 280 100 = 14 g 100 m(H 2 O) = 280 – 14 = 266 g 15

Cik gramu Na. Cl un cik gramu ūdens vajadzīgs, lai pagatavotu 800 g 20% nātrija hlorīda šķīdumu? . m(Na. Cl) = 0, 2 • 800 = 160 g m(H 2 O) = 800 – 160 = 640 g 16

Paldies! 17