mija 8 klase dens cilvka dzv 6 1











- Slides: 17

Ķīmija 8. klase Ūdens cilvēka dzīvē 6. 1. Ūdens molekulārā uzbūve, īpašības 1

, Dzīvoš ilgi, ne tik ilgi, Saules mūžu nedzīvošu. Ūdentiņis, akmentiņis, Tie dzīvos saules mūžu. L. t. dz. 2

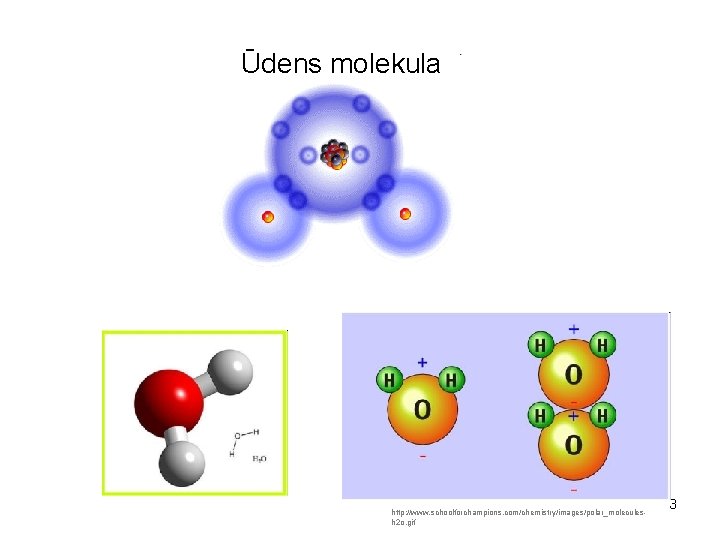
Ūdens molekula http: //www. schoolforchampions. com/chemistry/images/polar_moleculesh 2 o. gif 3

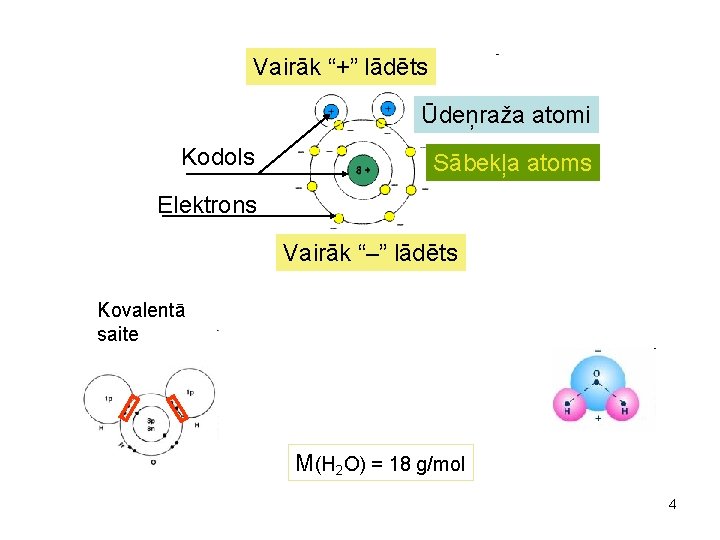
Vairāk “+” lādēts Ūdeņraža atomi Kodols Sābekļa atoms Elektrons Vairāk “–” lādēts Kovalentā saite M(H 2 O) = 18 g/mol 4

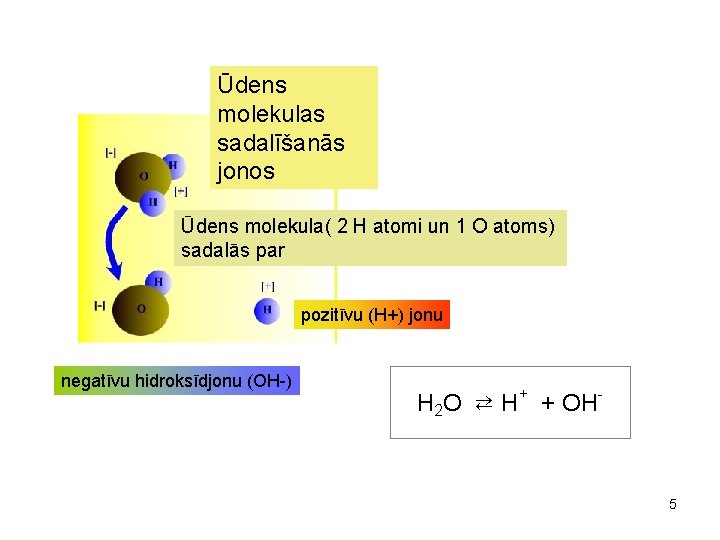
Ūdens molekulas sadalīšanās jonos Ūdens molekula( 2 H atomi un 1 O atoms) sadalās par pozitīvu (H+) jonu negatīvu hidroksīdjonu (OH-) + H 2 O H + OH- ← 5

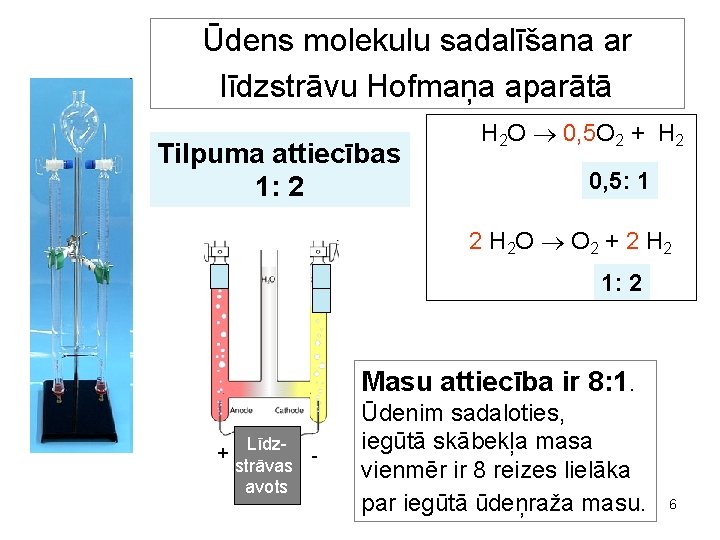
Ūdens molekulu sadalīšana ar līdzstrāvu Hofmaņa aparātā Tilpuma attiecības 1: 2 H 2 O 0, 5 O 2 + H 2 0, 5: 1 2 H 2 O O 2 + 2 H 2 1: 2 Masu attiecība ir 8: 1. + Līdzstrāvas avots Ūdenim sadaloties, iegūtā skābekļa masa vienmēr ir 8 reizes lielāka par iegūtā ūdeņraža masu. 6

Analīze – vielas sastāva noteikšana, to sadalot. Sintēze – sarežģītāka sastāva vielas Var uzzināt, kādā masu vai daudzuma iegūšana no attiecībā elementi ir vienkāršākām vielām. savienojušies. Savienošana. Ūdens molekulas var iegūt no ūdeņraža un skābekļa, iedarbojoties ar elektrisko dzirksteli. 7

Elementu masu attiecības aprēķini ūdenim H 2 O Ar (H) = 1 Ar (O) = 16 2 Ar (H) : Ar (O) 2 • 1 : 16 /: 2 1 : 8 36 = x +8 x 36 = 9 x x = 36: 9 x = 4 36 = 4 +32 4 : 32 = 1: 8 Masas nezūdamības likums 4 g H 2 32 g O 2 8

Ūdens krāsa, garša, smarža Tīram ūdenim ir ļoti vāji zila krāsa, kas redzama tikai tad, ja ūdens ir lielā tilpumā. Tīrs ūdens ir bez smaržas un garšas. 9

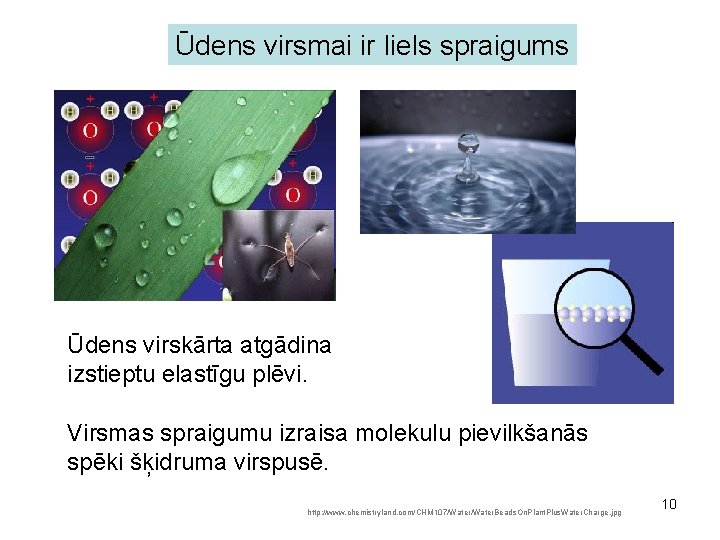
Ūdens virsmai ir liels spraigums Ūdens virskārta atgādina izstieptu elastīgu plēvi. Virsmas spraigumu izraisa molekulu pievilkšanās spēki šķidruma virspusē. http: //www. chemistryland. com/CHM 107/Water. Beads. On. Plant. Plus. Water. Charge. jpg 10

Ūdens lēni sasilst un lēni atdziest. Tam piemīt liela siltumietilpība. Okeāni uzņem aptuveni 80% no siltuma, kuru rada siltumnīcas gāzes. 11

Kādēļ ledus peld? Temperatūra ˚C Blīvums g/cm 3 0 (ciets) 0. 9150 0 (šķidrs) 0. 9999 4 1. 0000 20 0. 9982 40 0. 9922 60 0. 9832 80 0. 9718 100 (gāzveida) 0. 0006 Ūdens sasalstot izplešas 12

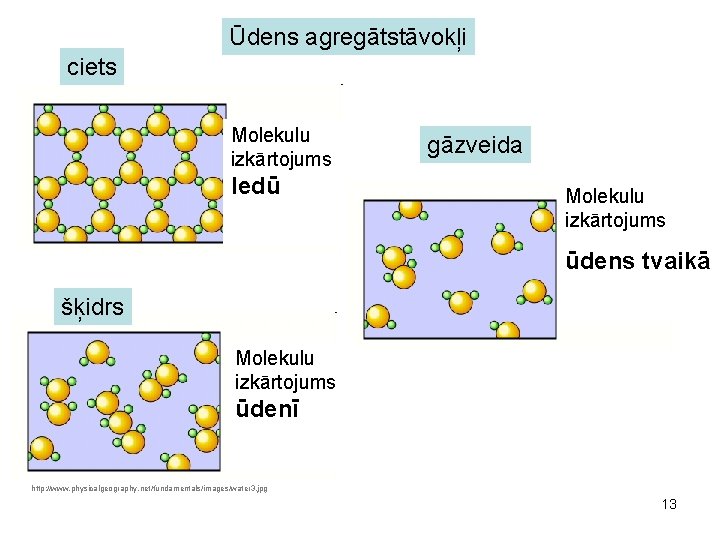
Ūdens agregātstāvokļi ciets Molekulu izkārtojums ledū gāzveida Molekulu izkārtojums ūdens tvaikā šķidrs Molekulu izkārtojums ūdenī http: //www. physicalgeography. net/fundamentals/images/water 3. jpg 13

Sniegpārsliņas vienmēr ir sešstūrainas 14

• Japāņu zinātnieks Dr. Masaru Emoto veica virkni eksperimentus, kuros ūdens vispirms tika pakļauts dažādai informatīvai ietekmei, bet pēc tam uz 2 stundām ievietots saldētavā. Sasaldētie ūdens kristāli tika pētīti zem mikroskopa un fotografēti, ar palielinājumu no 200 līdz 500 reizēm 15

Ūdens struktūras izmaiņas Sasalstot un pēc tam atkūstot, ūdens no savas atmiņas dzēš visu informāciju, atstājot vienu vienīgo – bāzes informāciju, dzīvības programmu. 16

Paldies! 17