Microbiologa de Alimentos ALTERACIN DE LPIDOS RANCIDEZ 6

Microbiología de Alimentos ALTERACIÓN DE LÍPIDOS RANCIDEZ 6º Química 2014 Escuela Técnica ORT

Deterioro de lípidos IMPORTANCIA • Es una de las principales causas de deterioro durante el almacenamiento • Se pierde el valor nutricional • Salubridad • Características organolépticas
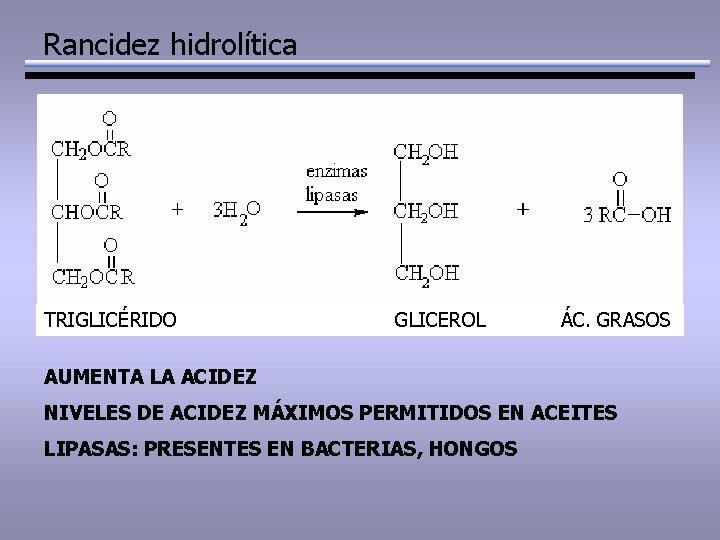
Rancidez hidrolítica TRIGLICÉRIDO GLICEROL ÁC. GRASOS AUMENTA LA ACIDEZ NIVELES DE ACIDEZ MÁXIMOS PERMITIDOS EN ACEITES LIPASAS: PRESENTES EN BACTERIAS, HONGOS

Rancidez oxidativa • AFECTA ÁCIDOS GRASOS INSATURADOS • SE FORMAN HIDROPERÓXIDOS • DAN LUGAR A COMPUESTOS CARBONÍLICOS VOLÁTILES ALDEHÍDOS, CETONAS DE OLOR Y SABOR DESAGRADABLES (OLOR RANCIO) NIVELES DE PERÓXIDOS MÁXIMOS EN ACEITES

Factores ALIMENTO • Composición de ácidos grasos: Saturados/Insaturados, nº de dobles enlaces • Prooxidantes (Fe, Cu) • Antioxidantes (naturales, sintéticos) • Aw (máximo cuando es menor de 0. 2) MEDIO AMBIENTE • O 2 • Energía radiante

Rancidez oxidativa MECANISMO POR RADICALES LIBRES EN 3 ETAPAS: • INICIACIÓN - H alfa al doble enlace - Formación de radicales libres • PROPAGACIÓN - Formación de hidroperóxidos, descomposición y formación de nuevos radicales libres • TERMINACIÓN - Agotamiento de radicales libres
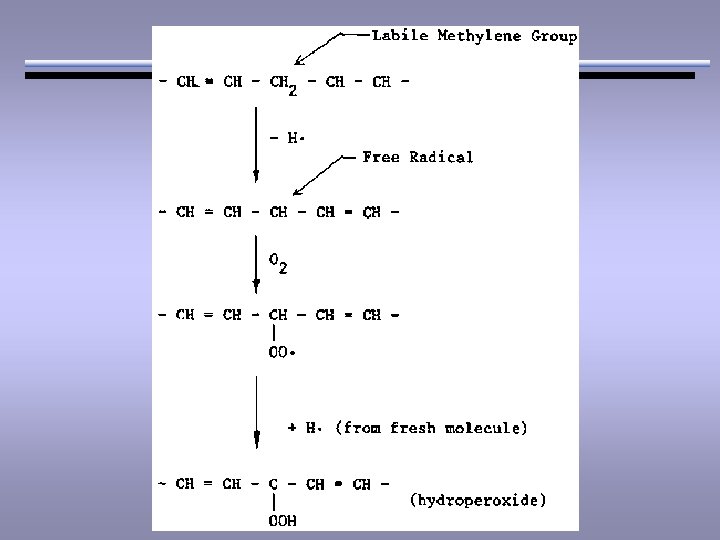

Iniciación ACIDO GRASO: R-COOH LO ESCRIBIMOS RH RH luz UV, radicales libres, Fe, Cu (catalizadores) R. Captación de O 2 R. + O 2 ROO.
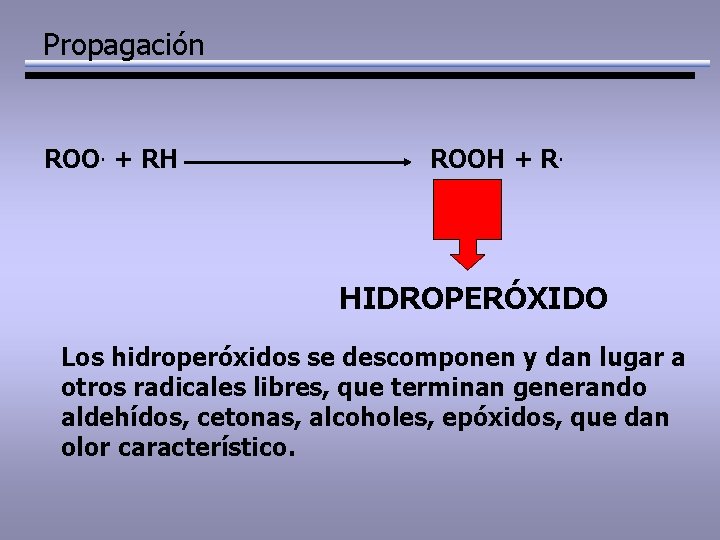
Propagación ROO. + RH ROOH + R. HIDROPERÓXIDO Los hidroperóxidos se descomponen y dan lugar a otros radicales libres, que terminan generando aldehídos, cetonas, alcoholes, epóxidos, que dan olor característico.
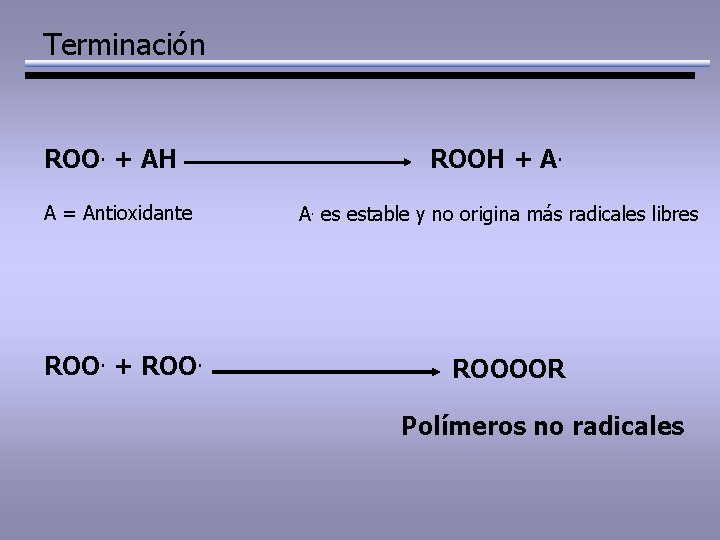
Terminación ROO. + AH A = Antioxidante ROO. + ROOH + A. A. es estable y no origina más radicales libres ROOOOR Polímeros no radicales
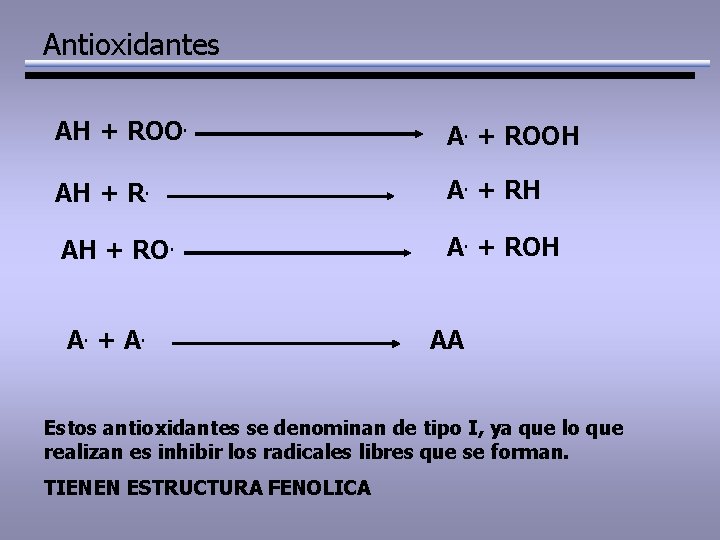
Antioxidantes AH + ROO. A. + ROOH AH + R. A. + RH AH + RO. A. + ROH A. + A. AA Estos antioxidantes se denominan de tipo I, ya que lo que realizan es inhibir los radicales libres que se forman. TIENEN ESTRUCTURA FENOLICA
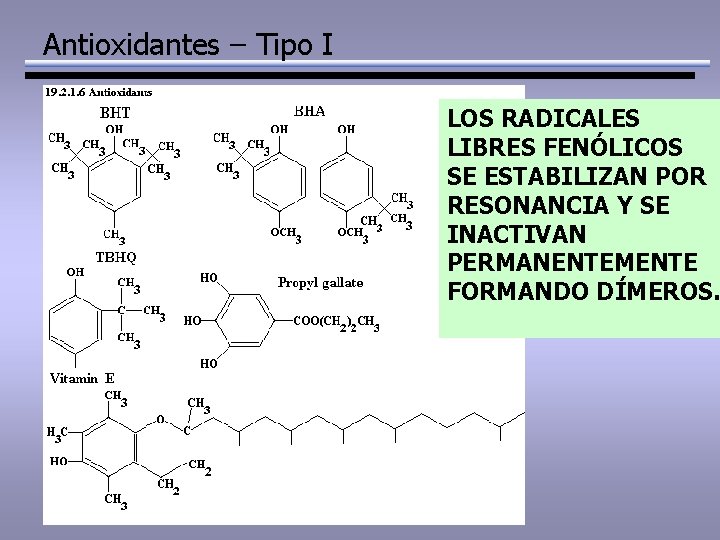
Antioxidantes – Tipo I LOS RADICALES LIBRES FENÓLICOS SE ESTABILIZAN POR RESONANCIA Y SE INACTIVAN PERMANENTEMENTE FORMANDO DÍMEROS.

Antioxidantes – Tipo II Los antioxidantes de tipo II no reaccionan directamente con los radicales libres, sino que evitan su formación mediante la complejación de los iones Fe 2+ y Cu 2+, que actúan como cofactores. Ejemplos: ácido cítrico, H 3 PO 4, citratos
- Slides: 13