MHENDSLK FAKLTES EVRE MHENDSL MB 238 evre Kimyas

MÜHENDİSLİK FAKÜLTESİ ÇEVRE MÜHENDİSLİĞİ ÇMB 238 – Çevre Kimyası II Prof. Dr. Gülfem BAKAN

KİMYASAL OKSİJEN İHTİYACI TAYİNİ ÇMB 238 – Çevre Kimyası II Hafta – 10

Teori • Kimyasal oksijen ihtiyacı (KOI), evsel ve endüstriyel atık suların organik kirlilik derecesini belirlemede kullanılan en önemli parametrelerden biridir. • KOI numunedeki organik maddenin kuvvetli kimyasal oksidasyon maddeleri yardımı ile oksidasyonu sırasında harcanan oksijen miktarını ifade eder. Belirli kaynaklardan üretilen atıklar için Kimyasal Oksijen İhtiyacı (KOI), ampirik olarak Biyokimyasal Oksijen İhtiyacı (BOI), organik karbon veya organik madde içeriği ile orantılıdır.

Teori • Biyokimyasal oksijen ihtiyacı gibi ancak ondan farklı olarak organik maddenin biyokimyasal reaksiyonlara değil redoks reaksiyonlarıyla oksitlenmesi esasına dayanır.

• Yöntem birkaç istisna dışında tüm organik maddelerin, kuvvetli oksitleyicilerle asit ortamlarında oksitlenebilecekleri esasına dayanmaktadır. Oksidasyon ortamında karbonlu organik maddeler CO 2 ve H 2 O’ya, azotlu organik maddeler ise NH 3’e dönüşürler. • Ölçüm yöntemi bir redoks reaksiyonuna bağlı olduğu için, elektron transferinin olmadığı reaksiyonlara giren maddelerin KOI’sinden söz etmek olanaksızdır. KOI’nin aynı amaçla kullanılmakta olan BOI’ye göre en önemli üstünlüğü laboratuvarda kısa sürede belirlenebilmesidir. BOI değerinin tesbiti en az 5 gün sürmesine karşılık, KOI değeri yaklaşık 3 saat gibi kısa bir sürede ölçülebilmektedir. Bu nedenle bir çok durumda BOI yerine tercih edilir.

• Evsel atıksularda KOI değeri BOI 5’ in 2 katı civarındadır. • KOI deneyinde, biyolojik yollarla ayrışabilen ve ayrışamayan organik maddelerin ayırt edilmesinin olanaksızlığı, bu parametre için en büyük sakıncadır. • KOI testinde BOI’de olduğu gibi suyun ister doğada, isterse biyolojik arıtmada karşılaşacağı biyokimyasal reaksiyonları yerine, kimyasal reaksiyonlar kulla nılmaktadır.

• KOI tayininde sudaki birçok organik maddeler H 2 SO 4 ile asitlendirilmiş ortamda potasyum bikromat (ya da potasyum permanganat) ile geri soğutucu altında 2 saat süre ile ısıtılırsa tamamen kimyasal yükseltgenmeye uğrarlar. Potasyum bikromatın fazlası ferroin indikatörü eşliğinde ayarlı amonyum demir 2 sülfat çözeltisi ile geri titre edilerek KOI parametresi tayin edilir. Yükseltgenme sırasında bikromat iyonu aşağıdaki denkleme göre krom(3)'e indirgenir • Cr 2 O 7 2+ 14 H+ + 6 e → 2 Cr+3 + 7 H 2 O

• Tepkimenin yeterli hızda oluşabilmesi için katalizör olarak Ag 2 SO 4 katılmalıdır. • 6 Cl + Cr 2 O 7 2 + 14 H+ → 3 Cl 2 + 2 Cr+3 + 7 H 2 O • denklemine göre, klor iyonları da reaksiyona girerek sonucu etkileyebileceği ve aynı zamanda Ag+ iyonları ile çökerek Ag 2 SO 4'ün katalitik etkisini kaldırabileceği için; klor iyonları daha önce civa iyonlarıyla çöktürülerek ortamdan ayrılmalıdır.

ANORGANİK GİRİŞİMLER • Bazı indirgen anorganik iyonlar, KOI testi ile benzer koşullarda okside olabilirler ve hatalı sonuçların ortaya çıkmasına neden olurlar. Ortam da klorür bulunması halinde, bu iyon hem (Ag+) ’nun çöktürülmesi, hem potasyum bikromat ile redoks reaksiyonuna girmesi bakımından girişim oluşturur :

ANORGANİK GİRİŞİMLER • Klorür girişimi, ortama civa sülfat ilavesi ile giderilebilir. Civa iyonu klorür iyonu ile birleşerek zayıf iyonize olabilen civa klorür kompleksini teşkil eder. • Nitritler, nitrata okside edilirler ve bunların girişimi, bikromat çözeltisine sülfamik asit ilavesi ile giderilebilir.

KOI Verisinin Kullanımı • KOI deneyi, bileşenleri iyi bilinen su ve atıksularda, bu maddelerin konsantrasyonlarındaki değişmeleri incelemek üzere yaygın olarak kullanılır. • Çeşitli nedenlerle BOI testinin çok başarılı olmadığını bildiğimiz endüstriyel atıksularda, arıtma tesislerinin çalışmasını denetlemede KOI testine çok sık başvurulur. • BOI deneyi ile birlikte yapılacak KOI deneyleri toksik durumların ortaya çıkarılmasında ve biyolojik olarak indirgenemeyen organik maddelerin belirlenmesinde oldukça faydalıdır.

Deney için Gerekli Reaktifler • Standart potasyum dikromat çözeltisi (0, 25 N) : 12. 259 g (K 2 Cr 2 O 7), 103°C'de 2 saat kurutulup destile suda çözülür ve 1000 m. L' ye seyreltilir. • Gümüş sülfat: Reaktif veya teknik saflıkta, kristal veya toz halde. • Sülfürik asit reaktifi: 1 L derişik H 2 SO 4 üzerine 10, 2326 g Ag 2 SO 4 ilave edilir ve bir iki gün Ag 2 SO 4'ün çözünmesi için beklenir. • Sülfürik asit: Derişik (%96 saflıkta)

Deney için Gerekli Reaktifler • Standart demir amonyum sülfat titrasyon maddesi (yaklaşık 0. 25 N): 98 g Fe(NH 4)2(SO 4)2. 6 H 2 O, destile suda çözülür, 20 ml derişik H 2 SO 4 ilave edilir, soğutulur, 1000 ml'ye seyreltilir. Bu çözelti günlük olarak standart K 2 Cr 2 O 7 çözeltisine karşı standardize edilir. • 10 ml standart K 2 Cr 2 O 7 çözeltisi 100 ml' ye seyreltilir. 30 ml derişik H 2 SO 4 katılır ve soğutulur. Demir amonyum sülfat titrasyon maddesi ile 0. 10 0. 15 ml (2 3 damla) ferroin varlığında titre edilir. • Demir Amonyum Sülfat (DAS) Normalitesi = [Titre edilen 0. 25 N K 2 Cr 2 O 7 çözeltisi hacmi, ml] x 0. 25 / Tıtrasyonda kullanılan demir amonyum sülfat hacmi, ml

DENEYİN YAPILIŞI • 10 ml veya destile su ile 10 ml'ye seyreltilmiş numune 500 ml'lik KOI balonuna konur. 0, 2 g cıva sülfat katılır, karıştırılır. • 1 ml sülfürik asit reaktifi katılır, cıva sülfat çözünene kadar karıştırılır, soğutulur ve 5 ml 0. 25 N K 2 Cr 2 O 7 çözeltisi ilavesiyle karıştırılır. • KOI balonu geri soğutucuya bağlanır ve soğutma suyu devresi açılır. • Kalan 14 ml sülfürik asit KOI balonunun ağzından ilave edilir ve hemen geri soğutucu kapatılarak kaynatmaya başlanır. • Karışım geri soğutucu altında 2 saat süre ile kaynatılır. • Kaynatma tamamlanınca kondenser soğutulur ve yıkanır.

DENEYİN YAPILIŞI • KOI balonunun içindeki çözelti hacmi saf su ile yaklaşık iki katına seyreltilir, oda sıcaklığına kadar soğutulur. • Daha sonra 0, 10 0, 15 m. L (2 3 damla) ferroin ilavesi ile demir amonyum sülfat titrasyon çözeltisi ile titre edilir. • Titrasyon dönüm noktası olarak mavi yeşilden kırmızı kahverengiye doğru ilk renk değişiminin olduğu an esas alınır ve titrasyona son verilir. • Eğer numune hacmi 50 ml’den az ise, tablodaki oranları uygulayarak reaktif hacimleri seçilir. • Aynı şekilde saf su ile şahit numune hazırlanır, benzer şekilde reaktifler katılır ve geri soğutucu altında kaynatılır. Seyreltilerek, titrasyon işlemine tabi tutulur.
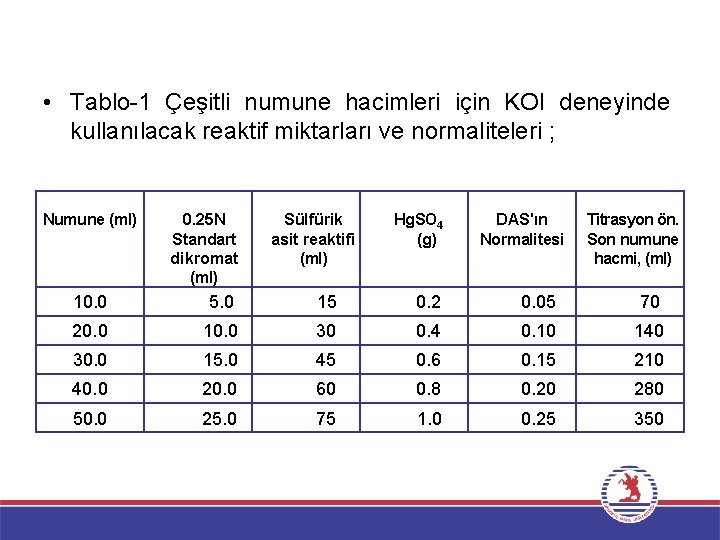
• Tablo 1 Çeşitli numune hacimleri için KOI deneyinde kullanılacak reaktif miktarları ve normaliteleri ; Numune (ml) 0. 25 N Standart dikromat (ml) Sülfürik asit reaktifi (ml) Hg. SO 4 (g) DAS'ın Normalitesi Titrasyon ön. Son numune hacmi, (ml) 10. 0 5. 0 15 0. 2 0. 05 70 20. 0 10. 0 30 0. 4 0. 10 140 30. 0 15. 0 45 0. 6 0. 15 210 40. 0 20. 0 60 0. 8 0. 20 280 50. 0 25. 0 75 1. 0 0. 25 350

Veri Analizi Ve Hesaplamalar • Deney sonucunun hesaplanması için aşağıdaki ifadeden yararlanılır; • • Burada; A: Şahit numune için kullanılan DAS çözeltisi miktarı, m. L B: Numune için kullanılan DAS çözeltisi miktarı, m. L N: DAS çözeltisinin normalitesidir.

TARTIŞMA VE SORULAR 1. KOI verisini BOI değerinden ayıran hususlar nelerdir, tartışınız? 2. KOI verisinin uygulama alanlarına örnekler veriniz? 3. KOI deneyinde hatalı sonuca neden olabilecek anorganik girişimler nasıl giderilebilir, tartışınız. ?
- Slides: 18