Mezclas y sustancias puras 1 Clasificacin de los



- Slides: 11

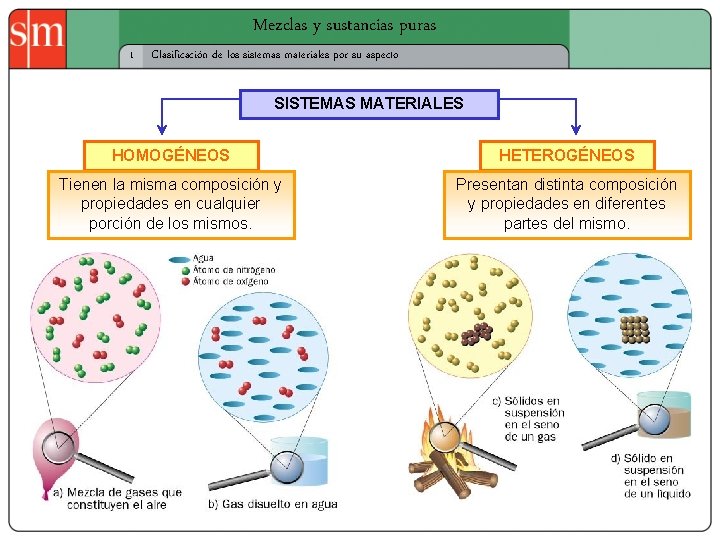
Mezclas y sustancias puras 1 Clasificación de los sistemas materiales por su aspecto SISTEMAS MATERIALES HOMOGÉNEOS HETEROGÉNEOS Tienen la misma composición y propiedades en cualquier porción de los mismos. Presentan distinta composición y propiedades en diferentes partes del mismo.

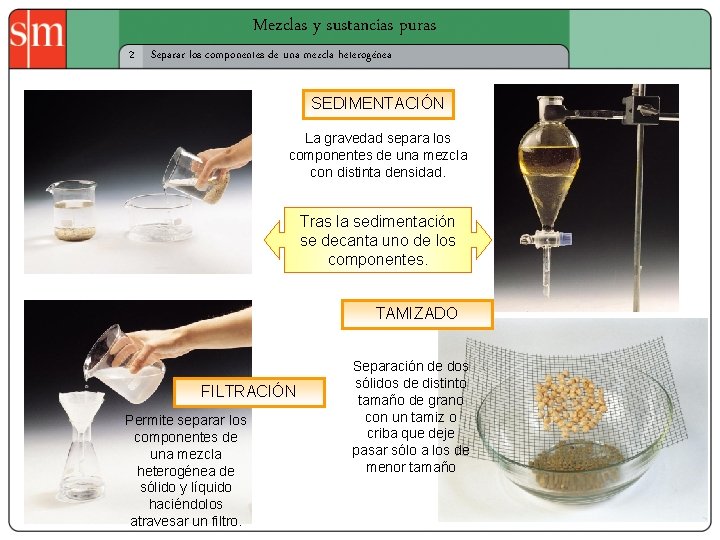
Mezclas y sustancias puras 2 Separar los componentes de una mezcla heterogénea SEDIMENTACIÓN La gravedad separa los componentes de una mezcla con distinta densidad. Tras la sedimentación se decanta uno de los componentes. TAMIZADO FILTRACIÓN Permite separar los componentes de una mezcla heterogénea de sólido y líquido haciéndolos atravesar un filtro. Separación de dos sólidos de distinto tamaño de grano con un tamiz o criba que deje pasar sólo a los de menor tamaño

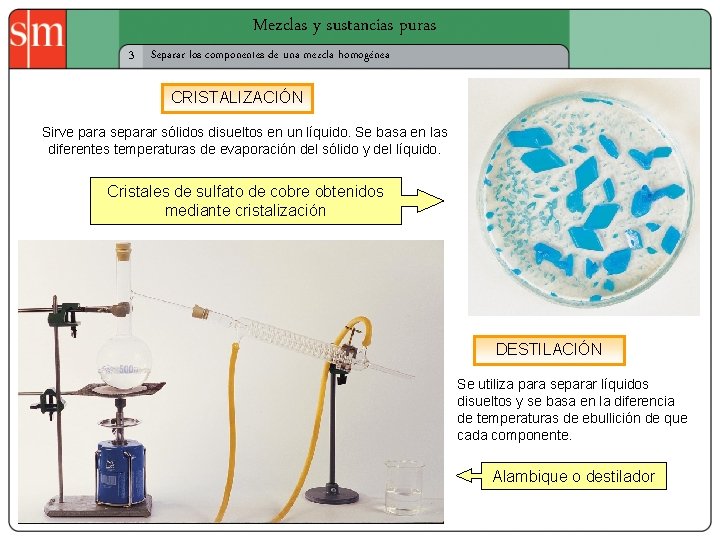
Mezclas y sustancias puras 3 Separar los componentes de una mezcla homogénea CRISTALIZACIÓN Sirve para separar sólidos disueltos en un líquido. Se basa en las diferentes temperaturas de evaporación del sólido y del líquido. Cristales de sulfato de cobre obtenidos mediante cristalización DESTILACIÓN Se utiliza para separar líquidos disueltos y se basa en la diferencia de temperaturas de ebullición de que cada componente. Alambique o destilador

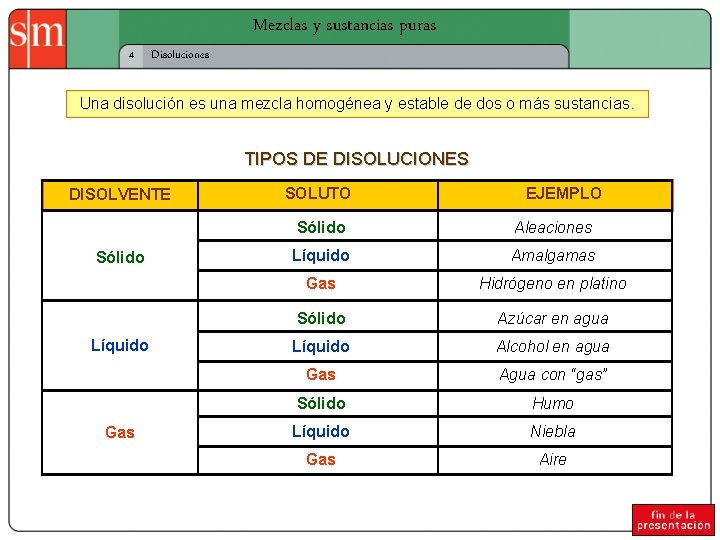
Mezclas y sustancias puras 4 Disoluciones Una disolución es una mezcla homogénea y estable de dos o más sustancias. TIPOS DE DISOLUCIONES DISOLVENTE Sólido Líquido Gas SOLUTO EJEMPLO Sólido Aleaciones Líquido Amalgamas Gas Hidrógeno en platino Sólido Azúcar en agua Líquido Alcohol en agua Gas Agua con “gas” Sólido Humo Líquido Niebla Gas Aire

Mezclas y sustancias puras 7 Solubilidad es la máxima cantidad de soluto que se puede disolver en una cantidad de disolvente a una temperatura determinada. DISOLUCIÓN SATURADA Aquella que no admite más soluto, a no ser que se añada más disolvente o se modifique la temperatura. Puede ser DILUIDA El soluto se disuelve poco en el disolvente. CONCENTRADA El soluto es muy soluble en el disolvente.

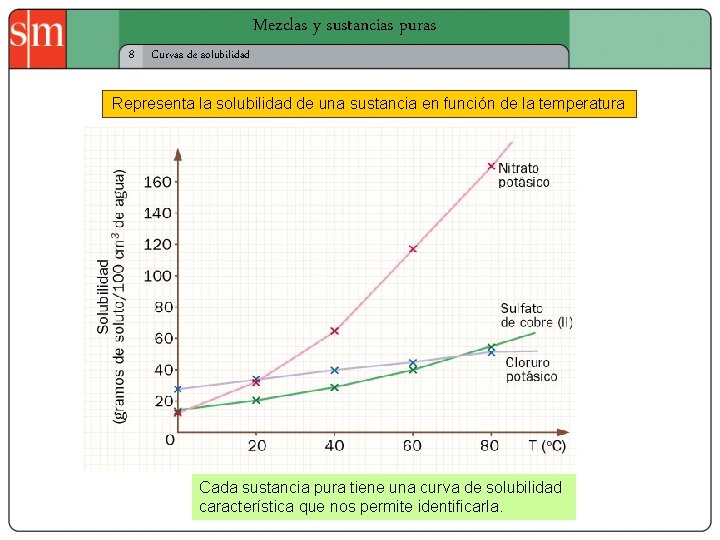
Mezclas y sustancias puras 8 Curvas de solubilidad Representa la solubilidad de una sustancia en función de la temperatura Cada sustancia pura tiene una curva de solubilidad característica que nos permite identificarla.

Factores que afectan la solubilidad Los factores que afectan la solubilidad son: a) Superficie de contacto: La interacción soluto-solvente aumenta cuando hay mayor superficie de contacto y el cuerpo se disuelve con más rapidez ( pulverizando el soluto). b) Agitación: Al agitar la solución se van separando las capas de disolución que se forman del soluto y nuevas moléculas del solvente continúan la disolución c) Temperatura: Al aument 6 ar la temperatura se favorece el movimiento de las moléculas y hace que la energía de las partículas del sólido sea alta y puedan abandonar su superficie disolviéndose. d) Presión: Esta influye en la solubilidad de gases y es directamente proporcional.

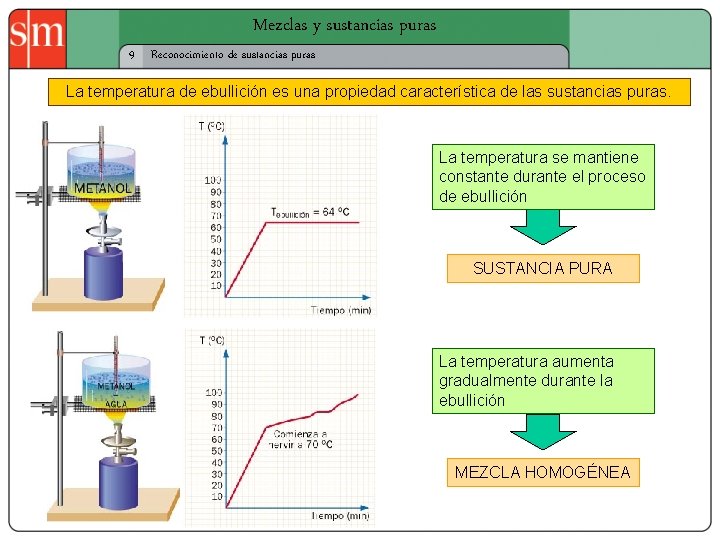
Mezclas y sustancias puras 9 Reconocimiento de sustancias puras La temperatura de ebullición es una propiedad característica de las sustancias puras. La temperatura se mantiene constante durante el proceso de ebullición SUSTANCIA PURA La temperatura aumenta gradualmente durante la ebullición MEZCLA HOMOGÉNEA

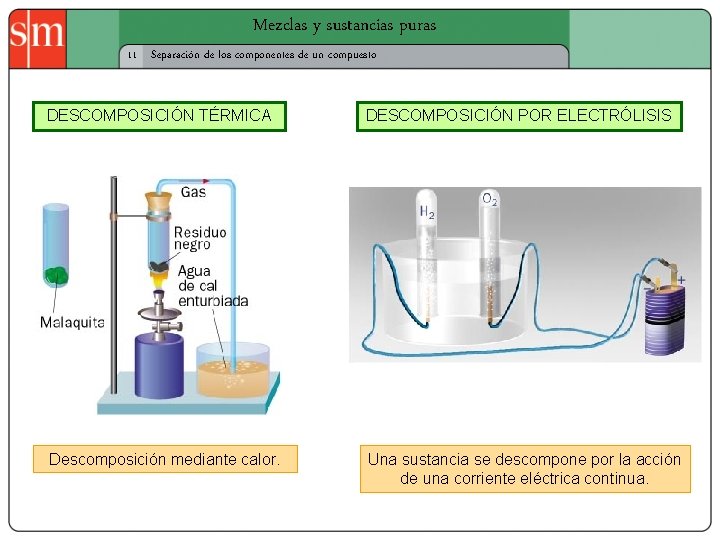
Mezclas y sustancias puras 11 Separación de los componentes de un compuesto DESCOMPOSICIÓN TÉRMICA DESCOMPOSICIÓN POR ELECTRÓLISIS Descomposición mediante calor. Una sustancia se descompone por la acción de una corriente eléctrica continua.

Ejercicios 1. - Completa las frases con las siguientes palabras: elementos-combinar-sustancias puras-compuestos-mezcla. La materia está formada por ______________ o por mezclas. La __________ es materia que está formada por dos o más sustancias puras. A las sustancias puras que no se las puede descomponer en otras más simples se las llama __________. Los elementos se pueden _________ entre sí dando lugar a los ____________. 2. - Une según corresponda: Imantación Se calienta la disolución para separar el componente que tiene el punto de ebullición más bajo. Evaporación Es cuando se separa un sólido y un líquido en mezcla heterogénea haciendo pasar el líquido por un filtro. Filtración Se aprovecha las propiedades magnéticas. El componente es atraído por un imán, quedando separado del resto. Cristalización Decantación El componente más denso cae al fondo y el menos denso se queda arriba Se deja reposar la disolución hasta que comiencen a aparecer pequeños cristales del sólido.

Responde las siguientes preguntas en tu cuaderno. 1. ¿Cómo separarías una mezcla de limaduras de hierro y serrín? 2. Has echado sal en un vaso con agua. ¿Es posible recuperar la sal? Indica el procedimiento que seguirías para hacerlo. 3. Recogemos una muestra de lodo y aceite. Indica cómo procederías para separar los componentes. 4. ¿En qué consiste la destilación? 5. Idea un procedimiento para averiguar si la tinta de un rotulador o de un bolígrafo es una sustancia pura o una mezcla. Nota: ten en cuenta que la tinta se disuelve en alcohol, no en agua.