Mezclas Una mezcla est formada por la unin

















- Slides: 19

Mezclas � Una mezcla está formada por la unión de sustancias en cantidades variables y que no se encuentran químicamente combinadas. � Por lo tanto, una mezcla no tiene un conjunto de propiedades únicas, sino que cada una de las sustancias constituyentes aporta al todo con sus propiedades específicas.

Mezclas homogéneas �Las mezclas homogéneas son aquellas cuyos componentes no son identificables a simple vista, es decir, se aprecia una sola fase física (monofásicas). Ejemplo: aire, agua potable.

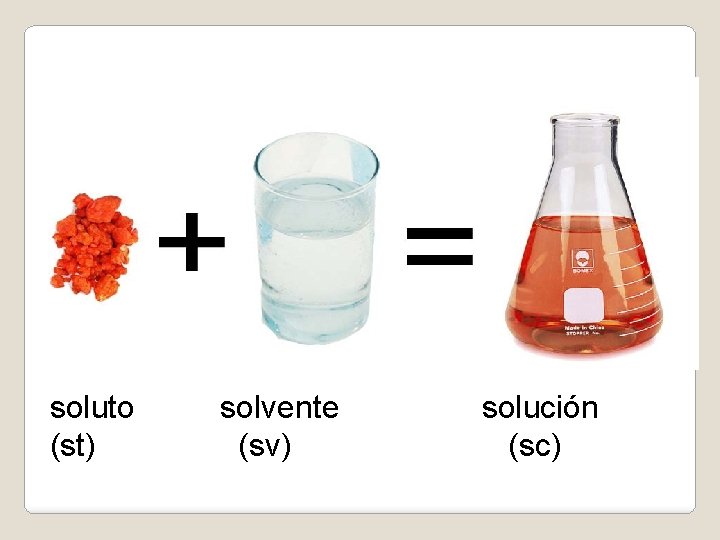
Soluciones Químicas �Son mezclas homogéneas (una fase) que contienen dos o más tipos de sustancias denominadas soluto y solvente; que se mezclan en proporciones variables; sin cambio alguno en su composición, es decir no existe reacción química. Soluto + Solvente → Solución

soluto (st) solvente (sv) solución (sc)

El soluto es un líquido y el solvente también es un líquido SOLUCIÓN LÍQUIDA, Cuando: Ejemplo: alcohol disuelto en agua El soluto es un sólido y el solvente es un líquido Ejemplo: azúcar en agua. El soluto es un gas y el solvente es un líquido. Ejemplo: dióxido de carbono (CO 2) disuelto en agua (refresco)

El soluto es un sólido y el solvente también es un sólido. Ejemplo: (Bronce) zinc en cobre SOLUCION SÓLIDA, Cuando: El soluto es un líquido y el solvente es un sólido Ejemplo: amalgama de mercurio disuelto en plata (se usa en dentadura) El soluto es un gas y el solvente es un sólido

El soluto es un sólido y el solvente es un gas. Ejemplo: vapor de yodo en aire SOLUCION GASEOSA, Cuando: El soluto es un líquido y el solvente es un gas. Ejemplo: agua en aire El soluto es un gas y el solvente también es un gas. Ejemplo: la solución de oxígeno y otros gases en nitrógeno (constituyen el aire)

Soluto �Es la sustancia que se disuelve, dispersa o solubiliza y siempre se encuentra en menor proporción, ya sea en peso o volumen. �A la naturaleza del soluto se deben el color, el sabor y la conductividad eléctrica de las soluciones. �El soluto da el nombre a la solución.

Solvente o disolvente �Es la sustancia que disuelve o dispersa al soluto y generalmente se encuentra en mayor proporción. �Existen solventes polares (agua, alcohol etílico y amoníaco) y no polares (benceno, éter, tetracloruro de carbono). �En las soluciones líquidas se toma como solvente universal al agua debido a su alta polaridad. �El solvente da el aspecto físico de la solución.

�La relación entre la cantidad de sustancia disuelta (soluto) y la cantidad de disolvente se conoce como concentración. �Esta relación se expresa cuantitativamente en forma de unidades físicas y unidades químicas, debiendo considerarse la densidad y el peso molecular del soluto. CONCENTRACIÓN DE UNA SOLUCIÓN

Hablar de solución diluida o concentrada, resulta muy inexacto. Por eso existen formas de determinar cuantitativamente las concentraciones de las soluciones. Existen dos tipos de unidades: - Unidades físicas - Unidades químicas

Concentración en Unidades Físicas �Porcentaje masa en masa (% m/m o % p/p): Indica la masa de soluto en gramos, presente en 100 gramos de solución. Xg soluto → 100 g solución �Ej: Una solución de azúcar en agua, contiene 20 g de azúcar en 70 g de solvente. Expresar la solución en % p/p. soluto + solvente → solución 20 g 70 g 90 g 20 g azúcar → 90 g solución Xg azúcar → 100 g solución X = 20 * 100 = 22, 22 p/p 90

Porcentaje masa en volumen (% m/v o % p/v) �Indica la masa de soluto en gramos disuelto en 100 m. L de solución. Xg soluto → 100 ml solución �Ej: Una solución salina contiene 30 g de Na. Cl en 80 m. L de solución. Calcular su concentración en % p/v. 30 g Na. Cl → 80 ml solución Xg Na. Cl → 100 ml solución X = 30 * 100 = 37, 5 %p/v 80

Porcentaje en volumen (% v/v) �Indica el volumen de soluto, en m. L, presente en 100 m. L de solución. X ml soluto → 100 ml solución � Ej: Calcular la concentración en volumen de una solución alcohólica, que contiene 15 m. L de alcohol disueltos en 65 m. L de solución. 15 ml alcohol X ml alcohol → → X = 15 * 100 65 65 ml solución 100 ml solución = 23 %v/v

Concentración común (g/L) � Indica la masa de soluto en gramos, presente en un litro de solución (recordar que 1 L = 1000 m. L, por lo que es lo mismo decir mg/m. L). Xg soluto → 1 L o 1000 m. L solución � EJ: Una solución de KCl contiene 10 g de sal en 80 m. L de solución. Calcular su concentración en gramos por litro. 10 g KCl Xg KCl → → 80 m. L solución 1000 m. L solución X = 10 * 1000 80 = 125 g/L

EJERCICIO 1 Explica con detalle cómo prepararías 250 cm 3 de una solución de cloruro de sodio de composición en masa 20 g/l. # Vamos a calcular, en primer lugar, la masa de soluto que se necesita; para ello, despeja la masa de soluto en la expresión de la concentración en masa. # Calcula la masa de soluto (cloruro de sodio). # Describe el procedimiento que seguirías para prepara la citada disolución, incluyendo los aparatos utilizados. 1. Se pesan 5 g de cloruro de sodio en una balanza. 2. Se añade agua al recipiente que contiene el cloruro de sodio y se agita hasta que se disuelva. 3. Se vierte esta disolución en un matraz aforado de 250 cm 3. 4. Se añade agua al matraz hasta el enrase.

EJERCICIO 2 Se disuelven 8 g de hidróxido de sodio en agua y se obtienen 200 cm 3 de solución. (a) Calcula la concentración en masa de la solución. (b) Calcula el volumen de una solución de la misma concentración en masa que contiene 100 g de hidróxido de sodio. # Escribir la expresión de la concentración en masa en función de la masa de soluto y el volumen de disolución # Hallar el volumen de la solución en litros o su equivalente dm 3. # Calcula la concentración en masa de la disolución. # Despeja el volumen de solución en la expresión de la concentración en masa. # Calcula el volumen de solución que contiene los 100 g de hidróxido de sodio. V = 200 cm 3 = 0, 200 l

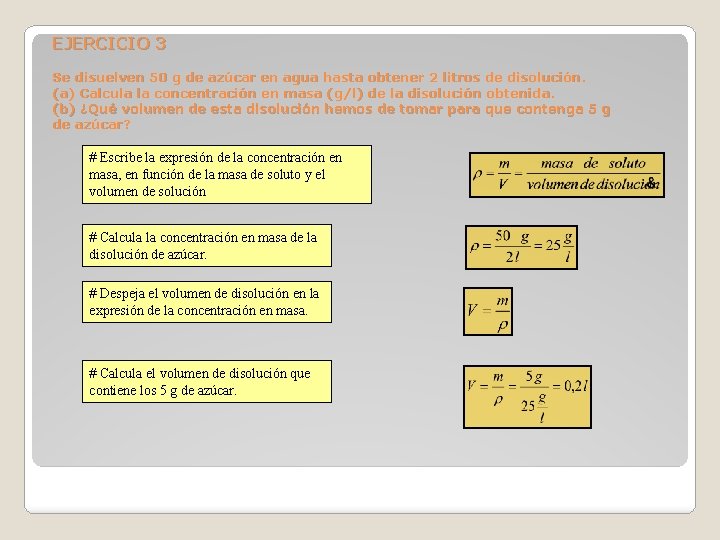
EJERCICIO 3 Se disuelven 50 g de azúcar en agua hasta obtener 2 litros de disolución. (a) Calcula la concentración en masa (g/l) de la disolución obtenida. (b) ¿Qué volumen de esta disolución hemos de tomar para que contenga 5 g de azúcar? # Escribe la expresión de la concentración en masa, en función de la masa de soluto y el volumen de solución # Calcula la concentración en masa de la disolución de azúcar. # Despeja el volumen de disolución en la expresión de la concentración en masa. # Calcula el volumen de disolución que contiene los 5 g de azúcar.

Concentración (cualitativo) Esta dada por la proporción de soluto en la solución. Por la abundancia relativa del soluto en las soluciones, estas pueden ser: a). - Diluida: cuando proporcionalmente tienen poco soluto b). -Concentrada: cuando proporcionalmente tienen abundante soluto c). - Saturadas: cuando la abundancia de soluto es tal que el solvente ya no es capaz de disolver mas soluto. d). - Sobre Saturada: cuando tiene mas soluto que su punto de saturación, la sobre saturación se logra mediante procedimientos especiales como por ejemplo calentar la solución.