Metody otrzymywania wybranych zwizkw organicznych cz V metody

Metody otrzymywania wybranych związków organicznych (cz. V) Ø Ø metody otrzymywania eterów, metody otrzymywania laktamów, metody otrzymywania laktonów, metody otrzymywanie laktydów
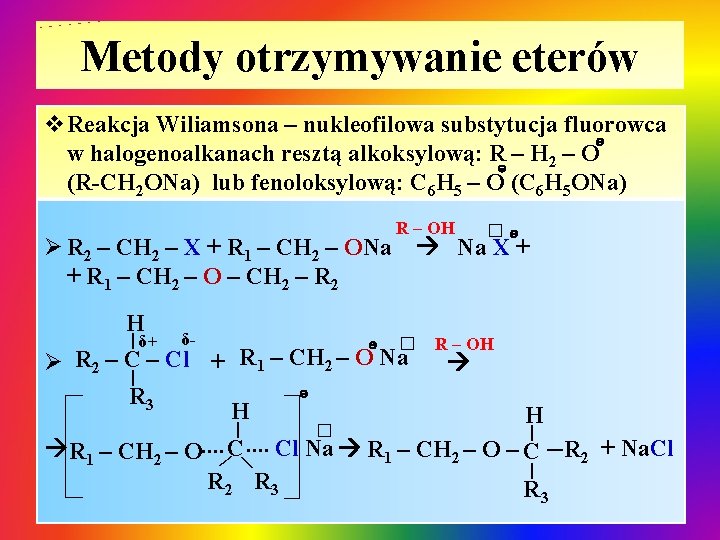
Metody otrzymywanie eterów v. Reakcja Wiliamsona – nukleofilowa substytucja fluorowca ɵ w halogenoalkanach resztą alkoksylową: Rɵ – H 2 – O (R-CH 2 ONa) lub fenoloksylową: C 6 H 5 – O (C 6 H 5 ONa) R – OH �ɵ Ø R 2 – CH 2 – X + R 1 – CH 2 – ONa Na X + + R 1 – CH 2 – O – CH 2 – R 2 H | δ+ δ- ɵ � R – OH | Ø R 2 – Cl + R 1 – CH 2 – O Na | ɵ R 3 H H | � | …. R 1 – CH 2 – O…. C Cl Na R 1 – CH 2 – O – C R 2 + Na. Cl | R 2 R 3 R | | 3
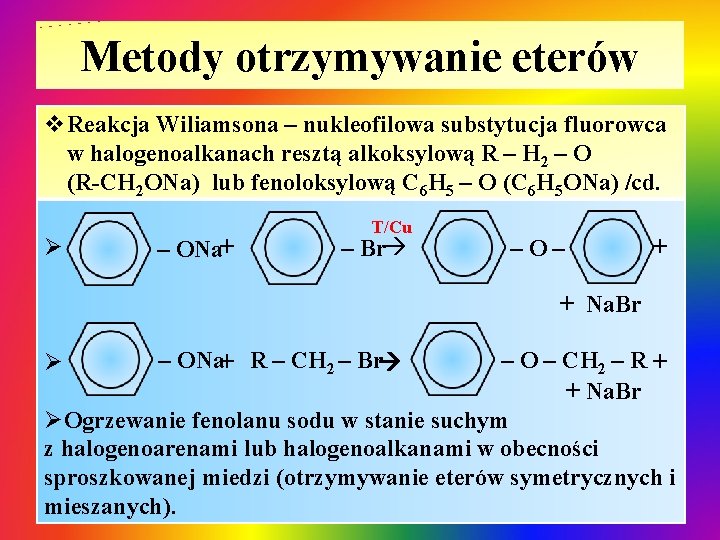
Metody otrzymywanie eterów v. Reakcja Wiliamsona – nukleofilowa substytucja fluorowca w halogenoalkanach resztą alkoksylową R – H 2 – O (R-CH 2 ONa) lub fenoloksylową C 6 H 5 – O (C 6 H 5 ONa) /cd. Ø – ONa+ T/Cu – Br –O– + + Na. Br – O – CH 2 – R + + Na. Br ØOgrzewanie fenolanu sodu w stanie suchym z halogenoarenami lub halogenoalkanami w obecności sproszkowanej miedzi (otrzymywanie eterów symetrycznych i mieszanych). Ø – ONa+ R – CH 2 – Br
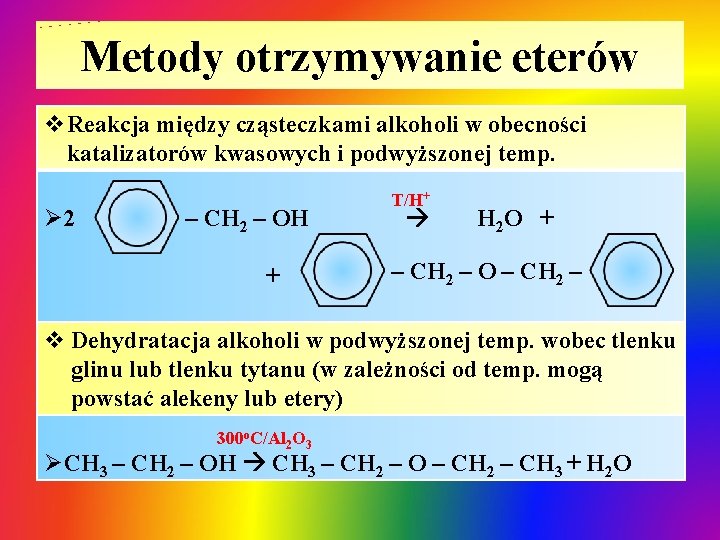
Metody otrzymywanie eterów v. Reakcja między cząsteczkami alkoholi w obecności katalizatorów kwasowych i podwyższonej temp. Ø 2 – CH 2 – OH + T/H+ H 2 O + – CH 2 – O – CH 2 – v Dehydratacja alkoholi w podwyższonej temp. wobec tlenku glinu lub tlenku tytanu (w zależności od temp. mogą powstać alekeny lub etery) 300 o. C/Al 2 O 3 ØCH 3 – CH 2 – OH CH 3 – CH 2 – O – CH 2 – CH 3 + H 2 O
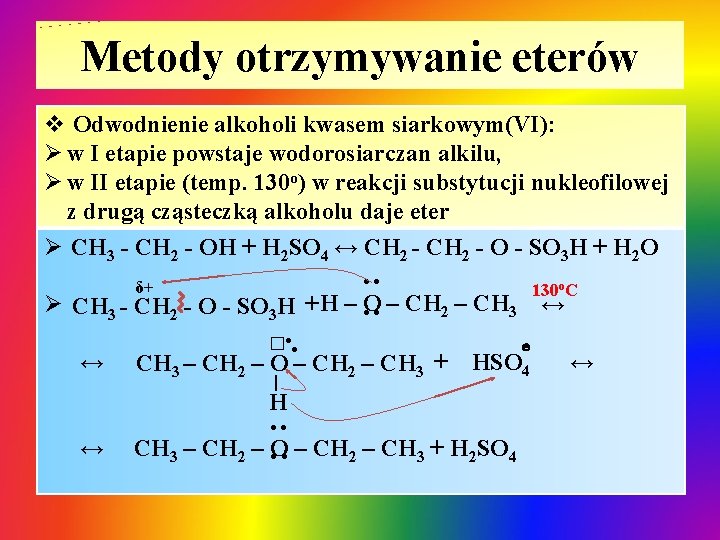
Metody otrzymywanie eterów v Odwodnienie alkoholi kwasem siarkowym(VI): Ø w I etapie powstaje wodorosiarczan alkilu, Ø w II etapie (temp. 130 o) w reakcji substytucji nukleofilowej z drugą cząsteczką alkoholu daje eter Ø CH 3 - CH 2 - OH + H 2 SO 4 ↔ CH 2 - O - SO 3 H + H 2 O ●● δ+ 130 o. C Ø CH 3 - CH 2 - O - SO 3 H + H – O ↔ ● ● – CH 2 – CH 3 ●● ↔ � CH 3 – CH 2 – O – CH 2 – CH 3 + | HSO 4 H ●● ↔ ɵ CH 3 – CH 2 – O ● ● – CH 2 – CH 3 + H 2 SO 4 ↔
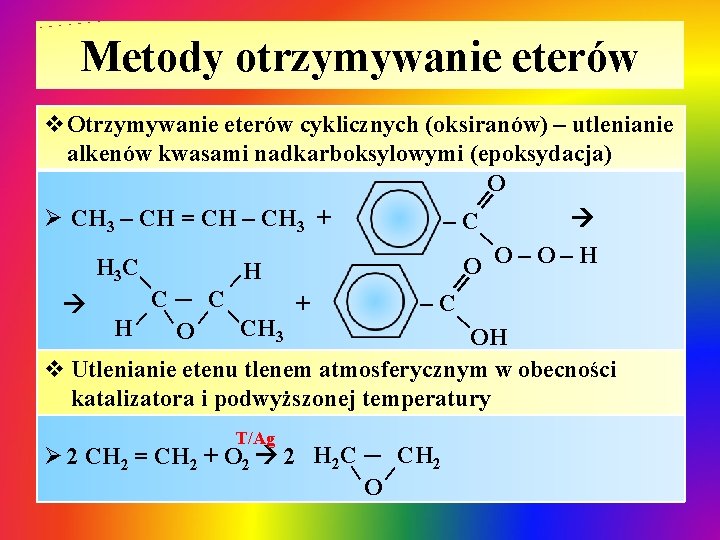
Metody otrzymywanie eterów ˭ v. Otrzymywanie eterów cyklicznych (oksiranów) – utlenianie alkenów kwasami nadkarboksylowymi (epoksydacja) O Ø CH 3 – CH = CH – CH 3 + –C O–O–H O H 3 C | H | C– C –C + | | H CH 3 O OH v Utlenianie etenu tlenem atmosferycznym w obecności katalizatora i podwyższonej temperatury ˭ T/Ag – CH 2 | | Ø 2 CH 2 = CH 2 + O 2 2 H 2 C O
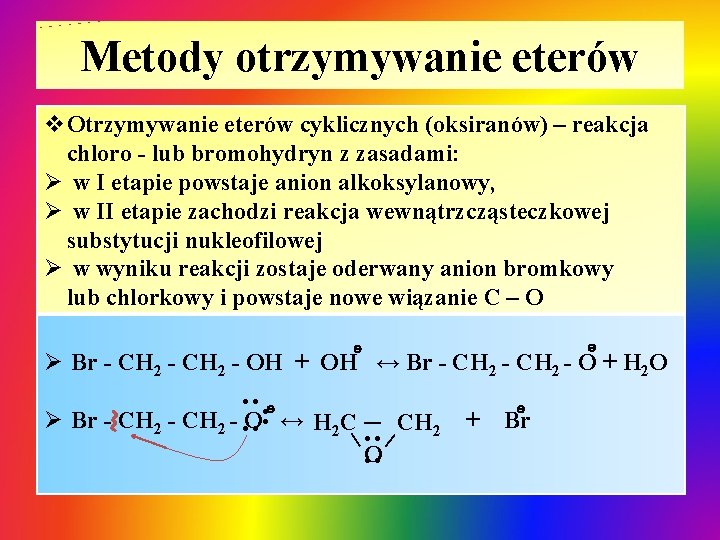
Metody otrzymywanie eterów v. Otrzymywanie eterów cyklicznych (oksiranów) – reakcja chloro - lub bromohydryn z zasadami: Ø w I etapie powstaje anion alkoksylanowy, Ø w II etapie zachodzi reakcja wewnątrzcząsteczkowej substytucji nukleofilowej Ø w wyniku reakcji zostaje oderwany anion bromkowy lub chlorkowy i powstaje nowe wiązanie C – O ɵ ɵ Ø Br - CH 2 - OH + OH ↔ Br - CH 2 - O + H 2 O ●● ɵ ●● Ø Br - CH 2 - ●O● ↔ H 2 C – CH 2 |● ● | O● ● + ɵ Br
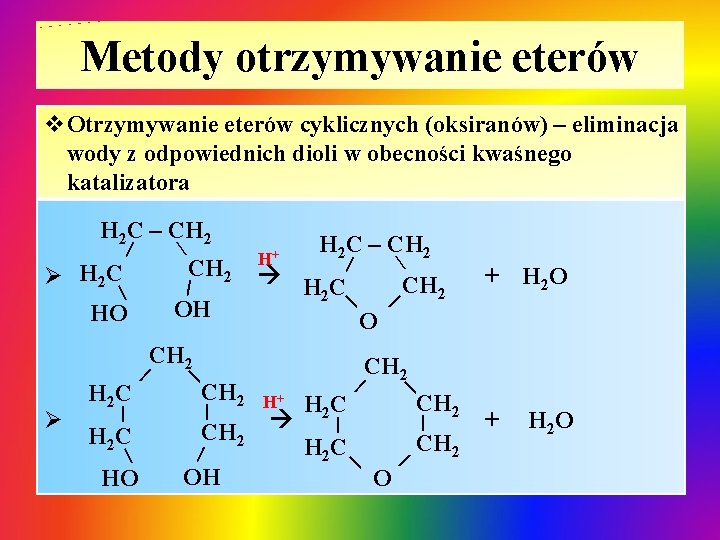
Metody otrzymywanie eterów v. Otrzymywanie eterów cyklicznych (oksiranów) – eliminacja wody z odpowiednich dioli w obecności kwaśnego katalizatora H 2 C – CH 2 Ø H 2 C | OH HO Ø | H 2 C HO | | CH 2 | OH | HC 2 CH 2 H+ H 2 C | CH 2 H 2 O + H 2 O | CH 2 | | H 2 C + O CH 2 O | | | CH 2 H 2 C – CH 2 | | H 2 C CH 2 H+ | |
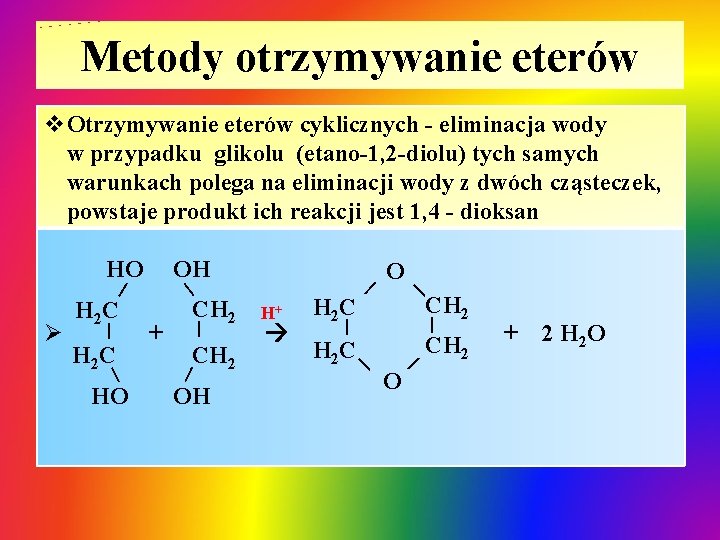
Metody otrzymywanie eterów v. Otrzymywanie eterów cyklicznych - eliminacja wody w przypadku glikolu (etano-1, 2 -diolu) tych samych warunkach polega na eliminacji wody z dwóch cząsteczek, powstaje produkt ich reakcji jest 1, 4 - dioksan HO OH Ø H 2 C | | HO CH 2 | + | CH 2 OH H+ H 2 C O | CH 2 | | H 2 C CH 2 O | H 2 C | | + 2 H 2 O
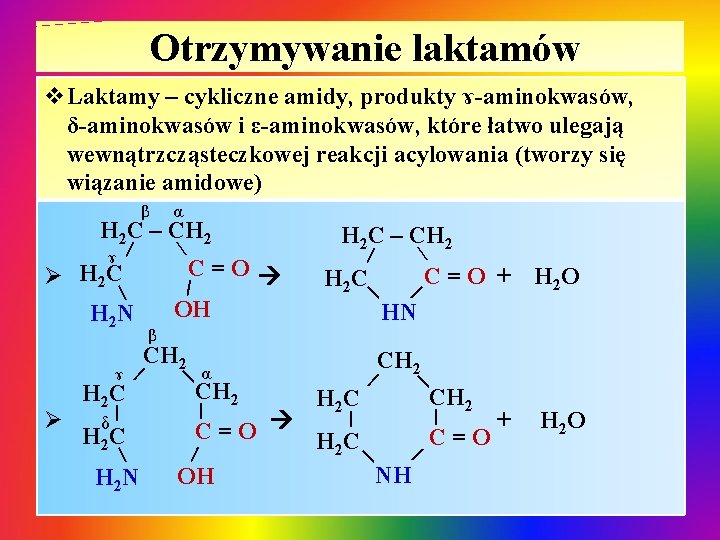
Otrzymywanie laktamów v. Laktamy – cykliczne amidy, produkty ɤ-aminokwasów, δ-aminokwasów i ε-aminokwasów, które łatwo ulegają wewnątrzcząsteczkowej reakcji acylowania (tworzy się wiązanie amidowe) α H 2 C – CH 2 | | H 2 N ɤ | Ø H 2 C δ | H 2 C H 2 N H 2 C β CH 2 |α CH 2 | | C=O + H 2 C | H 2 O HN CH 2 | | + C=O H 2 C | NH OH | | C=O | OH Ø H 2 C – CH 2 | ɤ | | β H 2 O
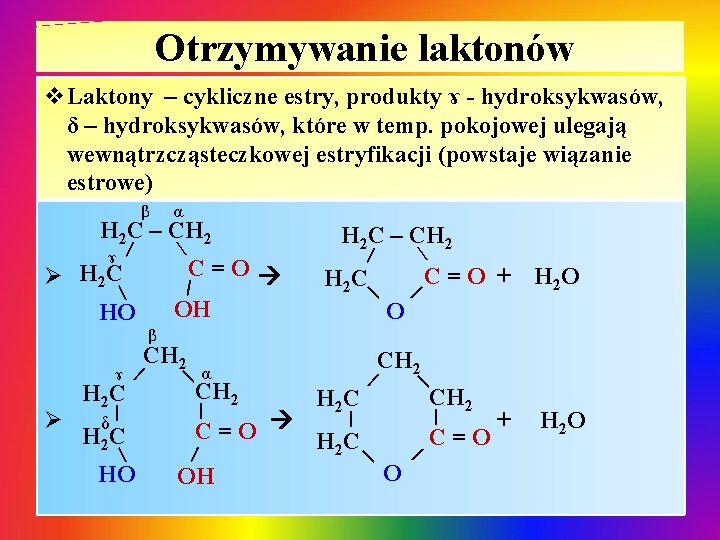
Otrzymywanie laktonów v. Laktony – cykliczne estry, produkty ɤ - hydroksykwasów, δ – hydroksykwasów, które w temp. pokojowej ulegają wewnątrzcząsteczkowej estryfikacji (powstaje wiązanie estrowe) α H 2 C – CH 2 | ɤ | Ø H 2 C δ | H 2 C HO |α CH 2 | C=O + H 2 C β CH 2 | H 2 C | O CH 2 | C=O H 2 C | O OH H 2 O | CH 2 | C=O | OH | | Ø H 2 C | HO H 2 C – CH 2 | ɤ | | β + H 2 O
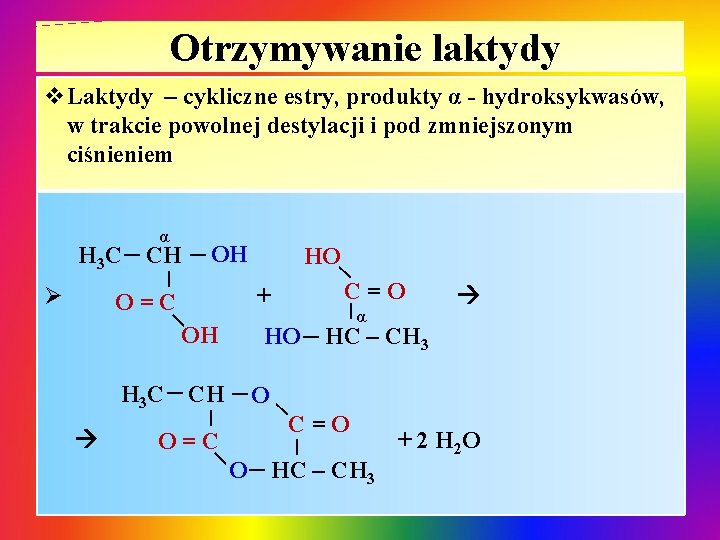
Otrzymywanie laktydy v. Laktydy – cykliczne estry, produkty α - hydroksykwasów, w trakcie powolnej destylacji i pod zmniejszonym ciśnieniem | | Ø CH OH | O=C C=O + | OH | | | HO | | HC – CH 3 C=O | O=C O |α | H 3 C CH HO | H 3 C α HC – CH 3 + 2 H 2 O
- Slides: 12