Metody otrzymywania wybranych zwizkw organicznych cz III otrzymywanie

Metody otrzymywania wybranych związków organicznych (cz. III) Ø otrzymywanie hydroksykwasów, Ø otrzymywanie hydroksyaldehydów, hydroksyketonów, ketonokwasów (oksokwasów), Ø otrzymywanie aminokwasów, Ø otrzymywanie amin, Ø otrzymywanie związków nitrowych, Ø otrzymywanie amidów, Ø otrzymywanie halogenków kwasowych (halogenków acylowych)
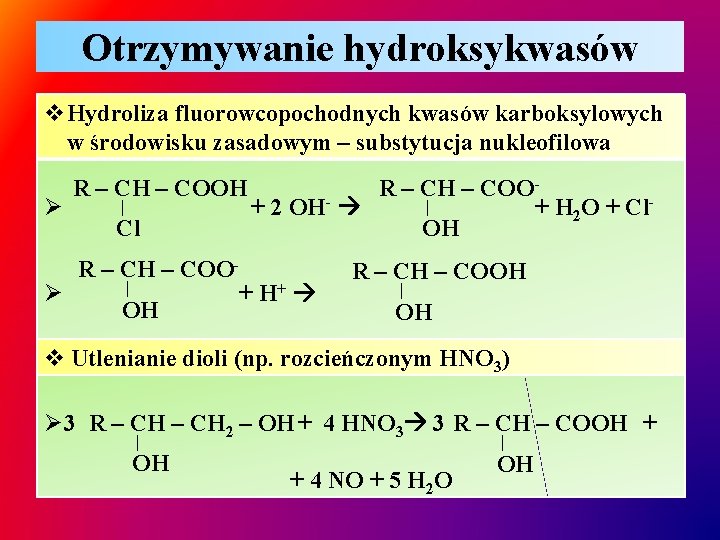
Otrzymywanie hydroksykwasów v. Hydroliza fluorowcopochodnych kwasów karboksylowych w środowisku zasadowym – substytucja nukleofilowa Ø R – CH – COOH | Cl R – CH – COO | + 2 OH- + H 2 O + Cl. OH R – CH – COO| Ø + H+ OH R – CH – COOH | OH v Utlenianie dioli (np. rozcieńczonym HNO 3) Ø 3 R – CH 2 – OH + 4 HNO 3 3 R – CH – COOH + | OH | + 4 NO + 5 H 2 O OH
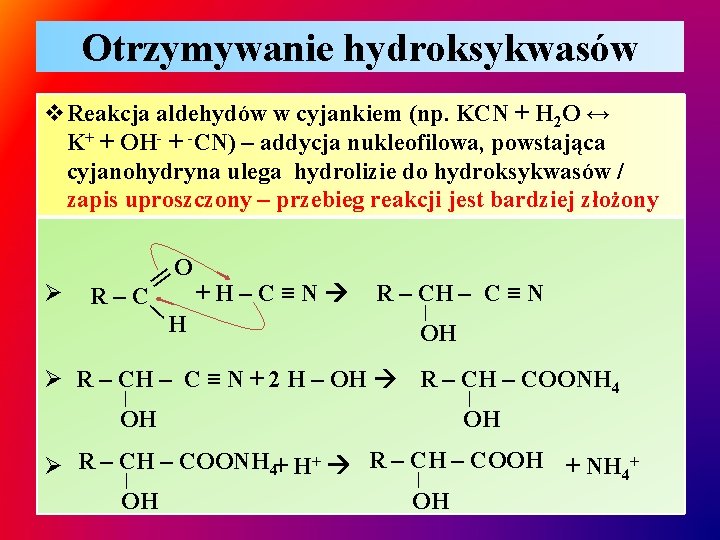
Otrzymywanie hydroksykwasów v. Reakcja aldehydów w cyjankiem (np. KCN + H 2 O ↔ K+ + OH- + -CN) – addycja nukleofilowa, powstająca cyjanohydryna ulega hydrolizie do hydroksykwasów / zapis uproszczony – przebieg reakcji jest bardziej złożony || ∕ Ø O R–C H +H–C≡N R – CH – C ≡ N | OH Ø R – CH – C ≡ N + 2 H – OH R – CH – COONH 4 | OH – COONH 4+ H+ R – CH – COOH + NH 4+ Ø R – CH | | OH OH
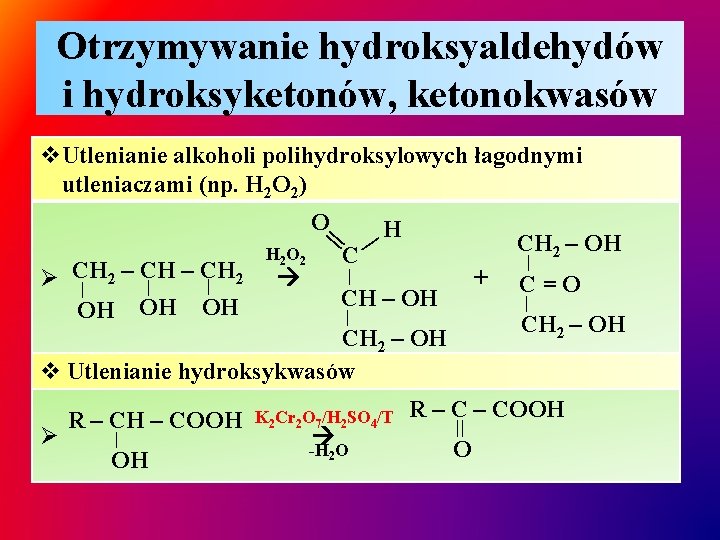
Otrzymywanie hydroksyaldehydów i hydroksyketonów, ketonokwasów v. Utlenianie alkoholi polihydroksylowych łagodnymi utleniaczami (np. H 2 O 2) C H CH 2 – OH | 2 – CH Ø CH | 2 | | OH OH OH H 2 O 2 || O + | CH – OH Ø | OH K 2 Cr 2 O 7/H 2 SO 4/T -H O 2 C=O | | CH 2 – OH v Utlenianie hydroksykwasów R – CH – COOH | R – COOH || O
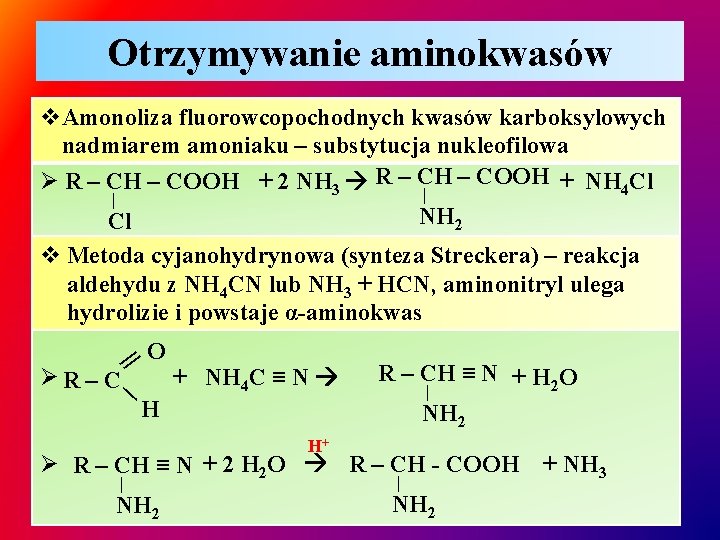
Otrzymywanie aminokwasów v. Amonoliza fluorowcopochodnych kwasów karboksylowych nadmiarem amoniaku – substytucja nukleofilowa – COOH + NH 4 Cl Ø R – CH – COOH + 2 NH 3 R – CH | | NH 2 Cl v Metoda cyjanohydrynowa (synteza Streckera) – reakcja aldehydu z NH 4 CN lub NH 3 + HCN, aminonitryl ulega hydrolizie i powstaje α-aminokwas || ∕ O ØR – C + NH 4 C ≡ N H R – CH ≡ N + H 2 O | NH 2 H+ Ø R – CH ≡ N + 2 H 2 O R – CH - COOH + NH 3 | NH 2
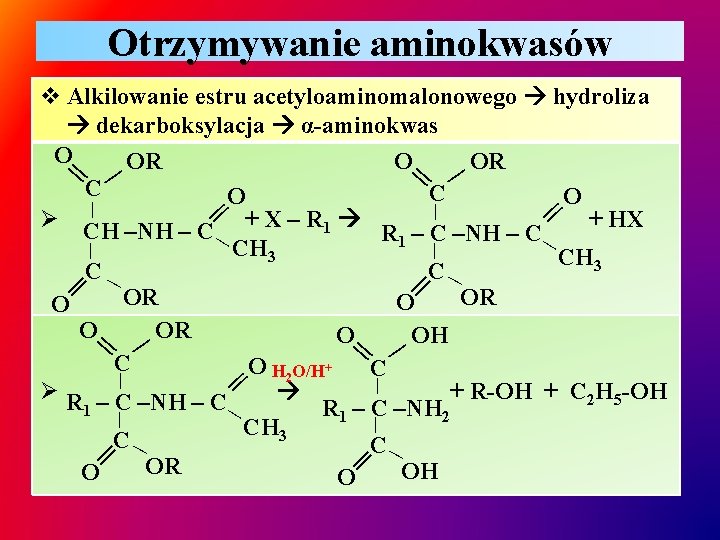
Otrzymywanie aminokwasów || || | | v Alkilowanie estru acetyloaminomalonowego hydroliza dekarboksylacja α-aminokwas O O OR OR C C O O | | Ø CH –NH – C + X – R 1 + HX R 1 – C –NH – C | | CH 3 C C OR OR O OH C O H 2 O/H+ C | | Ø R – C –NH – C + R-OH + C 2 H 5 -OH R 1 – C –NH 2 1 | | CH 3 C C OR OH O O || || || | || ||
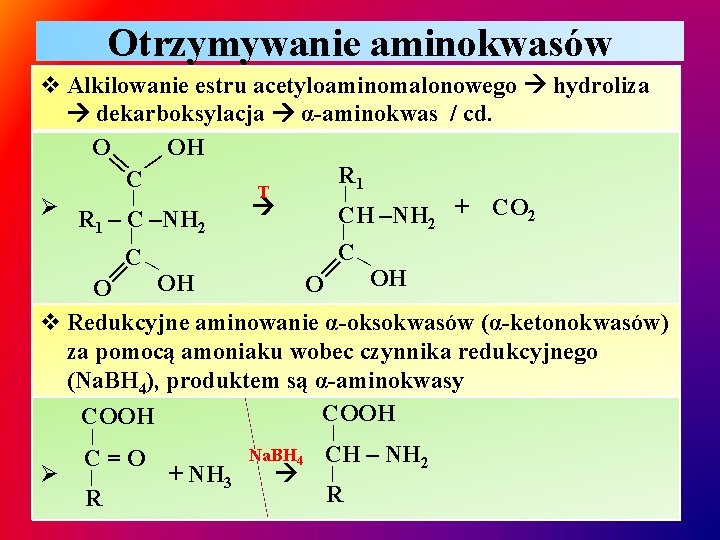
Otrzymywanie aminokwasów || | v Alkilowanie estru acetyloaminomalonowego hydroliza dekarboksylacja α-aminokwas / cd. O OH R 1 C T | | Ø R – C –NH + CO 2 CH –NH 2 1 2 | | C || || | OH OH O O v Redukcyjne aminowanie α-oksokwasów (α-ketonokwasów) za pomocą amoniaku wobec czynnika redukcyjnego (Na. BH 4), produktem są α-aminokwasy COOH | | Ø C=O | R + NH 3 Na. BH 4 CH – NH 2 | R

Otrzymywanie amin v Reakcja substytucji nukleofilowej amoniaku (otrzymywanie amin 1 o) aminy 1 o (otrzymywanie amin 2 o) lub aminy 2 o (otrzymywanie aminy 3 o) z halogenoalkanami lub halogenoarenami R 1 H δ+ δ| | Ø H – N | + R 1 – X H – N | + HX | | H R 1 | Ø H – N| | | + R 2 – X | H R 1 R 2 R 1 H – N| R 3 – N | | R 2 + HX | | Ø H – N| + R 3 – X | R 2 + HX
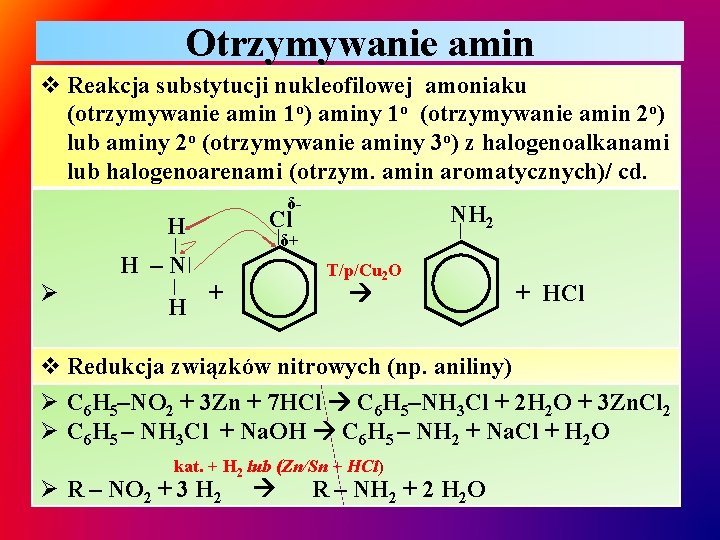
Otrzymywanie amin v Reakcja substytucji nukleofilowej amoniaku (otrzymywanie amin 1 o) aminy 1 o (otrzymywanie amin 2 o) lub aminy 2 o (otrzymywanie aminy 3 o) z halogenoalkanami lub halogenoarenami (otrzym. amin aromatycznych)/ cd. δ- H – N| | H | |δ+ | Ø NH 2 Cl H T/p/Cu 2 O + + HCl v Redukcja związków nitrowych (np. aniliny) Ø C 6 H 5–NO 2 + 3 Zn + 7 HCl C 6 H 5–NH 3 Cl + 2 H 2 O + 3 Zn. Cl 2 Ø C 6 H 5 – NH 3 Cl + Na. OH C 6 H 5 – NH 2 + Na. Cl + H 2 O kat. + H 2 lub (Zn/Sn + HCl) Ø R – NO 2 + 3 H 2 R – NH 2 + 2 H 2 O
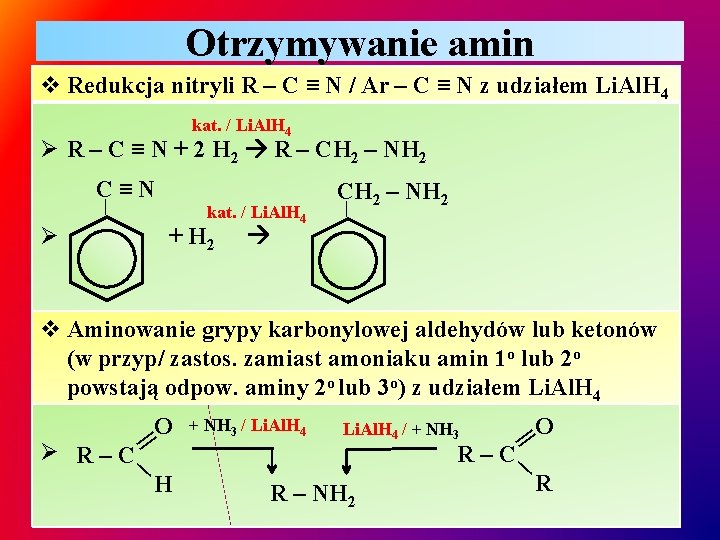
Otrzymywanie amin v Redukcja nitryli R – C ≡ N / Ar – C ≡ N z udziałem Li. Al. H 4 kat. / Li. Al. H 4 Ø R – C ≡ N + 2 H 2 R – CH 2 – NH 2 C≡N | Ø kat. / Li. Al. H 4 + H 2 CH 2 – NH 2 | v Aminowanie grypy karbonylowej aldehydów lub ketonów (w przyp/ zastos. zamiast amoniaku amin 1 o lub 2 o powstają odpow. aminy 2 o lub 3 o) z udziałem Li. Al. H 4 H + NH 3 / Li. Al. H 4 / + NH 3 O || ∕ Ø R–C O R–C R – NH 2 R
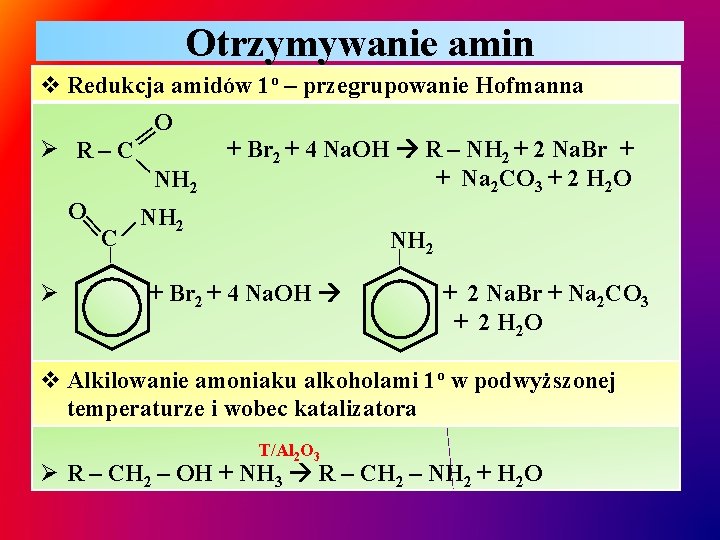
Otrzymywanie amin v Redukcja amidów 1 o – przegrupowanie Hofmanna O || ∕ Ø R–C NH 2 + Br 2 + 4 Na. OH R – NH 2 + 2 Na. Br + + Na 2 CO 3 + 2 H 2 O O| | C ∕ NH 2 | Ø | + Br 2 + 4 Na. OH + 2 Na. Br + Na 2 CO 3 + 2 H 2 O v Alkilowanie amoniaku alkoholami 1 o w podwyższonej temperaturze i wobec katalizatora T/Al 2 O 3 Ø R – CH 2 – OH + NH 3 R – CH 2 – NH 2 + H 2 O
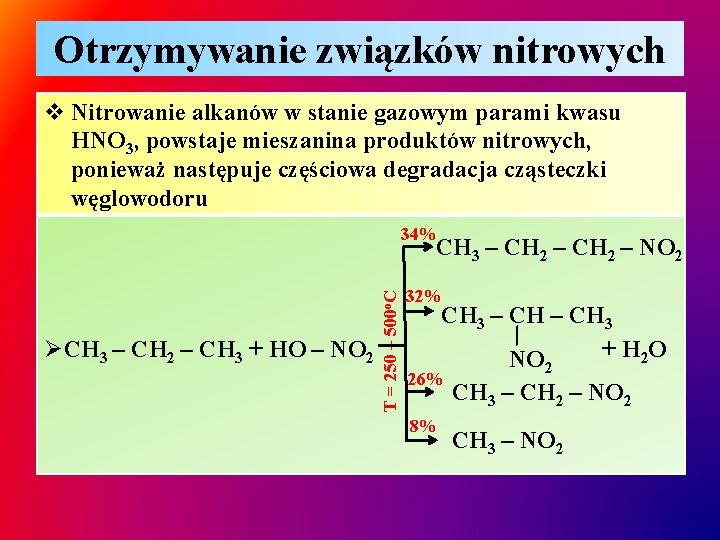
Otrzymywanie związków nitrowych v Nitrowanie alkanów w stanie gazowym parami kwasu HNO 3, powstaje mieszanina produktów nitrowych, ponieważ następuje częściowa degradacja cząsteczki węglowodoru 34% 32% CH 3 – CH 3 + H 2 O NO ∕ ØCH 3 – CH 2 – CH 3 + HO – NO 2 T = 250 – 500 o. C CH 3 – CH 2 – NO 2 26% 8% 2 CH 3 – CH 2 – NO 2 CH 3 – NO 2
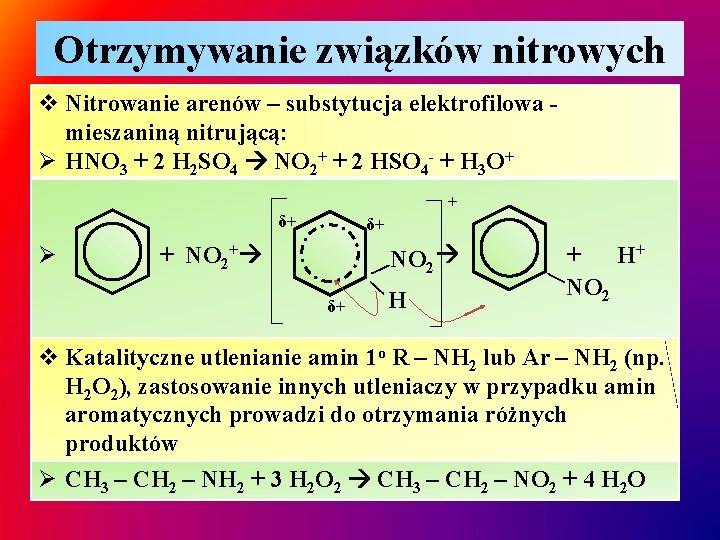
Otrzymywanie związków nitrowych v Nitrowanie arenów – substytucja elektrofilowa mieszaniną nitrującą: Ø HNO 3 + 2 H 2 SO 4 NO 2+ + 2 HSO 4 - + H 3 O+ + δ+ Ø δ+ + NO 2+ δ+ + H+ NO 2 ∕ ∕ ∕ NO 2 H v Katalityczne utlenianie amin 1 o R – NH 2 lub Ar – NH 2 (np. H 2 O 2), zastosowanie innych utleniaczy w przypadku amin aromatycznych prowadzi do otrzymania różnych produktów Ø CH 3 – CH 2 – NH 2 + 3 H 2 O 2 CH 3 – CH 2 – NO 2 + 4 H 2 O
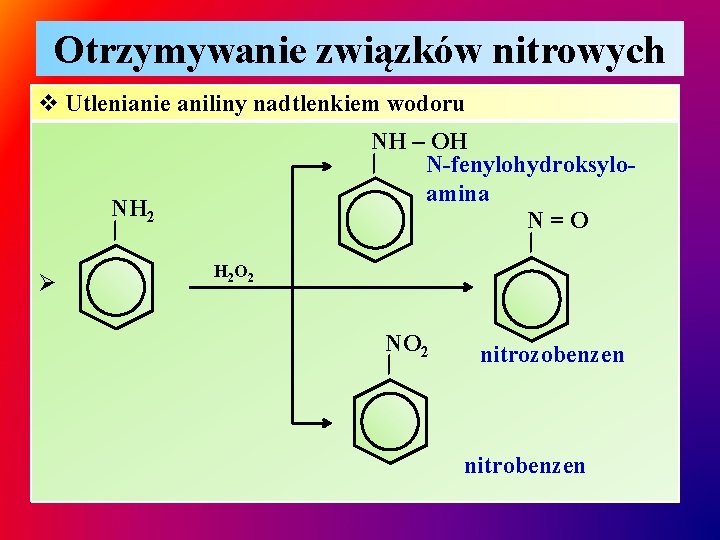
Otrzymywanie związków nitrowych v Utlenianie aniliny nadtlenkiem wodoru NH – OH ∕ N-fenylohydroksyloamina N=O ∕ NH 2 ∕ Ø H 2 O 2 NO 2 ∕ nitrozobenzen nitrobenzen
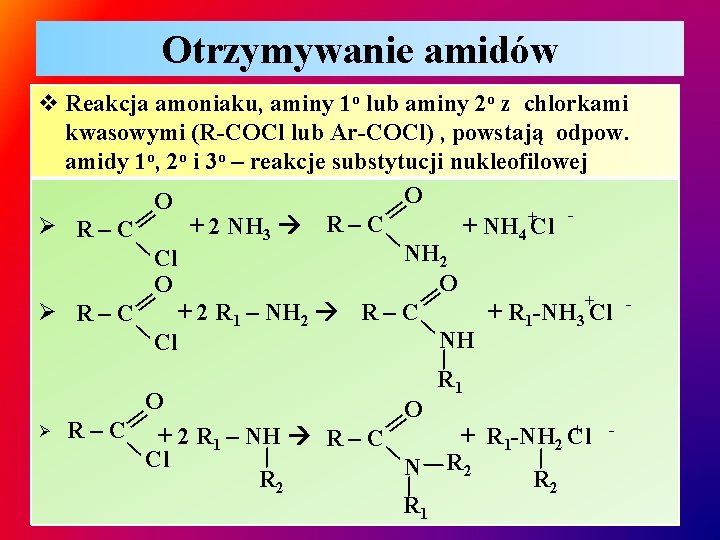
Otrzymywanie amidów || ∕ || ∕ ∕ || ∕ v Reakcja amoniaku, aminy 1 o lub aminy 2 o z chlorkami kwasowymi (R-COCl lub Ar-COCl) , powstają odpow. amidy 1 o, 2 o i 3 o – reakcje substytucji nukleofilowej O O + Ø R–C + 2 NH 3 R – C + NH 4 Cl NH 2 Cl O O + R – C Ø R–C + 2 R 1 – NH 2 + R 1 -NH 3 Cl NH Cl ∕ R 1 O O + Ø R–C + 2 R 1 – NH R – C + R 1 -NH 2 Cl ∕ ∕ Cl N R 2 R 2 ∕ R 1
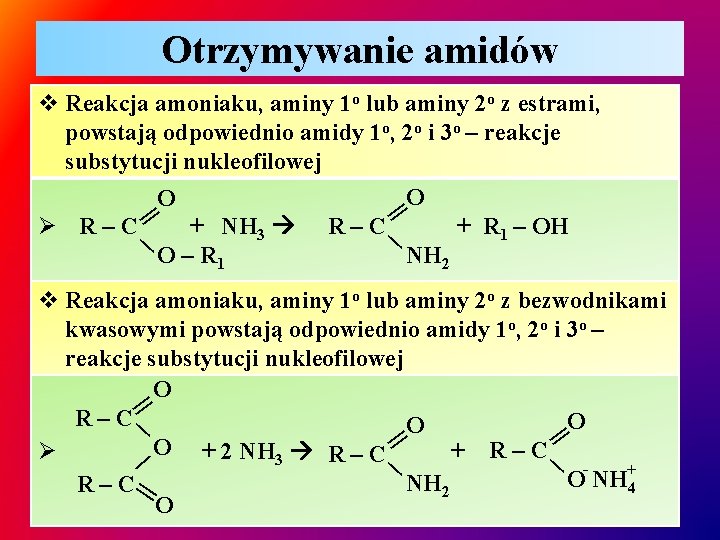
Otrzymywanie amidów || ∕ v Reakcja amoniaku, aminy 1 o lub aminy 2 o z estrami, powstają odpowiednio amidy 1 o, 2 o i 3 o – reakcje substytucji nukleofilowej O O Ø R–C + NH 3 R – C + R 1 – OH NH 2 O – R 1 || ∕ v Reakcja amoniaku, aminy 1 o lub aminy 2 o z bezwodnikami kwasowymi powstają odpowiednio amidy 1 o, 2 o i 3 o – reakcje substytucji nukleofilowej O R–C O O O + 2 NH 3 R – C Ø + R–C + O NH NH 2 R–C 4 O || ∕ ∕ ||
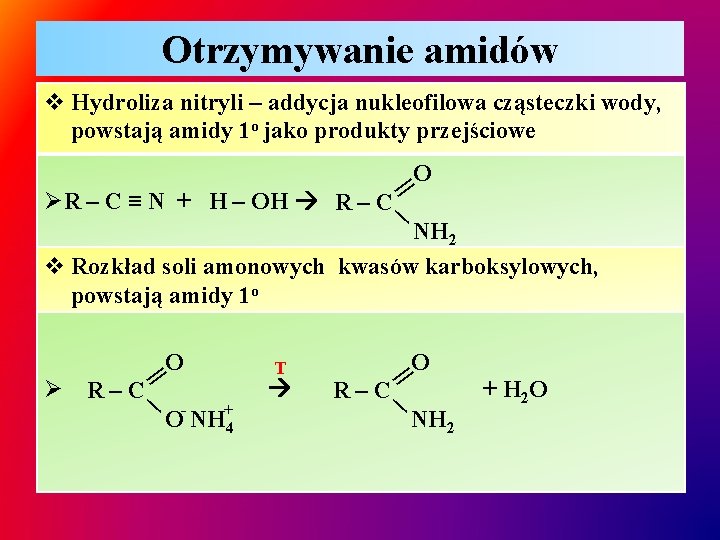
Otrzymywanie amidów v Hydroliza nitryli – addycja nukleofilowa cząsteczki wody, powstają amidy 1 o jako produkty przejściowe O || ∕ ØR – C ≡ N + H – OH R – C NH 2 v Rozkład soli amonowych kwasów karboksylowych, powstają amidy 1 o - T + O NH 4 O || ∕ Ø R–C O R–C NH 2 + H 2 O
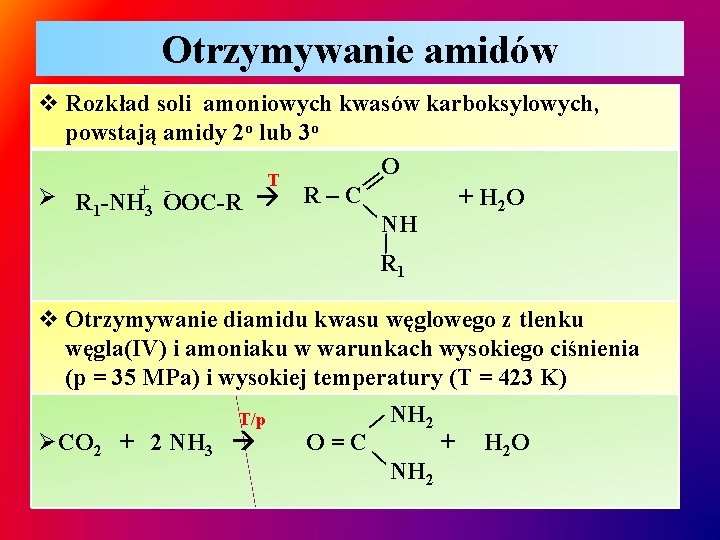
Otrzymywanie amidów || ∕ v Rozkład soli amoniowych kwasów karboksylowych, powstają amidy 2 o lub 3 o O T Ø R 1 -NH+3 OOC-R R–C + H 2 O NH ∕ R 1 v Otrzymywanie diamidu kwasu węglowego z tlenku węgla(IV) i amoniaku w warunkach wysokiego ciśnienia (p = 35 MPa) i wysokiej temperatury (T = 423 K) NH 2 T/p ØCO 2 + 2 NH 3 + H 2 O O=C NH 2 ∕ ∕
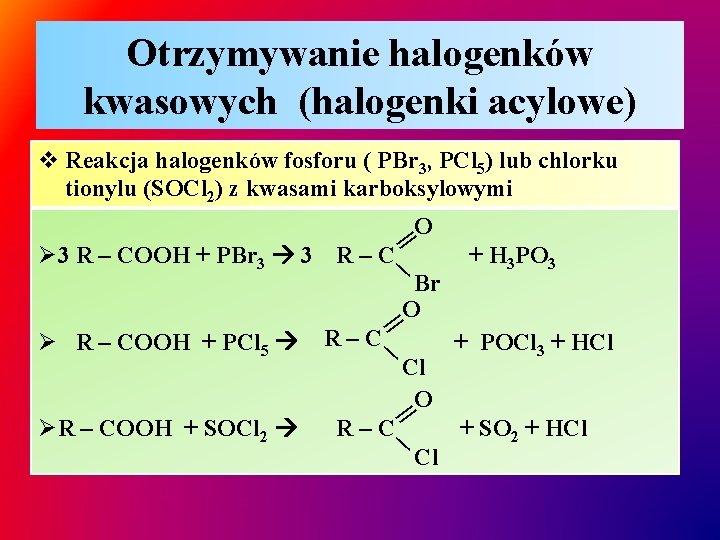
Otrzymywanie halogenków kwasowych (halogenki acylowe) v Reakcja halogenków fosforu ( PBr 3, PCl 5) lub chlorku tionylu (SOCl 2) z kwasami karboksylowymi O || ∕ Ø 3 R – COOH + PBr 3 3 R – C R–C Cl O || ∕ ØR – COOH + SOCl 2 || ∕ Ø R – COOH + PCl 5 Br O R–C Cl + H 3 PO 3 + POCl 3 + HCl + SO 2 + HCl
- Slides: 19