METODE ZASNOVANE NA REDOKSREAKCIJAMA OKSIDIMETRIJA I REDUKTOMETRIJA brojnije

METODE ZASNOVANE NA REDOKS-REAKCIJAMA. OKSIDIMETRIJA I REDUKTOMETRIJA. - brojnije su i raznovrsnije od bilo koje druge grupe volumetrijskih metoda - niz elemenata se može pojavljivati u više oksidacionih stanja - izbor standardnih rastvora i reagenasa je veći nego kod drugih metoda - primena se proširuje dodatkom kompleksirajućih supstanci, koje građenjem kompleksa mogu menjati elektrodni potencijal titrovane supstance ili reagensa čime reakcija postaje brža i kvantitativnija TITRACIONE KRIVE -mogu se dobiti nanošenjem negativnog logaritma brojčane vrednosti koncentracije titrovane supstance u zavisnosti od zapremine dodatog reagensa - ipak se na ordinatu nanosi elektrodni potencijal !!!

1. Elektrodni potencijal je logaritamska funkcija koncentracija supstanci koje reaguju. 2. Korišćenje elektrodnih potencijala olakšava izbor redoks-indikatora (i oni su redoks parovi i reaguju na promenu potencijala). Podela titracija: 1. titracije kod kojih se pojavljuje isti broj elektrona u obe jednačine polureakcija 2. titracije kod kojih se pojavljuje različit broj elektrona u jednačinama polureakcija 3. titracije kod kojih se u jednačina polureakcije pojavljuju voda i njeni joni 4. titracije kod kojih jedan jon ili molekul rektanata daju više jona ili molekula proizvoda reakcije ili obrnuto

Titracije sa istim brojem elektrona u obe jednačine polureakcija Titracija Fe(II) sa Ce(IV) Titruje se 100, 00 ml rastvora Fe 2+ c=0, 100 mol/l rastvorom Ce 4+ c=0, 100 mol/L u sulfatno-kiselom rastvoru c(H 2 SO 4)=1 mol/l Fe 2+ + Ce 4+ Fe 3+ + Ce 3+ *** u H 2 SO 4 se Ce 4+ nalazi u obliku [Ce(SO 4)3]21. Na početku titracije u rastvoru su samo joni Fe 2+ Rastvor sadrži i malu, nepoznatu koncentraciju Fe 3+ (oksidacija vazdušnim kiseonikom), pa se elektrodni potencijal ne može izračunati !!!

2. Do T. E. u rastvoru su neistitrovani joni Fe 2+, ekvivalentne količine Fe 3+ i Ce 3+, kao i vrlo mala (zanemarljiva) količinu Ce 4+ - jednostavnije, do T. E, jer se konc. Fe(II) i Fe(III) mogu lako izračunati na osnovu količine dodatog reagensa 3. T. E. u rastvoru su ekvivalentne količine Fe 3+ i Ce 3+, kao i vrlo mala (zanemarljiva) količina Ce 4+ i Fe 2+ (iz povratne rekacije) a. A + b. B c. C + d. D
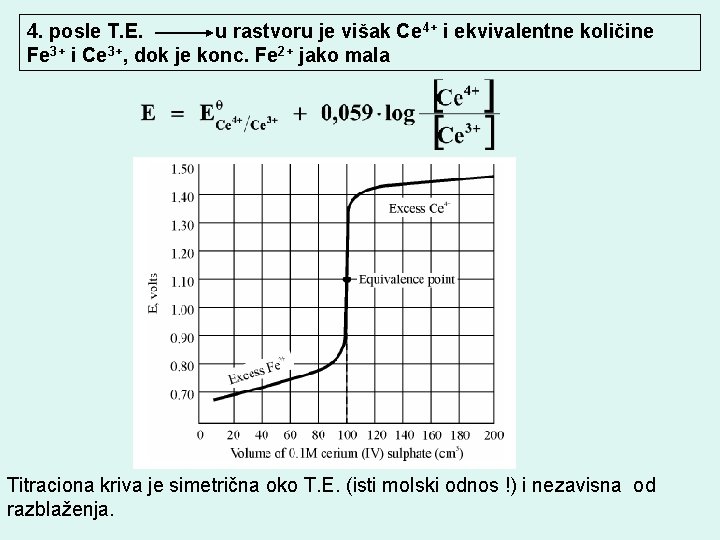
4. posle T. E. u rastvoru je višak Ce 4+ i ekvivalentne količine Fe 3+ i Ce 3+, dok je konc. Fe 2+ jako mala Titraciona kriva je simetrična oko T. E. (isti molski odnos !) i nezavisna od razblaženja.
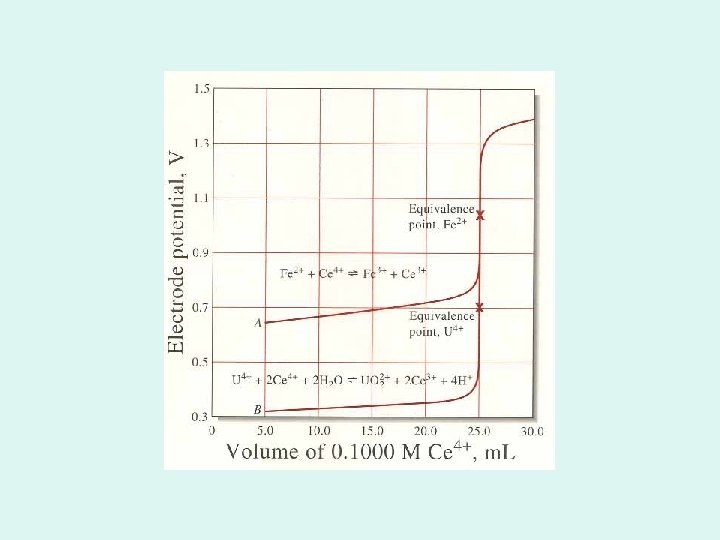

Titracije sa različitim brojem elektrona u jednačinama polureakcija Titracija Sn(II) sa Fe(III) Titruje se 100, 00 ml rastvora Sn 2+ c=0, 100 mol/l rastvorom Fe 3+ c=0, 100 mol/L u hloridno-kiselom rastvoru c(HCl)=1 mol/l Sn 2+ + 2 Fe 3+ 2 Fe 2+ + Sn 4+

2. Do T. E. u rastvoru su neistitrovani joni Sn 2+, ekvivalentne količine Fe 2+ i Sn 4+, kao i vrlo mala (zanemarljiva) količinu Fe 3+ - jednostavnije, do T. E, jer se konc. Sn(II) i Sn(IV) mogu lako izračunati na osnovu količine dodatog reagensa 3. T. E. u rastvoru su ekvivalentne količine Fe 2+ i Sn 4+, kao i vrlo mala (zanemarljiva) količina Sn 2+ i Fe 3+ (iz povratne rekacije) 4. posle T. E. u rastvoru je višak Fe 3+ i ekvivalentne količine Fe 2+ i Sn 4+, dok je konc. Sn 2+ jako mala
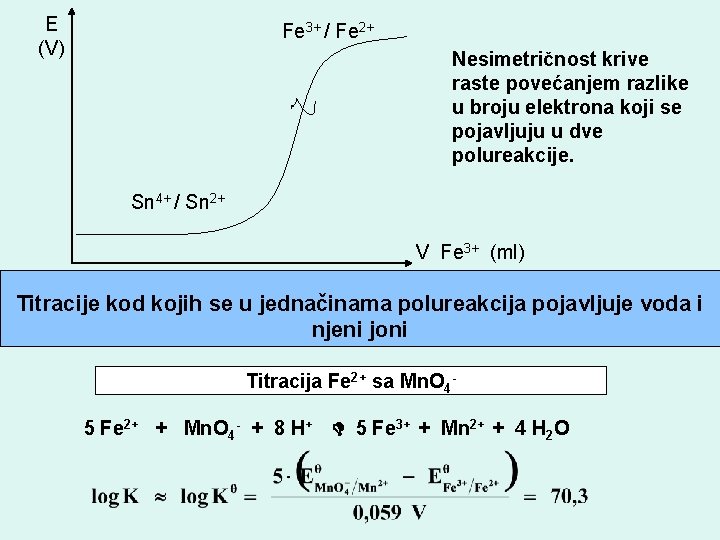
E (V) Fe 3+ / Fe 2+ Nesimetričnost krive raste povećanjem razlike u broju elektrona koji se pojavljuju u dve polureakcije. Sn 4+ / Sn 2+ V Fe 3+ (ml) Titracije kod kojih se u jednačinama polureakcija pojavljuje voda i njeni joni Titracija Fe 2+ sa Mn. O 45 Fe 2+ + Mn. O 4 - + 8 H+ 5 Fe 3+ + Mn 2+ + 4 H 2 O

Titruje se 100, 00 ml rastvora Fe 2+ c=0, 100 mol/l rastvorom Mn. O 4 c=0, 020 mol/L u kiseloj sredini c(H+)=1 mol/l 2. Do T. E. u rastvoru su neistitrovani joni Fe 2+, ekvivalentne količine Fe 3+ i Mn 2+, kao i vrlo mala (zanemarljiva) količina Mn. O 4 - - jednostavnije, do T. E, jer se konc. Fe(II) i Fe(III) mogu lako izračunati na osnovu količine dodatog reagensa 3. T. E. u rastvoru su ekvivalentne količine Fe 3+ i Mn 2+, kao i vrlo mala (zanemarljiva) količina Mn. O 4 - i Fe 2+ (iz povratne rekacije)
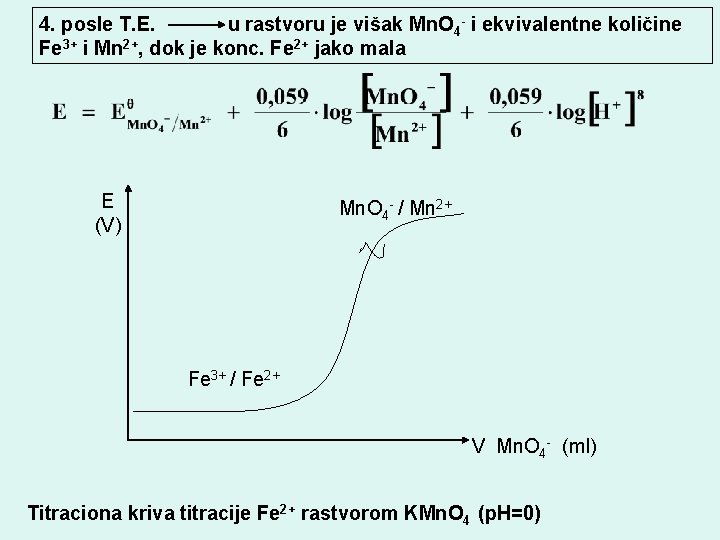
4. posle T. E. u rastvoru je višak Mn. O 4 - i ekvivalentne količine Fe 3+ i Mn 2+, dok je konc. Fe 2+ jako mala E (V) Mn. O 4 - / Mn 2+ Fe 3+ / Fe 2+ V Mn. O 4 - (ml) Titraciona kriva titracije Fe 2+ rastvorom KMn. O 4 (p. H=0)

Titracije gde jedan molekul ili jon reaktanata daje dva ili više molekula ili jona proizvoda reakcije ili obrnuto Cr 2 O 72 - + 14 H+ + 6 e 2 Cr 3+ + 7 H 2 O S 4 O 62 - + 2 e 2 S 2 O 32***koncentracioni članovi Ox i Red oblika u Nernstovoj jednačini imaju različite eksponente, pa elektrodni potencijali zavise od razblaženja rastvora Titracija Fe 2+ sa Cr 2 O 726 Fe 2+ + Cr 2 O 72 - + 14 H+ 2 Cr 3+ + 7 H 2 O
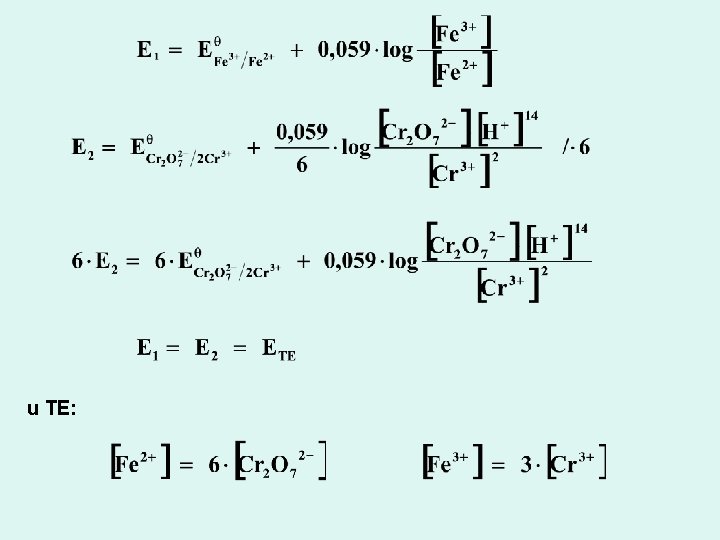
u TE:

REDOKS INDIKATORI - Organske supstance koje se ponašaju kao slabi oksidansi ili reduktori - Boja oksidovanog i redukovanog oblika je različita - Boja se menja u zavisnosti od elektrodnog potencijala rastvora. Inox + z e Inred boja 1 Dvobojni indikatori: Interval prelaza: boja 2 Eoin

Jednobojni indikatori: c 0 ukupna koncentracija cmin minimalna koncentracija neophodna de se primeti obojenost rastvora Neki redoks indikatori Indikator E 0, V Boja oksidovanog oblika Boja redukovanog oblika Tris(5 -nitro-1, 10 fenatrolin) Fe(II)-sulfat, nitroferoin 1. 25 svetlo plav crven Tris (1, 10 -fenantrolin) Fe(II)-sulfat feroin 1. 06 svetlo plav crven Tris (2, 2’-bipiridin) Fe(II)-sulfat 0. 97 svetlo plav crven Difenilamin-sulfonska kiselina ( i njene soli) 0. 84 ljubičastoplav bezbojan Difenilamin 0. 76 ljubičast bezbojan Difenilbenzidin 0. 76 ljubičast bezbojan Metilensko plavo 0. 53 zelenoplav bezbojan
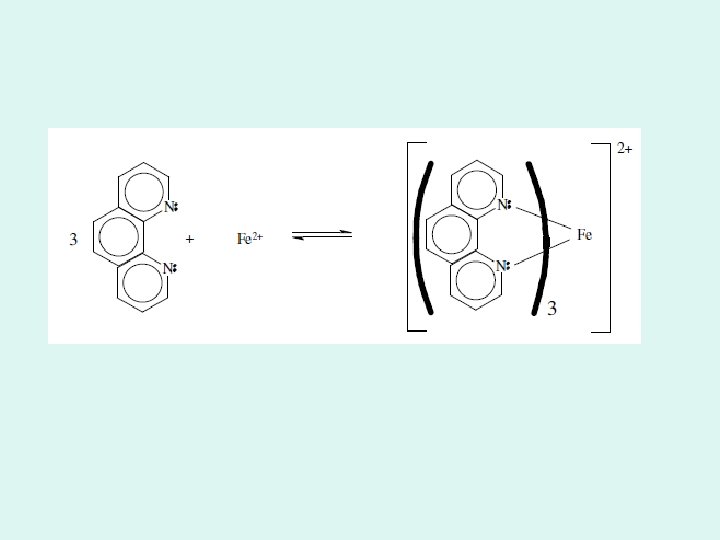
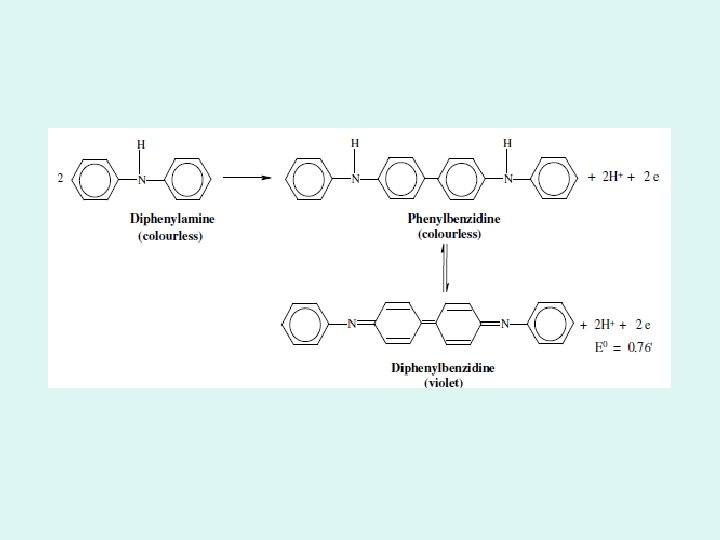

Prethodne oksidacije ili redukcije Analizirana supstanca mora biti u određenom oksidacionom stanju koje brzo i stehiometrijski reaguje sa reagensom Reagensi koji se primenjuju za prethodne oksidacije ili redukcije 1. Dovoljno jaki kao oksidansi ili reduktori, a da pri tom ne reaguju sa drugim komponentama tako da se dobije proizvod koji bi reagovao sa reagensom 2. Mogućnost da se višak ovih pomoćnih reagenasa ukloni iz rastvora (malo rastvorna jedinjenja, metali, gasovi. . -u različitoj fazi, ILI lako se razaraju-npr. na povišenoj temperaturi) OKSIDACIONE SUPSTANCE Natrijum-bizmutat, Natrijum-bizmutat obično Na. Bi. O 3 -smeđ nerastvoran prah Na. Bi. O 3 + 6 H+ + 2 e ↔ Bi 3+ + Na+ + 3 H 2 O E 0≈1. 7 V Kisela sredina (HNO 3)-Mn(II) u Mn(VII), Cr(III) u Cr(VI), Ce(III) u Ce(IV). . . Višak se uklanja filtracijom

Ag. O(s) + 2 H+ Srebro (II)-oksid, Ag. O + e ↔ Ag+ + H 2 O E 0≈1. 9 V Kisela sredina (HNO 3 ili HCl. O 4 2 -5 M)- Mn(II) u Mn(VII), Cr(III) u Cr(VI), Ce(III) u Ce(IV), V(IV) u V(V). Višak se uklanja razaranjem na povišenoj temperaturi 4 Ag 2+ 2 H 2 O ↔ 4 Ag+ + O 2 + 4 H+ Perokso-disulfat (persulfat) S 2 O 82 - + 2 e ↔ 2 SO 42 E 0=2. 0 V Kiseli, topli rastvori u prisustvu katalizatora (Ag+)- Mn(II) u Mn(VII), Cr(III) u Cr(VI), Ce(III) u Ce(IV), Fe(II) u Fe(III). Može se priomenjivati i u baznoj sredini. Višak reagensa se uklanja kuvanjem u toku 10 minuta 2 S 2 O 82 - + 2 H 2 O → 4 SO 42 - + O 2 + 4 H+ Natrijum-peroksid i vodonik-peroksid H 2 O 2 + 2 H+ + 2 e ↔ 2 H 2 O E 0=1. 77 V Oksidans je i u kiseloj i u baznoj sredini Uklanja se kuvanjem rastvora u toku nekoliko minuta 2 H 2 O 2 →O 2 + 2 H 2 O

REDUKCIONE SUPSTANCE Metali ili metalni amalgami. Reduktorske kolone U vodenom rastvoru-Mg, Al, Zn, Fe, Cd, Ni, Sn, Pb, Sb, Bi, Cu, Ag i Hg Nevodena sredina-alkalni metali Metali-u toku reakcije se oslobađa vodonik, reakcija je burna, troši se mnogo metala, u analizirani rastvor se unosi mnogo metalnih jona. . . Primena amalgama (visok nadnapon vodonika na živi) Jones (Džons)-ov reduktor Amalgamirani metal ima samo malo smanjenu redukcionu sposobnost, ali se sprečava redukcija H+ jona Walden(Valden)-ov reduktor Granulisano elementarno srebro u hlorovodoničnoj kiselini-slabo redukciono sredstvo-veća selektivnost Sumpor-dioksid i vodonik-sulfid *Gasovi, lako rastvorni u vodi, blaga redukciona sredstva *Kisela sredina-Fe(III) u Fe(II), V(V) u V(IV), permangant, dihroma, Ce(IV) *Višak se uklanja kuvanjem u toku pola sata ili provođenjem struje CO 2 *Toksičan, redukcije spore, H 2 S izdvaja koloidni S koji reaguje sa jakim oksidacionim sredstvima

Kalaj(II)-hlorid, Sn. Cl 2 Redukcija Fe(III) u Fe(II), pre permanganometrijskog, dihromatometrijskog ili cerimetrijskog određivanja gvožđa Sn(IV) + 2 e ↔ Sn(II) E 0’=0. 14 V uz c. HCl=1 M Višak se uklanja dodavanjem Hg(II)-hlorida Sn(II) + 2 Hg. Cl 2(višak) →Sn(IV) + Hg 2 Cl 2(s) + 2 Cl- O 2 Vodonik-peroksid + 2 H+ + 2 e ↔H 2 O 2 Kisela sredina- redukuje Mn. O 2, Pb. O 2, Co 2 O 3. . . Višak se uklanja kuvanjem E 0=0. 682 V
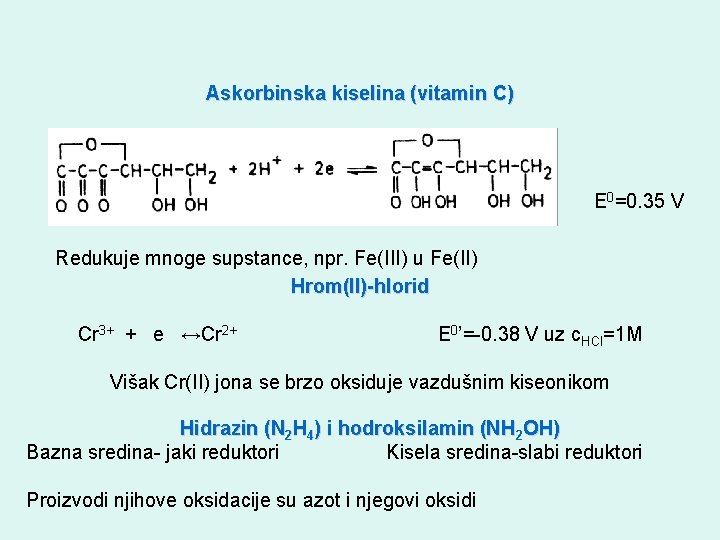
Askorbinska kiselina (vitamin C) E 0=0. 35 V Redukuje mnoge supstance, npr. Fe(III) u Fe(II) Hrom(II)-hlorid Cr 3+ + e ↔Cr 2+ E 0’=-0. 38 V uz c. HCl=1 M Višak Cr(II) jona se brzo oksiduje vazdušnim kiseonikom Hidrazin (N 2 H 4) i hodroksilamin (NH 2 OH) Bazna sredina- jaki reduktori Kisela sredina-slabi reduktori Proizvodi njihove oksidacije su azot i njegovi oksidi

PODELA REDOKS METODA na osnovu toga da li se koristi standardni rastvor okidansa ili reduktora oksidimetrija reduktometrija na osnovu toga koji se standardni rastvor koristi u konkretnom slučaju bromatometrija cerimetrija dihromatometrija jodometrija permanganometrija jodimetrija. . .
- Slides: 23













































