Metoda linearne kombinacije nekih zadanih funkcija temelj MO
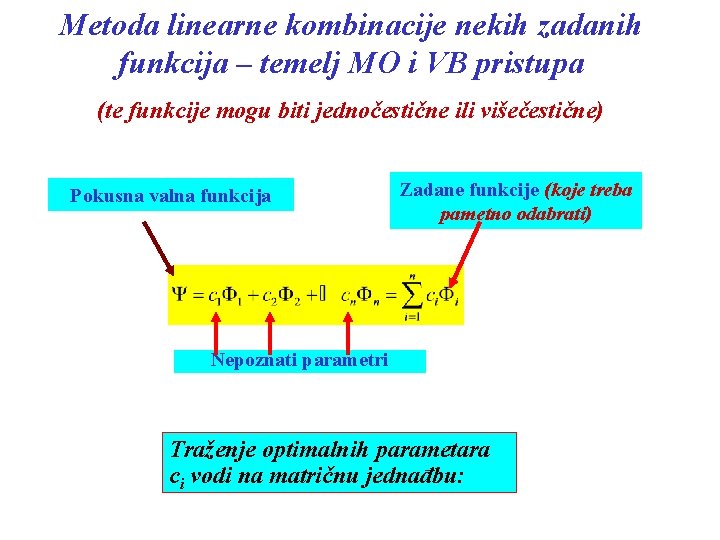
Metoda linearne kombinacije nekih zadanih funkcija – temelj MO i VB pristupa (te funkcije mogu biti jednočestične ili višečestične) Pokusna valna funkcija Zadane funkcije (koje treba pametno odabrati) Nepoznati parametri Traženje optimalnih parametara ci vodi na matričnu jednađbu:
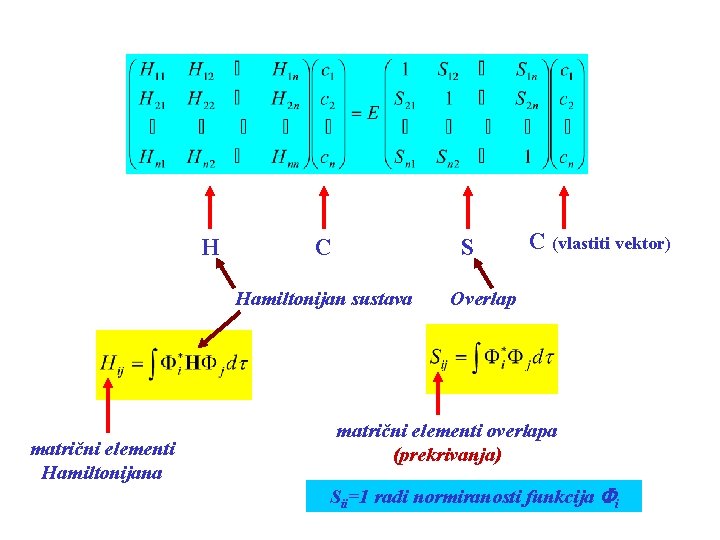
H C S Hamiltonijan sustava matrični elementi Hamiltonijana C (vlastiti vektor) Overlap matrični elementi overlapa (prekrivanja) Sii=1 radi normiranosti funkcija Fi

HC=E SC (1) Poopćena jednađba vlastitih vrijednosti. Formalno slična Schrödingerovoj jednađbi! (H-ES)C=0 Homogeni sustav n jednađbi u n nepoznanica. Netrivijalno rješenje postoji onda i samo onda ako je determinanta sustava nula: Eksplicitno: Sekularna determinanta. Rješenje te determinante daje n energija E. (E 1, E 2, . . . , En). Uvrštavanjem u (1) svaka od tih energija daje n koeficjenata ci, odnosno svaka energija daje odgovarajuću valnu funkciju Y : Y=c 1 F 1+c 2 F 2+. . . +cn. Fn

HC=E SC Ako su funkcije Fi ortonormirane (Sij=dij) tada je S=I (jedinična matrica) HC=E C Obična jednađba vlastitih vrijednosti Puno je lakše riješiti običnu jednađbu vlastitih vrijednosti. Zato se metode koje zahtjevaju rješenje poopćene jednađbe vlastitih vrijednosti obično izbjegavaju ( naročito u vrijeme kada kompjuteri nisu bili dostupni)

Dva temeljna pristupa (zavisno o izboru funkcija Fi) Metoda molekularnih orbitala (MO) • Funkcije Fi su atomske orbitale (AO): Svaka AO sadrži jednu česticu (elektron). To je metoda linearne kombinacije atomskih orbitala (LCAO). Funkcije Fi su orthonormirane! Metoda valentnih struktura (VB) • Funkcije Fi su rezonantne strukture : Svaka RS sadrži sve elektrone sustava (molekule ili e. g. p-elektronskog sustava molekule). Rezonantne strukture nisu ortonormirane!
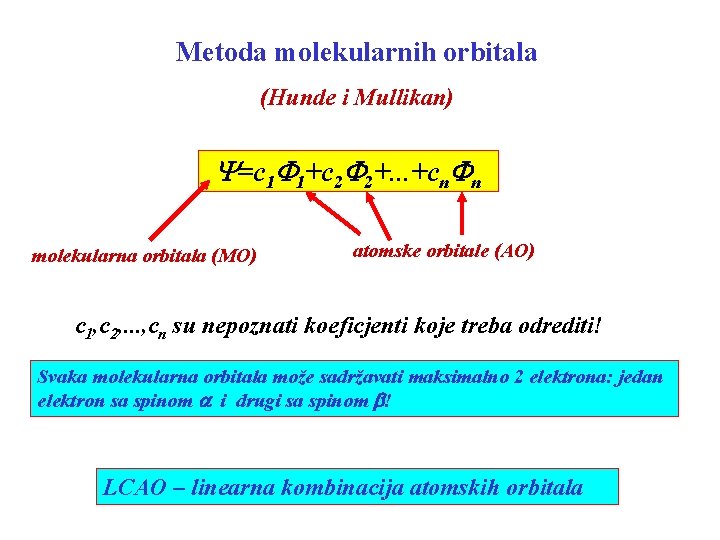
Metoda molekularnih orbitala (Hunde i Mullikan) Y=c 1 F 1+c 2 F 2+. . . +cn. Fn molekularna orbitala (MO) atomske orbitale (AO) c 1, c 2, . . . , cn su nepoznati koeficjenti koje treba odrediti! Svaka molekularna orbitala može sadržavati maksimalno 2 elektrona: jedan elektron sa spinom a i drugi sa spinom b! LCAO – linearna kombinacija atomskih orbitala
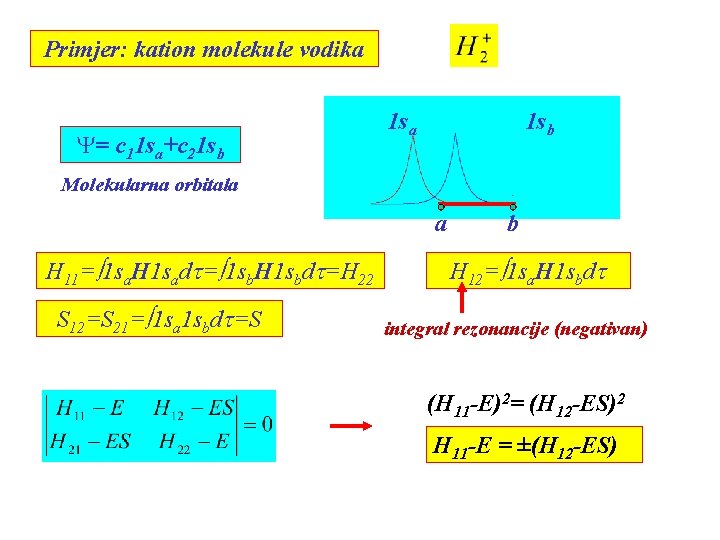
Primjer: kation molekule vodika Y= c 11 sa+c 21 sb 1 sa 1 sb Molekularna orbitala a H 11= 1 sa. H 1 sadt= 1 sb. H 1 sbdt=H 22 S 12=S 21= 1 sa 1 sbdt=S b H 12= 1 sa. H 1 sbdt integral rezonancije (negativan) (H 11 -E)2= (H 12 -ES)2 H 11 -E = ±(H 12 -ES)
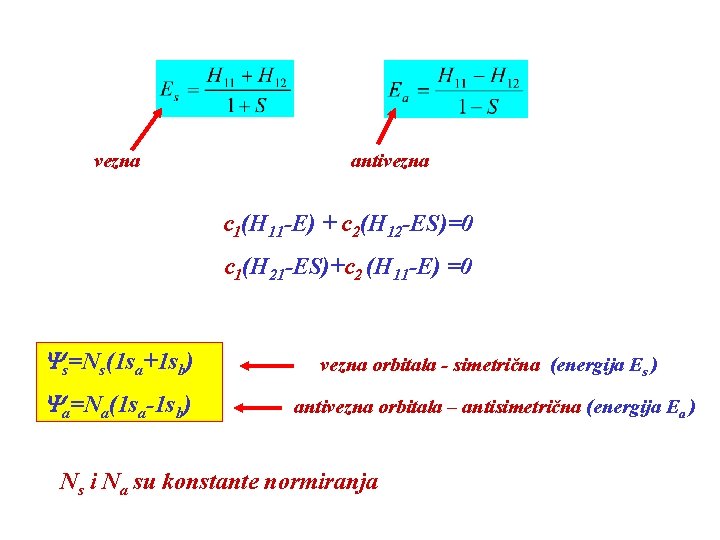
vezna antivezna c 1(H 11 -E) + c 2(H 12 -ES)=0 c 1(H 21 -ES)+c 2 (H 11 -E) =0 Ys=Ns(1 sa+1 sb) vezna orbitala - simetrična (energija Es ) Ya=Na(1 sa-1 sb) antivezna orbitala – antisimetrična (energija Ea ) Ns i Na su konstante normiranja
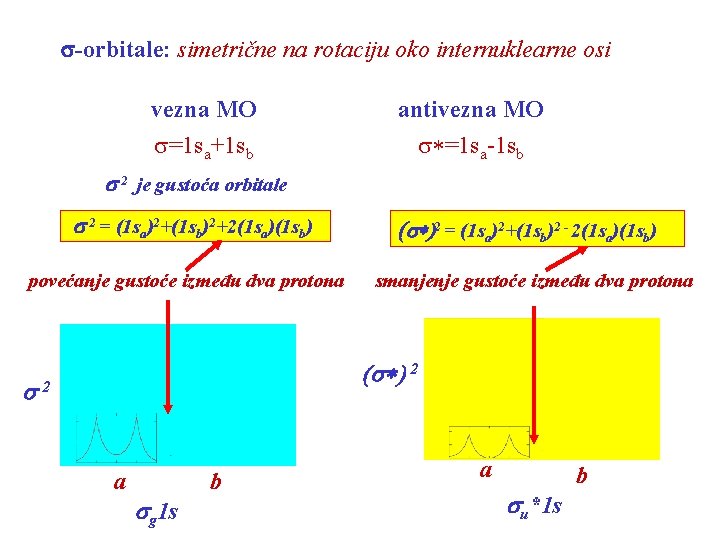
s-orbitale: simetrične na rotaciju oko internuklearne osi vezna MO antivezna MO s=1 sa+1 sb s*=1 sa-1 sb s 2 je gustoća orbitale s 2 = (1 sa)2+(1 sb)2+2(1 sa)(1 sb) povećanje gustoće između dva protona (s*)2 = (1 sa)2+(1 sb)2 - 2(1 sa)(1 sb) smanjenje gustoće između dva protona (s*) 2 s 2 a sg 1 s b a su*1 s b
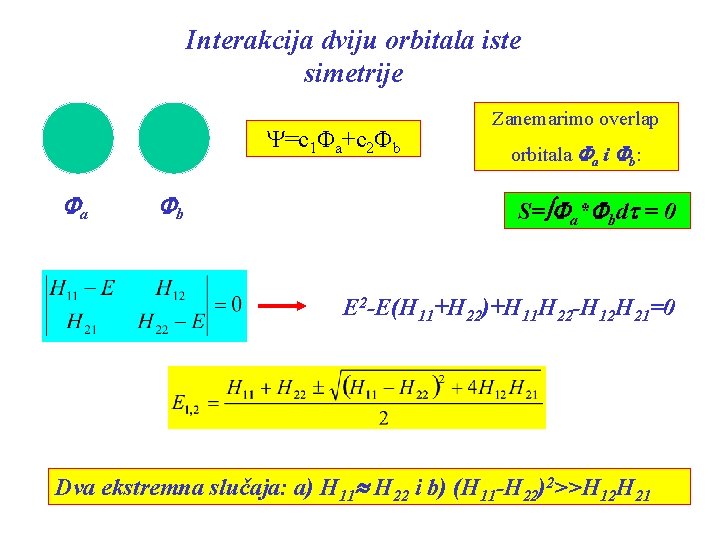
Interakcija dviju orbitala iste simetrije Y=c 1 Fa+c 2 Fb Fa Fb Zanemarimo overlap orbitala Fa i Fb: S= Fa*Fbdt = 0 E 2 -E(H 11+H 22)+H 11 H 22 -H 12 H 21=0 Dva ekstremna slučaja: a) H 11 H 22 i b) (H 11 -H 22)2>>H 12 H 21
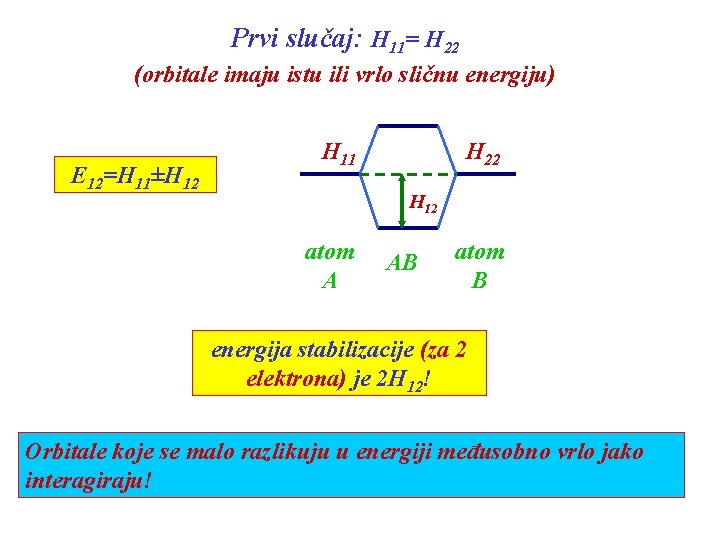
Prvi slučaj: H 11= H 22 (orbitale imaju istu ili vrlo sličnu energiju) E 12=H 11±H 12 H 11 H 22 H 12 atom A AB atom B energija stabilizacije (za 2 elektrona) je 2 H 12! Orbitale koje se malo razlikuju u energiji međusobno vrlo jako interagiraju!
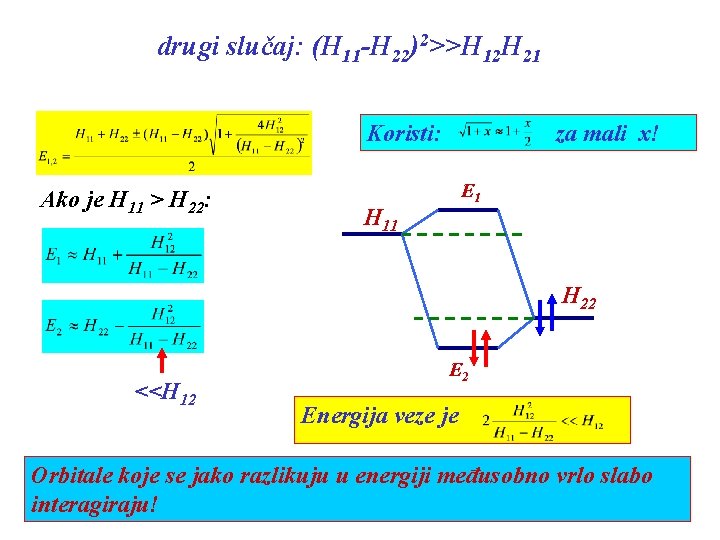
drugi slučaj: (H 11 -H 22)2>>H 12 H 21 Koristi: Ako je H 11 > H 22: za mali x! E 1 H 11 H 22 <<H 12 E 2 Energija veze je Orbitale koje se jako razlikuju u energiji međusobno vrlo slabo interagiraju!
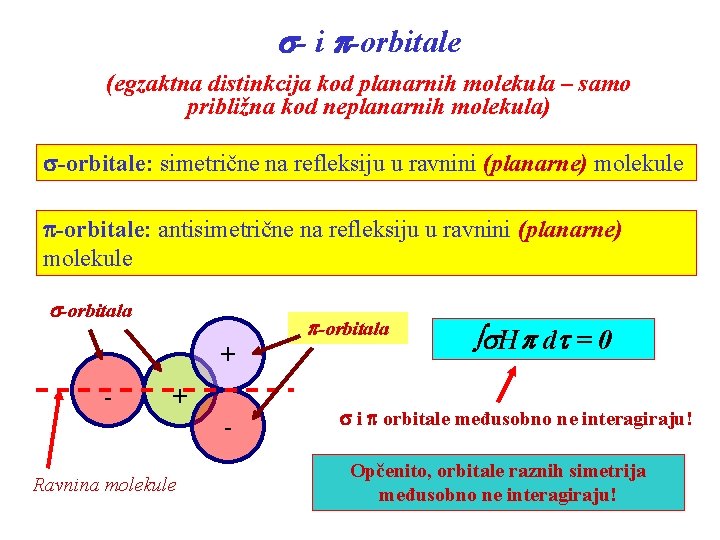
s- i p-orbitale (egzaktna distinkcija kod planarnih molekula – samo približna kod neplanarnih molekula) s-orbitale: simetrične na refleksiju u ravnini (planarne) molekule p-orbitale: antisimetrične na refleksiju u ravnini (planarne) molekule s-orbitala p-orbitala + - Ravnina molekule s. Hp dt = 0 s i p orbitale međusobno ne interagiraju! Opčenito, orbitale raznih simetrija međusobno ne interagiraju!
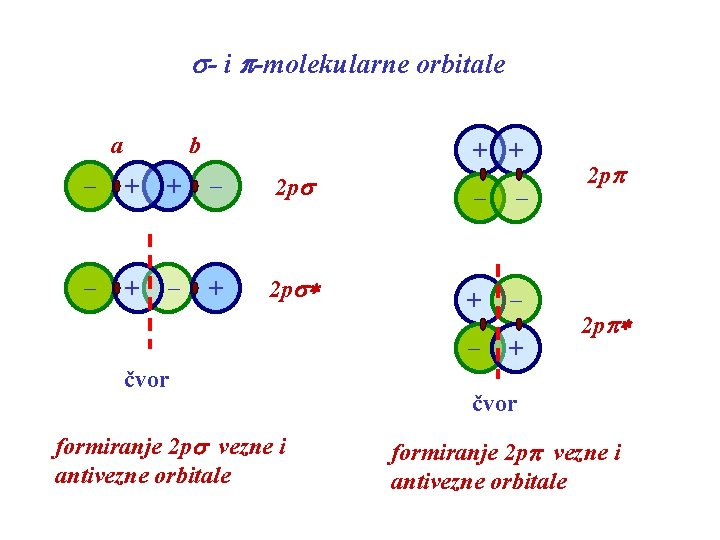
s- i p-molekularne orbitale a b _ + + _ 2 ps _ + 2 ps* čvor formiranje 2 ps vezne i antivezne orbitale + + _ _ + _ 2 pp _ + 2 pp* čvor formiranje 2 pp vezne i antivezne orbitale
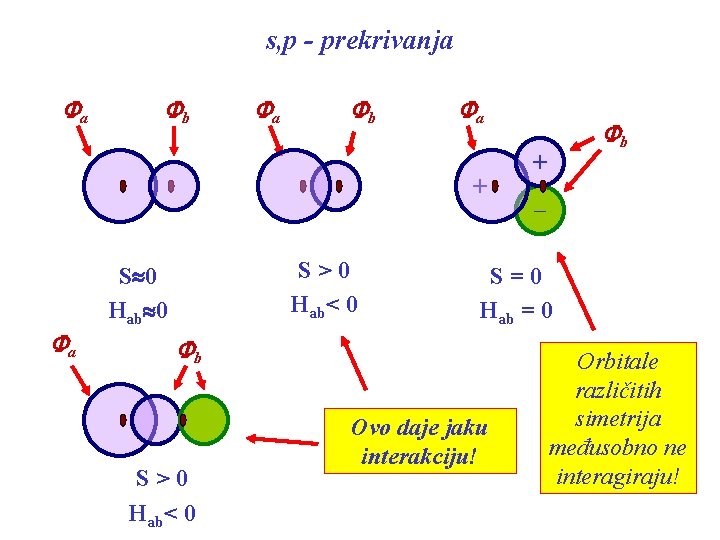
s, p - prekrivanja Fa Fb Fa + Fa S>0 Hab< 0 S 0 Hab 0 + _ S=0 Hab = 0 Fb S>0 Hab< 0 Fb Ovo daje jaku interakciju! Orbitale različitih simetrija međusobno ne interagiraju!
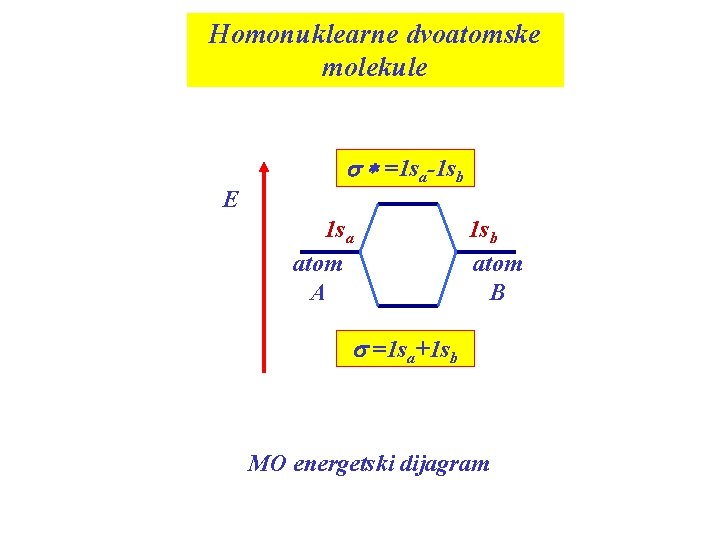
Homonuklearne dvoatomske molekule E s * =1 sa-1 sb 1 sa atom A 1 sb atom B s =1 sa+1 sb MO energetski dijagram
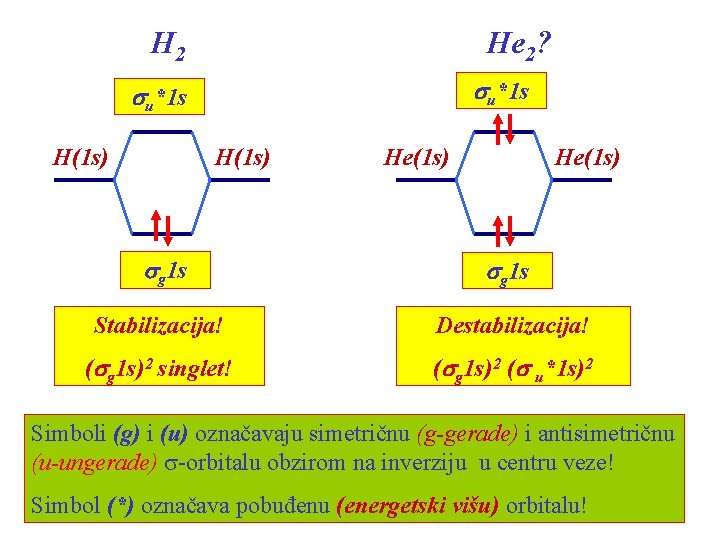
H 2 He 2? su*1 s H(1 s) He(1 s) sg 1 s Stabilizacija! Destabilizacija! (sg 1 s)2 singlet! (sg 1 s)2 (s u*1 s)2 Simboli (g) i (u) označavaju simetričnu (g-gerade) i antisimetričnu (u-ungerade) s-orbitalu obzirom na inverziju u centru veze! Simbol (*) označava pobuđenu (energetski višu) orbitalu!
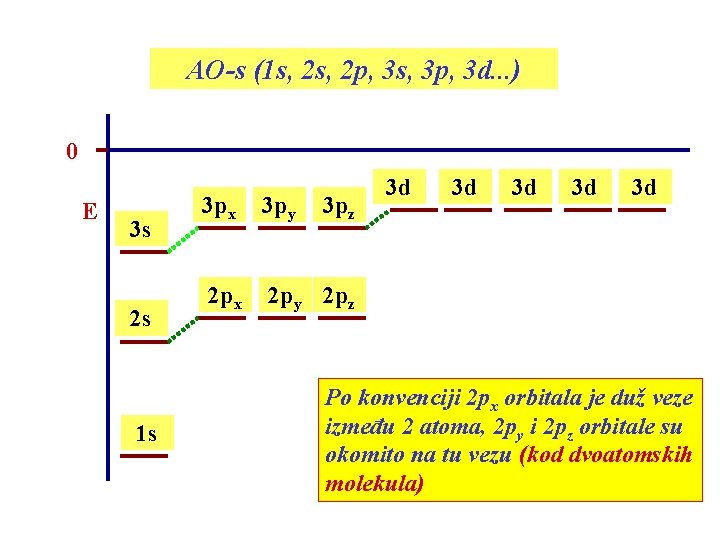
AO-s (1 s, 2 p, 3 s, 3 p, 3 d. . . ) 0 E 3 s 2 s 1 s 3 px 3 py 3 pz 2 px 2 py 2 pz 3 d 3 d 3 d Po konvenciji 2 px orbitala je duž veze između 2 atoma, 2 py i 2 pz orbitale su okomito na tu vezu (kod dvoatomskih molekula)
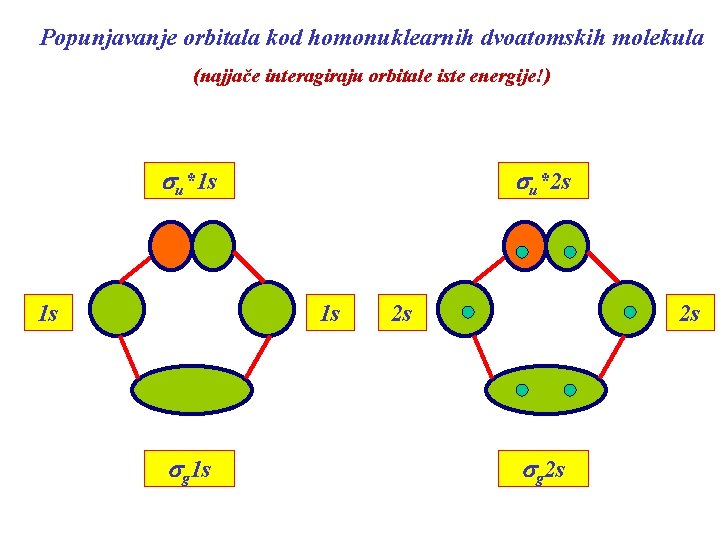
Popunjavanje orbitala kod homonuklearnih dvoatomskih molekula (najjače interagiraju orbitale iste energije!) su*1 s 1 s su*2 s 1 s sg 1 s 2 s 2 s sg 2 s
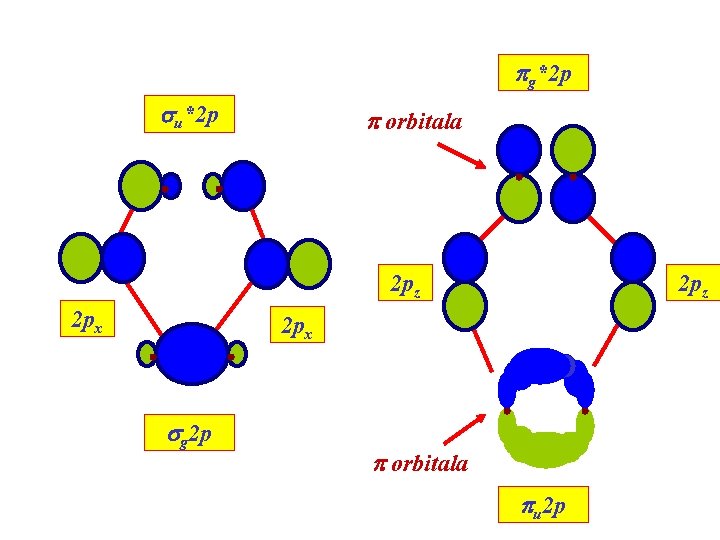
pg*2 p su*2 p p orbitala 2 pz 2 px sg 2 p p orbitala pu 2 p
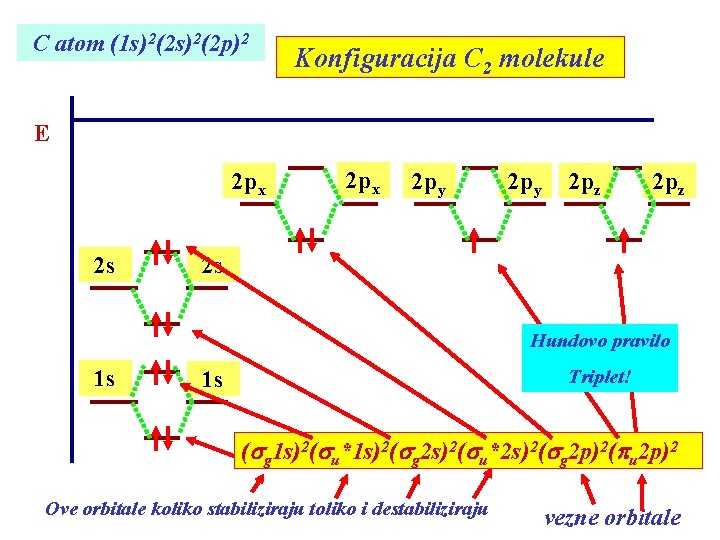
C atom (1 s)2(2 p)2 Konfiguracija C 2 molekule E 2 px 2 s 2 px 2 py 2 pz 2 s Hundovo pravilo 1 s Triplet! 1 s (sg 1 s)2(su*1 s)2(sg 2 s)2(su*2 s)2(sg 2 p)2(pu 2 p)2 Ove orbitale koliko stabiliziraju toliko i destabiliziraju vezne orbitale
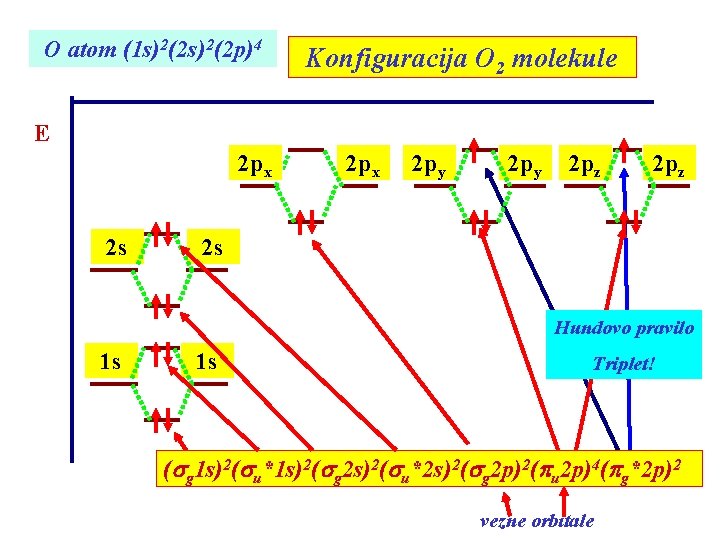
O atom (1 s)2(2 p)4 Konfiguracija O 2 molekule E 2 px 2 s 2 px 2 py 2 pz 2 s Hundovo pravilo 1 s 1 s Triplet! (sg 1 s)2(su*1 s)2(sg 2 s)2(su*2 s)2(sg 2 p)2(pu 2 p)4(pg*2 p)2 vezne orbitale

Pitanja LCAO
- Slides: 23