METALLAR Metallarn icmal tbitd taplmas v alnmasnn mumi

METALLAR Metalların icmalı, təbiətdə tapılması və alınmasının ümumi üsulları. Metalların ərintiləri

Məlum olan 118 kimyəvi elementin 90 -dan çoxu metaldır.
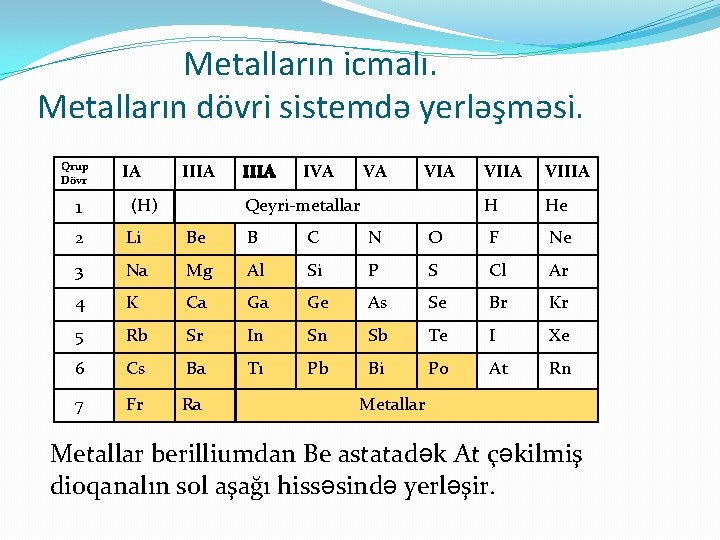
Metalların icmalı. Metalların dövri sistemdə yerləşməsi. Qrup Dövr IA IIIA IVA VA 1 (H) Qeyri-metallar 2 Li Be B C N 3 Na Mg Al Si 4 K Ca Ga 5 Rb Sr 6 Cs 7 Fr VIA VIIIA H He O F Ne P S Cl Ar Ge As Se Br Kr In Sb Te I Xe Ba Tı Pb Bi Po At Rn Ra Metallar berilliumdan Be astatadək At çəkilmiş dioqanalın sol aşağı hissəsində yerləşir.

Metallar güclü reduksiyaedicidir. Birləşmələrdə müsbət oksidləşmə dərəcəsi göstərir. Qızı l Mis Gümüş

Metalların təbiətdə tapılması. �Yer qabığında ən çox yayılmış metal alüminiumdur. Alüminium oksigen və silisiumdan sonra təbiətdə yayılmasına görə üçüncü elementdir. Sonrakı yerləri dəmir, kalsium, natrium, kalium, maqnezium və titan tutur. Dəmir Alüminium

�Respublikamızda bir neçə filiz yataqları aşkar edilmişdir. Bunlara bir neçə nümunə gətirə bilərik. Məsələn: 1) Filizçayda polimetal 2) Daşkəsəndə dəmir 3) Zəylikdə alunit 4) Parağaçayda (Naxçıvan) molibden Söyüdlü-Zod qızıl yatağı 5) Gümüşlüdə (Naxçıvan) qurğuşun-sink � Daşkəsən dəmir filizi əsasında Rustavi şəhərində metallurgiya zavodu işləyir. Zəylik aluniti əsasında dünyada ilk dəfə olaraq Gəncə alüminium zavodunda Al₃O₃, Sumqayıt alüminium zavodunda isə Al metalı istehsal olunur.

Metalların alınmasının ümumi üsulları � Sənayedə metalları almaq üçün yararlı olan təbii birləşmələr filiz adlanır. �Ən çox istifadə olunan filizlər bunlardır: 1. Oksidlər: Al 2 O 3 n. H 2 O - boksit; Fe₃O 4 - maqnetit 2. Sulfidlər: Fe 2 S - pirit; Hg. S - kinovar 3. Karbonatlar: Ca. CO 3 - əhəngdaşı, Fe. CO 3 - siderit 4. Xloridlər: Na. Cl qalit, KCl - silvin 5. Sulfatlar: Ca. SO 4 2 H 2 O - gips, Ba. SO 4 - ağır şpat �Filizlərdən metallar metal kationlarının reduksiyası ilə alınır: Mⁿ⁺+ne⁻―› M⁰ �Metalların alınmasında birinci mərhələ filizlərin saflaşdırılmasıdır. Saflaşdırılmış filizlərdən metallar əsasən üç üsulla alınır. 1)Pirometallurgiya üsulu 2)Hidrometallurgiya üsulu

Pirometallurgiya üsulu � Bu prosesdə metallar reduksiyaedicilərin (C, CO, H₂, aktiv metallar) iştirakı ilə yüksək temperturda filizdən reduksiya olunur. Bu üsulda sulfidlər və karbonatlar əvvəlcə oksidlərə t çevrilir. t 1. Cu₂O + C ―› 2 Cu + Co t 2. Fe₂O₃ + 3 CO ―› 2 Fe + 3 CO₂ t 3 a. 2 Zn. S + 3 O₂―› 2 Zn. O + 2 SO₂ 3 b. Zn. O + C ―› Zn + CO Reduksiyaedici kimi aktiv metallardan (Al, Mg, Na) və hidrogendən istifadə edilirsə, proses müvafiq olaraq metallotermiya və hidrogenotermiya adlanır. t Cr₂O₃ + 2 Al ―› 2 Cr + Al₂O₃ alüminotermiya t Mo. O₃ + 3 H₂ ―› Mo + 3 H₂O hidrogenotermiya

Hidrometallurgiya üsulu �Hidrometallurgiya üsulunda metalın birləşməsi məhlula keçirilir və həmin məhluldan metal özündən daha aktiv metalla və ya elektrik cərəyanı ilə reduksiya olunur. Bu yolla qızıl, gümüş, mis, sink, volfram (W) və s. metallar alınır: Cu. O + H 2 SO₄ ―› Cu. SO₄ + H₂O məhlul misin alınması Cu. SO₄(məhlul) + Fe ―› Cu + Fe. SO₄

Elektrometallurgiya üsulu �Elektrometallurgiya üsulunda metal onun birləşməsinin ərintisindən elektrolizlə alınır. Adətən, bu yolla aktiv metallar (Na, K, Ca, Al və s. ) alınır. el-z 2 Na. Cl(ərinti) ―› 2 Na + Cl₂ el-z 2 Al₂O₃(ərinti) ―› 4 Al + 3 O₂ 2 KCl (ərinti) ―› 2 K + Cl₂ Ca. Cl₂(ərinti) ―› ca + Cl₂

Əridilmiş duz və qələvilərin elektrolizi �Əgər natrium-xlorid ərintisinə salınmış elektrodları sabit cərəyan mənbəyinə qoşsaq, müsbət yüklü Na+ kationları katoda (K–), mənfi yüklü Cl– anionları anoda (A+) tərəf hərəkət edəcək. Na+ kationları katoddan özlərinə elektron birləşdirib reduksiya olunur, Cl– anionları isə öz elektronlarını anoda verib oksidləşir: katodda Na, anodda isə xlor ayrılır. Bu iki prosesin elektron tənlikləri belə göstərilir: Katod (K⁻): Na⁺ + e⁻ ―› Na Anod (A⁺) : 2 Cl – 2 e⁻ ―› Cl₂ Sabit elektrik cərəyanının təsiri ilə elektrodlarda baş verən oksidləşməreduksiya reaksiyalarına elektroliz deyilir. Na. Cl ərintisinin elektrolizi

Metalların ərintiləri (xəlitələr) �İki və daha artıq metaldan, yaxud metal və qeyrimetaldan ibarət sistemlərə ərintilər deyilir. Polad Çuqundan hazırlanmış tava

Təsnifatı �Texnikada ərintilər müxtəlif əlamətlərə görə təsnif edilir. 1) Xarakterik xassələrinə görə: çətinəriyən – nixrom asanəriyən – tunc, bürünc, lehim Çuqun paslanmayan – xromlanmış polad 2) Ərintinin əsasını təşkil edən metala görə: qara – çuqun, polad əlvan – tunc, bürünc, melxior yüngül – düralüminium, elektron 3)Ərintinin komponentlərinin sayina görə: ikili, üçlü, dördlü və s. Nixrom

�Ərintilərin tərkibinə bəzi metal və qeyri-metalları əlavə etdikdə faydalı xassəli ərintilər alınır. Belə proses legirlənmə adlanır. Məsələn: 1) Xrom Cr - ərintiyə bərklik və korroziyaya davamlılıq verir. 2) Silisium Si – turşuların təsirinə qarşı davamlılıq verir. 3) Volfram W – bərklik və istiyə qarşı möhkəmlik verir. 4) Titan Ti – istiyə və korroziyaya davamlılıq, həmçinin mexaniki möhkəmlik verir. Beş ən çox istifadə edilən metalın tətbiqinin azalması sırası: dəmir, alüminium, mis, sink, manqan. Titan Volfram Silisium

E-resurs � http: //mesafedenmekteb. edu. az/ru/fenler/520 -dmendeleyevinkimyevi-elementlerin-dovru-sistemi-cedveli. html � https: //az. wikipedia. org/wiki/Mis#/media/File: Nat. Copper. jpg � https: //az. wikipedia. org/wiki/Qızıl#/media/File: Gold-crystals. jpg � https: //tr. wikipedia. org/wiki/Gümüş#/media/File: Silver_crystal. jpg � https: //ru. wikipedia. org/wiki/Железо#/media/File: Iron_electrolytic_a nd_1 cm 3_cube. jpg � https: //ru. wikipedia. org/wiki/Алюминий#/media/File: Aluminium 4. jpg � http: //kimya. ccess. info/1_6_3_0. html � http: //e-derslik. edu. az/books/151/units/unit-1/page 10. xhtml � http: //www. shagird. info/maraqlidir/mundericat/main. html? id=29 � https: //az. wikipedia. org/wiki/Çuqun#/media/File: Cast-Iron-Pan. jpg � http: //stroyres. net/metallicheskie/vidyi/chyornyie/chugun/ponyatieosobennosti. html � https: //ru. wikipedia. org/wiki/Титан_(элемент)#/media/File: Titancrystal_bar. JPG � https: //az. wikipedia. org/wiki/Volfram#/media/File: Wolfram_evaporat ed_crystals_and_1 cm 3_cube. jpg � https: //en. wikipedia. org/wiki/Silicon#/media/File: Silicon. Croda. jpg
- Slides: 15