Metabolizmus Ako bunka zskava energiu z vonkajieho prostredia

Metabolizmus • Ako bunka získava energiu z vonkajšieho prostredia? • Ako bunky syntetizujú stavebné látky makromolekúl? Integrovaná sieť chemických reakcii

Princípy metabolizmu • Živiny sú degradované a veľké makromolekuly sú syntetizované postupne sériou reakcii – metabolickými dráhami (metabolizmus – súbor procesov) • Použitie jednotného zdroja energie vo všetkých formách života (prepojenie energiu-uvoľňujúcich a energiu-spotrebujúcich dráh) • Oxidácia uhlíkových palív – syntéza ATP • Opakujúci sa limitovaný počet aktivovaných intermediátov • Použitie niekoľkých (opakujúcich sa) typov reakcii s jednoduchými mechanizmami • Metabolické dráhy sú vysoko regulovateľné

Potreba neustáleho prísunu voľnej energie - Mechanická práca - svalová kontrakcia a bunkový pohyb - Aktívny transport molekúl a iónov - Syntéza makromolekúl a iných biomolekúl z jednoduchých prekurzorov • Anabolizmus – tvorba komplexných molekúl • Katabolizmus – degradácia živín a ich transformácia do bunkovej energie (ATP)

Spriahnutie endergonických a exergonických reakcií • Voľná energia (ΔG), ktorá hovorí o povahe danej reakcie • ΔG reakcie závisí od prírody reaktantov (ΔGo) a od ich koncentrácie [C][D] ΔG = ΔG°´ + RT ln [A][B] • Celková zmena voľnej energie ΔG série reakcií sa rovná súčtu zmien voľných energií jednotlivých reakcií
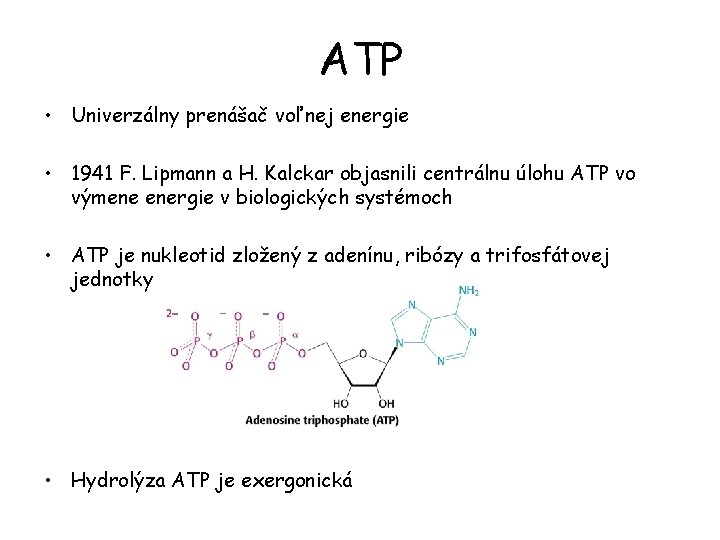
ATP • Univerzálny prenášač voľnej energie • 1941 F. Lipmann a H. Kalckar objasnili centrálnu úlohu ATP vo výmene energie v biologických systémoch • ATP je nukleotid zložený z adenínu, ribózy a trifosfátovej jednotky • Hydrolýza ATP je exergonická
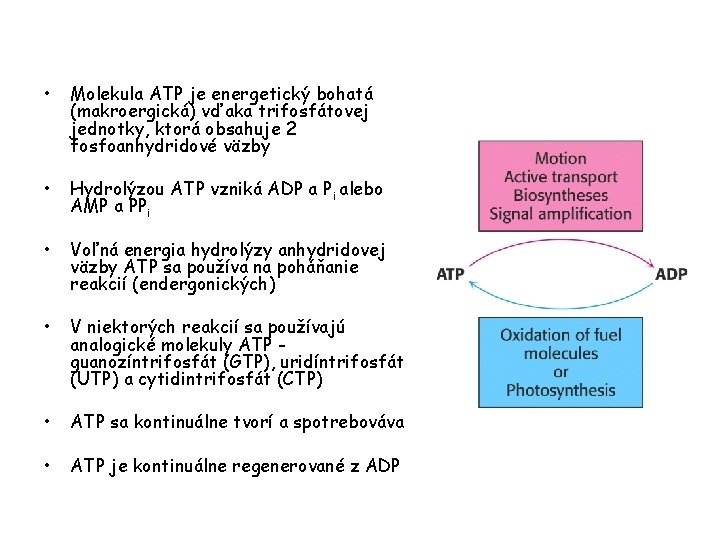
• Molekula ATP je energetický bohatá (makroergická) vďaka trifosfátovej jednotky, ktorá obsahuje 2 fosfoanhydridové väzby • Hydrolýzou ATP vzniká ADP a Pi alebo AMP a PPi • Voľná energia hydrolýzy anhydridovej väzby ATP sa používa na poháňanie reakcií (endergonických) • V niektorých reakcií sa používajú analogické molekuly ATP guanozíntrifosfát (GTP), uridíntrifosfát (UTP) a cytidintrifosfát (CTP) • ATP sa kontinuálne tvorí a spotrebováva • ATP je kontinuálne regenerované z ADP
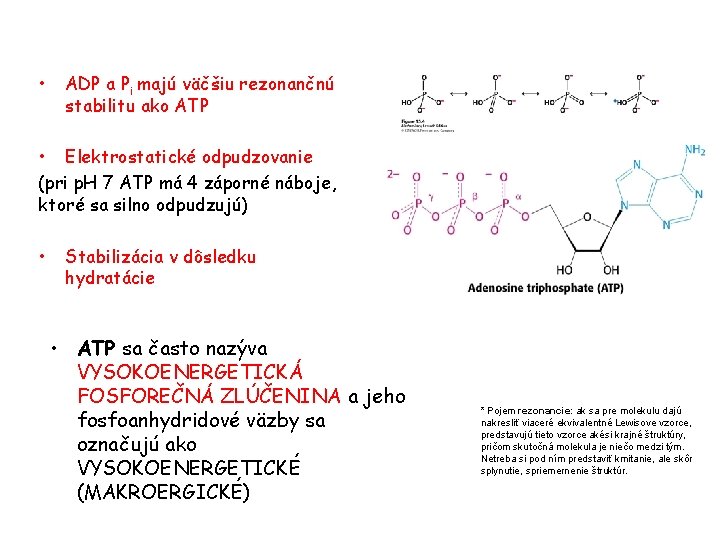
• ADP a Pi majú väčšiu rezonančnú stabilitu ako ATP • Elektrostatické odpudzovanie (pri p. H 7 ATP má 4 záporné náboje, ktoré sa silno odpudzujú) • Stabilizácia v dôsledku hydratácie • ATP sa často nazýva VYSOKOENERGETICKÁ FOSFOREČNÁ ZLÚČENINA a jeho fosfoanhydridové väzby sa označujú ako VYSOKOENERGETICKÉ (MAKROERGICKÉ) * Pojem rezonancie: ak sa pre molekulu dajú nakresliť viaceré ekvivalentné Lewisove vzorce, predstavujú tieto vzorce akési krajné štruktúry, pričom skutočná molekula je niečo medzi tým. Netreba si pod ním predstaviť kmitanie, ale skôr splynutie, spriemernenie štruktúr.


- Prepojenie oxidácie uhlíka a ATP syntézy - 100 g ATP v tele – vysoký obrat tohto množstva Napr. 40 kg ATP za 24 hodín – v kľude; Pri námahe spotreba ATP 0, 5 kg/min; 2 hodinový beh spotreba 60 kg ATP - Neustála regenerácia ATP z ADP! - Tvorba ATP je primárna úloha katabolizmu - Iónový gradient naprieč membránou – bunková energia prepojená so syntézou ATP
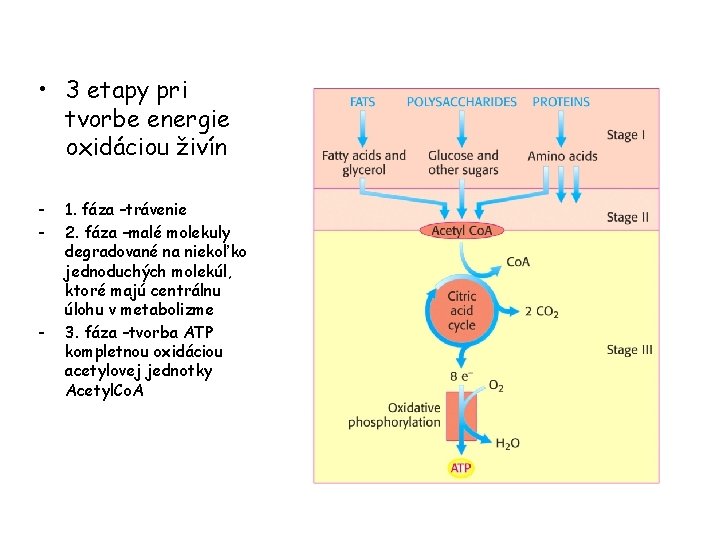
• 3 etapy pri tvorbe energie oxidáciou živín - - 1. fáza –trávenie 2. fáza –malé molekuly degradované na niekoľko jednoduchých molekúl, ktoré majú centrálnu úlohu v metabolizme 3. fáza –tvorba ATP kompletnou oxidáciou acetylovej jednotky Acetyl. Co. A

NADH a FADH 2 • Chemotrofy získavajú energiu oxidáciou živín ako sú glc a mastné kyseliny • U aeróbnych organizmov hlavný elektrónový akceptor je O 2 • Elektróny sú prenášane najskôr na pyridínové nukleotidy alebo flavíny • Prenos elektrónov z koenzýmov pomocou dýchacieho reťazca na O 2 • Výsledok prietoku elektrónov týmto reťazcom je syntéza ATP (oxidačná fosforylácia)
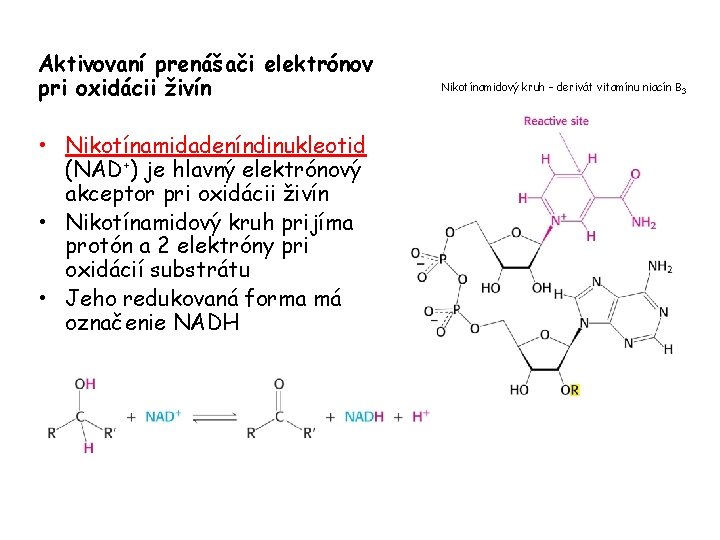
Aktivovaní prenášači elektrónov pri oxidácii živín • Nikotínamidadeníndinukleotid (NAD+) je hlavný elektrónový akceptor pri oxidácii živín • Nikotínamidový kruh prijíma protón a 2 elektróny pri oxidácií substrátu • Jeho redukovaná forma má označenie NADH Nikotínamidový kruh – derivát vitamínu niacín B 3
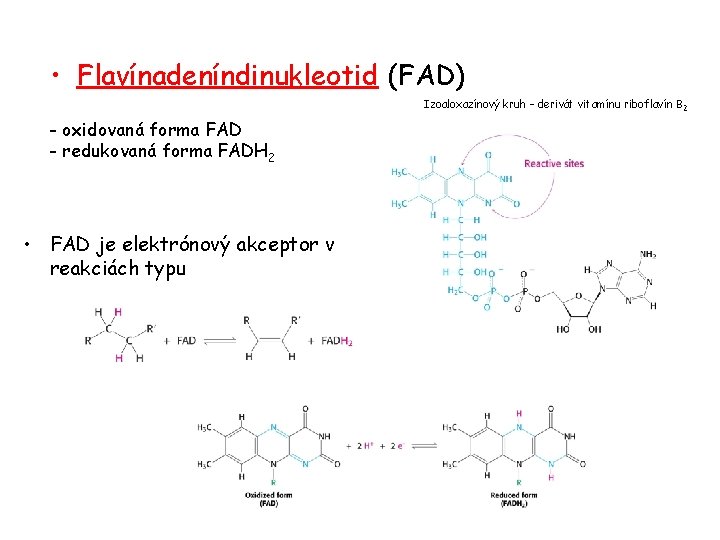
• Flavínadeníndinukleotid (FAD) Izoaloxazínový kruh – derivát vitamínu riboflavín B 2 - oxidovaná forma FAD - redukovaná forma FADH 2 • FAD je elektrónový akceptor v reakciách typu

Aktivovaný prenášač elektrónov pre redukčné biosyntézy - Elektrón-donor pre väčšinu redukčných biosyntéz je NADPH • Je to redukovaná forma nikotínamidadeníndinukleotid fosfát • Fosfátova skupina slúži ako usmerňovač k biosyntetickým enzýmom
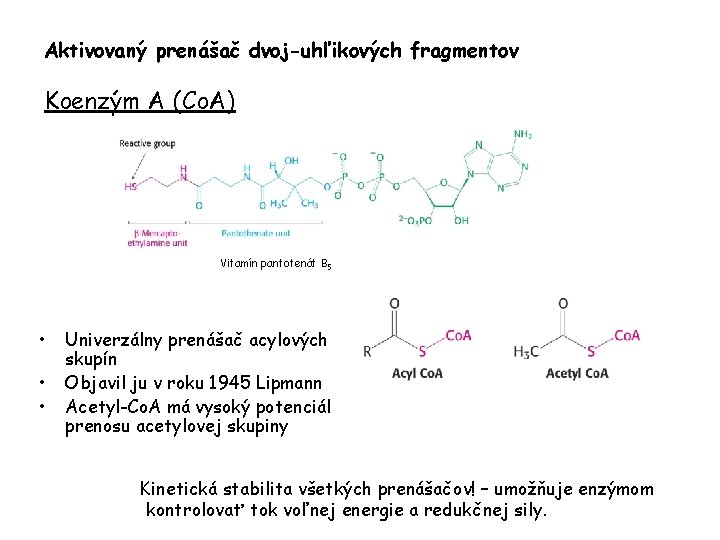
Aktivovaný prenášač dvoj-uhľikových fragmentov Koenzým A (Co. A) Vitamín pantotenát B 5 • • • Univerzálny prenášač acylových skupín Objavil ju v roku 1945 Lipmann Acetyl-Co. A má vysoký potenciál prenosu acetylovej skupiny Kinetická stabilita všetkých prenášačov! – umožňuje enzýmom kontrolovať tok voľnej energie a redukčnej sily.



Kľúčové reakcie sa opakujú 1. Oxidačno-redukčné – prenos elektrónov 2. Ligácia (ATP) - tvorba kovalentnej väzby 3. Izomerizácia – úprava atómov pričom vznikajú izoméry 4. Prenos skupín – prenos funkčnej skupiny z jednej molekuly na druhú 5. Hydrolytické – štiepenie väzby v prítomnosti vody 6. Pridanie alebo odstránenie funkčnej skupiny – tvorba dvojitej väzby
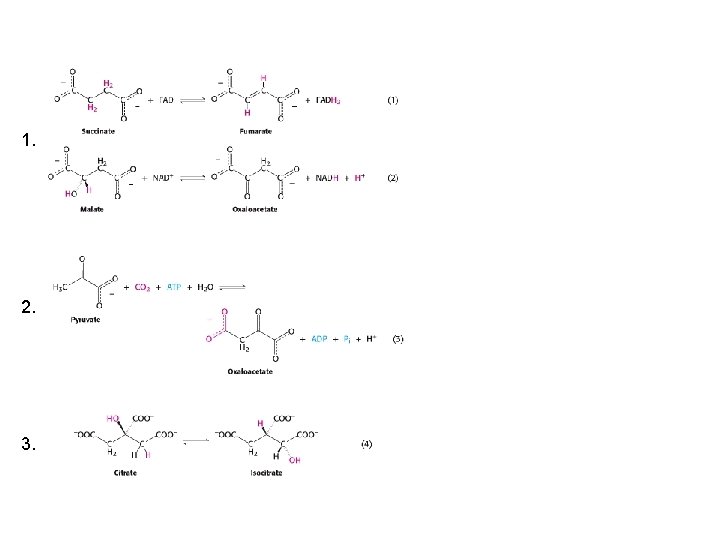
1. 2. 3.
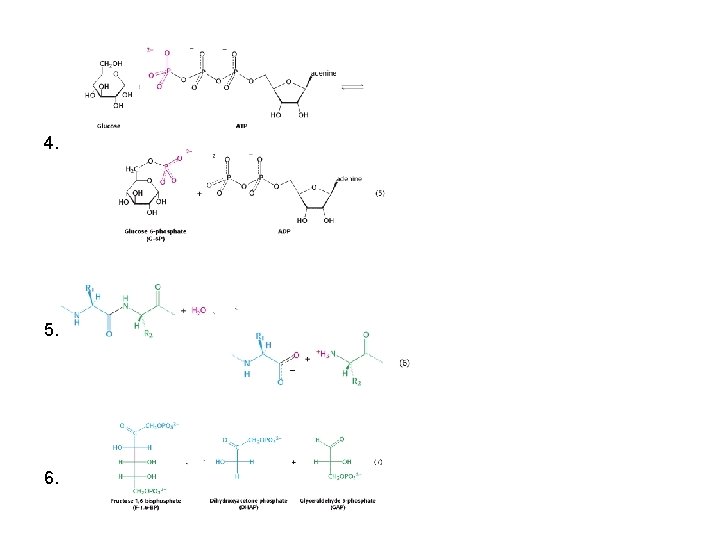
4. 5. 6.
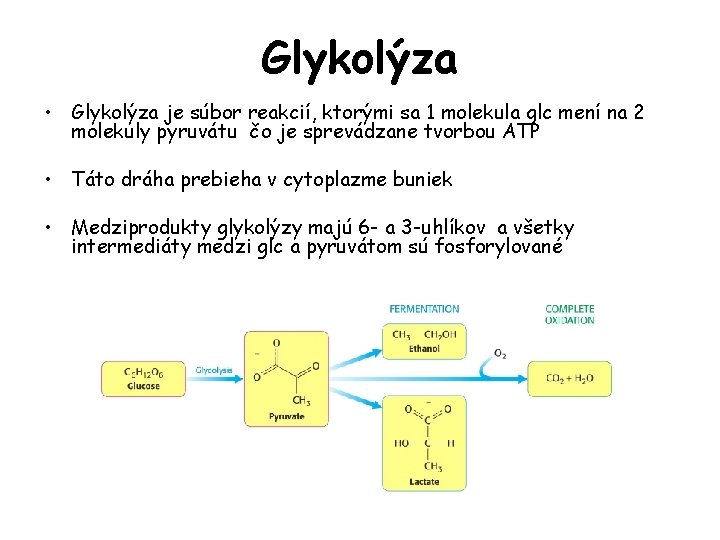
Glykolýza • Glykolýza je súbor reakcií, ktorými sa 1 molekula glc mení na 2 molekuly pyruvátu čo je sprevádzane tvorbou ATP • Táto dráha prebieha v cytoplazme buniek • Medziprodukty glykolýzy majú 6 - a 3 -uhlíkov a všetky intermediáty medzi glc a pyruvátom sú fosforylované


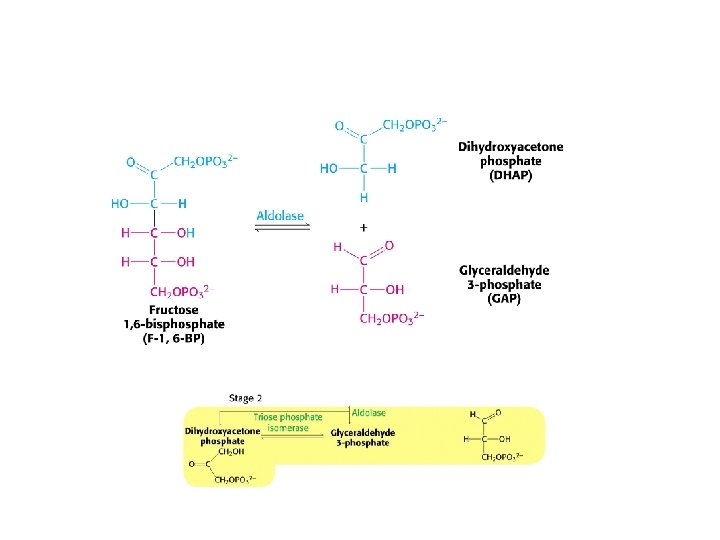

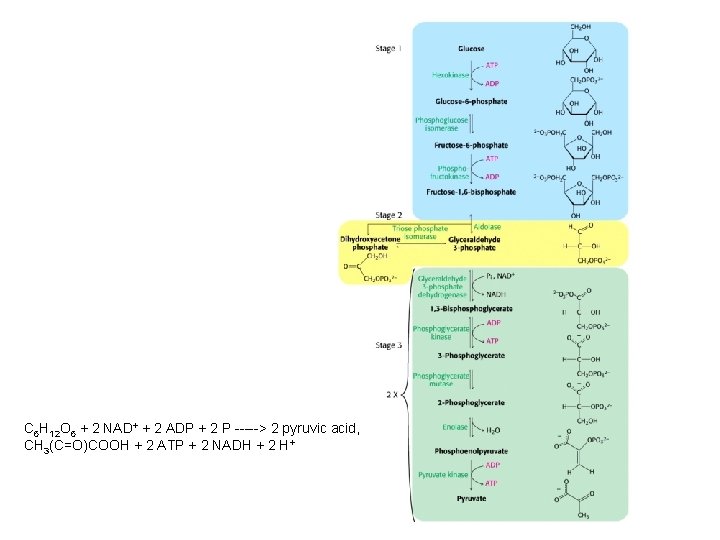
C 6 H 12 O 6 + 2 NAD+ + 2 ADP + 2 P -----> 2 pyruvic acid, CH 3(C=O)COOH + 2 ATP + 2 NADH + 2 H+

Kontrola glykolýzy • Glykolýza má dvojitú úlohu: degradovať glc aby sa tvorilo ATP a poskytovať stavebné látky pre biosyntézy • V metabolických dráhach enzýmy katalyzujúce nevratné reakcie sú potenciálnymi miestami regulácie • V glykolýze sú to hexokináza, fosfofruktokináza a pyruvátkináza (kontrolne miesta glykolýzy) • Fosfofruktokináza je kľúčový enzým v kontrole glykolytickej dráhy

• Fosfofruktokináza je inhibovaná alosterický vysokou konc. ATP (ktorý znižuje afinitu enzýmu k fru-6 -P) • Inhibičné pôsobenie sa ruší prítomnosťou AMP, a tak sa aktivita enzýmu zvyšuje keď je nízky ATP/AMP pomer • Inhibičný účinok na fosfofruktokinázu má aj citrát (ktorý inhibuje enzým zvyšovaním inhibičného efektu ATP) • 1980 H. G. Hers a E. Van Schaftinger objavili ďalší aktivátor fosfofruktokinázy – fruktóza-2, 6 bisfosfát

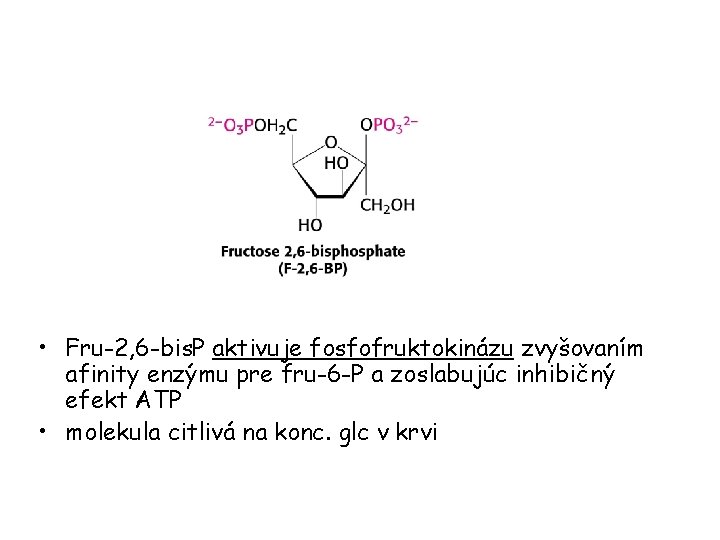
• Fru-2, 6 -bis. P aktivuje fosfofruktokinázu zvyšovaním afinity enzýmu pre fru-6 -P a zoslabujúc inhibičný efekt ATP • molekula citlivá na konc. glc v krvi

• Fru-2, 6, -bis. P je syntetizovaná fosfofruktokinázou 2 (PFK 2) z glu-6 -P, a späť je hydrolyzovaná na glu-6 -P enzýmom fruktózabisfosfatáza 2 (FBPase 2) • Jeden polypeptidový reťazec obsahujúci obidve enzýmové aktivity – tandemový enzým • Fru-6 -P urýchľuje syntézu fru-2, 6 -bis. P a inhibuje jej hydrolýzu • Nadbytok fru-6 -P vedie k zvyšovaniu konc. fru-2, 6 -bis. P, ktorá stimuluje fosfofruktokinázu – „feed-forward stimulation“
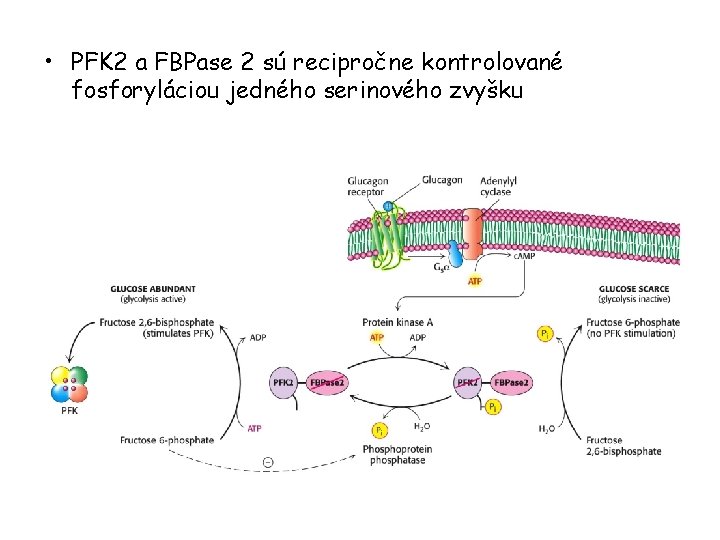
• PFK 2 a FBPase 2 sú recipročne kontrolované fosforyláciou jedného serinového zvyšku
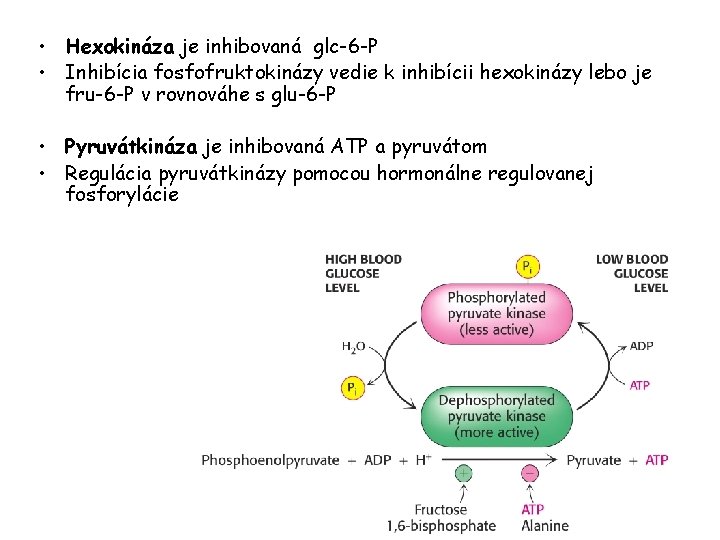
• Hexokináza je inhibovaná glc-6 -P • Inhibícia fosfofruktokinázy vedie k inhibícii hexokinázy lebo je fru-6 -P v rovnováhe s glu-6 -P • Pyruvátkináza je inhibovaná ATP a pyruvátom • Regulácia pyruvátkinázy pomocou hormonálne regulovanej fosforylácie
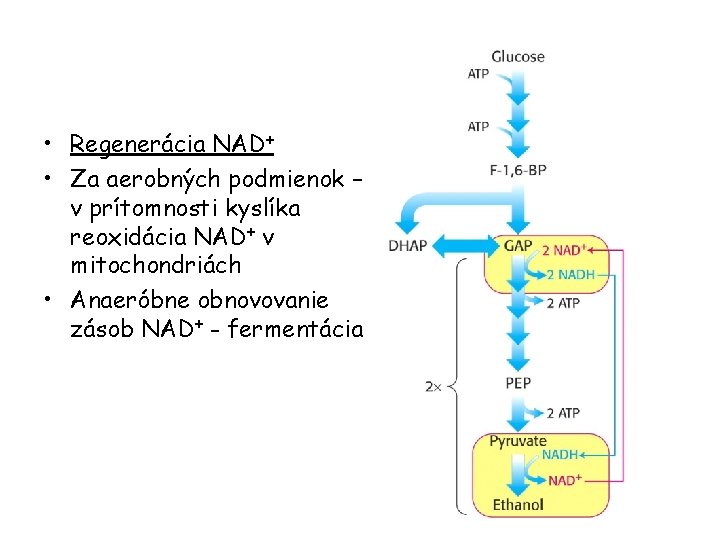
• Regenerácia NAD+ • Za aerobných podmienok – v prítomnosti kyslíka reoxidácia NAD+ v mitochondriách • Anaeróbne obnovovanie zásob NAD+ - fermentácia
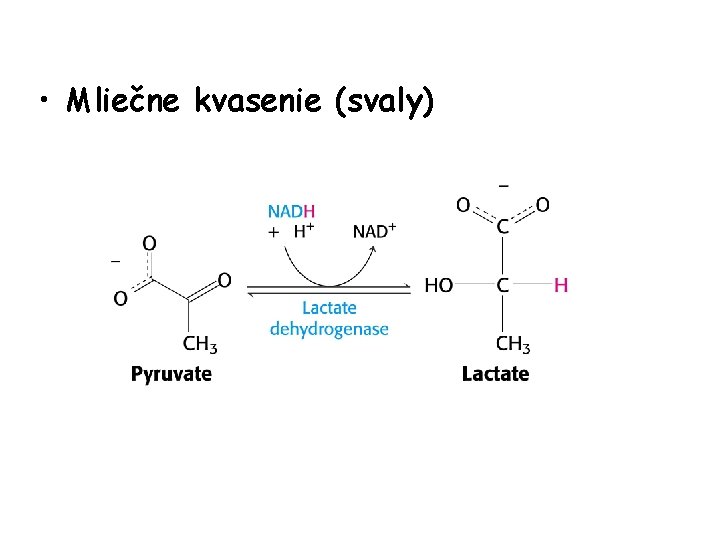
• Mliečne kvasenie (svaly)
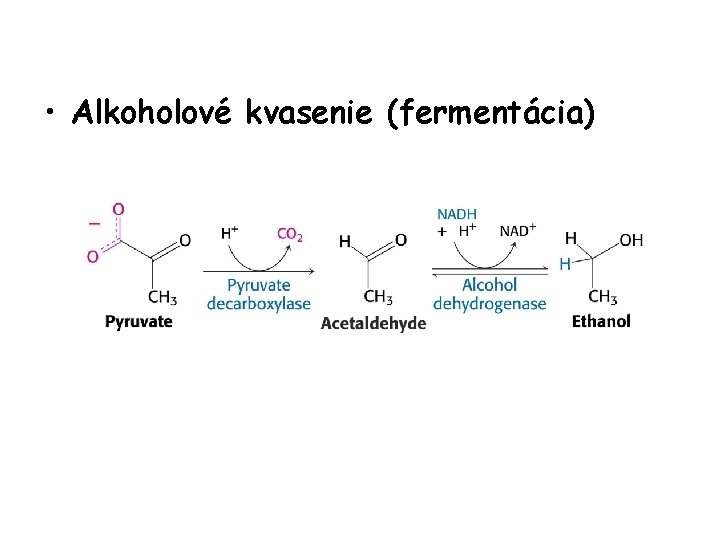
• Alkoholové kvasenie (fermentácia)
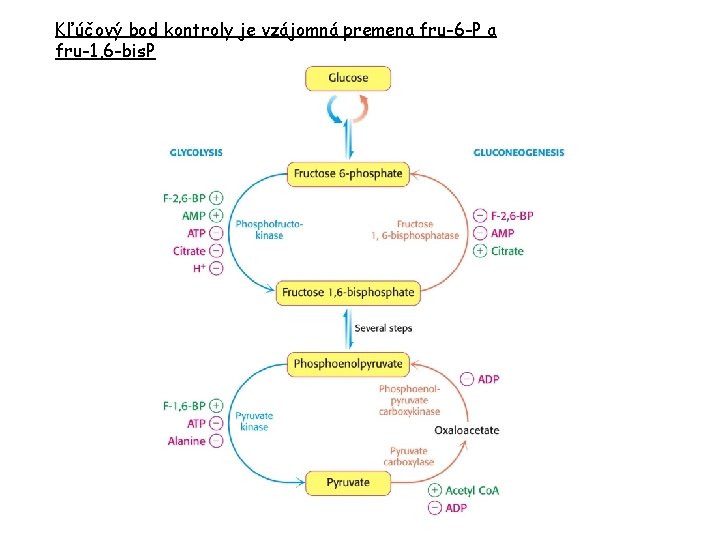
Kľúčový bod kontroly je vzájomná premena fru-6 -P a fru-1, 6 -bis. P
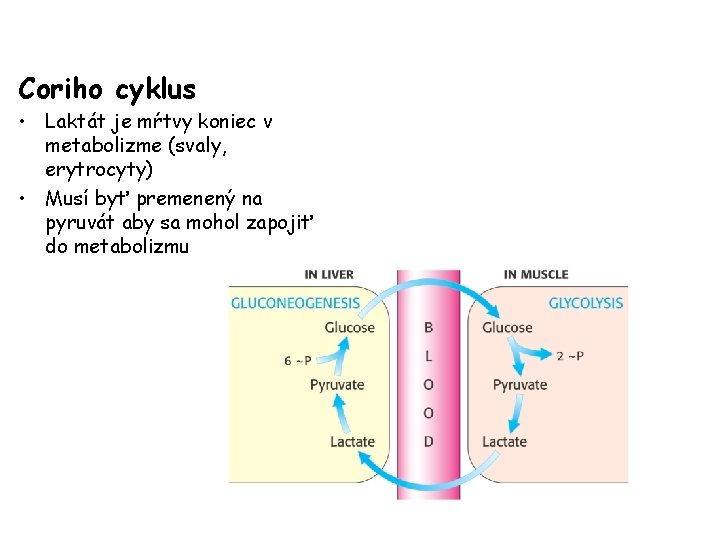
Coriho cyklus • Laktát je mŕtvy koniec v metabolizme (svaly, erytrocyty) • Musí byť premenený na pyruvát aby sa mohol zapojiť do metabolizmu
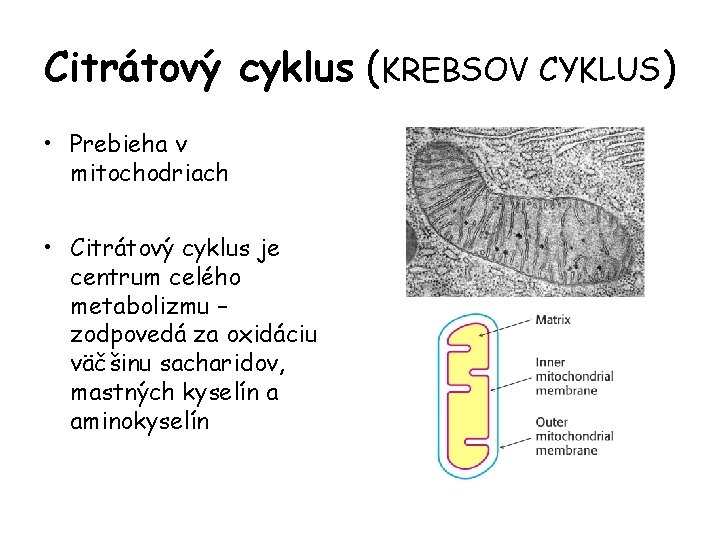
Citrátový cyklus (KREBSOV CYKLUS) • Prebieha v mitochodriach • Citrátový cyklus je centrum celého metabolizmu – zodpovedá za oxidáciu väčšinu sacharidov, mastných kyselín a aminokyselín
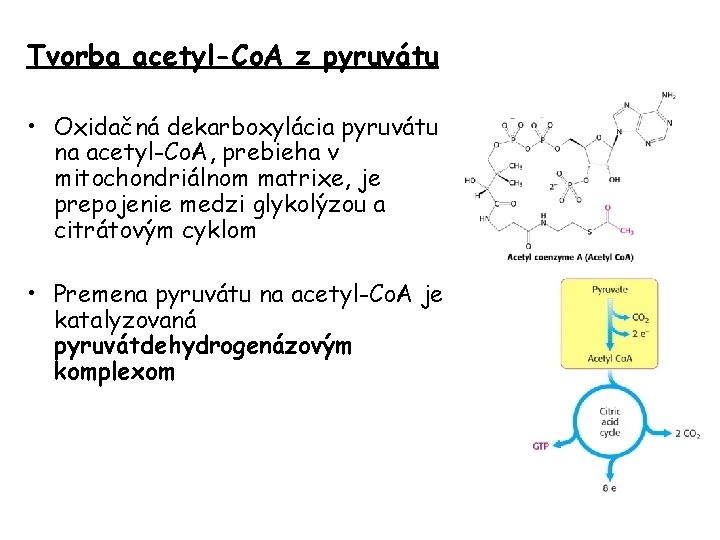
Tvorba acetyl-Co. A z pyruvátu • Oxidačná dekarboxylácia pyruvátu na acetyl-Co. A, prebieha v mitochondriálnom matrixe, je prepojenie medzi glykolýzou a citrátovým cyklom • Premena pyruvátu na acetyl-Co. A je katalyzovaná pyruvátdehydrogenázovým komplexom
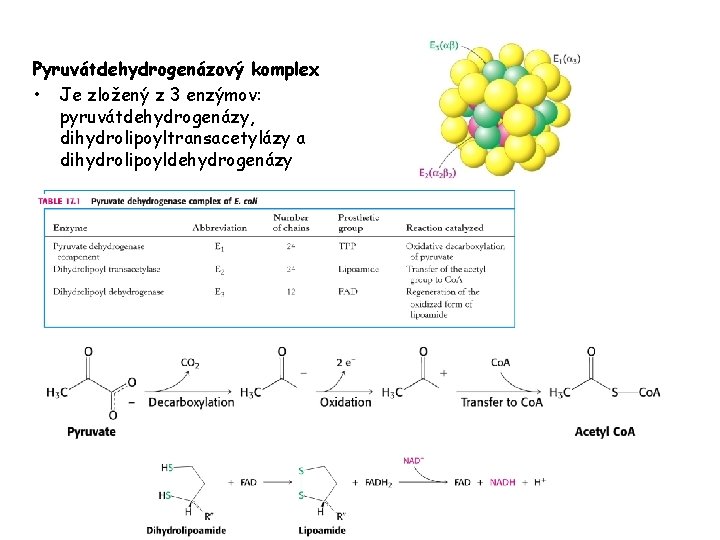
Pyruvátdehydrogenázový komplex • Je zložený z 3 enzýmov: pyruvátdehydrogenázy, dihydrolipoyltransacetylázy a dihydrolipoyldehydrogenázy
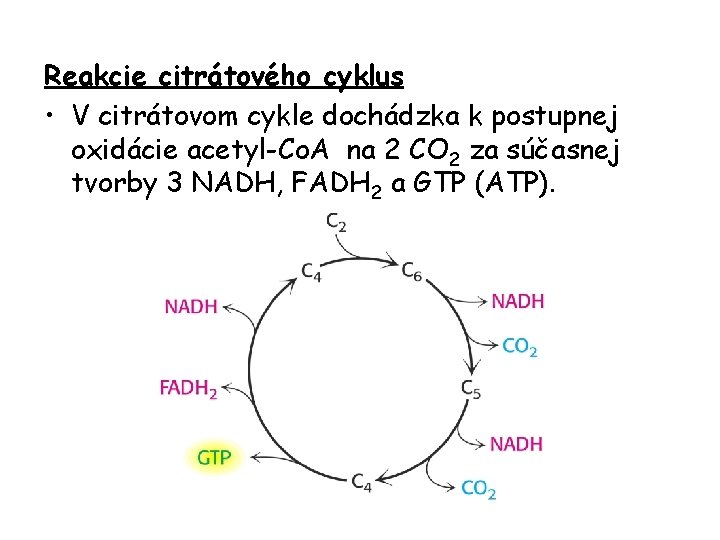
Reakcie citrátového cyklus • V citrátovom cykle dochádzka k postupnej oxidácie acetyl-Co. A na 2 CO 2 za súčasnej tvorby 3 NADH, FADH 2 a GTP (ATP).


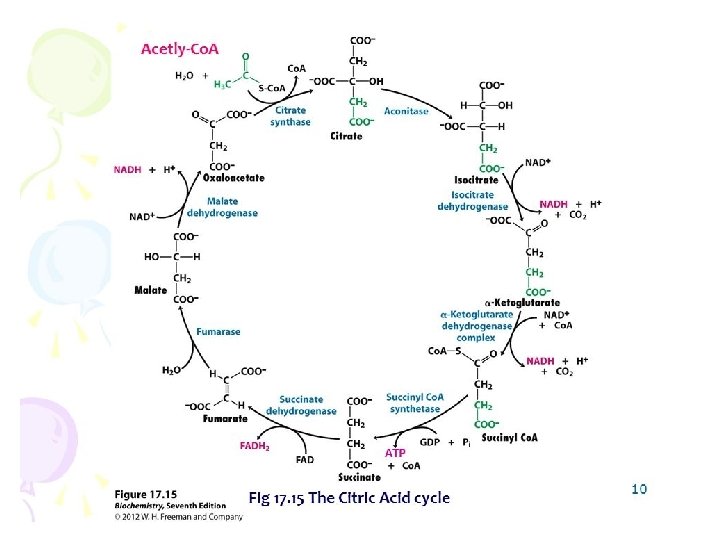
tiež ATP
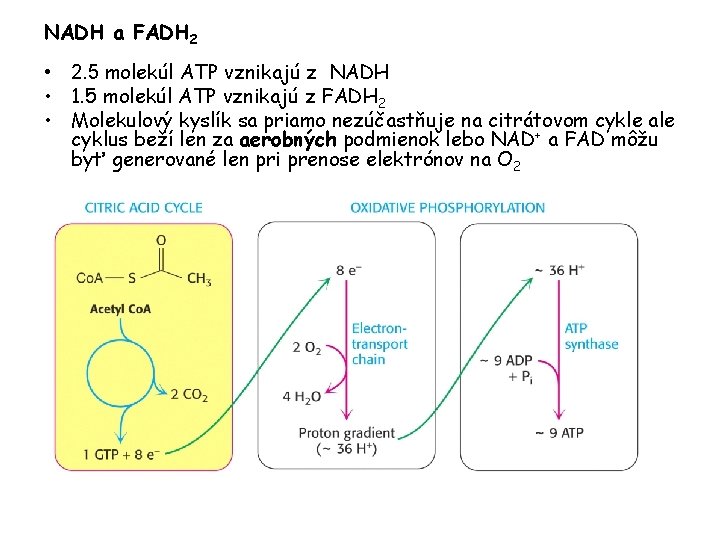
NADH a FADH 2 • 2. 5 molekúl ATP vznikajú z NADH • 1. 5 molekúl ATP vznikajú z FADH 2 • Molekulový kyslík sa priamo nezúčastňuje na citrátovom cykle ale cyklus beží len za aerobných podmienok lebo NAD+ a FAD môžu byť generované len pri prenose elektrónov na O 2
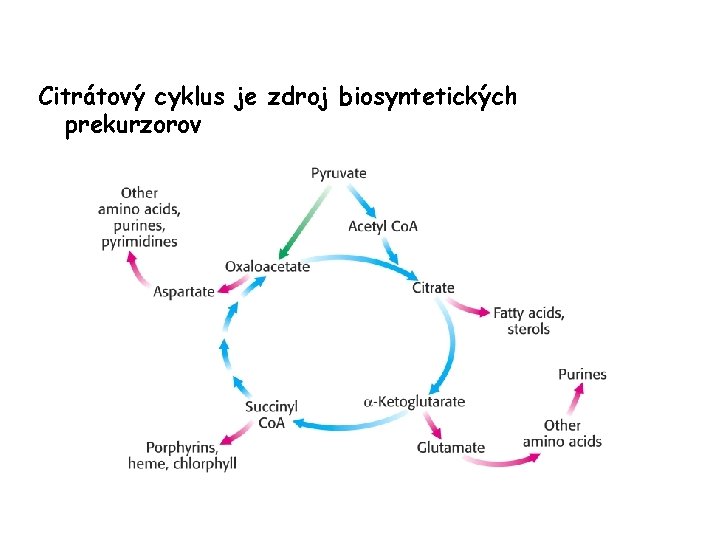
Citrátový cyklus je zdroj biosyntetických prekurzorov

Regulácia pyruvátdehydrogenázového komplexu • Inhibíciou produktmi (NADH súťaží s NAD+ pre naviazanie na E 3 , Acetyl Co. A súťaží s Co. A pre naviazanie na E 2) • Spätná -väzobná regulácia nukleotidmi • Regulácia vratnou fosforyláciou
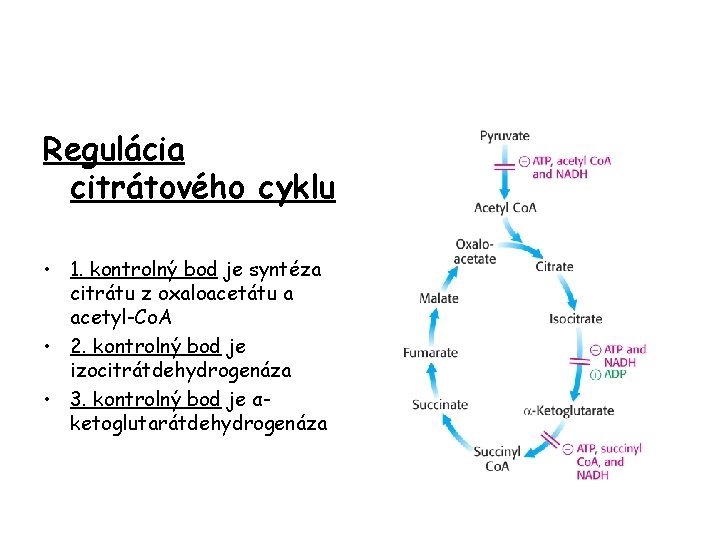
Regulácia citrátového cyklu • 1. kontrolný bod je syntéza citrátu z oxaloacetátu a acetyl-Co. A • 2. kontrolný bod je izocitrátdehydrogenáza • 3. kontrolný bod je αketoglutarátdehydrogenáza
- Slides: 49