METABOLISMO DE LOS COMPUESTOS NITRIGENADOS Bases nitrogenadas Aminocidos

METABOLISMO DE LOS COMPUESTOS NITRIGENADOS • Bases nitrogenadas • Aminoácidos • Proteínas


El hígado genera urea como desecho metabólico de las proteínas (a través del ciclo de la urea). Normalmente una persona adulta tiene alrededor de 8. 0 - 20. 0 mg de nitrógeno ureico por 100 ml de sangre.

Características del nitrógeno Muy abundante en la naturaleza Casi químicamente inerte La incorporación de N 2 a las moléculas orgánicas comienza por la fijación del N 2 por los organismos procariotas

Características del nitrógeno El nitrógeno molecular o dinitrógeno(N 2) (generalmente llamado solo nitrógeno) es una molécula diatómica homonuclear formada por dos átomos de nitrógeno. Es un gas (a condiciones normales de presión y temperatura) que constituye del orden del 78 % del aire atmosférico.
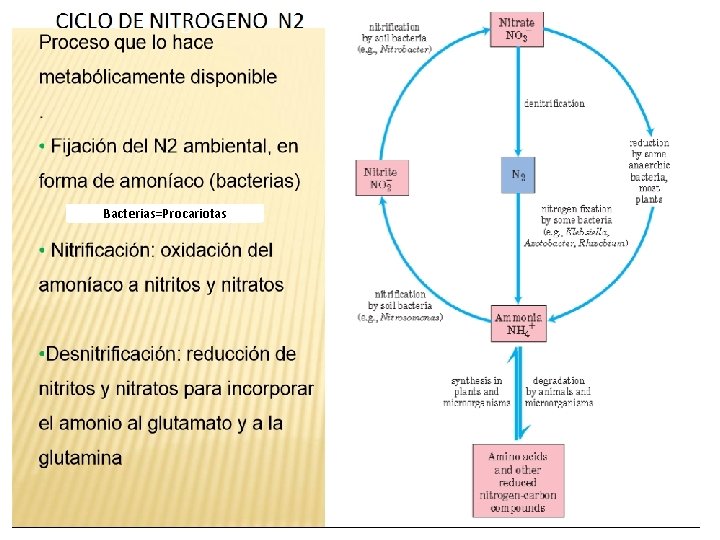
Bacterias=Procariotas
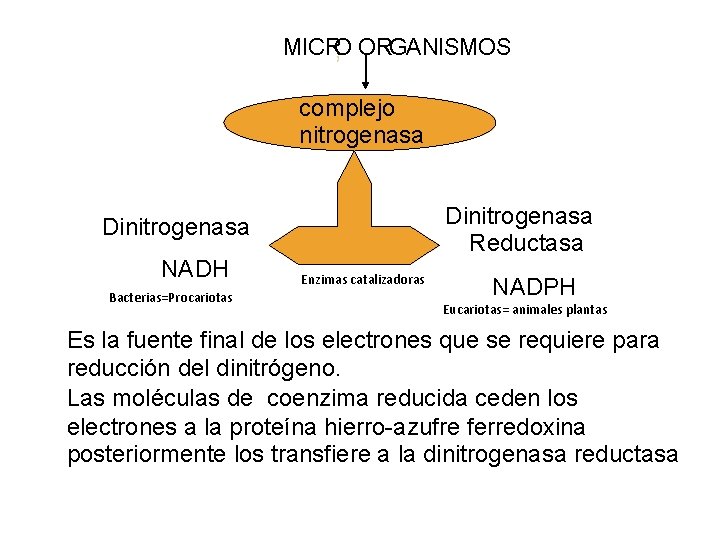
MICRO , ORGANISMOS complejo nitrogenasa Dinitrogenasa Reductasa Dinitrogenasa NADH Bacterias=Procariotas Enzimas catalizadoras NADPH Eucariotas= animales plantas Es la fuente final de los electrones que se requiere para reducción del dinitrógeno. Las moléculas de coenzima reducida ceden los electrones a la proteína hierro-azufre ferredoxina posteriormente los transfiere a la dinitrogenasa reductasa

La incorporación de N 2 a las biomoléculas requiere la reducción enzimática de N 2 a NH 3, con un alto costo energético. Se calcula que por cada mol de N 2 reducido a NH 3 se gastan 16 moles de ATP, de acuerdo a la siguiente reacción: N 2 + 8 e + 16 ATP + 16 H 2 O 2 NH 3 + H 2 + 16 ADP + 16 Pi + 8 H+ (e = electrones) N 2: Dinitrogeno, NH 3: Nitrato H 2: Dihidrogeno H+: ion hidrogeno

sustrato para la síntesis de proteínas Glutamato: (aa no esencial) Fuente de grupos amino de la mayoría de los aa (reacciones de transaminación) Glutamina: Dona grupos amino para muchos procesos biosintéticos (célula y en fluidos extracelulares) Su concentración es mayor que los otros aa y se regula de acuerdo a requerimientos de nitrógeno de célula y del balance osmótico entre citosol y el medio externo.
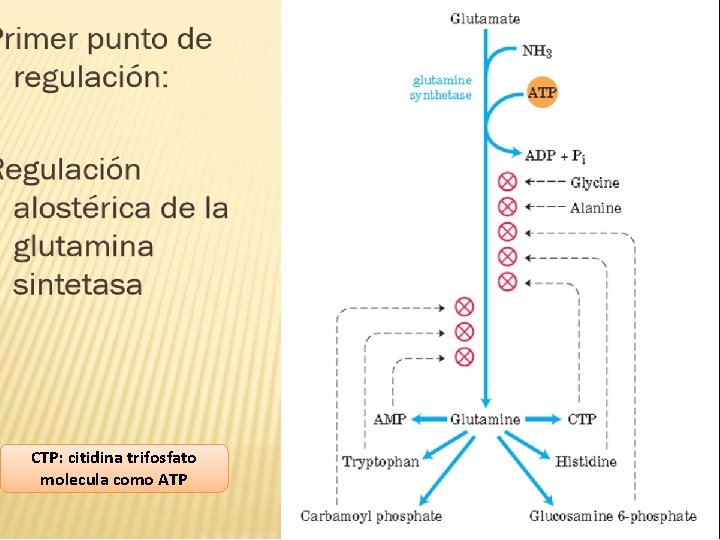
CTP: citidina trifosfato molecula como ATP
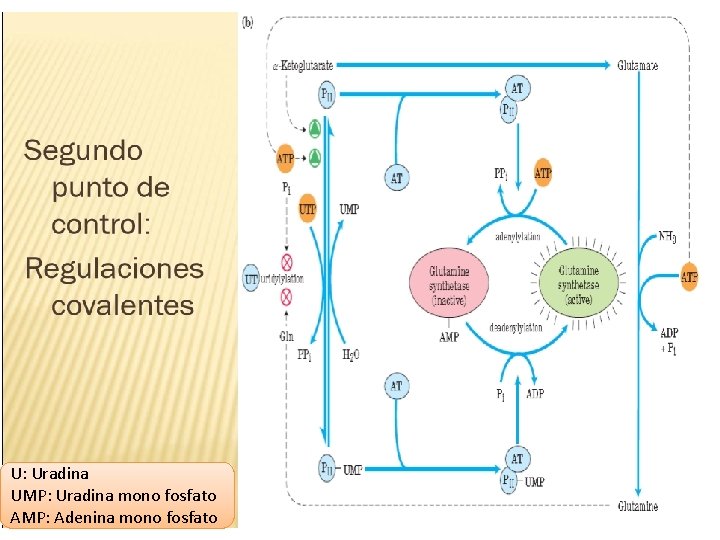
U: Uradina UMP: Uradina mono fosfato AMP: Adenina mono fosfato

Aminoácidos Esenciales Valina (Val) Leucina (Leu) Isoleucina (Ile) Fenilalanina (Phe) Metionina (Met) Treonina (Thr) Lisina (Lys) Triptófano (Trp) Histidina (His) Aminoácidos No esenciales Arginina (Arg) Alanina (Ala) Prolina (Pro) Glicina (Gly) Serina (Ser) Cisteina (Cys) Asparagina (Asn) Glutamina (Gln) Tirosina (Tyr) Ácido aspártico (Asp) Ácido glutámico (Glu)

Aminoácido de cadena ramificada (ACR) Los ACE representan una forma principal de transporte del nitrógeno amino desde el hígado a otros tejidos donde se utiliza para la síntesis de los ANE que se requiere para la síntesis de proteína y ciertos derivados de aminoácidos. Reacciones de transaminación Estas dominan el metabolismo de los aminoácidos. Están catalizadas por un grupo de enzimas denominadas aminotransferasas o transaminasa, los grupos alfaamino, se transfieren desde un alfa-aminoácido a un alfacetoacido ACE; Aminoácidos esenciales ANE: Aminoacidos no esenciales


La mayor cantidad de las proteínas en el cuerpo se encuentran en forma de músculos. Cuando las exigencias de aminoácidos no son satisfechas, el músculo es degradado en aminoácidos, que son enviados entonces a la reserva de aminoácidos para ser usados en consecuencia.

A fin de satisfacer las demandas de los tejidos del cuerpo, el mismo necesita nuevos aminoácidos. La proteína alimenticia es nuestra fuente primaria de aminoácidos. De todos los macronutrientes la proteína es la única con un subsidio diario recomendado (RDA). RDA es corriente en adultos sedentarios es de 0. 83 gramos de proteínas por kilogramo de peso corporal


Equilibrio de Nitrógeno = Nt (consumo total) - Nu (en orina) - Nf (en heces) - Ns (en sudor) cuando la ecuación es =0: equilibrio nitrogenado Proteína adicional es utilizada: ≥ 0: equilibrio de nitrógeno positivo Nuevos tejidos ≤ 0: equilibrio nitrogenado negativo proteína debe ser usada para obtenergía.

El cuerpo no almacena la proteína como lo hace con la grasa (tejido adiposo) o glucosa (glucógeno), que son ambos fácilmente accesibles. Cualquier proteína ingerida, participa en el proceso necesario para mantener el volumen de proteínas, Por lo tanto, el cuerpo debe romper tejido funcional, músculo esquelético, para encontrar energía cuando el equilibrio del nitrógeno es negativo.

El Balance Nitrogenado (BN) depende de los siguientes factores: a) Cantidad de proteína ingerida en dieta b) Calidad de la proteína ingerida o Valor Biológico (VB), referida al contenido de aminoácidos esenciales c) Relación Energía/Nitrógeno de la dieta d) Caracteristicas individuales: edad, estado fisiológico y de salud, actividad y sexo

El kwashiorkor Es una forma de mal nutrición que produce una ingestión insuficiente y prolongada de proteínas, Síntomas: • Retraso de crecimiento • Apatía • Ulceras • Hepatomegalia • Diarrea • Descenso de de la masa y función del corazón y riñones. Puede tratarse con una alimentación con gran cantidad de proteínas : leche, huevos y carne (Soya)
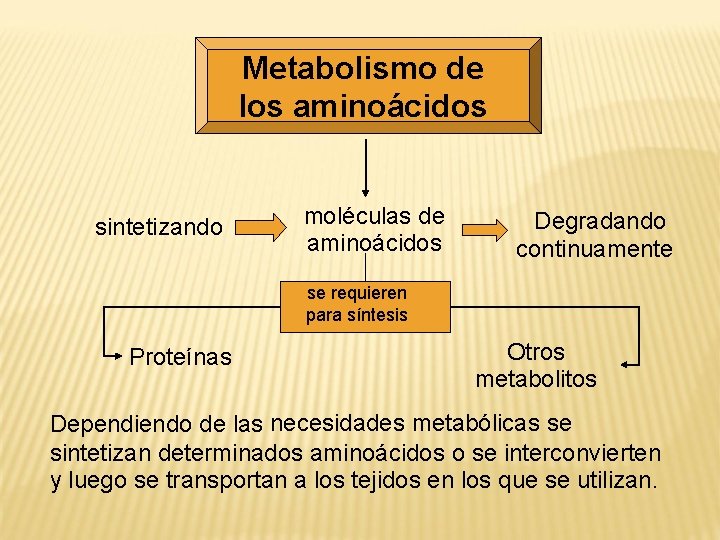
Metabolismo de los aminoácidos sintetizando moléculas de aminoácidos Degradando continuamente se requieren para síntesis Proteínas Otros metabolitos Dependiendo de las necesidades metabólicas se sintetizan determinados aminoácidos o se interconvierten y luego se transportan a los tejidos en los que se utilizan.
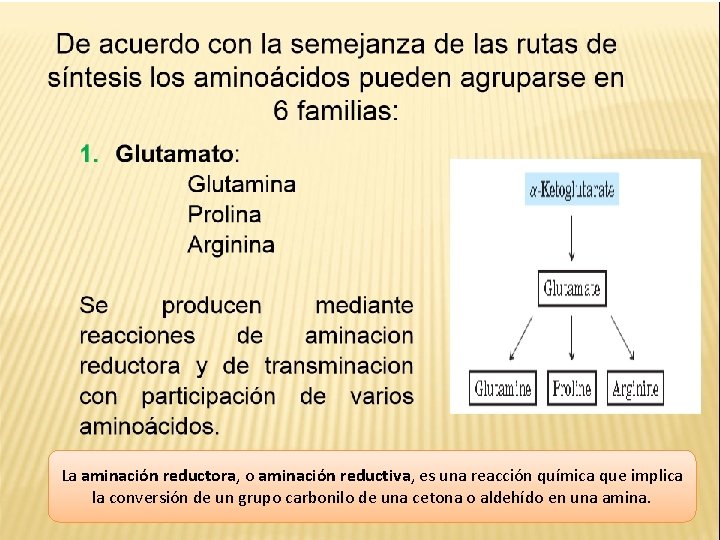
La aminación reductora, o aminación reductiva, es una reacción química que implica la conversión de un grupo carbonilo de una cetona o aldehído en una amina.
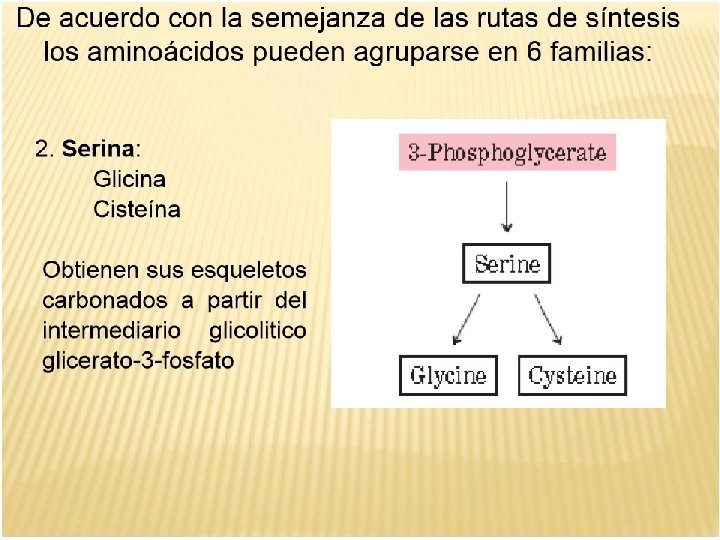
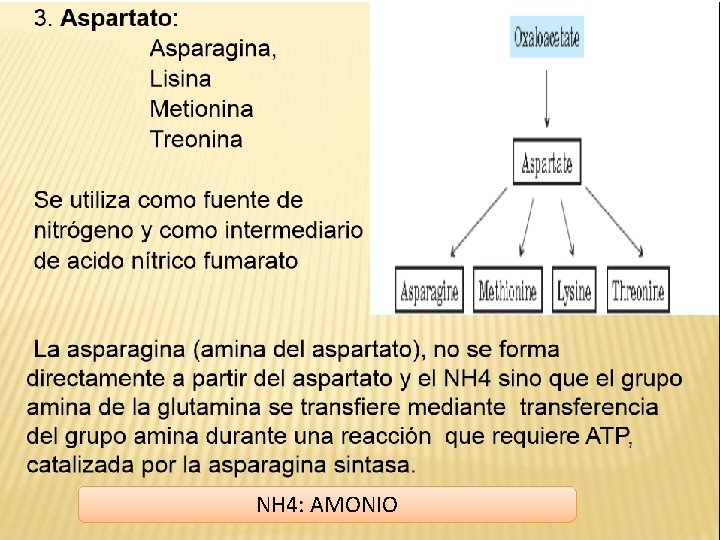
NH 4: AMONIO
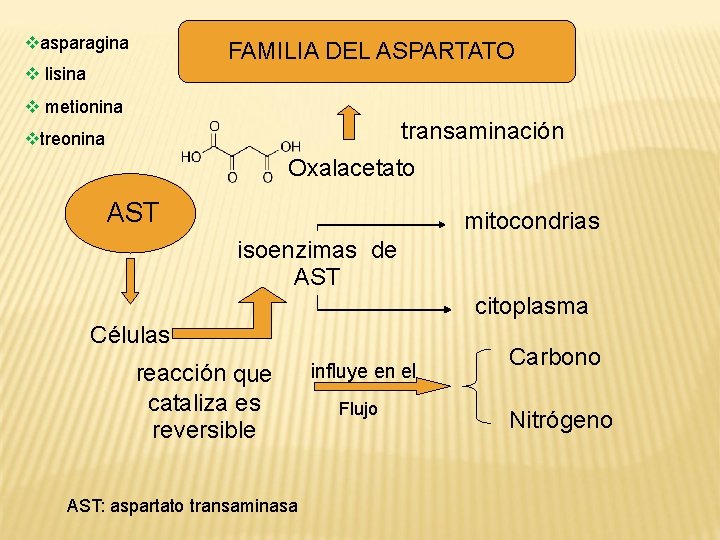
asparagina FAMILIA DEL ASPARTATO lisina metionina transaminación treonina Oxalacetato AST mitocondrias isoenzimas de AST citoplasma Células reacción que cataliza es reversible AST: aspartato transaminasa influye en el Flujo Carbono Nitrógeno

El ácido oxalacético o su forma ionizada, el oxalacetato, es un importante metabolito intermediario de varias rutas metabólicas; Ciclo de Krebs y la fotosíntesis C-4. Se puede sintetizar por dos reacciones: al pasar el piruvato a oxalacetato por carboxilación o de aspartato a oxalacetato por transaminación

nicotinamida adenina dinucleótido (abreviado NAD+) La nicotinamida adenina dinucleótido fosfato (abreviada NADP+
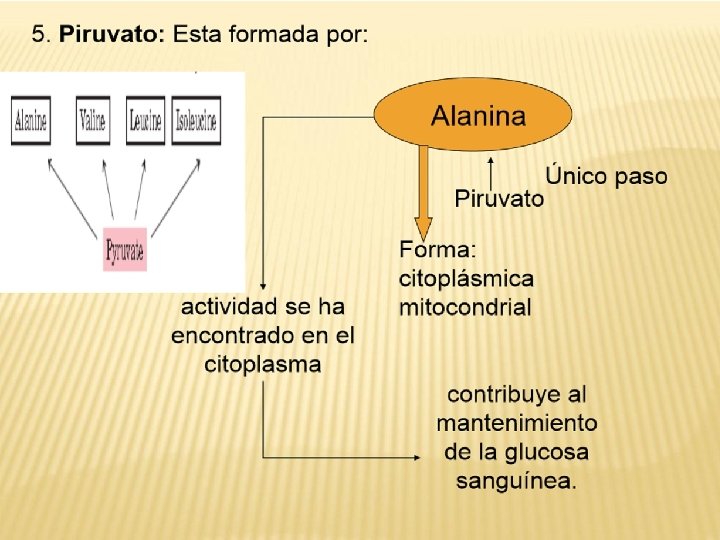
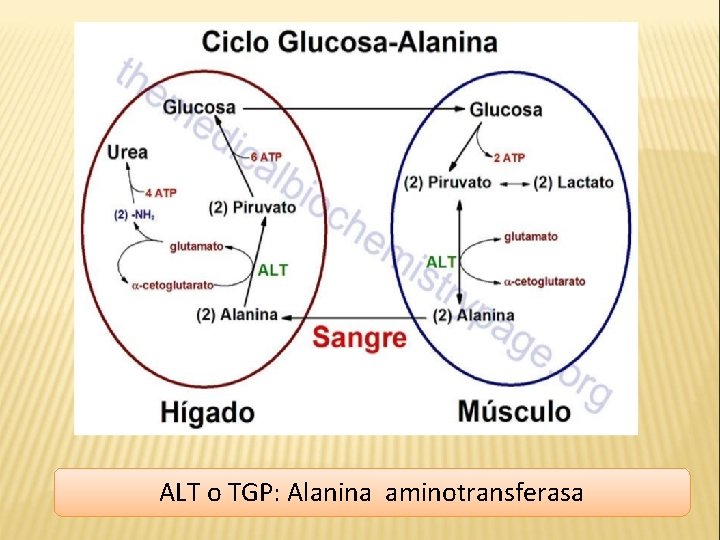
ALT o TGP: Alanina aminotransferasa


Regulación síntesis de aminoácidos Inhibición concertada (regulación alostérica): Más de un modulador, por retroalimentación negativa (generalmente los productos derivados del aa) con efectos aditivos Principal mecanismo: Retroalimentación negativa (inhibición de la 1º reacción por el producto final de la vía) • Generalmente la 1º reacción es irreversible • Catalizada por enzimas alostéricas

Moléculas derivadas de aminoácidos Precursores de: Porfirinas (glicina): Precursores del HEMO (Hb / Mb /Citocromos / Enzimas) Creatinina (lisina y arginina): Precursor de fosfocreatina, fosforilación a nivel de sustrato de ADP en músculo HEMO; HIERRO Los citocromos ; son proteínas que desempeñan una función vital en el transporte de energía química en todas las células vivas.

Moléculas derivadas de aminoácidos Precursores de: Glutatión (glicina, glutamato y cisteina): Amortiguador redox, mantiene los grupos sulfidrilos de las enzimas en estado reducido Oxido nítrico, mensajero biológico ( Arginina): Neurotransmisor, proceso de coagulación, control de la hipertensión sanguínea El termino redox representa procesos de reducción y oxidación que ocurren simultaneamente en soluciones acuosas

Moléculas derivadas de aminoácidos Precursores de: Aminas biológicas / Neurotransmisores: Tirosina: Catecolaminas: Dopamina, norepinefrina y epinefrina. Parkinson: baja producción dopamina Esquizofrenia: alta producción dopamina Glutamato: GABA (aminobutirato), neurotransmisor inhibitorio Episodios epilépticos: baja producción
CATABOLISMO Degradación Esqueletos carbonados (las partes no nitrogenadas). Eliminación del grupo AMINO Se elimina en la síntesis de urea
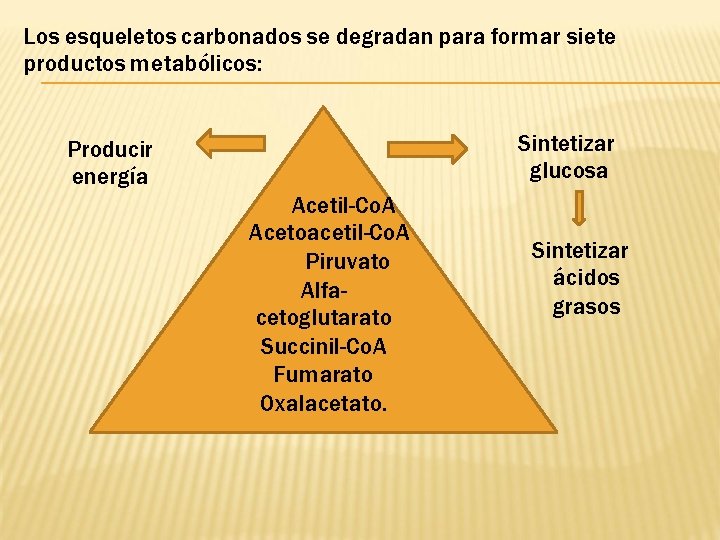
Los esqueletos carbonados se degradan para formar siete productos metabólicos: Sintetizar glucosa Producir energía Acetil-Co. A Acetoacetil-Co. A Piruvato Alfacetoglutarato Succinil-Co. A Fumarato Oxalacetato. Sintetizar ácidos grasos
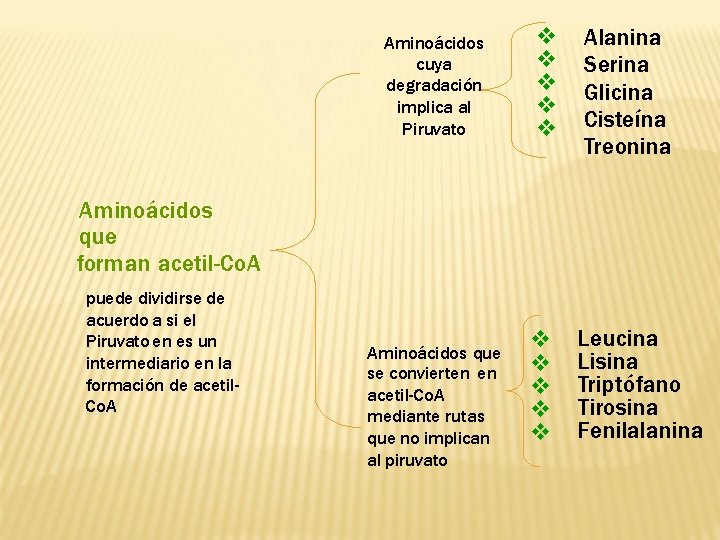
Aminoácidos cuya degradación implica al Piruvato Alanina Serina Glicina Cisteína Treonina Leucina Lisina Triptófano Tirosina Fenilalanina Aminoácidos que forman acetil-Co. A puede dividirse de acuerdo a si el Piruvato en es un intermediario en la formación de acetil. Co. A Aminoácidos que se convierten en acetil-Co. A mediante rutas que no implican al piruvato
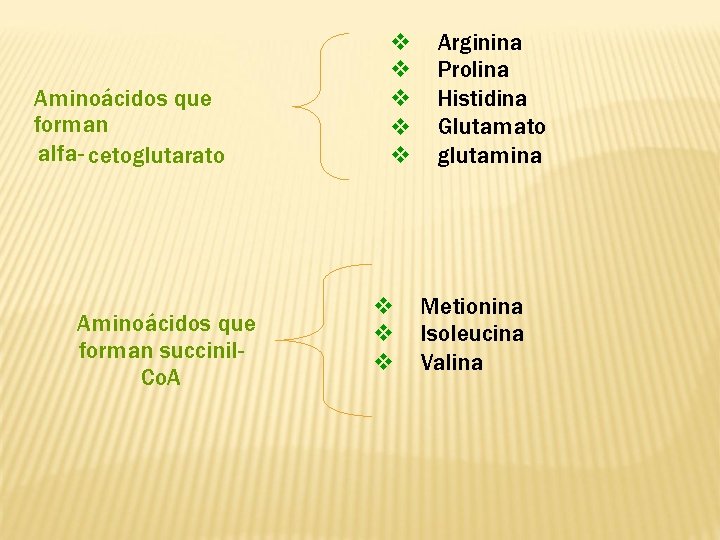
Aminoácidos que forman alfa- cetoglutarato Aminoácidos que forman succinil. Co. A Arginina Prolina Histidina Glutamato glutamina Metionina Isoleucina Valina
Aminoácidos que forman oxalacetato Aspartato Asparagina
Los aminoácidos que se degradan para formar acetil-Co. A o acetoacetil-Co. A se denominan cetogénicos, debido a que pueden convertirse en ácidos grasos o en cuerpos cetónicos. Los esqueletos carbonados de los aminoácidos glucogénicos, que se degradan a Piruvato o a un intermediario del acido cítrico, pueden utilizarse a continuación en la gluconeogénesis. Piruvato: Alanina, Serina, Eliminación del grupo amino Desaminación Glicina, Cisteína, Treonina. 2 reacciones Transaminación Transferencia del grupo amino a un ceto-ácido Desaminación oxidativa Ruptura de un grupo amino

UREA

Ureasa bacteriana Una fuente importante del amoniaco del hígado (aproximadamente el 25%) se produce por la acción de determinadas bacterias del intestino que contienen la enzima ureasa. La urea presente en la sangre circula a través de las membranas celulares dentro de la luz intestinal. Una vez hidrolizada la urea por la ureasa bacteriana para formar amoniaco, esta última sustancia difunde de vuelta a la sangre, que la transporta al hígado.

Ureasa bacteriana Bacterias patógenas productoras de Ureasa bacteriana 1. Helicobacter pylori. 2. Bacterias entéricas incluyendo Proteus, Klebsiella y Morganella. 3. Nocardia, una bacteria filamentosa. 4. Ureaplasma urealyticum, relacionada con Mycoplasma. 5. Cryptococcus, un hongo oportunista. 6. Coccidioides imitis, un hongo patogeno primario, ascomiceto. La ureasa (EC 3. 5. 1. 5) es una enzima que cataliza la hidrólisis de urea a dióxido de carbono y amoníaco.
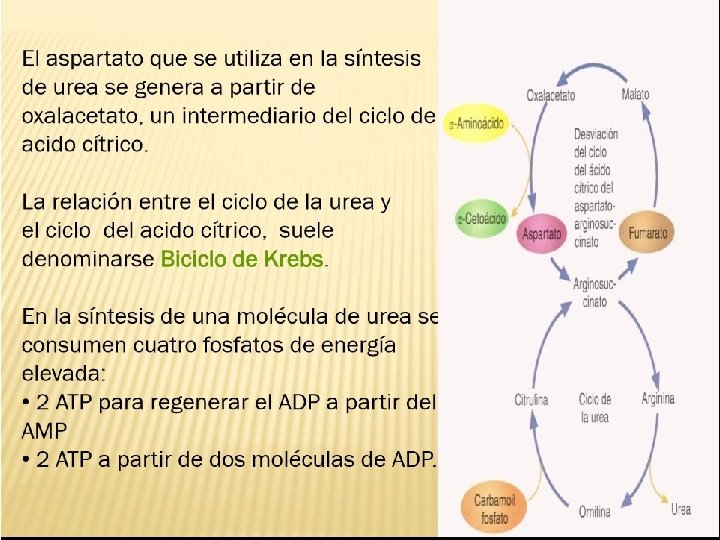
Ruta cíclica que se denomina ciclo de la urea. Formación de la urea Descubierto por: Hans Krebs y Kurt Henseleit AMONIACO UREA ASPARTAT O CO 2 El ciclo de la urea es un proceso metabólico en el cual se procesan los derivados proteicos y se genera urea como producto final.
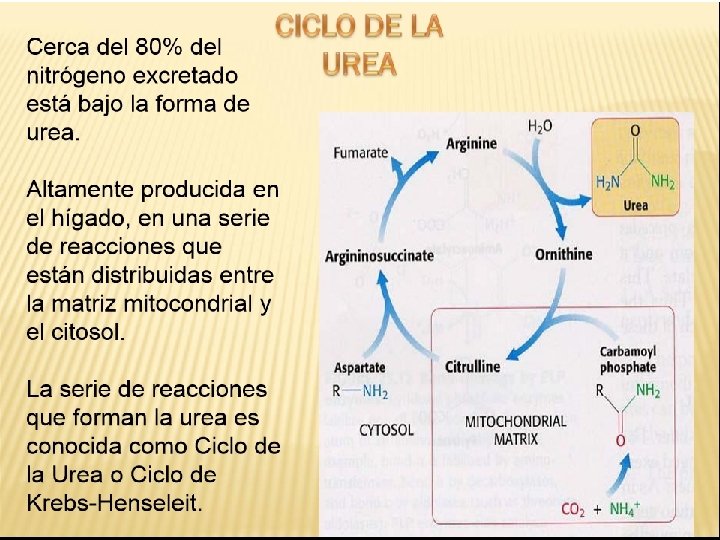
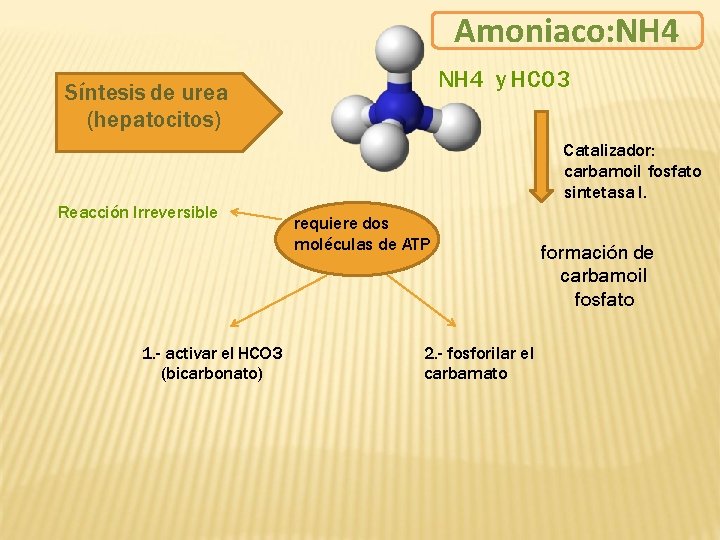
Amoniaco: NH 4 y HCO 3 Síntesis de urea (hepatocitos) Reacción Irreversible 1. - activar el HCO 3 (bicarbonato) Catalizador: carbamoil fosfato sintetasa I. requiere dos moléculas de ATP 2. - fosforilar el carbamato formación de carbamoil fosfato
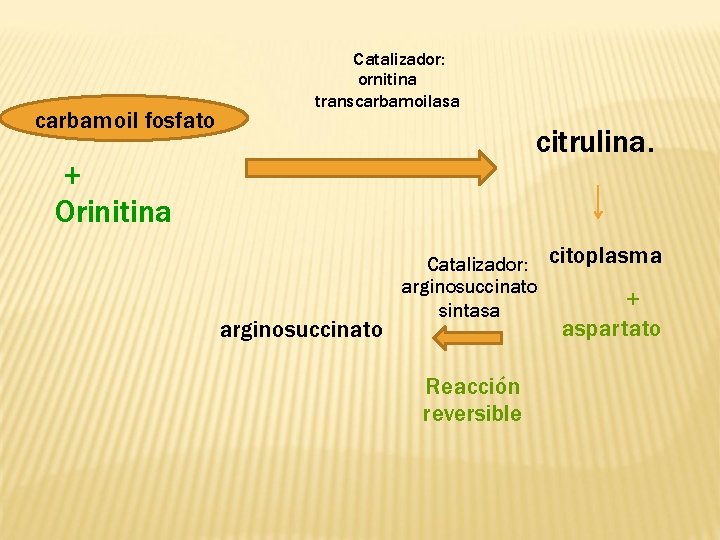
carbamoil fosfato Catalizador: ornitina transcarbamoilasa citrulina. + Orinitina arginosuccinato Catalizador: arginosuccinato sintasa Reacción reversible citoplasma + aspartato
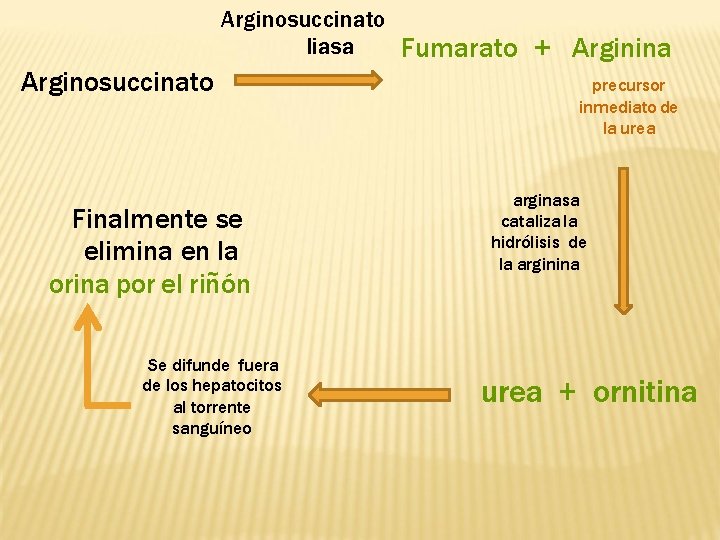
Arginosuccinato liasa Fumarato + Arginina Arginosuccinato Finalmente se elimina en la orina por el riñón Se difunde fuera de los hepatocitos al torrente sanguíneo precursor inmediato de la urea arginasa cataliza la hidrólisis de la arginina urea + ornitina
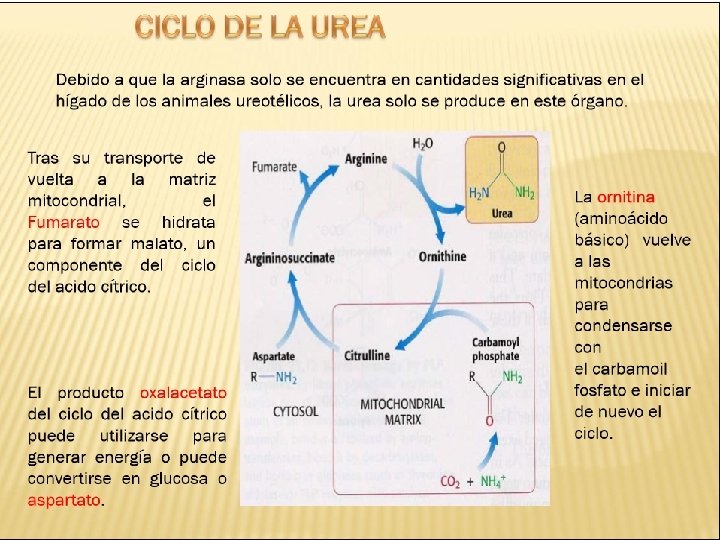

Regulación del ciclo de urea El ciclo de la urea funciona solo para eliminar el exceso de nitrógeno. En las dietas de alto contenido proteico los esqueletos de carbono de los aminoácidos son oxidados para energía o almacenados como grasa y glicógeno, pero el nitrógeno amino debe ser excretado.

Regulación del ciclo de urea Cuando las proteínas dietéticas aumentan significativamente, las concentraciones de las enzimas se elevan. De regreso a una dieta balanceada, los niveles de las enzimas decrecen. Bajo condiciones de inanición, los niveles de las enzimas se elevan mientras las proteínas son degradas y los esqueletos de carbono de los aminoácidos son usados para proporcionar energía, incrementando así la cantidad de nitrógeno que debe ser excretado.

Regulación del ciclo de urea La regulación a corto plazo: Carbamoil fosfato sintetasa (CPS-I, relativamente inactiva) Activadores alostéricos: • N-acetilglutamato. • arginina, la cual es un efector alostérico positivo de Nacetilglutamato sintasa.
- Slides: 55