METABOLISME PORFIRIN DAN SINTESIS HEME Ema Qurnianingsih dr

METABOLISME PORFIRIN DAN SINTESIS HEME Ema Qurnianingsih, dr. , M. Si
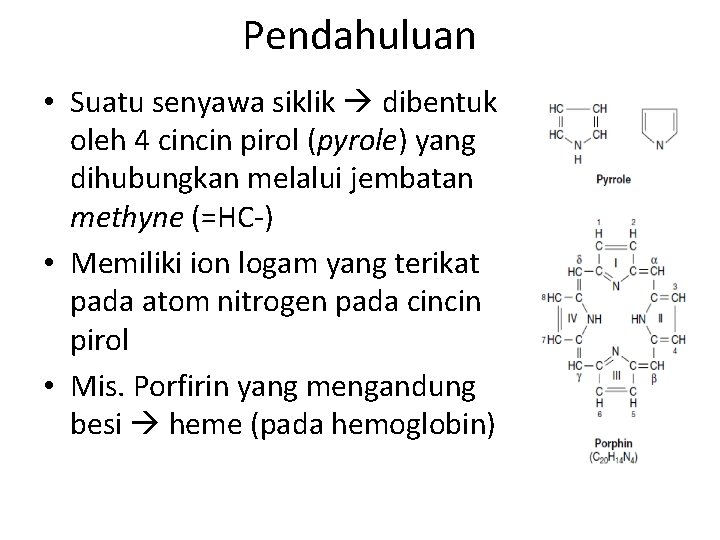
Pendahuluan • Suatu senyawa siklik dibentuk oleh 4 cincin pirol (pyrole) yang dihubungkan melalui jembatan methyne (=HC-) • Memiliki ion logam yang terikat pada atom nitrogen pada cincin pirol • Mis. Porfirin yang mengandung besi heme (pada hemoglobin)

SINTESIS HEME • Terjadi di banyak sel yang memiliki mitokondria, terutama : – sel 2 prekursor eritroid di sumsum tulang (kec. Eritrosit matur tdk punya mitokondria) : 85 % – Liver

• Tahapan reaksi : – Reaksi kondensasi antara suksinil Ko-A dan glisin (α-amino-ß-ketoadipat) dekarboksilasi α- aminolevulinat (ALA) • Suksinil ko-A berasal dari siklus asam sitrat • Memerlukan piridoksal fosfat mengaktifkan glisin • Enzim : ALA sintase
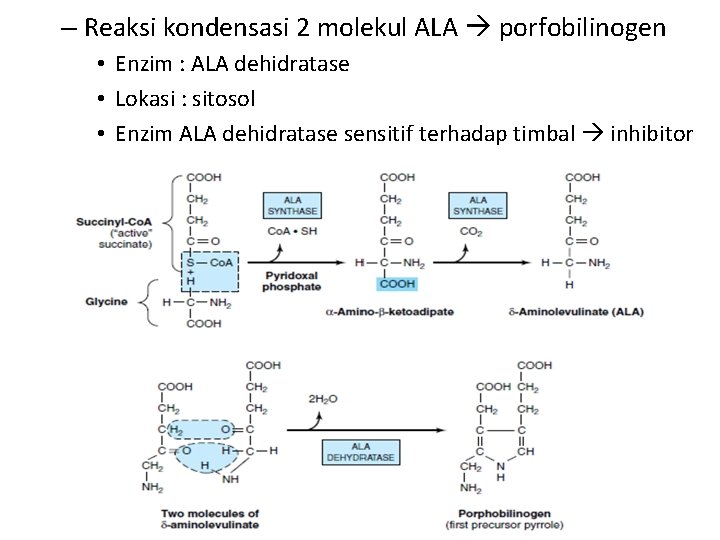
– Reaksi kondensasi 2 molekul ALA porfobilinogen • Enzim : ALA dehidratase • Lokasi : sitosol • Enzim ALA dehidratase sensitif terhadap timbal inhibitor

– Reaksi kondensasi 4 molekul porfobilinogen (PBG) hidroxymethylbilane (HMB) • Kondensasi dengan pola kepala berikatan dengan ekor linear tetrapyrole : hydroxymethylbilane • Enzim : uroporfirinogen I sintase = PBG deaminase = HMB sintase – HMB siklik • Spontan uroporfirinogen I • Dikatalisis enzim uroporfirinogen III sintase uroporfirinogen III (dalam kondisi normal mayoritas)

– Dekarboksilasi uroporfirinogen koproporfirinogen • Enzim : uroporfirinogen dekarboksilase • Dapat merubah uroporfirinogen I dan III • Koproporfirinogen III masuk mitokondria – Perubahan koproporfirinogen III protoporfirinogen III • Enzim : koproporfirinogen oksidase (hanya beraksi pada koproporfirinogen tipe III) • Proses : dekarboksilasi dan oksidasi

– Perubahan protoporfirinogen III protoporfirin III • Enzim : protoporfirinogen III oksidase – Inkorporasi ion besi pada protoporfirinogen III Heme • Enzim : ferrochelatase (heme sintase)
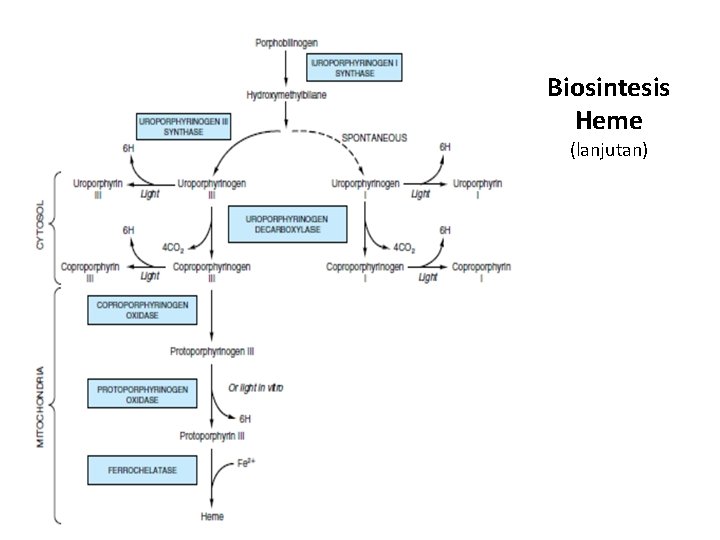
Biosintesis Heme (lanjutan)

• Lokasi enzim biosintesis Heme : – ALA sintase, koproporfirinogen oksidase, protoporfirinogen oksidase, ferrochelatase MITOKONDRIA – ALA dehidratase, uroporfirinogen I sintase, uroporfirinogen III sintase, uroporfirinogen dekarboksilase sitosol • Porfirinogen tdak berwarna • Porfirin berwarna

• ALA sintase (ALAS) : – Jenis ; • ALAS 1 di liver • ALAS 2 eritroid – Regulasi sintesis ALAS 1 di liver : • Meningkat (derepresi) bila kadar heme turun Penurunan kadar heme dapat dipicu oleh senyawa kimia asing (xenobiotics) mis. Obat 2 an, bahan tambahan dalam makanan, polutan o. k metabolismenya memerlukan sitokrom P 450 (hemoprotein) • Menurun (represi) pemberian glukosa, hematin

PORFIRIA • Suatu kelainan dikarenakan keabnormalan pada jalur biosintesis heme • Genetik atau didapat • Kelainan pada enzim biosintesis heme (kec. ALA sintase dan ALA dehidratase) • Gejala : – Nyeri perut – Gejala neurologis – Fotosensitif – Lab : ALA, PBG di urin meningkat

• Terapi : simtomatis • Edukasi : – Menghindari obat 2 an yang menginduksi sitokrom P 450 (mis. Barbiturat, griseofulvin) – Menghindari berbagai xenobiotics lainnya – Pemberian anti oksidan, mis. Beta karoten – Pamakaian tabir surya

KATABOLISME HEME • 1 -2 x 108 eritrosit dipecah/jam • Degradasi eritrosit hemoglobin heme dan globin • Globin asam amino sebagian besar digunakan kembali • Heme besi (digunakana kembali) dan porfirin (didegradasi)

DEGRADASI PORFIRIN • Terutama di liver, limpa dan sumsum tulang • Enzim : kompleks enzim heme oksigenase • Bilirubin yang terbentuk pada jaringan perifer dibawa ke liver melalui pembuluh darah dan terikat dengan albumin metabolisme lebih lanjut • Metabolisme bilirubin di liver, proses : – Pengambilan bilirubin oleh sel parenkim liver – Konjugasi bilirubin dengan glukoronat di retikulum endoplasma – Sekresi bilirubin terkonjugasi ke dalam empedu
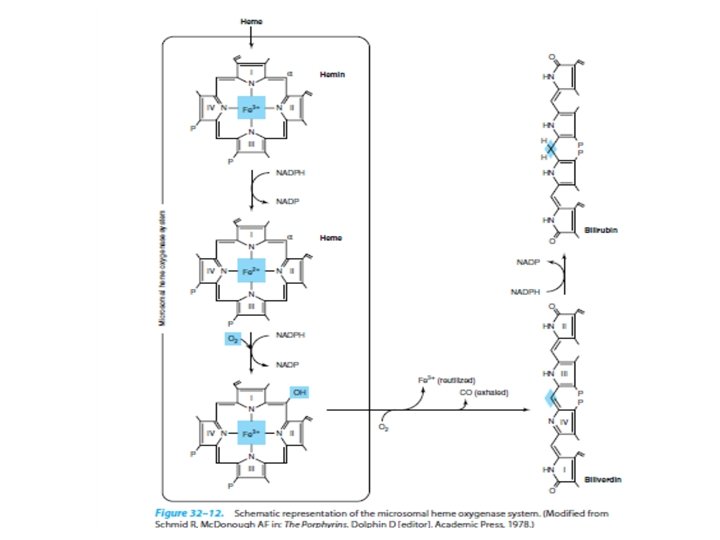

• Bilirubin yang belum terkonjugasi relatif tidak larut dalam plasma terikat dengan albumin meningkatkan kelarutan • Kadar bilirubin >> terikat secara ‘longgar’ dengan albumin lepas jaringan • Konjugasi bilirubin di liver : – Enzim : glucuronosyltransferase – Menggunakan UDP-glucuronic acid sebagai donor glucuronosyl bilirubin diglucuronide – Proses ini dapat diinduksi oleh fenobarbital

• Sekresi bilirubin terkonjugasi merupakan transport aktif empedu – Melibatkan protein transpor : MRP-2, MOAT – Dapat diinduksi oleh fenobarbital • Bilirubin terkonjugasi ileum & usus besar pelepasan glukoronat oleh enzim spesifik bakteri usus (ß-glucuronidase) reduksi pigmen oleh bakteri usus urobillinogen sebagian besar dioksidasi oleh bakteri usus ( urobilin berwarna), sebagian kecil diserap dan dire-ekskresikan ke liver (enterohepatic urobilinogen cycle)

HIPERBILIRUBINEMIA • Peningkatan kadar bilirubin dalam darah • Penyebab : 1. Produksi bilirubin >> : anemia hemolitik, neonatal “physiologic jaundice”, sindroma Crigler-Najjar pre hepatik 2. Kerusakan liver : oleh karena zat toksik/infeksi virus, mis. Chloroform, CCl 4, virus hepatitis, sirosis, dll hepatik 3. Obstruksi saluran empedu post hepatik No. 1 dan 2 bilirubin tak terkonjugasi >> No. 3 bilirubin terkonjugasi >> • Gejala : jaundice / ikterus

• Dalam keadaan normal : urobilinogen hampir tidak dijumpai di urin • Bilirubin tak terkonjugasi (larut lemak) dapat melewati blood brain barrier otak ensefalopati (Kernicterus) • Bilirubin terkonjugasi (larut air) >> kadar di urin >> • Bila ada obstruksi saluran empedu bilirubin tidak dapat dikeluarkan ke saluran cerna feses pucat

Skema Proses Katabolisme Bilirubin Beserta Beberapa Penyebab Jaundice

Terima Kasih
- Slides: 22