METABOLISME BACTERIEN I Introduction Le mtabolisme est lensemble

METABOLISME BACTERIEN

I- Introduction : Le métabolisme est l’ensemble des réactions biochimiques mises en jeu par un organisme vivant. Lorsque ces réactions sont convenablement équilibrées, elles permettent à l’organisme de croître et de se reproduire ; Lorsqu’elles sont dérégulées, elles provoquent sa mort. L’énergie produite au cours de ces réactions permet à la bactérie d’effectuer ; Ces biosynthèses (capsule, polyosides et protéines), le transport actif des ions et substances nutritives à travers l’enveloppe bactérienne, ou un travail mécanique (déplacement d’une bactérie flagellée). D’autre part l’étude du métabolisme présente un intérêt médical et permet : • De comprendre le mode de vie et l’habitat des diverses espèces dans la nature. • De connaître les meilleures conditions, pour obtenir en culture les bactéries pathogènes pour l’homme • Le diagnostic des espèces bactériennes. • De préciser certains aspects physiopathologiques de l’infection.

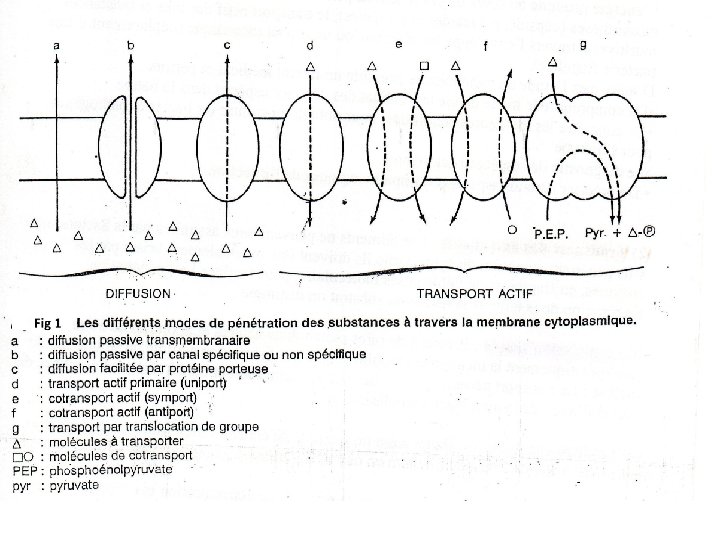
II- Transport des nutriments : Les aliments ne peuvent êtres assimilés par la bactérie que s’ils pénètrent au niveau du cytoplasme. Ils doivent être préalablement brisés par les enzymes, en fragments de faible poids moléculaire, pour faciliter leur pénétration. En fonction de la taille et la nature du substrat on distingue : 1. La diffusion simple : Permet à de rares métabolites neutres et apolaires de traverser non spécifiquement la membrane cytoplasmique, qui fonctionne comme un simple sac de dialyse : Le transport nécessite un gradient de concentration et tend à réaliser l’équilibre de part et d’autre de la membrane cytoplasmique. 2. La diffusion facilitée : Exige aussi un gradient de concentration, mais fonctionne plus vite que la diffusion simple. Elle met en œuvre des transporteurs stéréospécifiques.

3. LE transport actif : Est indépendant du gradient de concentration et nécessite de l’énergie, le substrat se concentre à grande vitesse (jusqu’à 100 fois) grâce à des enzymes qu’on appelle les perméases (qui sont spécifiques pour leurs substrats par exemple perméase du lactose). Ce type de transport est couple’ à des gradients ioniques ou électrochimiques, et comporte différents modèles : * Transport actif primaire ou uniport ; exemple (système ATPase K + membranaire qui permet la pénétration des ions K + à l’intérieur de la bactérie) * Transport active secondaire ou cotransport : Qui peut se faire dans le même sens du gradient ionique ( symport) , exemple ( transport du glucose couplé à un gradient de Na +) , ou dans le sens contraire du gradient ( antiport), par exemple transport de l’ion Ca++ contre un gradient de protons ( H+)

4. Transport par translocation de groupe : Dans ce dernier système, le transfert d’une substance à travers la membrane cytoplasmique s’accompagne d’une phosphorylation. Exemple Glucose +phosphoenolpyruvate → glucose 6 phosphate +pyruvate R-CH 2 OH + --OOC-C (CH 2)-O~PO 23 - →R-CH 2 -O-PO 2 -3 + CH 3 -CO-COOH

III. Source d’énergie: Selon la nature de la source primaire ; Deux voies principales s’offrent aux bactéries ; La phototrophie et la chimiotrophie. 1. La photosynthèse : C’est le processus par lequel les bactéries phototrophes tirent leur énergie, contrairement aux plantes il n’ya jamais de photolyse de l’eau et donc de libération O 2 2. Les réactions d’oxydations : C’est le processus par lequel les bactéries dites chimiotrophes ou chimio synthétiques tirent leur énergie. L’oxydation d’un substrat (A) organique ou inorganique peut être définie comme une perte d’electrons.

Oxydation: AH 2 Donneur d’e → A + 2 H + + 2 e produit oxydé Reduction: B + 2 H + + 2 e - → BH 2 Accepteur produit réduit Somme : AH 2 + B → A + BH 2 + Energie Au cours de ces réactions le transfert d’hydrogène ou des électrons , du substrat sur l’accepteur est réalisé par toute une série d’enzymes ( déshydrogénases et leurs coenzymes tels que FMN, FAD, NAD et NADP) qui forment une chaîne de transport électronique.
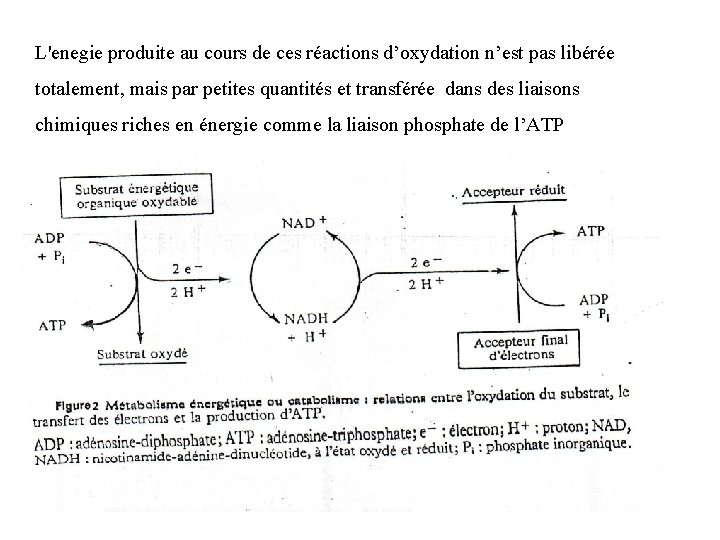
L'enegie produite au cours de ces réactions d’oxydation n’est pas libérée totalement, mais par petites quantités et transférée dans des liaisons chimiques riches en énergie comme la liaison phosphate de l’ATP

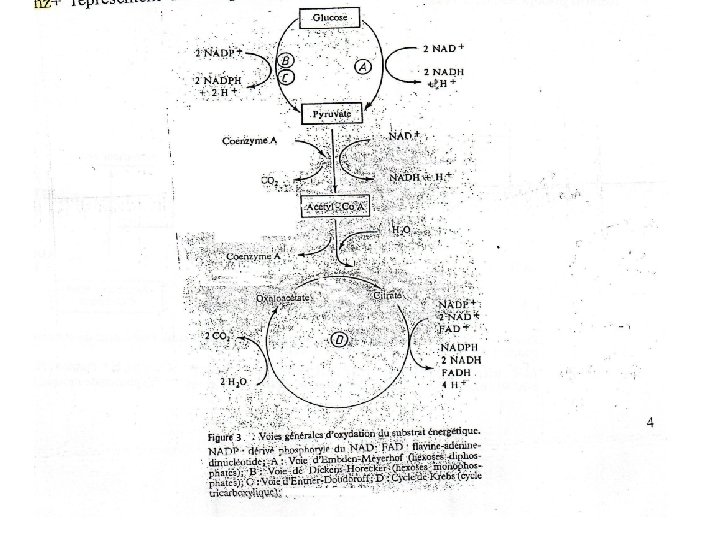
IV-Oxydation du glucose : Le glucose est considéré comme le substrat énergétique le plus universel. Au cours de la première partie des réactions catabolique qui se déroulent dans le cytoplasme, le glucose est oxydé en pyruvate. C 6 H 12 O 6 + 2 NAD + → 2 CH 3 -CO-COOH + 2 NADH + 2 H + Le pyruvate constitue une véritable plaque tournante du métabolisme et peut être obtenu par trois voies importantes : - Voie d’Embden-Meyerhof ou voie des hexoses-diphosphates. - Voie des hexoses -monophosphates ou cycle de Dickens- Horecker. Voie du 2 - ceto-3 desoxy-gluconate ou voie d’Entner- doudoroff.

Chez la plupart des bactéries aérobies, le processus d’oxydation du glucose peut se compléter par le jeu des enzymes du cycle tricarboxylique ou cycle de Krebs, qui permettent l’oxydation complète du pyruvate en gaz carbonique. CH 3 -CO-COOH + 5 Coenz + + 3 H 2 O → 3 CO 2 +5 COenz H + 5 H + Les 5 COenz+ représentent les cinq molécules oxydées (3 NAD +, 1 NADP + et 1 FAD +)

V- Réduction de l’accepteur final d’électrons : Selon la nature des transporteurs d’électrons et de l’accepteur final, on parle de : 1. Respiration aérobie : Lorsque l’accepteur final d’électrons est l’oxygène moléculaire. 2. Respiration anaérobie : Lorsque l’accepteur final d’electrons est un composé inorganique oxygéné (nitrate, sulfate ou carbonate) 3 -Fermentation : Quant l’accepteur final d’électrons est un composé organique.

VI- Respiration aérobie : Par définition, une respiration aérobie est une consommation d » oxygène moléculaire. Elle correspond à une série de transferts d’électrons jusqu'à un accepteur final qui est l’oxygène moléculaire et à une synthèse concomitante de molécules d’ATP ; L’ensemble de ces réactions couplées d’oxydo-reductions et de phosphorylation est désigné sous le nom de phosphorylation oxydative.
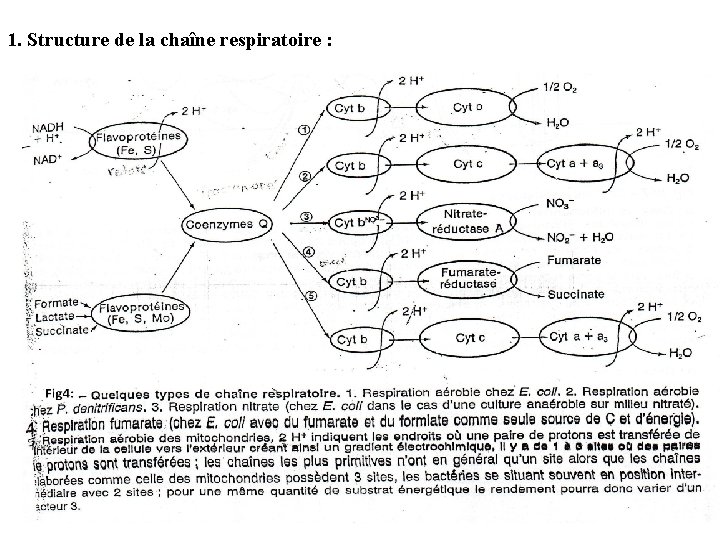
1. Structure de la chaîne respiratoire :

2. Fonctionnement de la chaîne respiratoire :
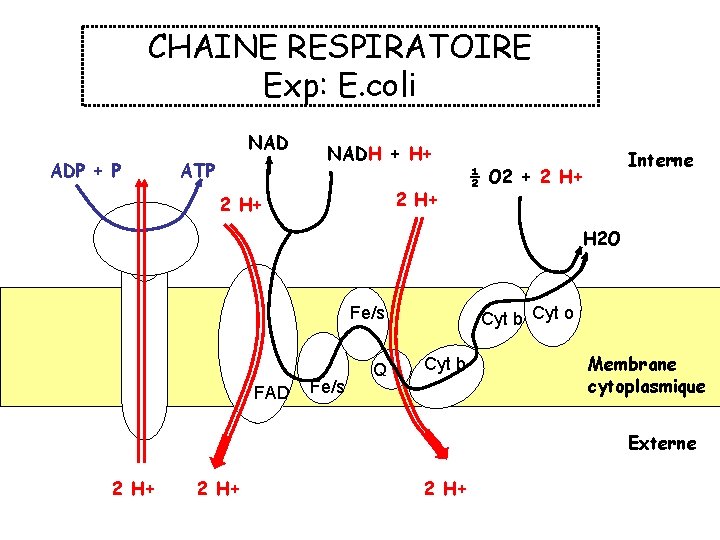
CHAINE RESPIRATOIRE Exp: E. coli NAD ADP + P ATP NADH + H+ 2 H+ Interne ½ O 2 + 2 H+ H 2 O Fe/s FAD Fe/s Q Cyt b Cyt o Cyt b Membrane cytoplasmique Externe 2 H+

3. Transfert des électrons et des protons : L’oxydation complète du glucose par voie aérobie du cycle de Krebs correspond à la réaction suivante C 6 H 1206 + 6 H 20 +12 NAD + → 6 CO 2 + 12 NADH +12 H + La chaîne respiratoire intervient pour réoxyder les coenzymes réduits (NADH) 12 NADH +12 H + + 6 CO 2 → 12 NAD + + 12 H 2 O La somme de ces deux réactions est : C 6 H 12 O 6 + 6 CO 2 → 6 CO 2 + 6 H 2 O

A u début de la chaîne respiratoire , les équivalents réducteurs ( H +) sont apportés par un transporteur soluble en général le NADH , celui- ci va transférer deux électrons et deux proton à Flavine-Adenine- Dinucleotide et va ainsi se réoxyder FAD + 2 e - + 2 H + → FADH 2 La FADH 2 est capable de découpler ces éléments ; elle éjecte les 2 H + dans l’espace périplasmique et transfert les 2 électrons vers l’espace via une protéine redox (protéine Fe/ S). Dans le deuxième segment de la chaîne , le COQ joue le rôle de transporteur navette entre les protéines redox réduites et les cytochromes oxydés situés à la surface externe de la membrane, il va capter les deux électrons issus des transporteurs précédents et en prélevant deux nouveau protons dans le cytoplasme. COQ + 2 e - + 2 H + → COQ H 2

Le COQ H 2 va à son tour découpler les protons et les électrons : les 2 H + excrétés dans le periplasme et les 2 e – sont transférés au premier cytochrome de la chaîne, lequel va les transférés à son tour à une série de cytochromes, le dernier cytochrome ( cytochrome oxydase ) ramène l’électron vers l’interface cytoplasmique et le transfert à l’oxygène. 1/2 O 2 + 2 e - + 2 H + → H 2 O

4. Phosphorylations oxydatives : La membrane cytoplasmique est associée à des ATPases qui comportent une partie incluse dans la membrane et une partie volumineuse faisant saillie vers l’intérieur de la bactérie. L’ATPase effectue spécifiquement la synthèse de l’ATP ADP + Pi + 2 H + → ATP + H 2 O Le passage transmembranaire des protons qui accompagne le flux des électrons le long de la chaîne , produit un gradient de protons à travers la membrane ( concentration cytoplasmique basse et concentration periplasmique élevée). La synthèse de l’ATP est due au passage des H + dans un canal ionique ménagé dans les ATPase , dans le sens contraire du gradient (entrée des protons dans la bactérie).

VII- Respiration anaérobie : En absence d’oxygène, les bactéries peuvent obtenir leur énergie par respiration anaérobie. C’est un processus cytochro-dependant, dont l’accepteur final d’électron est en général un composé inorganique. 1. respiration des nitrates. Lorsqu’une souche d’E/Coli est cultivée en anaérobiose en présence de nitrate, avec du lactate (composé non fermentescible) comme substrat énergétique, la synthèse de deux protéines est induite : Un cytochrome (CYT b ) et une enzyme, la nitrate réductase, cette dernière qui réduit les nitrates et les chlorates est désignée sous le nom de nitrate réductase de type A ou NAR (A), elle catalyse la réaction suivante. NO 3 + NADH + H → NO 2 +NAD + H 20

Cette réaction est une réduction dissimilatrice ou (respiration des nitrates) car les nitrites qui s’accumulent dans le milieu sont toxiques et donc non assimilés par la bactérie. Avec d’autres bactéries comme le Pseudomonas aeroginosa, d’autres enzymes membranaires autre que la NAR (A) sont induites lors de la respiration anaérobie des nitrates, qui permettent une réduction des nitrates au stade azote. 2 HNO 2 → (HOH=NOH) → NO 2 → N 2 Cette réaction dite de dénitrification est également dissimilatrice parce que le N 2 n’est pas assimilé par la bactérie, cependant ils existe de nombreuses bactéries capables d’assimiler l’azote du nitrate en le réduisant totalement, en aérobiose ou en anaérobiose, jusqu'à l’ammoniac, ces bactéries possèdent une nitrate réductase cytoplasmique (NAR B), qui à une activité assimilatrice et non productrice d’énergie. HNO 2 → ½ (HOH =NOH) → NH 2 OH → NH 3

VIII-Fermentation: C’est un processus d’oxydo-reduction, mais les accepteurs finaux d’électrons sont des composés organiques. Il libère de l’énergie, mais à moins degré que la respiration, les produits terminaux d’une fermentation sont très variés et peuvent caractériser certains groupes taxonomiques. 1. Fermentation alcoolique ; Ce type de fermentation est caractéristique de quelques levures comme les Saccharomyces cerevisiae. Il est à la base de la fabrication du vin, la bière et du pain.

2. Fermentation homolactique : Est réalisée par les Streptococcus, de nombreux Lactobacillus et certains Bacillus et moisissures. Elle est à la base de production du yaourt et du fromage, le produit final de cette fermentation est de l’acide lactique. 3. Fermentation heterolactique : Caracteristique de certains Lactobacillus et de Leuconostoc, les produits finaux sont de l’acide lactique, éthanol et du CO 2. 4. Fermentation acide mixte : Est effectuée par un grand nombre d’entérobactéries dites VP négative, les produits finaux de cette fermentation sont : lactate, acétate, éthanol et formate. Chez les bactéries gazogènes comme E. coli qui possèdent la formate-hydrogenelyase , qui scinde l’acide formique en CO 2 et H 2 ( H-COOH → CO 2+H 2) ; les produits finaux sont dans ce cas ; Lactate , acétate , éthanol, CO 2, H 2 et du succinate. Le PH du milieu reste bas en raison de la prédominance des acides de fermentation.
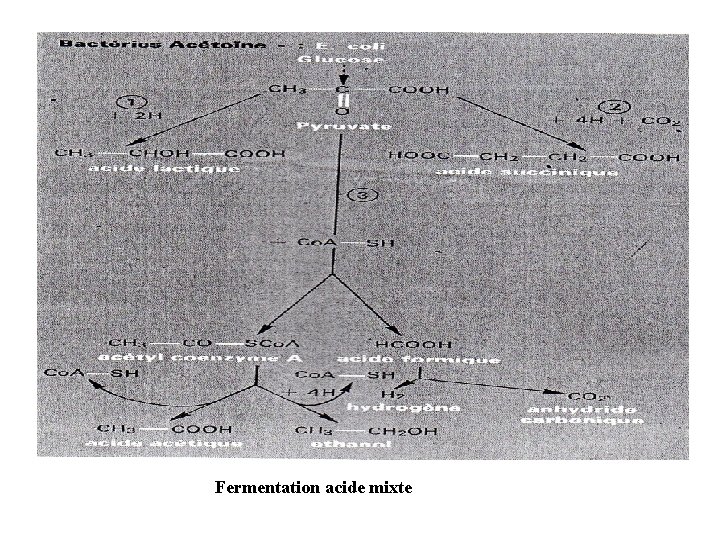
Fermentation acide mixte

5. Fermentation butanediolique : Est spécifiques à certaines bactéries (Klebsiella, Enterobacter et Serratia), la plupart des Vibrio et Aeromonas et quelques espèces de Bacillus. Ces bactéries possèdent une autre voie fermentaire dite butanediolique ou butyleneglycolique, qui donne un produit neutre le 2, 3 -butanediol, comme produit final, cette voie se met en jeu lorsque le PH du milieu est au dessus de 6 environ.
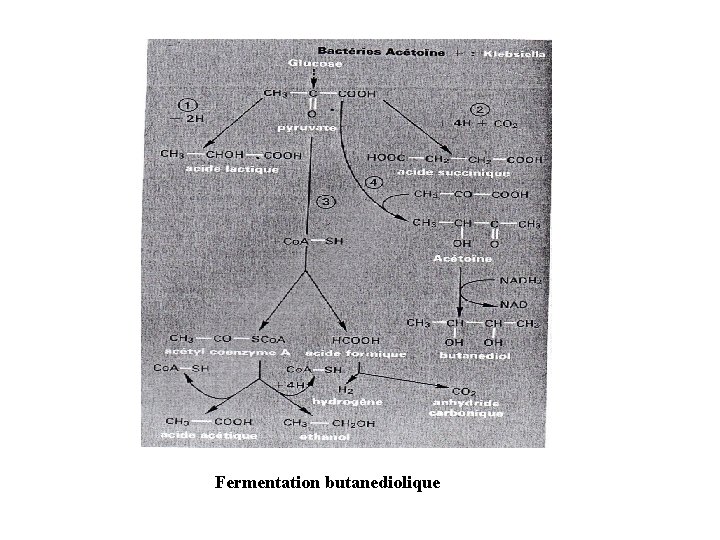
Fermentation butanediolique

6. Fermentation butyrique : Est réalisée par certaines clostridies dites saccharolytiques, les produits finaux sont : Acétate, butyrate, H 2 et CO 2

IX- Quelques applications au laboratoire (métabolisme) 1. Types respiratoires : Cette épreuve permet de définir le type respiratoire d’une bactérie, on utilise au laboratoire le milieu VF ( viande , foie), qui est régénéré et coulé en tube profond. Apres ensemencement des tubes et incubation à 37°c pendan 24 heures on a les résultats suivants : * Bactéries aérobies strictes poussent uniquement en surface du tube. * Bactéries aero-anaerobies facultatives poussent sur toute l’hauteur du tube. *Bactéries anaérobies strictes poussent au fond du tube. *Bactéries microaerophiles poussent à quelques millimètres de la surface
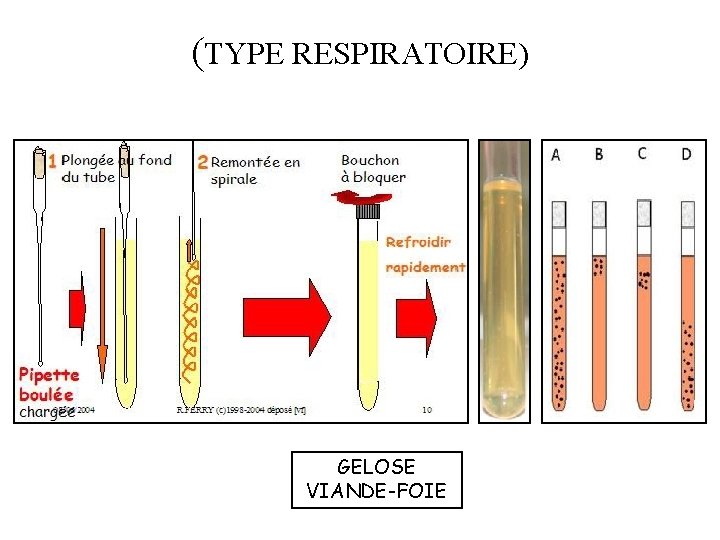
(TYPE RESPIRATOIRE) GELOSE VIANDE-FOIE


2. Mise en évidence du métabolisme fermentatif: Dans cette épreuve, on utilise soit le milieu MEVAG (milieu d’étude de la voie d’attaque des glucides), soit le milieu de Hugh et Leifson. Pour chaque épreuve on utilise deux tubes, l’un dit « ouvert » est fermé non hermétiquement ; L’autre dit « fermé » est recouvert d’une couche d’huile de vaseline (pour avoir l’anaérobiose), après incubation de 24 heures on observe : * Bactéries fermentantes → acidification (couleur jaune) des deux tubes. *Bactéries dépourvues de métabolisme fermentatif →pas de croissance dans le tube fermé (pas de virage au jaune) et une croissance avec ou non acidification dans le tube ouvert. ----→ Les bactéries fermentatives sont toutes anaérobies (strictes ou aerotolérantes). ----→Les bactéries dépourvues de métabolisme fermentatif sont toutes aérobies strictes Ou micro aérophiles. Si elles produisent une acidification en aérobiose, elles sont dites Oxydatives ; Sinon elles sont dites inactives ou non acidifiantes.
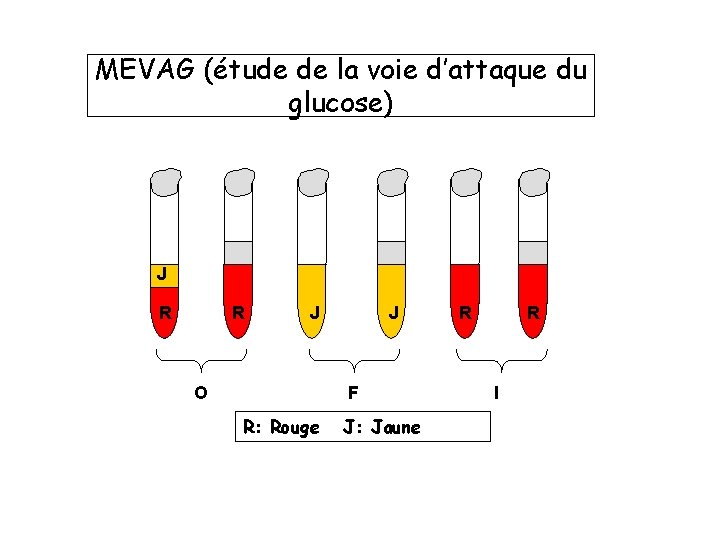
MEVAG (étude de la voie d’attaque du glucose) J R R J O J F R: Rouge J: Jaune R R I

MILIEU M. E. V. A. G MILIEU DE HUGH ET LEIFSON

3. Réaction de l’oxydase : Elle permet de mettre en évidence l’existence d’une chaîne respiratoire et comportant le cytochrome c, ce dernier à un potentiel redox identique à celui du TMPD (tétra- méthyle- paraphenylene diamine). Au contact des bactéries exerçant leur métabolisme, le TMPD s’oxyde en donnant une couleur rose carmin, * Les bactéries aérobies strictes et microaerophiles sont oxydase positive sauf Stenotrophomonas maltophilia et Acinetobacter. * Les bactéries aero-anaerobies facultatives sont oxydase négative sauf Vibrio et Aeromonas. * Les bactéries anaérobies (strictes ou aerotoletantes) sont oxydase négative.

OXYDASE + -

Ø La catalase : En présence d’H 2 O 2 la catalase donne : H 2 O+ ½ O 2 H 2 O 2 Catalase (+) (La pluparts des bactéries aérobies et aeroanaérobies)

4. Réaction RM (rouge de méthyle) met en évidence les fermentations acides (fermentation acide mixte) • Réaction RM positive = couleur rouge (PH < 4, 2) • Réaction RM négative = couleur jaune (PH> 6, 2) Exemple de bactéries RM positive : E. Coli, Salmonella, Shigella, Proteus positif négatif

5. Réaction V p (Voges – Prosckauer) met en évidence la voie butanediolique • Réaction VP positive = couleur rose Exemple de bactéries VP positive : (Klebsiella, Enterobacter et Serratia), Rq Si une bactérie est VP négative elle est obligatoirement RM positive et vice versa. positif négatif

Nitrate réductase : N. réductase Culture bactérienne en bouillon nitraté Nitrites (NO 2 -) (révélées par le réactif de Griess: Acide Sulfanilique et alpha-naphtylamine) ü Réaction (+) : couleur rouge. ü Réaction (-) : 2 éventualités : § Bactérie ne possède pas de Nitrate réductase. § Nitrites réduites à un stade avancé : ajouter la poudre de Zinc (réduit les nitrates en nitrites) : Couleur rouge (réaction -): pas de N. réductase. § Pas de couleur rouge (réaction +) nitrates réduites au stade azote.

Test de GRIESS –ILOSWAY

RECHERCHE DE NITRATE REDUCTASE - + Bouillon Nitraté + Milieu Mannitol. Mobilité
- Slides: 43