Metabolisma pamatprincipi Enzmi 4 lekcija Metabolisms nas misko

Metabolisma pamatprincipi Enzīmi 4. lekcija

Metabolisms = Šūnas ķīmisko reakciju kopums No grieķu valodas μεταβολή (metabole), «mainīt» Vielu aprite - makromolekulu, to sastāvdaļu un citu šūnas vielu biosintēze un noārdīšanās Enerģijas aprite – ķīmiskās enerģijas ieguve un izmantošana šūnas dzīvības norisēm Informācijas aprite – iedzimtības informācijas izmantošana, saglabāšana un pārraide
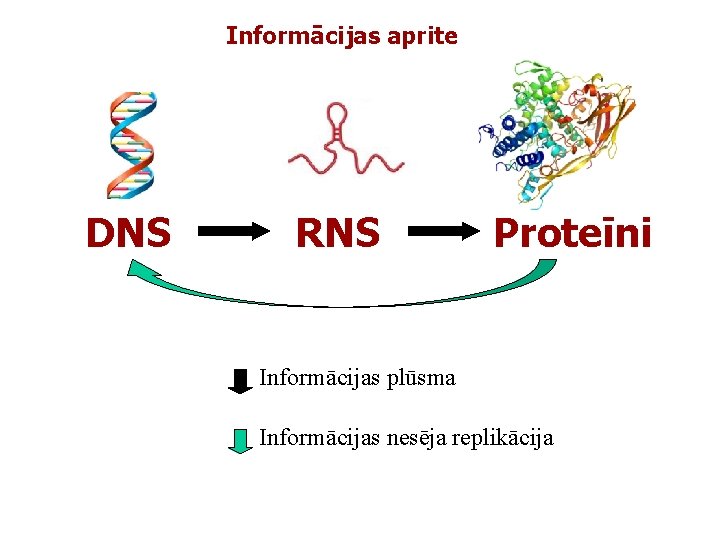
Informācijas aprite DNS RNS Proteīni Informācijas plūsma Informācijas nesēja replikācija

Metabolisms Katabolisms Anabolisms -Organisko vielu noārdīšana, lai iegūtu enerģiju un materiālu citu vielu sintēzei -Organisko savienojumu sintēze, izmantojot enerģiju
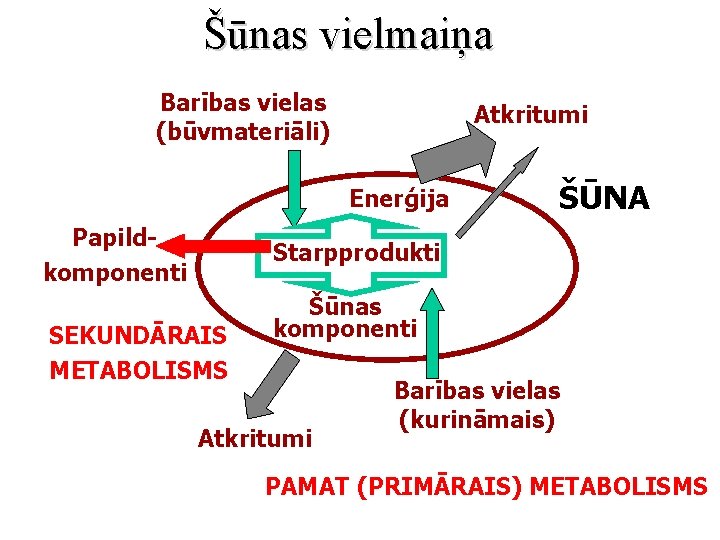
Šūnas vielmaiņa Barības vielas (būvmateriāli) Atkritumi Enerģija Papildkomponenti ŠŪNA Starpprodukti SEKUNDĀRAIS METABOLISMS Šūnas komponenti Atkritumi Barības vielas (kurināmais) PAMAT (PRIMĀRAIS) METABOLISMS

Primārais un sekundārais metabolisms • Primārais metabolisms – reakciju kopums, kurš ir absolūti nepieciešams organisma dzīvotspējai • Sekundārais metabolisms – reakciju kopums, kurš organismam ir noderīgs noteiktos apstākļos – piem. antibiotiķu un alkaloīdu sintēze
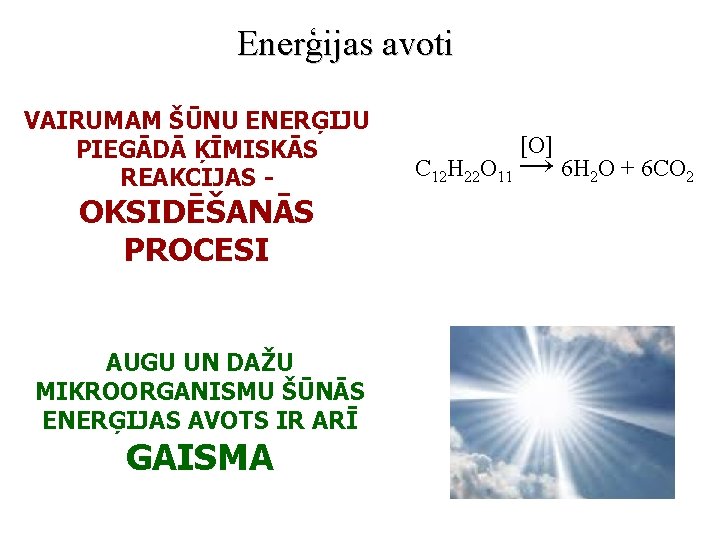
Enerģijas avoti VAIRUMAM ŠŪNU ENERĢIJU PIEGĀDĀ ĶĪMISKĀS REAKCIJAS - OKSIDĒŠANĀS PROCESI AUGU UN DAŽU MIKROORGANISMU ŠŪNĀS ENERĢIJAS AVOTS IR ARĪ GAISMA [O] C 12 H 22 O 11 → 6 H 2 O + 6 CO 2
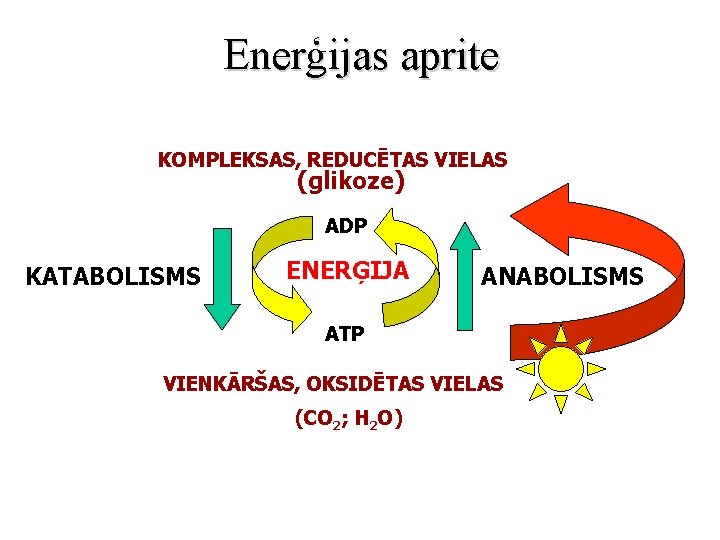
Enerģijas aprite KOMPLEKSAS, REDUCĒTAS VIELAS (glikoze) ADP KATABOLISMS ENERĢIJA ANABOLISMS ATP VIENKĀRŠAS, OKSIDĒTAS VIELAS (CO 2; H 2 O)
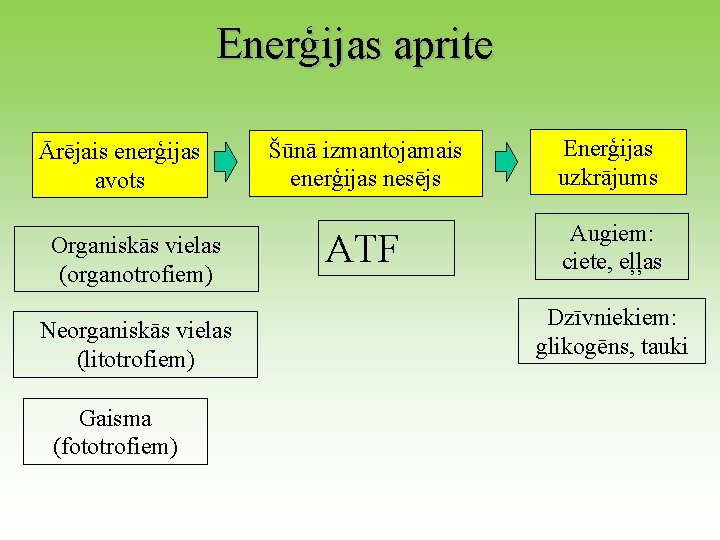
Enerģijas aprite Ārējais enerģijas avots Organiskās vielas (organotrofiem) Neorganiskās vielas (litotrofiem) Gaisma (fototrofiem) Šūnā izmantojamais enerģijas nesējs Enerģijas uzkrājums ATF Augiem: ciete, eļļas Dzīvniekiem: glikogēns, tauki
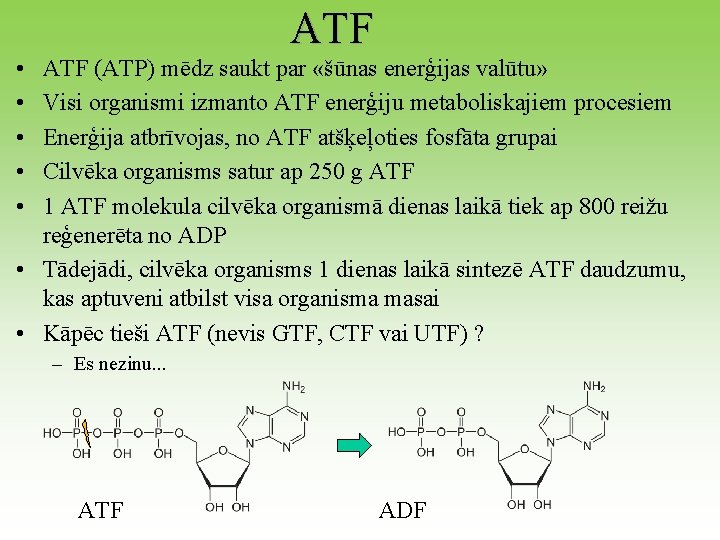
ATF • • • ATF (ATP) mēdz saukt par «šūnas enerģijas valūtu» Visi organismi izmanto ATF enerģiju metaboliskajiem procesiem Enerģija atbrīvojas, no ATF atšķeļoties fosfāta grupai Cilvēka organisms satur ap 250 g ATF 1 ATF molekula cilvēka organismā dienas laikā tiek ap 800 reižu reģenerēta no ADP • Tādejādi, cilvēka organisms 1 dienas laikā sintezē ATF daudzumu, kas aptuveni atbilst visa organisma masai • Kāpēc tieši ATF (nevis GTF, CTF vai UTF) ? – Es nezinu. . . ATF ADF
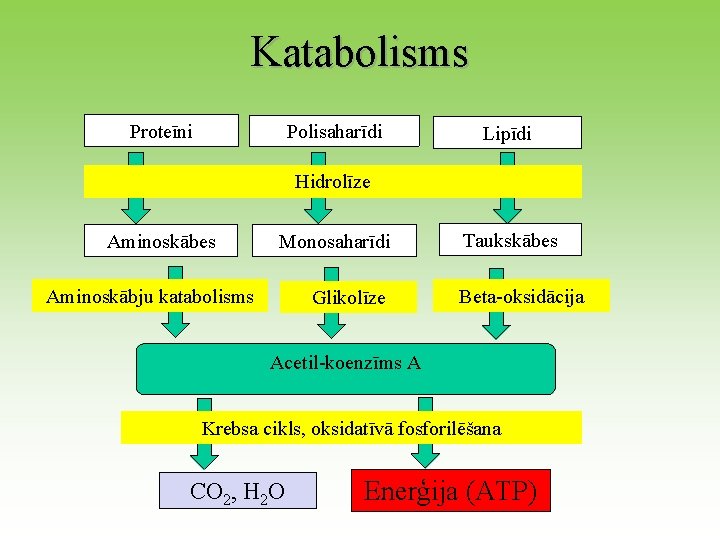
Katabolisms Proteīni Polisaharīdi Lipīdi Hidrolīze Aminoskābes Monosaharīdi Aminoskābju katabolisms Glikolīze Taukskābes Beta-oksidācija Acetil-koenzīms A Krebsa cikls, oksidatīvā fosforilēšana CO 2, H 2 O Enerģija (ATP)
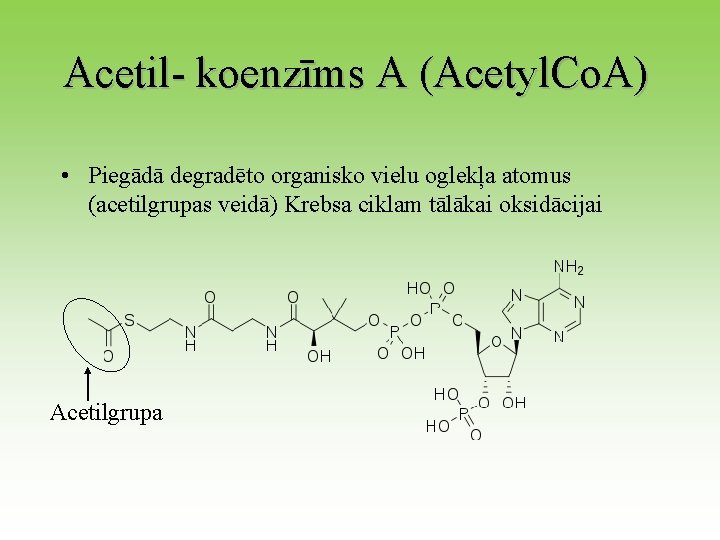
Acetil- koenzīms A (Acetyl. Co. A) • Piegādā degradēto organisko vielu oglekļa atomus (acetilgrupas veidā) Krebsa ciklam tālākai oksidācijai Acetilgrupa
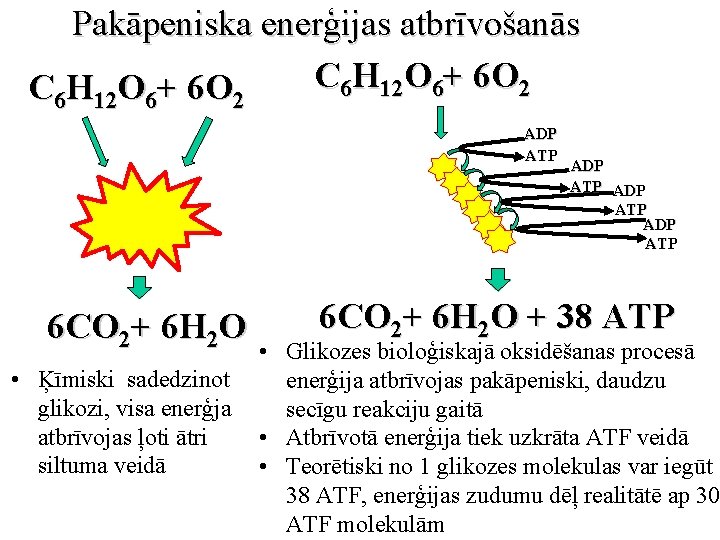
Pakāpeniska enerģijas atbrīvošanās C 6 H 12 O 6+ 6 O 2 ADP ATP 6 CO 2+ 6 H 2 O ADP ATP 6 CO 2+ 6 H 2 O + 38 ATP • Glikozes bioloģiskajā oksidēšanas procesā • Ķīmiski sadedzinot enerģija atbrīvojas pakāpeniski, daudzu glikozi, visa enerģja secīgu reakciju gaitā atbrīvojas ļoti ātri • Atbrīvotā enerģija tiek uzkrāta ATF veidā siltuma veidā • Teorētiski no 1 glikozes molekulas var iegūt 38 ATF, enerģijas zudumu dēļ realitātē ap 30 ATF molekulām

Metabolisma ceļi • Saistītas metabolisma reakcijas veido metabolisma ceļus • Metabolisma ceļi var būt: – Lineāri – Sazaroti • Konverģenti (parasti - katabolismā) • Diverģenti (parasti – anabolismā) – Cikliski
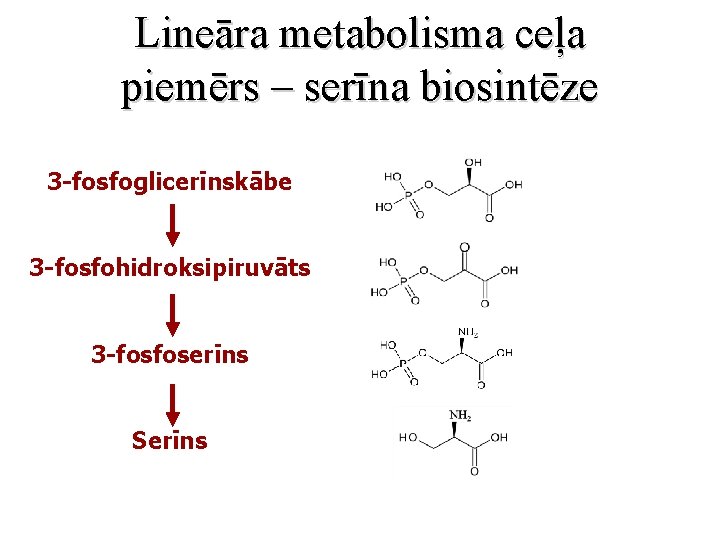
Lineāra metabolisma ceļa piemērs – serīna biosintēze 3 -fosfoglicerīnskābe 3 -fosfohidroksipiruvāts 3 -fosfoserīns Serīns
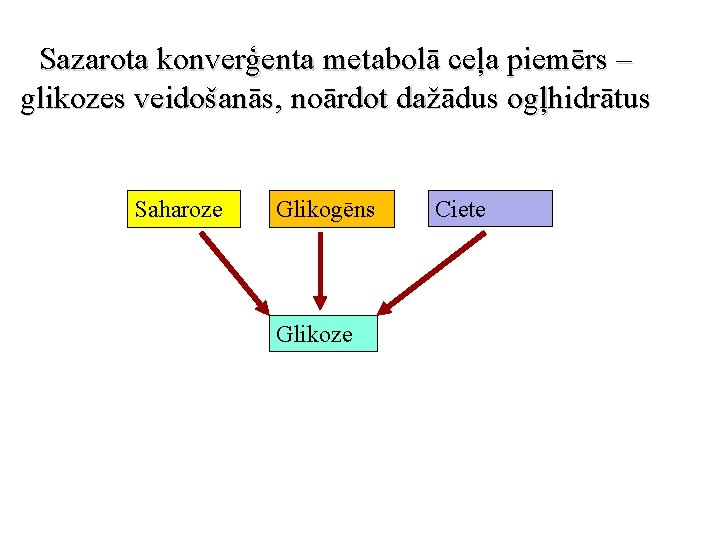
Sazarota konverģenta metabolā ceļa piemērs – glikozes veidošanās, noārdot dažādus ogļhidrātus Saharoze Glikogēns Glikoze Ciete
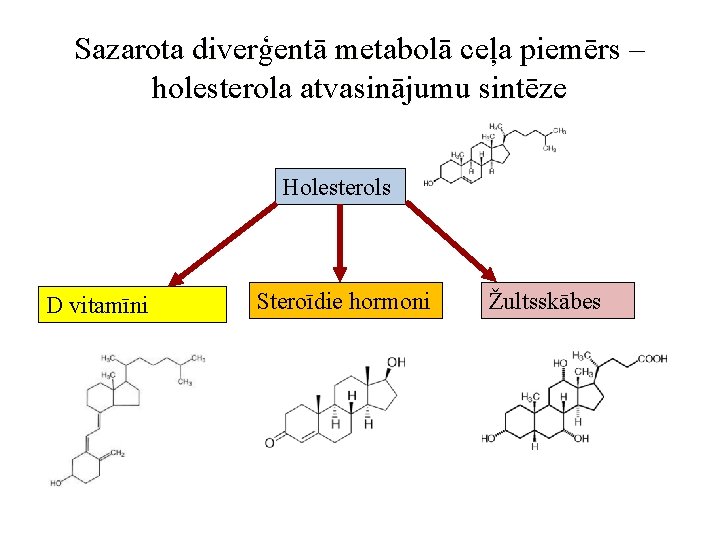
Sazarota diverģentā metabolā ceļa piemērs – holesterola atvasinājumu sintēze Holesterols D vitamīni Steroīdie hormoni Žultsskābes
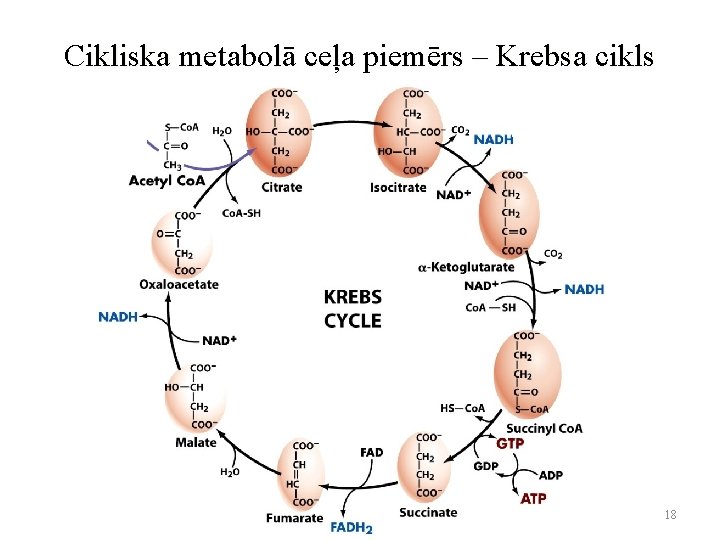
Cikliska metabolā ceļa piemērs – Krebsa cikls 18

Enzīmi • No grieķu valodas ενζυμον - «ieraugs» • Latviski mēdz saukt arī par fermentiem • Bioloģiskas makromolekulas, kuras katalizē dzīvības procesu ķīmiskās reakcijas • Gandrīz visi enzīmi ir proteīni • Dažām RNS arī piemīt katalītiskas funkcijas – piem. ribosomai • Vielas, kuras tiek pārveidotas enzīmu katalizētajās reakcijās - substrāti 20

Enzīmi – efektīvi katalizatori • Enzīmi katalizē reakcijas, kuras normālos apstākļos notiek ļoti lēni • Piemēram, cukurs maisos var glabāties gadiem, bez vērā ņemamas oksidēšanās par CO 2 un H 2 O vai spirtu • Enzīmi to pašu reakciju paveic daudz ātrāk • Enzīms orotidīna fosfāta dekarboksilāze reakciju paātrina 1017 reizes – tātad, reakcija, kura bez enzīma notiktu 78 miljonos gadu, notiek 18 milisekundēs • Atšķirībā no daudziem mazmolekulāriem katalizatoriem, enzīmi savu funkciju veic fizioloģiskos apstākļos 21

Enzīmu nomenklatūra • Daudzu enzīmu nosaukumā to subtrātam vai katalizētajam procesam tiek pievienota izskaņa –āze, piem. proteāze, polimerāze • Enzīmu sistemātiskajā nomenklatūrā tiek identificēta katalizējamā reakcija, piemēram enzīms, kurš katalizē reakciju: ATF + D-glikoze → ADF + D-glikozes-6 -fosfāts tiek saukts: ATF: glikozes fosfotransferāze • Daudziem enzīmiem lieto arī triviālos nosaukumus, piem. invertāze – enzīms, kurš hidrolizē saharozi par glikozi un fruktozi 22

Enzīmu klasifikācija • Visus enzīmus iedala 6 klasēs • Klases iedala apkšklasēs, u. t. t. Nosaukums Katalizēto reakciju veids EC 1 oksido-reduktāzes oksidēšanās – reducēšanās reakcijas EC 2 transferāzes funkcionālo grupu pārnese no vienas molekulas uz otru EC 3 hidrolāzes ķīmisko saišu hidrolīze EC 4 liāzes ķīmisko saišu saraušana no oksidēšnas un hidrolīzes atšķirīgā veidā EC 5 izomerāzes vienas molekulas izomerizācija EC 6 ligāzes divu molekulu savienošana ar kovalento saiti 23
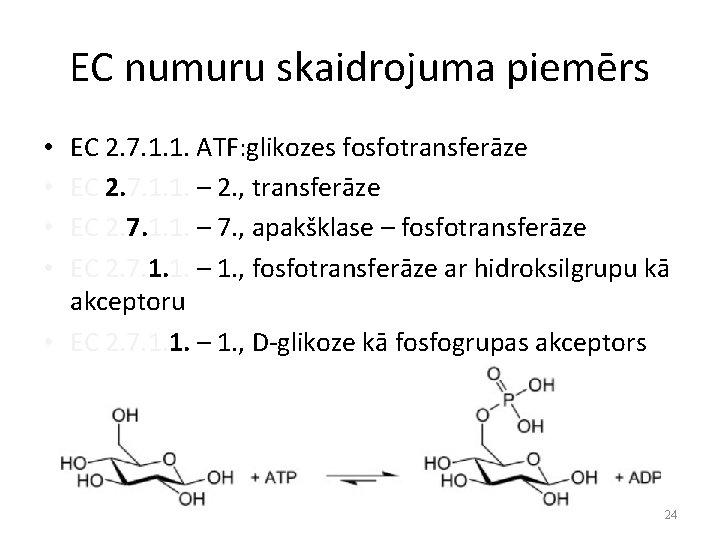
EC numuru skaidrojuma piemērs EC 2. 7. 1. 1. ATF: glikozes fosfotransferāze EC 2. 7. 1. 1. – 2. , transferāze EC 2. 7. 1. 1. – 7. , apakšklase – fosfotransferāze EC 2. 7. 1. 1. – 1. , fosfotransferāze ar hidroksilgrupu kā akceptoru • EC 2. 7. 1. 1. – 1. , D-glikoze kā fosfogrupas akceptors • • 24
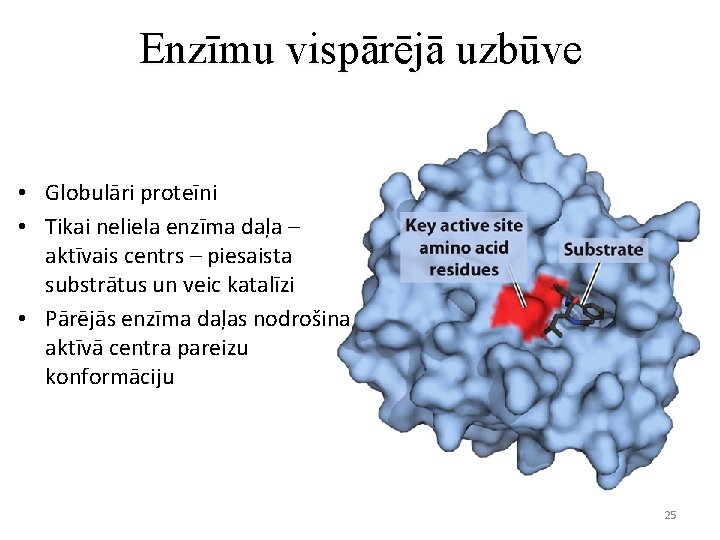
Enzīmu vispārējā uzbūve • Globulāri proteīni • Tikai neliela enzīma daļa – aktīvais centrs – piesaista substrātus un veic katalīzi • Pārējās enzīma daļas nodrošina aktīvā centra pareizu konformāciju 25
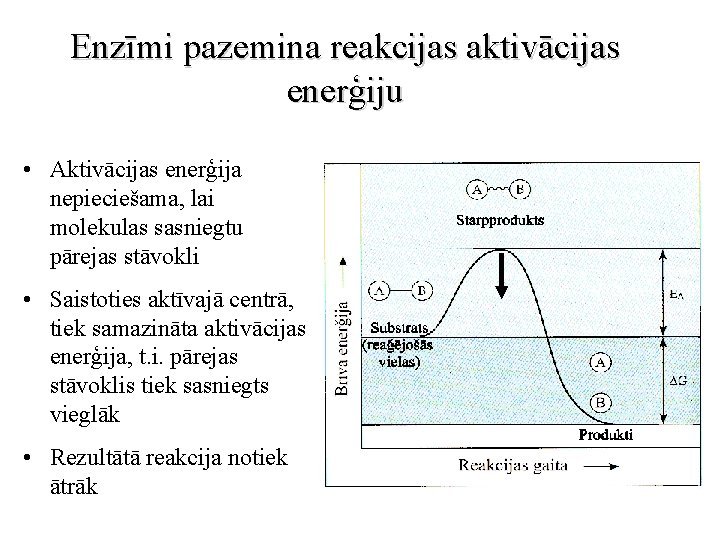
Enzīmi pazemina reakcijas aktivācijas enerģiju • Aktivācijas enerģija nepieciešama, lai molekulas sasniegtu pārejas stāvokli • Saistoties aktīvajā centrā, tiek samazināta aktivācijas enerģija, t. i. pārejas stāvoklis tiek sasniegts vieglāk • Rezultātā reakcija notiek ātrāk

Ko enzīmi var, un ko - nevar • Enzīmi paātrina ķīmiskā līdzsvara iestāšanos • Enzīmi nenobīda reakcijas ķīmisko līdzsvaru! • T. i. , enzīmi nevar paātrināt tikai tiešo vai tikai atgriezenisko ķīmisko reakciju • Enzīmi nepadara enerģētiski neizdevīgas reakcijas par izdevīgām • Enzīmi var sajūgt divas reakcijas – vienu enerģētiki izdevīgu un otru – neizdevīgu. Tādejādi abas reakcijas kopā var būt enerģētiski izdevīgas Piemērs – glikozes fosforilēšana 1. reakcija – ATP → ADP+Pi 2. reakcija – Pi + glikoze → glikoze-P
Enzīmi palielina sadursmju biežumu starp reaģējošajām molekulām
Enzīmi novieto substrātus optimālā telpiskā izkārtojumā – reaģējošo molekulu sadursmes ir ‘produktīvas’
Enzīmi novieto reaģējošo saiti optimālā polāru vai lādētu grupu tuvumā, lai varētu notikt katalīze
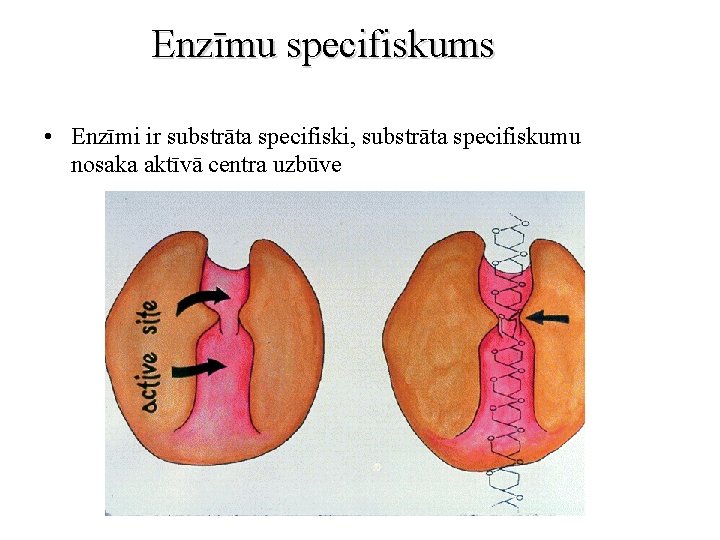
Enzīmu specifiskums • Enzīmi ir substrāta specifiski, substrāta specifiskumu nosaka aktīvā centra uzbūve

Enzīmu specifiskums • Absolūts specifiskums • Invertāze šķeļ tikai saharozi • Izteikts specifiskums • Alkoholdehidrogenāze oksidē metanolu un propanolu daudz lēnāk nekā etanolu • Saites vai grupas specifiskums • Fosfatāze atšķeļ fosfātu no DNS, RNS, proteīniem

Enzīmu specifiskums • Stereospecifiskums • Proteāzes (piem. , tripsīns) šķeļ tikai no L-aminoskābēm sastāvošus proteīnus • Vāji izteikts specifiskums • Himotripsīns hidrolizē ne tikai peptīdsaites, bet arī esterus
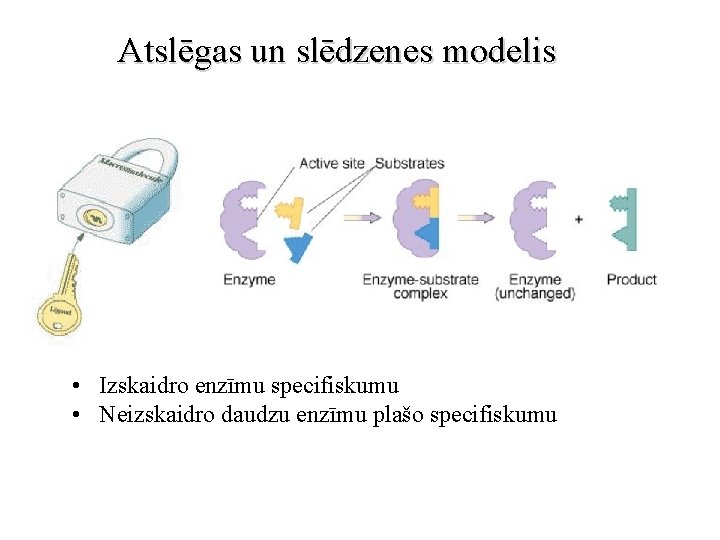
Atslēgas un slēdzenes modelis • Izskaidro enzīmu specifiskumu • Neizskaidro daudzu enzīmu plašo specifiskumu
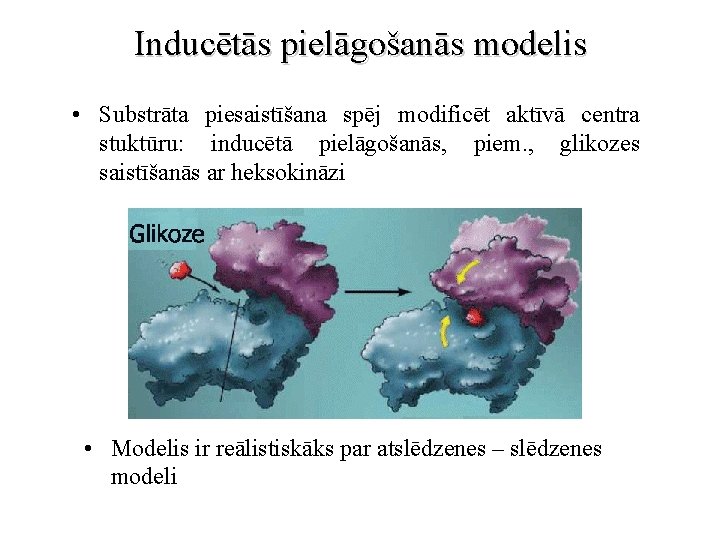
Inducētās pielāgošanās modelis • Substrāta piesaistīšana spēj modificēt aktīvā centra stuktūru: inducētā pielāgošanās, piem. , glikozes saistīšanās ar heksokināzi • Modelis ir reālistiskāks par atslēdzenes – slēdzenes modeli
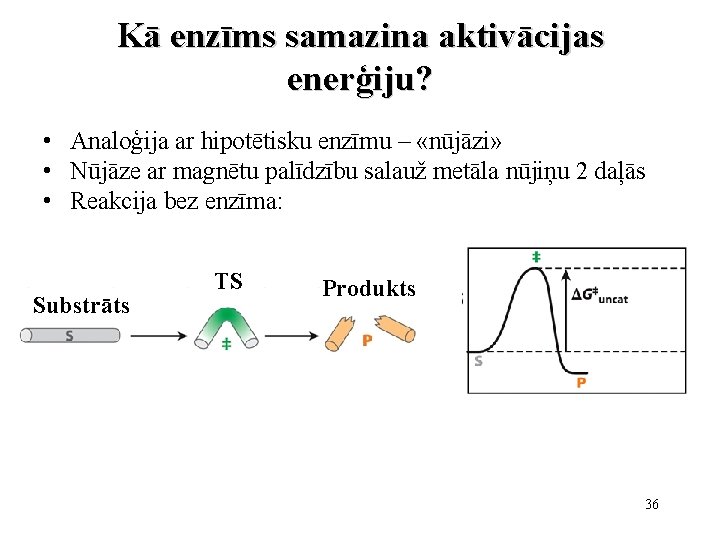
Kā enzīms samazina aktivācijas enerģiju? • Analoģija ar hipotētisku enzīmu – «nūjāzi» • Nūjāze ar magnētu palīdzību salauž metāla nūjiņu 2 daļās • Reakcija bez enzīma: Substrāts TS Produkts 36
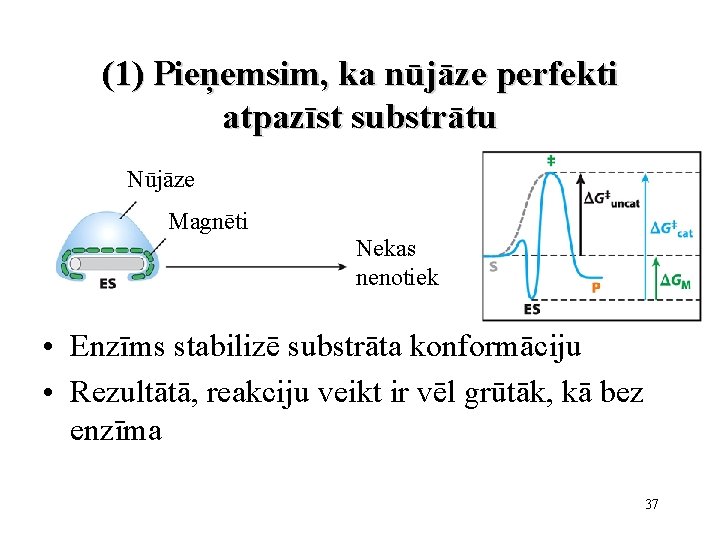
(1) Pieņemsim, ka nūjāze perfekti atpazīst substrātu Nūjāze Magnēti Nekas nenotiek • Enzīms stabilizē substrāta konformāciju • Rezultātā, reakciju veikt ir vēl grūtāk, kā bez enzīma 37
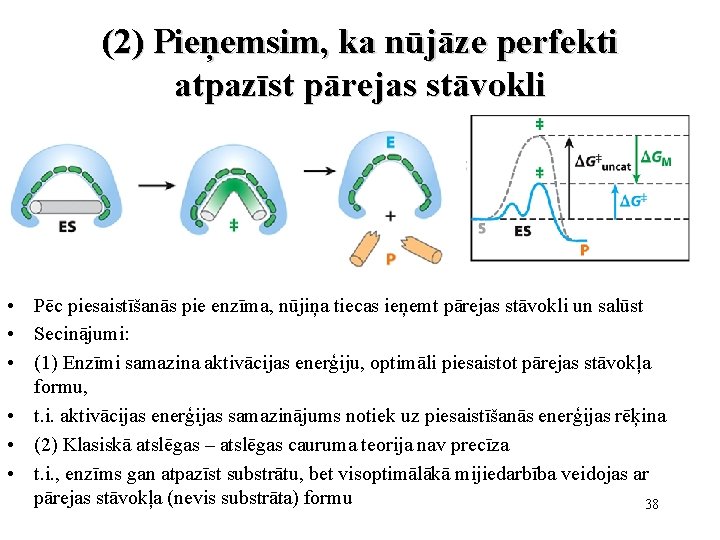
(2) Pieņemsim, ka nūjāze perfekti atpazīst pārejas stāvokli • Pēc piesaistīšanās pie enzīma, nūjiņa tiecas ieņemt pārejas stāvokli un salūst • Secinājumi: • (1) Enzīmi samazina aktivācijas enerģiju, optimāli piesaistot pārejas stāvokļa formu, • t. i. aktivācijas enerģijas samazinājums notiek uz piesaistīšanās enerģijas rēķina • (2) Klasiskā atslēgas – atslēgas cauruma teorija nav precīza • t. i. , enzīms gan atpazīst substrātu, bet visoptimālākā mijiedarbība veidojas ar pārejas stāvokļa (nevis substrāta) formu 38

Kofaktori • Daži enzīmi katalizē reakciju bez papildus savienojumu klātbūtnes • Citiem enzīmiem ir nepieciešami kofaktori – metālu joni vai organiski mazmolekulāri savienojumi, kuri tieši piedalās katalītiskās reakcijas veikšanā • Prostētiskās grupas ir mazmolekulāri savienojumi, kuri ir cieši saistīti ar enzīmu un no tā neatdalās reakcijas laikā • Koenzīmi ir mazmolekulāri savienojumi, kuri reakcijas laikā piesaistās un atdalās no enzīma • Neaktīvu enzīmu bez kofaktora sauc par apo-enzīmu, bet enzīmu ar kofaktoru – par holo-enzīmu Aktīvais • Dažiem enzīmiem ir vairāki kofaktori centrs • Daudzi vitamīni ir kofaktori Kofaktors 39

Enzīmu funkcionālo grupu iesaistīšana ķīmiskajās reakcijās • Dažu aminoskābju sānu ķēdes var iesaistīties skābjubāzu katalīzē – t. i. , darboties kā protonu akceptori vai donori • Skābju-bāzu katalīzē var iesaistīties arī pie enzīma piesaistītas ūdens molekulas • Aminoskābju sānu ķēdes un kofaktori var veidot kovalentas saites ar substrātiem • Dažkārt katalītisko efektu veic pie enzīma piesaistītie metālu joni (t. s. metālu jonu katalīze) • Visi minētie procesi var tikt kombinēti 40

Piemērs enzimātiskajai darbībai HIV proteāze • Vairāki HIV vīrusa proteīni tiek sintezēti kā poliproteīni, kurus nepieciešams sašķelt funkcionālās vienībās • Sašķelšanu veic HIV proteāze • HIV proteāze ir aspartilproteāze ar diviem aspartātiem aktīvajā centrā, pie kuriem ir piesaistījusies H 2 O molekula • HIV proteāze šķeļ polipeptīdu starp Phe un Pro atlikumiem, aktīvajā centrā ir hidrofoba kabata, kur piesaistas Phe un Pro sānu ķēdes • Aspartāta karboksilgrupa veicina H 2 O molekulas tiešu uzbrukumu peptīda saitei • HIV proteāze ir viens no galvenajiem mērķproteīniem jaunu zāļu izstrādei • Šobrīd komerciāli ir pieejami 10 FDA apstiprināti medikamenti, kuri darbojas kā HIV proteāzes inhibitori 41
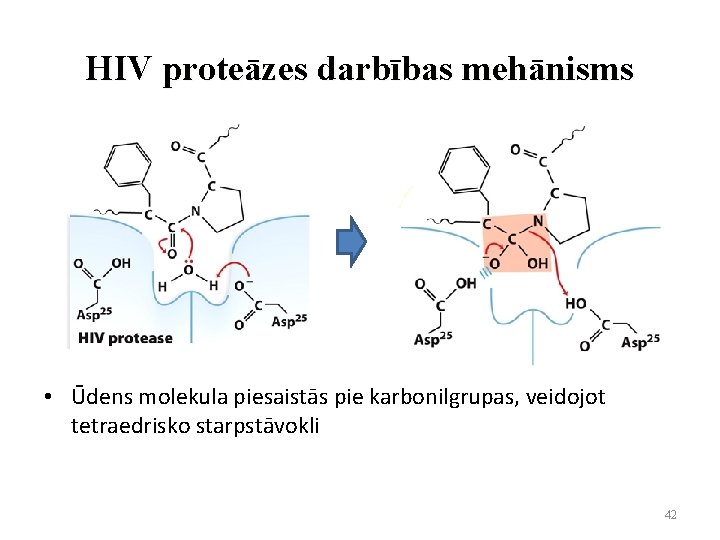
HIV proteāzes darbības mehānisms • Ūdens molekula piesaistās pie karbonilgrupas, veidojot tetraedrisko starpstāvokli 42
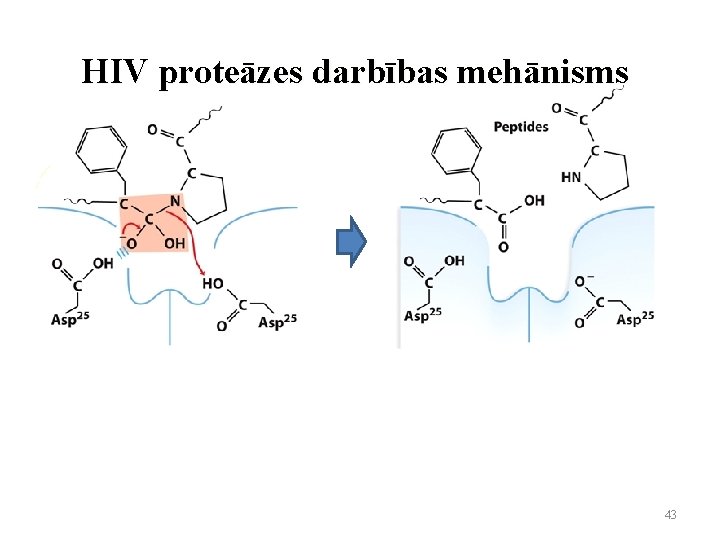
HIV proteāzes darbības mehānisms 43

Enzīmu aktivitātes regulācija • Enzīmu aktivitāte ir kritiski atkarīga no pareizas trīsimensionālās struktūras un aktīvā centra pieejamības • Daudzu enzīmu darbība ir nepieciešama tikai noteiktos apstākļos, tāpēc to darbību ir nepieciešams regulēt • Enzīmu darbību var regulēt dažādi inhibitori vai aktivatori, kuri var piesaistīties enzīma aktīvajā centrā vai izmainīt aktīvā centra struktūru vai pieejamību • Ievērojama daļa ārstniecisko preparātu ir enzīmu inhibitori 44
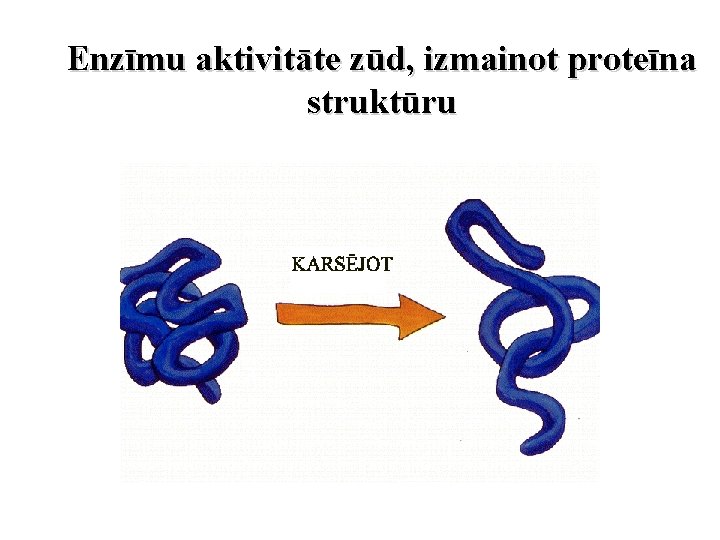
Enzīmu aktivitāte zūd, izmainot proteīna struktūru
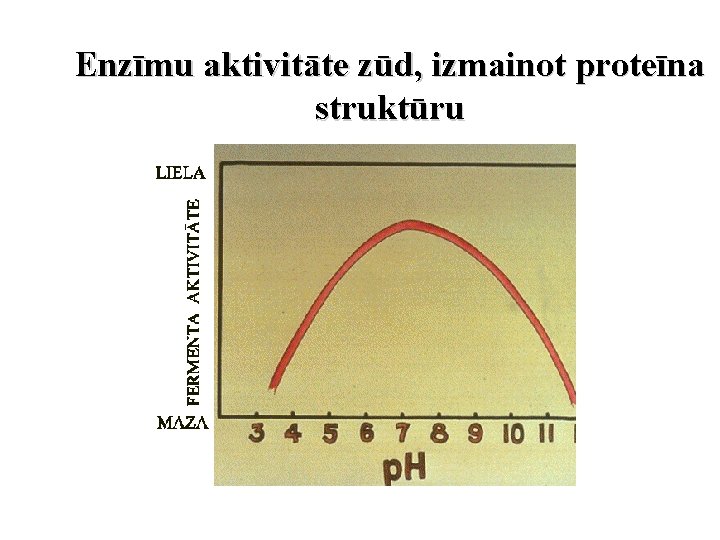
Enzīmu aktivitāte zūd, izmainot proteīna struktūru

Enzīmu inhibitori • Jebkuri aģenti, kuri kavē enzīma darbību • Nespecifiskie inhibitori kavē daudzu enzīmu darbību un parasti ir denaturējošie aģenti • Specifiskie inhibitori kavē noteikta enzīma darbību – Neatgriezeniskajā inhibīcijā enzīms tiek permanenti inaktivēts, parasti kovalenti modificējot aktivitātei nepieciešamu aktīvā centra atlikumu vai arī inhibitoram ļoti cieši piesaistoties enzīma aktīvajā centrā – Atgriezeniskajā inhibīcijā enzīma aktivitāti var atjaunot, samazinot inhibitora koncentrāciju – Atgriezeniskos inhibitorus sīkāk iedala konkurējošajos, nekonkurējošajos un jauktā tipa inhibitoros 47

Konkurējošie inhibitori • Konkurējošie inhibitori piesaistas pie enzīma aktīvā centra un tādejādi konkurē ar substrātu • Konkurējošie inhibitori parasti ir strukturāli līdzīgi substrātam S S I
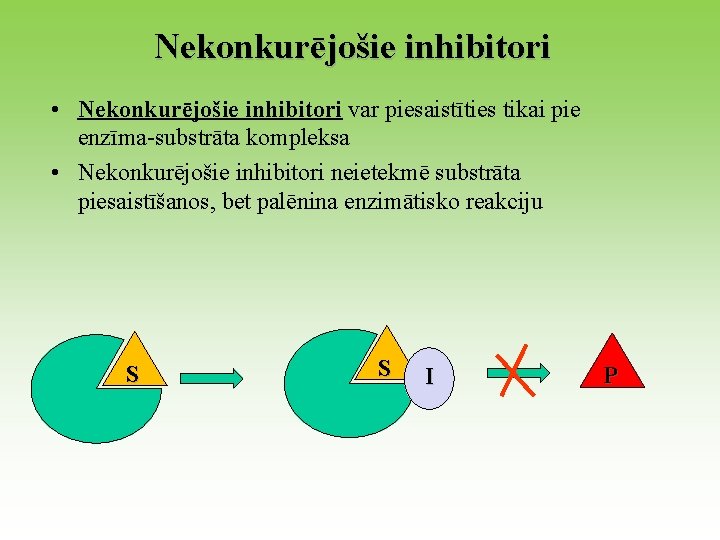
Nekonkurējošie inhibitori • Nekonkurējošie inhibitori var piesaistīties tikai pie enzīma-substrāta kompleksa • Nekonkurējošie inhibitori neietekmē substrāta piesaistīšanos, bet palēnina enzimātisko reakciju S S I P
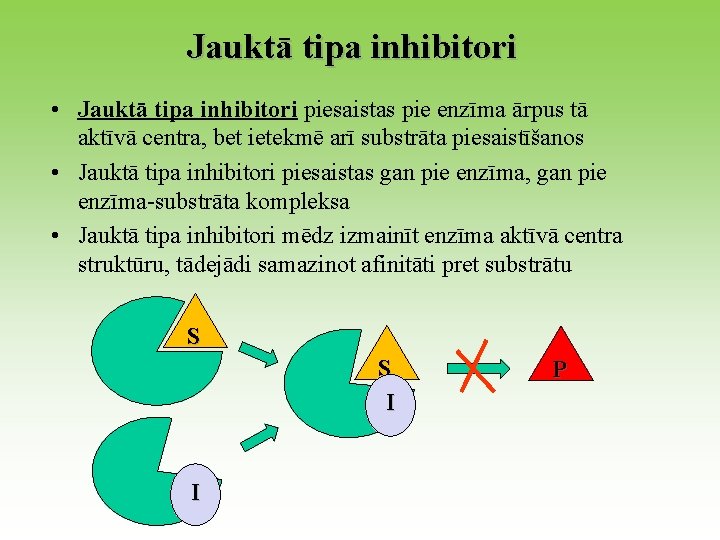
Jauktā tipa inhibitori • Jauktā tipa inhibitori piesaistas pie enzīma ārpus tā aktīvā centra, bet ietekmē arī substrāta piesaistīšanos • Jauktā tipa inhibitori piesaistas gan pie enzīma, gan pie enzīma-substrāta kompleksa • Jauktā tipa inhibitori mēdz izmainīt enzīma aktīvā centra struktūru, tādejādi samazinot afinitāti pret substrātu S S I I P
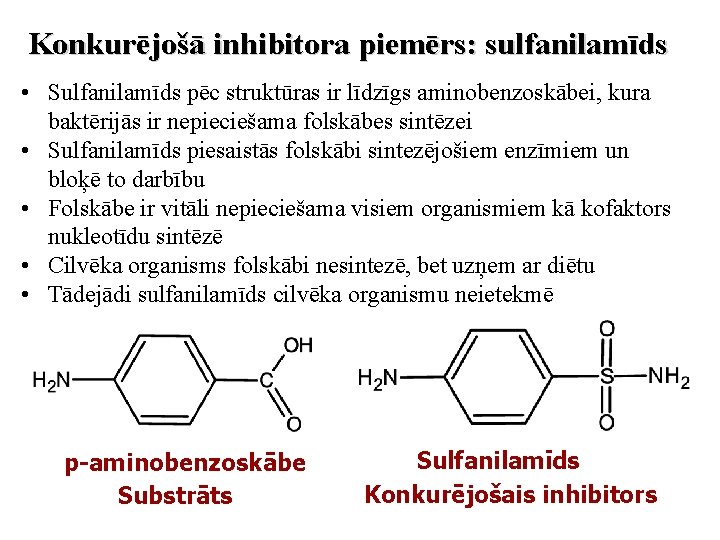
Konkurējošā inhibitora piemērs: sulfanilamīds • Sulfanilamīds pēc struktūras ir līdzīgs aminobenzoskābei, kura baktērijās ir nepieciešama folskābes sintēzei • Sulfanilamīds piesaistās folskābi sintezējošiem enzīmiem un bloķē to darbību • Folskābe ir vitāli nepieciešama visiem organismiem kā kofaktors nukleotīdu sintēzē • Cilvēka organisms folskābi nesintezē, bet uzņem ar diētu • Tādejādi sulfanilamīds cilvēka organismu neietekmē p-aminobenzoskābe Substrāts Sulfanilamīds Konkurējošais inhibitors
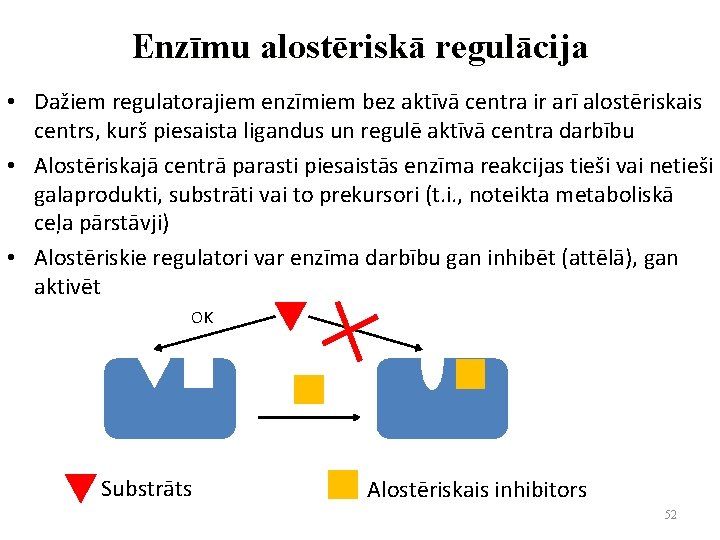
Enzīmu alostēriskā regulācija • Dažiem regulatorajiem enzīmiem bez aktīvā centra ir arī alostēriskais centrs, kurš piesaista ligandus un regulē aktīvā centra darbību • Alostēriskajā centrā parasti piesaistās enzīma reakcijas tieši vai netieši galaprodukti, substrāti vai to prekursori (t. i. , noteikta metaboliskā ceļa pārstāvji) • Alostēriskie regulatori var enzīma darbību gan inhibēt (attēlā), gan aktivēt OK Substrāts Alostēriskais inhibitors 52

Enzīmu kinētika • Enzīmu kinētika pēta enzimātisko reakciju ātrumu un tā izmaiņas eksperimentālajos apstākļos Reakcijas ātrums – substrāta vai produkta koncentrācijas izmaiņa laika vienībā S Enzīms P Pēc laika t produkta koncentrācija ir [P 1] un substrāta koncentrācija [S 1] Pēc laika t+Δt produkta koncentrācija ir [P 2] un substrāta koncentrācija [S 2] Mainoties substrāta koncentrācijai, mainās arī reakcijas ātrums Tādejādi, reakcijas ātrums mainās reakcijas gaitā 53
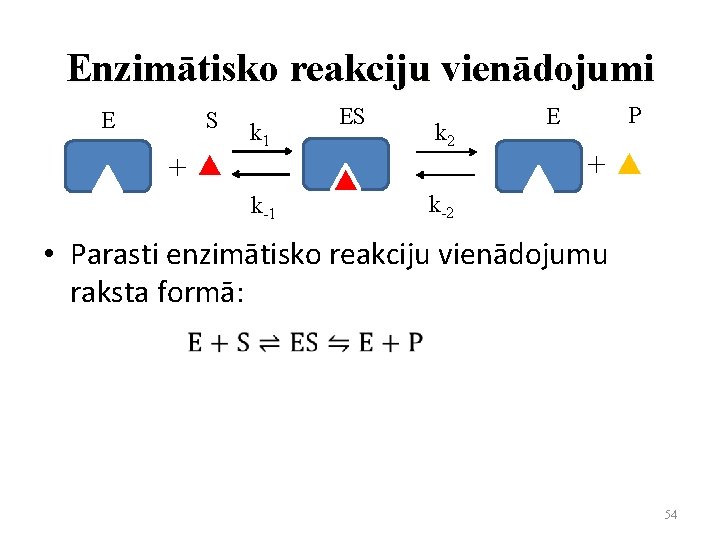
Enzimātisko reakciju vienādojumi E S + k 1 k-1 ES k 2 P E + k-2 • Parasti enzimātisko reakciju vienādojumu raksta formā: 54
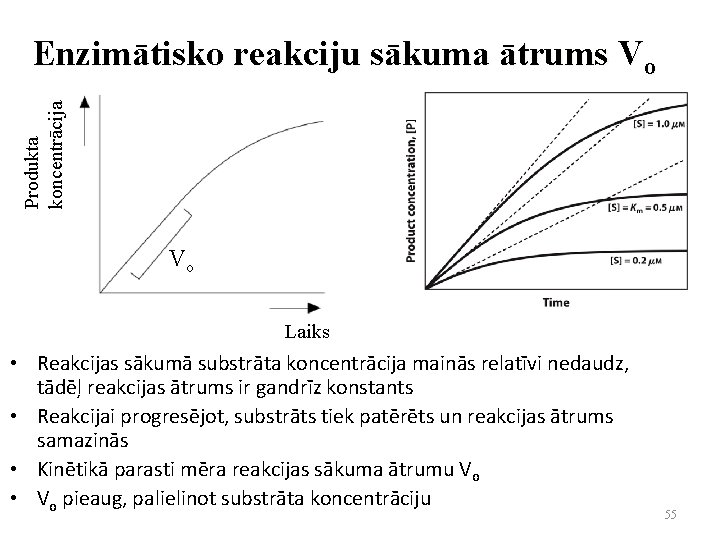
Produkta koncentrācija Enzimātisko reakciju sākuma ātrums Vo Vo Laiks • Reakcijas sākumā substrāta koncentrācija mainās relatīvi nedaudz, tādēļ reakcijas ātrums ir gandrīz konstants • Reakcijai progresējot, substrāts tiek patērēts un reakcijas ātrums samazinās • Kinētikā parasti mēra reakcijas sākuma ātrumu Vo • Vo pieaug, palielinot substrāta koncentrāciju 55
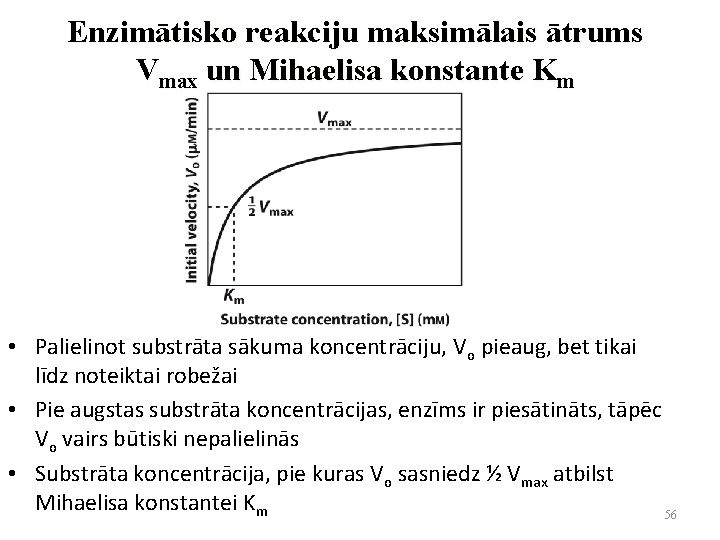
Enzimātisko reakciju maksimālais ātrums Vmax un Mihaelisa konstante Km • Palielinot substrāta sākuma koncentrāciju, Vo pieaug, bet tikai līdz noteiktai robežai • Pie augstas substrāta koncentrācijas, enzīms ir piesātināts, tāpēc Vo vairs būtiski nepalielinās • Substrāta koncentrācija, pie kuras Vo sasniedz ½ Vmax atbilst Mihaelisa konstantei Km 56

Mihaelisa-Mentenas vienādojums • Mihaelisa-Mentenas vienādojums ir vissvarīgākais vienādojums enzimoloģijā 57
![Lainvivera-Berka vienādojums 1 = Vo Km Vmax [S] 1 + Vmax • Mihaelisa-Mentenas vienādojuma Lainvivera-Berka vienādojums 1 = Vo Km Vmax [S] 1 + Vmax • Mihaelisa-Mentenas vienādojuma](http://slidetodoc.com/presentation_image/260309b66debddfc34908f36232bc042/image-58.jpg)
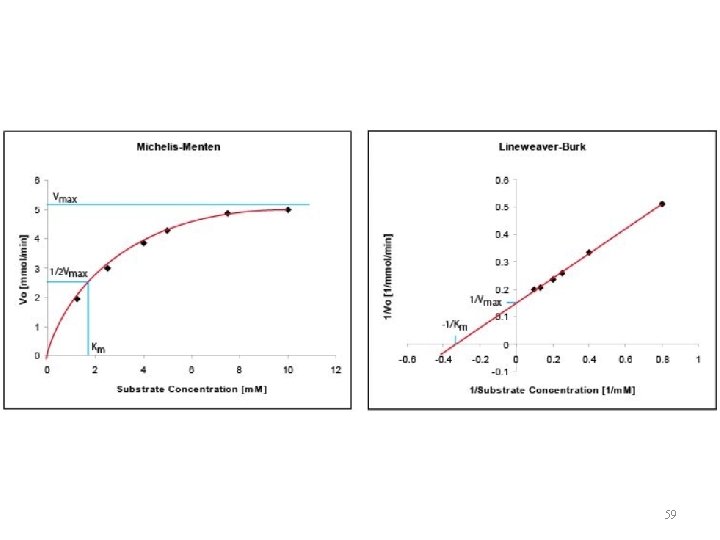
Lainvivera-Berka vienādojums 1 = Vo Km Vmax [S] 1 + Vmax • Mihaelisa-Mentenas vienādojuma pārveidojums, t. s. dubultinversais plots • Ļauj precīzāk no eksperimentālā grafika noteikt Vmax un Km 58
59
![Konkurējošo un nekonkurējošo inhibitoru dubultinversie ploti Konkurējošie 1/Vo Nekonkurējošie [I] > x [I] = Konkurējošo un nekonkurējošo inhibitoru dubultinversie ploti Konkurējošie 1/Vo Nekonkurējošie [I] > x [I] =](http://slidetodoc.com/presentation_image/260309b66debddfc34908f36232bc042/image-60.jpg)
Konkurējošo un nekonkurējošo inhibitoru dubultinversie ploti Konkurējošie 1/Vo Nekonkurējošie [I] > x [I] = x [I]=0 1/Vmax -1/Km 1/S • Konkurējošie inhibitori nesamazina • eksperimentā «redzamo» Vmax • Konkurējošie inhibitori palielina • eksperimentā «redzamo» Km Nekonkurējošie inhibitori samazina eksperimentā «redzamo» Vmax Nekonkurējošie inhibitori samazina eksperimentā «redzamo» Km 60
- Slides: 60