Mesa IV Disfuncin sexual y reproductora Yolanda Escobar

Mesa IV Disfunción sexual y reproductora Yolanda Escobar Álvarez

La sexualidad humana. ● Es un fenómeno complejo y multidimensional cuyo comportamiento normal es muy variado y subjetivo. ● En ella influyen aspectos biológicos, psicológicos, interpersonales y de comportamiento. ● La conducta sexual normal es muy variada y la define cada persona y su pareja, si la hay. ● Para cada persona actúan factores de género, edad, actitudes personales, valores y cultura. ● Ciclo de respuesta sexual humana en 4 fases: deseo, excitación, orgasmo y resolución.

Sexualidad y cáncer. ● Un 40 -100% de los pacientes con cáncer padecen algún tipo de disfunción sexual. ● Casi todos los tratamientos para el cáncer tienen el potencial de alterar la función sexual. ● Las alteraciones no siempre desaparecen al término del tratamiento antitumoral. ● Representa un factor muy importante para la calidad de vida de estos enfermos. ● Con el tratamiento adecuado, hasta un 70% de los pacientes pueden mejorar su función sexual.
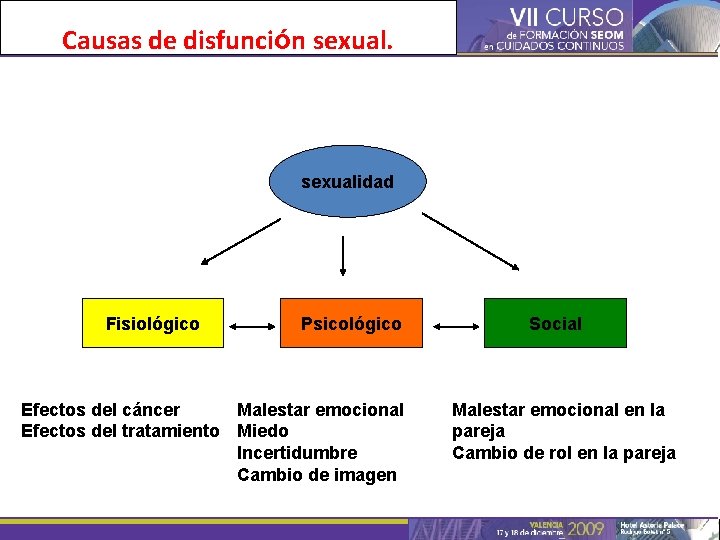
Causas de disfunción sexualidad Fisiológico Psicológico Efectos del cáncer Malestar emocional Efectos del tratamiento Miedo Incertidumbre Cambio de imagen Social Malestar emocional en la pareja Cambio de rol en la pareja

Tipos más frecuentes de D. S. en cáncer. ● En ambos sexos: Falta de deseo sexual. ● En varones: Disfunción eréctil. ● En mujeres: Dispareunia. ● Otras en varones: Aneyaculación. Eyaculación retrógrada. Anorgasmia. ● Otras en mujeres: Anorgasmia. Sensaciones genitales alteradas.

Disfunción sexual en la mujer. ● Quimioterapia/hormonoterapia: menstruaciones irregulares, menopausia precoz, calor, insomio, irritabilidad, depresión, sequedad vaginal, dispareunia, disminución de la libido, infertilidad. ● Radioterapia/braquiterapia: fibrosis de la pelvis, atrofia/estenosis vaginal, baja lubricación, alteraciones urinarias, edema, ulceraciones, irritación, disminución de la elasticidad y tamaño de la vagina. ● Cirugía: alteración de la imagen, dolor, menopausia, cambio en el tamaño y elaticidad vagina.

Disfunción sexual en el hombre. ● Quimioterapia/hormonoterapia: Disfunción eréctil, disminución de la libido, trastorno de la eyaculación, ginecomastia, atrofia de pene/testículos e infertilidad. ● Radioterapia/braquiterapia: problemas urinarios, impotencia, trastornos intestinales, atrofia pene/testicular. ● Cirugía: problemas urinarios, disfunción eréctil, alteración de la imagen, dolor, eyaculación retrógrada.

Amenorrea y quimioterapia.


F. relacionados con hormonoterapia. ● En mujeres. Hormonoterapia adyuvante – Tamoxifeno/Inhibidores de la Aromatasa: - sofocos - sudoración nocturna - > riesgo de menopausia precoz en mayores de 45 años - ligero aumento de dificultad para: excitación/orgasmo. Tamoxifeno. Resultados no definitivos. Relacionado con: - sequedad vaginal. - exceso de lubricación. - bajo deseo sexual. - retardo orgásmico. ● En varones. Ca. Próstata. Caída de andrógenos circulantes. Se afectan: -deseo sexual. -capacidad eréctil. -posibilidad de orgasmo.

Factores relacionados con cirugía. 1) CÁNCER DE MAMA: ● Pequeña diferencia entre tto. radical/conservador en: frecuencia coital facilidad para orgasmo satisfacción sexual ● Encuesta a menores de 50 años. Relación: mastectomía /desinterés sexual quimioterapia/disfunción sexual 2) CÁNCER COLORRECTAL: ● Causa principal: lesión de nervios autónomos pélvicos. ● Depende de: tipo de cirugía/ plano de disección. grado de conservación de estructuras nerviosas. amplitud de disección pélvica. ● Para mantener erección : indemnidad del plexo pélvico. ● Para mantener eyaculación y orgasmo: plexo pélvico y nervio hipogástrico. ● Ca. colorrectal con resección abdominoperineal: pared posterior vaginal.

Factores relacionados con cirugía (II). 3) OTROS TUMORES PÉLVICOS FEMENINOS: ● Ca. Vejiga: cistectomía radical; afecta a vagina dolor. ● Ca. Útero: histerectomía/remoción parcial de la vagina. ● Ca. Ovarios: ooforectomía. ● Ca. Vulva vulvectomía. Alteraciones en Histerectomía Radical: a) dificultad para alcanzar el orgasmo. b) relaciones incómodas por disminución tamaño vaginal durante los 6 primeros meses. c) carencia de lubricación y falta de interés durante 2 años. 4) CÁNCER DE PRÓSTATA: ● Erecciones funcionales tras PR: 10 -40%/ RTP clásica: 15 -33%; RTP tridimensional conformada: 30 -60% ● Estudios retrospectivos: mejores resultados con técnicas de preservación de nervios (¿sesgo de selección? ). ● Rev. sistemática 1997 -2003: los mayores determinantes en preservación función eréctil: selección de pacientes y técnica quirúrgica empleada. ● Recuperación: 1 año tras cirugía 2 -3 años tras RTP ● Mecanismo de daño: la PR lesiona nervios que dirigen sangre al pene; baja la oxigenación y aumentan depósitos de colágeno.

Factores farmacológicos. ● Opiodes: disminuyen la líbido por dos mecanismos: • Inhiben la LHRH: disminuyen tanto la LH como la testosterona. • Elevan niveles prolactina en sangre: aumenta la liberación de LH. Reacción similar ambos sexos: - cae la libido. - baja la LH. - baja testosterona en varones. - amenorrea/ciclo irregular en mujeres. ● ISRS: Inhiben recaptación de serotonina y se acumula en espacio sináptico: posible estimulación centros eréctiles inferiores. Se asocian a: - retardo orgásmico/anorgasmia. - poco deseo sexual y dificultad para estimularse. (Efectos relacionados con dosis y variables entre personas). ● IMAO, Litio, A. Tricíclicos también se relacionan con disfunción sexual. ● Antibióticos, antiparasitarios (Metronidazol), anticolinérgicos, anti. H 2, ansiolíticos e hipnóticos, diuréticos, neurolépticos, antihipertensivos (betabloqueantes).

Evaluación de la sexualidad. ● No hay pautas claras. Dar al paciente la opción de hablar. ● Hacer preguntas específicas de interpretación abierta. Incluir: estado sexual actual, estado premórbido, aspectos psicosociales, aspectos médicos y estilo de vida. ● Oportunidad para abordar el tema: las visitas de seguimiento. ● Se necesita tiempo y adiestramiento. ● Evaluación mínima: ¿Tiene usted algún problema o preocupación respecto a la sexualidad? . ● Red de especialistas (salud mental, ginecología, urología, infecundidad) ● Cuestionarios breves. Para varón: IIEF, BMSFI, SHIM Para mujer: BISF-W, SHF, CSFQ

Tratamiento de la D. S. en mujeres. ● Atrofia/sequedad/irritación vaginal: opciones. ● THS en caso de menopausia precoz sintomática (valorar). ● Ejercicios de KEGEL para relajar musculatura sacrococcígea. ● Dilatadores vaginales progresivos si calibre/profundidad. ● Gel analgésico para evitar dolor en zonas sensibles. ● Terapia clitoridiana EROS.

Tratamiento de D. S. en mujeres. Atrofia/sequedad/irritación vaginal: ● Lubricantes vaginales: – Usar antes y durante el acto sexual – Base de agua y/o vaselina ● Hidratante vaginal: – Replens: 3 veces a la semana, durante 3 meses como mínimo. (Los tejidos finos de la vagina se hidratan y ésta gana elasticidad). – Uso concomitante con lubricantes del acto sexual.

Tratamiento D. S. en mujeres (II). Atrofia/sequedad/irritación vaginal: ● Estrógenos vaginales: – Cremas: 2 -3 veces por semana. ● Aumentan niveles de estrogenos (los primeros 3 -4 meses) ● Contraindicados en pacientes con cáncer de mama. – Anillo de silicona (Estring) : lenta administración de estrógenos a nivel local en 3 meses. – Pastillas (Vagifem): administradas diariaspor la noche durante 2 semanas y, después, 2 veces por semana. ● Riesgo bajo para pacientes con cáncer de mama (aunque los estudios son cortos).
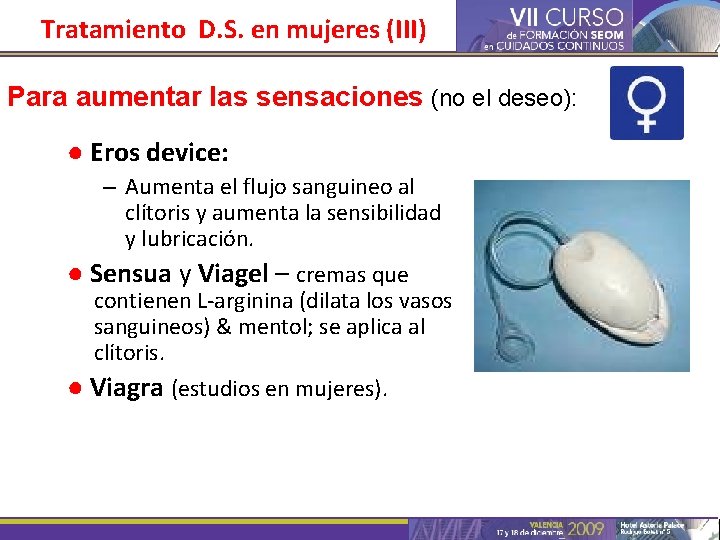
Tratamiento D. S. en mujeres (III) Para aumentar las sensaciones (no el deseo): ● Eros device: – Aumenta el flujo sanguineo al clítoris y aumenta la sensibilidad y lubricación. ● Sensua y Viagel – cremas que contienen L-arginina (dilata los vasos sanguineos) & mentol; se aplica al clítoris. ● Viagra (estudios en mujeres).

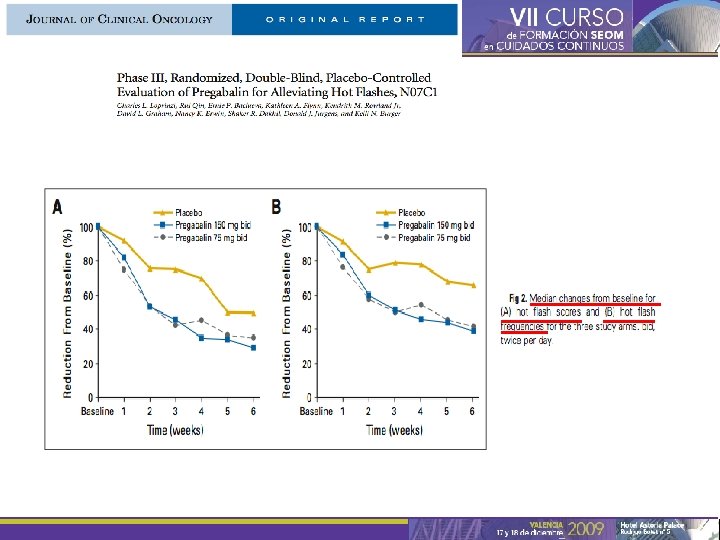
Para los sofocos menopáusicos:

INTRINSA: parche de testosterona para mujer. ● Indicado para trastorno de deseo sexual hipoactivo (TDSH). ● Mujeres con menopausia quirúrgica por ooforectomía e histerectomía (caída de hasta 50% en niveles tras la cirugía) ● En combinación con terapia estrogénica. ● Se coloca en abdomen dos veces por semana, cambiando de sitio. Contiene 8. 4 mg. de testosterona y libera 300 microg/24 horas. ● Requiere unos 6 meses para actuar plenamente; el efecto empieza a notarse a las 4 semanas. ● Receta médica. No cubierto por S. S.

Flibanserina. Lo último en llegar. ● Diseñada como antidepresivo, resultó poco eficaz pero con un efecto colateral: aumento de la libido. ● 4 ensayos clínicos (USA, Canadá y Europa) en 1946 mujeres premenopáusicas > 18 años con TDSH. ● Flibanserina en 4 dosis diferentes vs placebo durante 24 semanas. ● Resultados basados en dosis de 100 mg/día. ● Mejora significativa en: - nº de encuentros sexuales - deseo sexual - reducción malestar asociado a DS - funcionamiento sexual global

Tratamiento de la D. S. en varones. ● Suprimir/atenuar la causa si se conoce y es posible (síntomas, fármacos, depresión…). ● Medidas de educación sexual: - Reafirmar otras formas de contacto no coital. Ejercicios de “sensate focus”. - Reenfocar cognitivamente la masturbación. - Explorar posiciones sexuales más confortables. - Trucos para los colectores/bolsas. ● Medidas farmacológicas en varones: a) Inhibidores de la fosfodiesterasa-5. Tres en el mercado: - Sildenafilo (Viagra) - Vardenafilo (Levitra) - Tadalafilo (Cialis) b) Inyecciones en pene: Prostaglandina E 1 ● Otras modalidades en varones: Cirugía de prótesis de pene Dispositivos al vacío
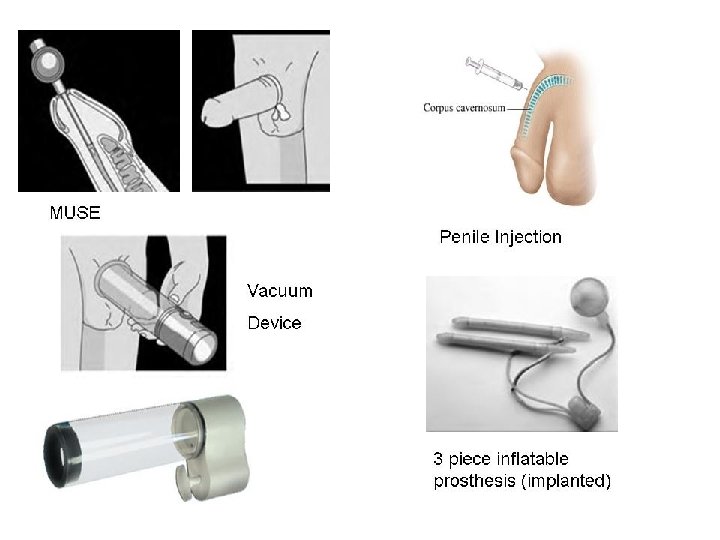

Inhibidores de la PDE-5. ● Viagra: se toma 1 hora antes y dura el efecto 4 horas. ● Levitra: tarda de 25 a 60 minutos en actuar. ● Cialis: la de vida media más larga. Se puede tomar hasta 36 h. antes. Mecanismo de acción: relajación de musculatura lisa del pene que aumenta el flujo de sangre a los cuerpos cavernosos.

Inhibidores de la PDE-5. ● Los tres se toman por vía oral. ● No hay estudios comparativos entre ellos. ● Globalmente, mejoran un 60 -70% de D. S. (mejor formas benignas). ● Constituyen el tto. de la D. S. con mejor aceptación entre los pacientes. ● No afectan al deseo sexual/orgasmo: precisan estímulo sexual. ● Viagra: el más estudiado por ser el 1º aprobado: - 72% de prostatectomías con preserv. nerv. Penetración. - 15% de prostatectomías sin preservación nerviosa. - eficaz en cir. de recto con interrup. parcial parasimpático. ( Aprox. 12% dejan de responder a los 3 años). ● Contraindicaciones: uso de nitratos, doxazosina y alfa-bloqueantes.

Rapsody in “blue”.

El papel del oncólogo. ● Conocimiento detallado de cómo el diagnóstico y tratamiento del cáncer puede afectar la función sexual. ● Información a los pacientes y sus parejas de las posibles alteraciones. ● Monitorización de la función sexual antes y durante el tratamiento.

El papel del oncólogo (II) ● Proveer de guías y sugerencias para que el paciente pueda adaptarse a los cambios: – Conservar energía durante el acto, alternativas a la penetración, cambios de posiciones, uso de almohadas para aliviar el dolor postural, medicación, relajación músculos pélvicos ( Kegel). – Crear el ambiente propicio (relajacion, vino, velas, música). – Sentido del humor. ● Referirlo a los especialistas implicados cuando sea necesario: – Ginecólogos. – Psicólogos/psiquiatras. – Consejeros de pareja con experiencia en pacientes diagnosticados de cáncer.

Conclusiones. ● La sexualidad es un fenómeno complejo y multidimensional. ● La interacción cáncer/sexualidad conlleva múltiples trastornos. ● El propio tumor y las terapias pueden estar implicados, además de factores psicológicos. ● La falta de deseo sexual es el principal problema en ambos sexos. ● La calidad de vida se deteriora: no minimizar. ● Una mínima evaluación ayuda a situar la cuestión. ● Tratamientos basados en educación sexual y medidas farmacológicas.

Infertilidad y cáncer. ● Un 5% de los tumores se diagnostican en < de 35 años. ● Aumento de los casos de pacientes afectos de cáncer en edad fértil y sin descendencia en el momento del diagnóstico. ● La esterilidad asociada al cáncer produce un impacto negativo psicológico y en la calidad de vida en los supervivientes de cáncer (1) (2). ● La mayoría de supervivientes de cáncer prefieren tener hijos biológicos a pesar del temor a los riesgos de malformaciones y problemas perinatales debidos al tratamiento oncológico, y a la ansiedad de saber que pueden dejarlos huérfanos. ● Los tratamientos de preservación de fertilidad ayudan emocionalmente a hacer frente al diagnóstico y tratamiento del cáncer (3) (4). ● La preservación de la fertilidad en pacientes que necesitan de un tratamiento oncológico es un reto para los profesionales. (1) Domar 1993; (2) Saito 2005, ( 3) Schover 2002, (4) Wenzel 2005

Causas de infertilidad en el paciente oncológico. ● El propio tumor. ● La alteración hormonal inducida. ● El daño o disminución del número de folículos primordiales (mujeres) y de las células madre gonadales ( hombres). ● Amenorrea (aunque la reaparición del ciclo menstrual no es sinónimo de una función fértil normal: fallo ovárico prematuro) ● Alteración en el número, movilidad, morfología e integridad del ADN de los espermatozoides.

Riesgo de infertilidad. El porcentaje de infertilidad, tanto permanente como temporal, asociada a los tratamientos antitumorales varía y depende de diversos factores (1): – – La propia enfermedad. El tipo y dosis de quimioterapia recibida. La dosis y localización de la radioterapia. Edad, sexo y estado de fertilidad antes del tratamiento. (1) Madanat 2008

Riesgo en mujeres según tratamiento. Degree of Risk High risk (> 80%): Cancer Treatment ● Hematopoietic stem cell transplantation with cyclophosphamide/total body irradiation or cyclophosphamide/busulfan ● External beam radiation to a field that includes the ovaries ● CMF, CEF, CAF x 6 cycles in women age 40 and older (adjuvant breast cancer therapy with combinations of cyclophosphamide, methotrexate, fluorouracil, doxorubicin, epirubicin) Intermediate risk: ( 20 -80%) ● CMF, CEF, CAF x 6 cycles in women age 30 -39 (adjuvant breast cancer therapy with combinations of cyclophosphamide, methotrexate, fluorouracil, doxorubicin, epirubicin) ● AC x 4 in women age 40 and older (adjuvant breast cancer therapy with doxorubicin/cyclophosphamide)

Riesgo en varones según tratamiento Agents (Cumulative dose for effect) Effects Radiation (2. 5 Gy to testis) Chlorambucil (1. 4 g/m 2) Cyclophosphamide (19 g/m 2) Procarbazine (4 g/m 2) Melphalan (140 mg/m 2) Cisplatin (500 mg/m 2) Prolonged azoospermia BCNU (1 g/m 2) CCNU (500 mg/m 2) Azoospermia in adulthood after treatment before puberty Busulfan (600 mg/m 2) Ifosfamide (42 g/m 2) BCNU (300 mg/m 2) Nitrogen mustard Actinomycin D Azoospermia likely, but always given with other highly sterilizing agents Carboplatin (2 g/m 2) Prolonged azoospermia not often observed at indicated dose Doxorubicin (Adriamycin) (770 mg/m 2) Thiotepa (400 mg/m 2) Cytosine arabinoside (1 g/m 2) Vinblastine (50 g/m 2) Vincristine (8 g/m 2) Can be additive with above agents in causing prolonged azoospermia, but cause only temporary reductions in sperm count when not combined with above agents Amsacrine, bleomycin, dacarbazine, daunorubicin, epirubicin, etoposide, fludarabine, fluorouracil, 6 -mercaptopurine, methotrexate, mitoxantrone, Only temporary reductions in sperm count at doses used in conventional regioments, but additive effects are possible

Opciones para la preservar la fertilidad en mujeres ANTES de iniciar el tratamiento. ● Criopreservación de ovocitos/embriones tras estimulación ovárica (fertilización in vitro): tasa de éxito del 20 -25% y 40% respectivamente. ● Supresión ovárica con análogos o antagonistas de Gn. Rh para proteger el tejido ovárico durante quimioterapia o radioterapia (experimental). ● Ooforopexia ( si RT pélvica) o traquelectomia radical (resección cervical con preservación del útero). ● Criopreservación de tejido ovárico y reimplantación tras el tratamiento (experimental). Donnez J et al. Hum Reprod Update, vol 12 nº 5. 2006 Lee SJ et al. ASCO recommendations…JCO, vol 24 nº 18. 2006 Mandavilli A. Nature Medicine, vol. 14 nº 1170. 2008 María Sánchez. The Valencia Programme for Fertility Preservation. Clin Transl. Oncol 10. 2008
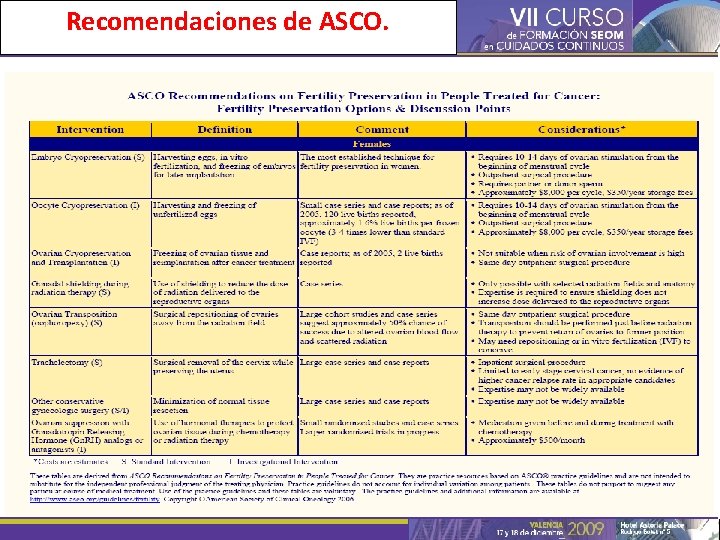
Recomendaciones de ASCO.

Congelación o vitrificación de ovocitos

Opciones para la preservación de la fertilidad en mujeres DESPUÉS de iniciar tratamiento. ● Medios naturales: – 20 -30% de recuperación de la ovulación (1) (2). – ¿Cuándo después de finalizar tratamiento? A los 2 -3 años (3). – ¿Hay riesgos? (4) • Análisis de 15, 000 mujeres afectas de cáncer tratadas con QT no evidencia de aumento de riesgo de recurrencia por embarazo y no hay aumento de incidencia de abortos/malformaciones • Aumento en un 23% en riesgo de aborto en mujeres diagnosticadas de cáncer a edad menor de 20 años y tratadas con RT (5). ● Reproducción asistida (edad, función ovárica). ● Donación de óvulos. ● Adopción. (1). Muller BA et al, 2003, (2) Blakely et al, 2004; (3) Meirow et al, 2005; (4)Maltaris et al, 2008; (5) Winther 2008

Pregnancy after treatment of breast cancer--a population-based study on behalf of Danish Breast Cancer Cooperative Group. Department of Breast and Endocrine Surgery, Rigshospitalet, Copenhagen, Denmark. Kroman N, Jensen MB, Wohlfahrt J, Eilertsen B, Danish breast Cancer Cooperative Group BACKGROUND: Estrogen is an established growth factor in breast cancer and it has been hypothesized that pregnancy associated estrogens may increase the risk of recurrence of breast cancer. In 1997 we published a population-based Danish study indicating no negative prognostic effect of pregnancy after breast cancer treatment. The present study is a ten-year update. MATERIAL AND METHODS: Danish Breast Cancer Cooperative Group has since 1977 collected population-based data on tumour characteristics, treatment regimes, and follow-up status on Danish women with breast cancer. Pregnancy history was added from the Danish Civil Registration System, the National Birth Registry, and the National Induced Abortion registry. Cox regression was used to estimate the risk ratio of dying among women with a pregnancy after breast cancer treatment compared with women without such experience. RESULTS: In all, 10 236 women with primary breast cancer aged 45 years or less at the time of diagnosis were followed for 95 616 person years. Among these, 371 women experienced pregnancy after treatment of breast cancer. In a multivariate analysis that included age at diagnosis, stage of disease, and pregnancy history prior to diagnosis, women who had a full-term pregnancy subsequent to breast cancer treatment were found to have a reduced risk of dying (relative risk: 0. 73; 95% confidence interval: 0. 54 -0. 99) compared with other women with breast cancer. The effect was not significantly modified by age at diagnosis, tumour size, nodal status, or pregnancy history before diagnosis of breast cancer. Neither spontaneous abortions nor induced abortions subsequent to breast cancer treatment had a negative impact on prognosis. CONCLUSION: In line with our previous study, but based on more than twice the patient material, we found no evidence that a pregnancy after treatment of breast cancer has a negative influence the prognosis.

Opciones para la preservación de la fertilidad en hombres ANTES de iniciar tratamiento. ● Criopreservación de esperma: depósito, congelado y almacenamiento de esperma recolectado a través de la masturbación, electroeyaculación rectal, aspirado testicular o en la orina postmasturbación. – inyección intracitoplasmática de espermatozoides (ICSI). ● Supresión testicular con análogos de la Gn. Rh para proteger el tejido testicular durante quimioterapia o radioterapia. ● Otros: criopreservación de tejido testicular y reimplantación, stem cells.

Conclusiones. ● El riesgo de infertilidad asociado a los tratamientos antitumorales es variable y multifactorial. ● La esterilidad es un factor que impacta negativamente en la calidad de vida de los pacientes. ● El riesgo de infertilidad y las opciones de preservación deben ser discutidos por el oncólogo. ● Más y mejores opciones para la preservación de la fertilidad. ● Equipo multidisciplinar para valorar riesgo oncológico/ técnicas de preservación.

Caso Clínico. Mujer de 36 años, con pareja estable y sin hijos previos. Profesional de la Publicidad. Diagnóstico de enfermedad de Hodgkin estadio II-A con afectación no bulky. Se plantea tratamiento con quimioterapia.

¿Cuál de los siguientes esquemas elegiría usted de cara a alterar lo menos posible la fertilidad? MOPP ABVD CHOP CDDP-5 FU

Respuesta: (1) (2) (3) ● ABVD es el menos gonadotóxico y preserva la fertilidad en aprox. un 90% de pacientes, sin reducir la efectividad. ● MOPP es el más gonadotóxico. ● CHOP no es un esquema para Hodgkin. ● CDDP- 5 FU no es un esquema para Hodgkin. (1) Fossa & Magelsen. Annals of Oncology 15, 2004 (2) Howell S. Endocrinol Metab Clin North Am 27 (4), 1998 (3) Robinson. Cancer 71, 1993

Evolución del caso. ● A la paciente se le administraron 6 ciclos de MOPP/ABVD alternantes. ● Obtuvo una remisión completa de su enfermedad. ● A los 12 meses de terminar el tratamiento refiere: - Disminución/ausencia de menstruación durante los 6 últimos meses. - Sofocos, sudoración nocturna, sequedad vaginal y disminución del deseo sexual.

¿Cuál es el diagnóstico de sospecha? ● Embarazo. ● Recidiva de la enfermedad de Hodgkin con síntomas B. ● Fallo ovárico precoz. ● Segundo tumor: Carcinoide.

¿Cuál es el diagnóstico de sospecha? ● Embarazo. ● Recidiva de la enfermedad de Hodgkin con síntomas B. ● Fallo ovárico precoz. ● Segundo tumor: Carcinoide.

Definición de fallo ovárico precoz. (1) Amenorrea de 6 o más meses de duración que tiene lugar antes de los 40 años de edad. (1) Fossa & Magelsen. Annals of Oncology 15, 2004

¿Qué determinaciones haría para afianzar su diagnóstico? (1) (2) ● Biopsia ovárica. ● Beta 2 microglobulina. ● Niveles de estrógenos circulantes y determinación de FSH/LH. ● Test de embarazo. (1) Kreuser. 21 St ESMO: Educ. Book, 1996 (2) Myers. Sem Oncol 19, 1992

¿Qué determinaciones haría para afianzar su diagnóstico? (1) (2) ● Biopsia ovárica. ● Beta 2 microglobulina. ● Niveles de estrógenos circulantes y determinación de FSH/LH. ● Test de embarazo. (1) Kreuser. 21 St ESMO: Educ. Book, 1996 (2) Myers. Sem Oncol 19, 1992

Resultados. (1) ● No se realiza biopsia ovárica en primera instancia. ● No se sospecha recidiva de Hodgkin. ● Los estrógenos están bajos y la FSH y la LH elevadas, en rango menopáusico. ● No se sospecha embarazo. (1) Schwartz et al. Survivors of Childhood Cancer: Assessment and Management. St Louis, Mo. Mosby 1994

La paciente presenta un fallo ovárico precoz y solicita tratamiento. Le exponemos que: ● La THS es la única que controla los síntomas físicos de la menopausia. ● Las isoflavonas de soja son el tratamiento que mejor resultado muestra en los estudios. ● La TSH controla los síntomas a expensas de un aumento del riesgo de cáncer de mama y ovario. ● Le explicamos que la menopausia es un proceso normal a cualquier edad y no precisa ningún tratamiento.

La paciente presenta un fallo ovárico precoz y solicita tratamiento. Le exponemos que: ● La THS es la única que controla los síntomas físicos de la menopausia. ● Las isoflavonas de soja son el tratamiento que mejor resultado muestra en los estudios. ● La TSH controla los síntomas a expensas de un aumento del riesgo de cáncer de mama y ovario. ● Le explicamos que la menopausia es un proceso normal a cualquier edad y no precisa ningún tratamiento.

Evolución. ● La paciente opta por no tratar sus síntomas y un año después de acabado el tratamiento de QTP. vuelve a tener la regla y niveles hormonales premenopáusicos en sangre. ● Nos pregunta sus posibilidades de concebir un hijo y los riesgos que corre dicho hijo de presentar malformaciones o enfermedades congénitas.

A la pregunta sobre riesgos del hijo respondemos que: (1) ● Nunca se debe concebir después de haber recibido QTP. ● EL hijo tendría, al menos, un 20% de posibilidades de padecer malformaciones. ● No hay mayor tasa de malformaciones entre los hijos de madres que han recibido QTP. ● La inmunosupresión del embarazo podría facilitar la recaída del Hodgkin. (1) Simon B. CA Cancer J Clin 55 (4) 2005

A la pregunta sobre riesgos del hijo respondemos que: (1) ● Nunca se debe concebir después de haber recibido QTP. ● EL hijo tendría, al menos, un 20% de posibilidades de padecer malformaciones. ● No hay mayor tasa de malformaciones entre los hijos de madres que han recibido QTP. ● La inmunosupresión del embarazo podría facilitar la recaída del Hodgkin. (1) Simon B. CA Cancer J Clin 55 (4) 2005

A la pregunta acerca de sus posibilidades de concebir respondemos que: (1) (2) ● Tiene las mismas posibilidades que cualquier otra mujer de su edad. ● No tiene ninguna posibilidad de concebir de forma natural. ● Repetimos niveles hormonales otro par de veces para asegurarnos. ● Le comentamos que tener la menstruación no es sinónimo de fertilidad y que las posibilidades de concebir pueden estar disminuídas. (1) Blumenfeld Z. Ann Oncol 13, 2002 (2) S. D. Fossa & H. Magelsen. Ann. Oncol 15, 2004

A la pregunta acerca de sus posibilidades de concebir respondemos que: (1) (2) ● Tiene las mismas posibilidades que cualquier otra mujer de su edad. ● No tiene ninguna posibilidad de concebir de forma natural. ● Repetimos niveles hormonales otro par de veces para asegurarnos. ● Le comentamos que tener la menstruación no es sinónimo de fertilidad y que las posibilidades de concebir pueden estar disminuídas. (1) Blumenfeld Z. Ann Oncol 13, 2002 (2) S. D. Fossa & H. Magelsen. Ann. Oncol 15, 2004

Evolución. ● Al cabo de dos años de intentarlo, la paciente no consigue quedarse embarazada y ha perdido la regla de forma definitiva. ● Nos consulta acerca de técnicas o procedimientos que puedan ayudarla a concebir. ● Le hablamos de la donación de óvulos y la fertilización “in vitro”. La enviamos a una Unidad de Fertilidad.

Epílogo. ● La paciente nunca logró quedarse embarazada y nunca quiso adoptar. ● Cada vez que la vemos nos preguntamos qué distintas podrían ser las cosas si se hubiera considerado la fertilidad antes de empezar el tratamiento. Pensamos cuál hubiera sido la mejor técnica para ella……

¡Lo habéis hecho muy bien! ¡Gracias!
- Slides: 62