MENGUASAI KEMAHIRAN MENULIS FORMULA DAN PERSAMAAN KIMIA Apabila

MENGUASAI KEMAHIRAN MENULIS FORMULA DAN PERSAMAAN KIMIA

• Apabila disuruh menulis persamaan kimia bagi suatu tindak balas, pelajar-pelajar biasanya akan cuba menceraikan huruf-huruf dalam formula yang diberikan dan cuba menyusun atau mengabungkan semula huruf tersebut untuk menghasilkan sesuatu "formula" yang mereka sendiri pun tidak faham.
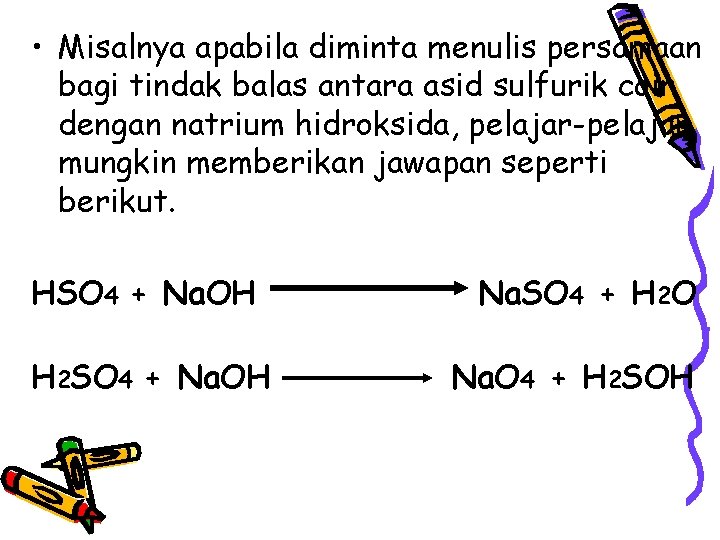
• Misalnya apabila diminta menulis persamaan bagi tindak balas antara asid sulfurik cair dengan natrium hidroksida, pelajar-pelajar mungkin memberikan jawapan seperti berikut. HSO 4 + Na. OH H 2 SO 4 + Na. OH Na. SO 4 + H 2 O Na. O 4 + H 2 SOH

Pelajar-pelajar yang membuat demikian disebabkan mereka tidak faham atau tidak tahu langsung tentang peraturan untuk menulis persamaan kimia.

PERATURAN UNTUK MENULIS PERSAMAAN KIMIA

1. Meramalkan hasil tindak balas eg, Asid + Alkali Garam + air maka, asid sulfurik cair (asid) + natrium hidroksida (alkali) natrium sulfat (garam) + air Sekiranya anda tidak ada pengetahuan langsung tentang sesuatu tindak balas, maka adalah tidak mungkin untuk meramalkan apakah hasil tindak balas itu. Seterusnya anda tidak dapat menulis persamaan kimia tindak balas tersebut.

2. Menulis formula yang betul (a) Setiap unsur, molekul, sebatian atau ion mempunyai formula yang tersendiri. Formula tersebut adalah tetap dan tidak boleh diubah. Eg, formula bagi natrium hidroksida ialah Na. OH, maka anda tidak boleh menulis formulanya sebagai Na. H, Na. OOH, Na(OH)2 dan sebagainya. Anda perlu menghafalkan formula bagi beberapa unsur, molekul dan ion yang umum.

(b) Formula bagi sebatian ionik Jumlah cas dalam formula bagi sesuatu sebatian ionik adalah neutral. Jadi kita boleh menentukan formula bagi sesuatu sebatian ionik, misalnya magnesium klorida, seperti berikut.

Magnesium klorida Mg 2+ Cl- <----- Tuliskan formula bagi setiap 1 2 ion. Tuliskan bilangan cas secara bersilang Mg. Cl 2<------ Jadi formula tersebut terdiri daripada 1 ion Mg 2+ dan 2 ion Cl-.

• Perhatian : • Nombor yang mewakili bilangan ion ditulis pada sebelah kanan, di bahagian bawah ion tersebut. • Nombor 1 tidak perlu dituliskan. • Misalnya, Na 2 SO 4 (2 ion natrium dan 1 ion sulfat) Al 2 O 3 (2 ion Aluminium dan 3 ion oksigen) Ba(OH)2 (1 ion barium dan 2 ion hidroksida)

3. Menulis persamaan kimia yang seimbang. asid sulfurik + natrium hidroksida natrium sulfat + air H 2 SO 4 + Na. OH Na 2 SO 4 + H 2 O

• Persamaan tadi belum lengkap. Suatu persamaan mesti seimbang, iaitu jumlah atom setiap unsur di sebelah kiri mesti sama dengan yang di sebelah kanan. • H 2 SO 4 + Na. OH Na 2 SO 4 + H 2 O • (kiri =1 Na) (kanan = 2 Na) Tidak seimbang

• Jadi, tambahkan 2 di depan Na. OH supaya bilangan Na sama dengan bilangan Na di sebelah kanan dan semak bilangan atom bagi setiap unsur semula. • H 2 SO 4 + 2 Na. OH Na 2 SO 4 + H 2 O (kiri = 2 H + 2 H = 4 H) (kanan = 2 H) Tidak seimbang • Tambahkan 2 di depan H 2 O dan semak bilangan atom bagi setiap unsur semula. Anda akan mendapati persamaan sudah seimbang. • H 2 SO 4 + 2 Na. OH Na 2 SO 4 + 2 H 2 O

• Semak : Unsur H S Na O Kiri 4 1 2 6 Kanan 4 1 2 6

• Sesuatu persamaan kimia yang seimbang perlu juga dilabelkan keadaan fiziknya. Berikut ialah beberapa simbol yang digunakan. • Pepejal (p), Cecair (ce) , Gas (g) , Larutan akueus-- ak • Maka, persamaan kimia yang lengkap bagi tindak balas di antara asid sulfurik dan natrium hidroksida ialah : • H 2 SO 4(ak) + 2 Na. OH(ak) • Na 2 SO 4(ak) + 2 H 2 O(ce)

TAMAT
- Slides: 16