Medikamentse Behandlungsoptionen bei Patienten mit einer Suchterkrankung Teil

Medikamentöse Behandlungsoptionen bei Patienten mit einer Suchterkrankung Teil II Medikamenten- und Opioidabhängigkeit Lars Stark; 1. März 2016; l. stark@arud. ch
Arud Zentren für Suchtmedizin Sämtliche Drogen Kokain – Alkohol – Heroin – Cannabis – Medikamente – Designerdrogen – Tabak – Mischkonsum Fachleute Konsumierende Angehörige, Umfeld www. arud. ch aus einer Hand: • Information, Beratung, Abklärung, Behandlung • ambulante Therapien: Einzel-, Familien-, Gruppentherapien • psychiatrische Behandlungen • medizinische Behandlungen • Sozialarbeit Ärzt. Innen, Psycholog. Inne n, Sozialdienste, Beratungen, Justiz, usw • Kooperationsangebote Checkpoint Zürich, Drogeninformationszentrum Zürich, Beratungsstelle für Angehörige Personalverantwortliche, Vorgesetzte 058 360 50 00 Arbeitgeber

Inhalt • Behandlungsansätze Benzodiazepine - Einführung - Ansätze bei Abhängigkeit • Substitution Opioidabhängigkeit - Substitutionsmittel - Off-Lable-Substanzen • Schmerzmittelabhängigkeit - Schmerzmittel und iatrogene Opioidabhängigkeit

Benzodiazepine: Therapieprinzipien Wirkungssprktrum Benzodiazepine • Anxiolytisch: Angst, Erregungszustände • Hypnotisch/sedierend: Schlafstörung • Muskelrelaxierend: Spasmen, motorische Spannungen • Antikonvulsiv: Epileptische Ereignisse, Alkoholentzug • Amnestisch: Prämedikation Operation Wirkung ist schnell, zuverlässig, gute Verträglichkeit, grosse therapeutische Breite

Toleranzentwicklung Eine Dosissteigerung zur Wirkungserhaltung ist notwendig. Eine Toleranzentwicklung ist bekannt gegenüber den Wirkungen: • sedierend > myorelaxierend > antikonvulsiv • Bei der Anxiolyse tritt selten eine Toleranzentwicklung auf. Royal Collage of Psychiatrists: Verordnung nur auf kurzfristigen Gebrauch empfohlen (2 -4 Wochen) USA: Nur bei Sedation Vorsicht geboten

Kreuztoleranz • Bei längerem Alkoholkonsum sind zur wirksamen Anxiolyse und/oder Sedierung höhere Dosen eines Benzodiazepins notwendig. • Eine Kreuztoleranz wird auch bei anderen Substanzen vermutet: GHB, GBL, „ 3 Z“ (Zolpidem/Stilnox , Zopiclon/Imovane , Zaleplon/Sonata ), Opioide, Baclofen (Lioresal ).

Abhängigkeit • Epidemiologische Daten kontrovers (Selection Bias) • Risiko einer Abhängigkeit erhöht bei - längerer Behandlung - hoher Dosis ? kurz wirksamen Substanzen • Absetz- und Entzugssymptomen: Nach 4 -monatiger Behandlung in therap. Dosis damit zu rechnen. Bereits nach 4 Wochen möglich (individuell)

Low-Dose-Abhängigkeit (therapeutic-dosedependency): Langzeitbehandlung zu therapeutischer Dosis, ohne Dosissteigerung High-Dose-Abhängigkeit: Mehrfaches der Maximaldosis Gefährdete Patientengruppen: - Alkohol- und Drogenabhängigkeit - chronische körperliche Krankheiten (Schmerzen) - Persönlichkeitsstörungen - Schlafstörungen

Eisberg-Phänomen Sichtbare Probleme Nicht stark Beeinträchtigende Probleme

Benzodiazepine prescribing to the Swiss adult population: Results from a national survey of community pharmacies (Petitjean et al. 2007) Ziel der Studie: Prävalenz von Benzodiazepingebrauch in der Schweiz Verschreibungen von 520 000 Patienten während 6 Monaten untersucht 9, 1 % mindestens 1 Benzo-Verschreibung in 6 Monaten Davon 44% Einzelverschreibung für kurze Zeit, niedrig/normal dosiert; 56% Langzeitverschreibung; 1, 6% in sehr hoher Dosis

Entzugssymptomatik Reboundsyndrom: Unruhe, Angst, Schlaflosigkeit - bis einige Tage Rückfallsyndrom: wiederkehrende Angstsymptomatik - längere Zeit anhaltend Eigentliches Entzugssymptom: Symptome, die vor Verordnung nicht vorhanden waren - Beginn 2 -10 Tage nach Absetzen - Dauer 5 -15 Tage - Protrahierte Verläufe: bis 6 Monate

Leichte Entzugssymptome • Angst, innere Unruhe • Muskelverspannungen • Schwitzen • Übelkeit, Erbrechen • Kopfschmerzen • Reizbarkeit, Irritabilität • Tremor • Schlaflosigkeit

Schwere Entzugssymptome • Verwirrtheit • Depersonalisation • Psychose/Delir • Ängste/Depressivität • Epileptische Ereignisse • Faszikulationen • Reizüberempfindlichkeit (Geräusche, Licht, Geruch, Berührung) • Dysästhesien • Bewegungsstörungen • Tremor

Abbau/Entzug: Abbauschemata Schädlicher Gebrauch absetzen ohne Bedenken Abhängigkeit oder bei zu erwartenden Absetzsymptomen allmähliche ausschleichen Ambulante Behandlung: Abbauzeit 4 -10 Wochen (Bélanger et al. 2005) Beginn: wöchentlich -10% – -25% der Ausgangsdosis Gegen Ende: kleinere Schritte AWMF-Leitlinien: www. uni-duesseldorf. de/AWMF/II/076 -009. htm

Abbauschema (II) Grundregeln: (J Clin Psychiatry 2005; 66 (suppl 2)) Arzt – Patient: Gemeinsam Abbau und Schritte besprechen Aufklärung über Dauer, Symptome, Gefahr abrupten Absetzens Mindestzeit 4 Wochen (von therapeutischer Dosis) Maximal: Reduktion um ¼ der Tagesdosis / Woche
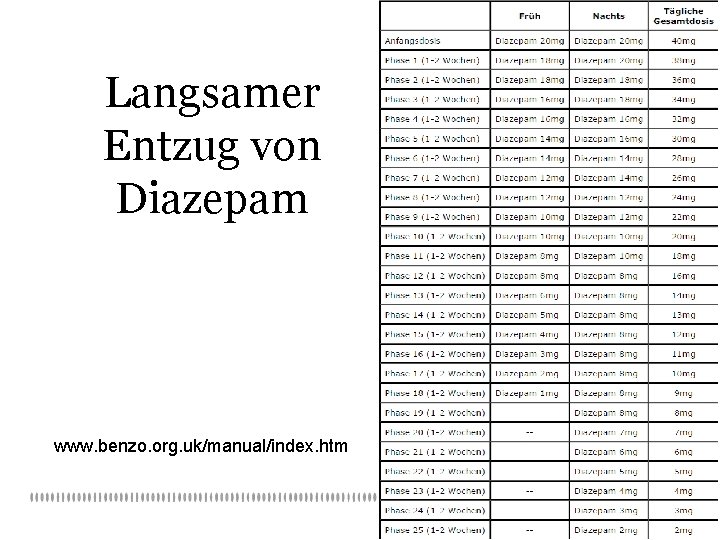
Langsamer Entzug von Diazepam www. benzo. org. uk/manual/index. htm

Ambulante Erfahrungen: abgestimmter Abbau 1. Patient als Experte: Vorgehen gemeinsam und individuell festgelegt, Geschwindigkeit änderbar 2. Unterstützende medikamentöse Behandlung: SSRI, Antiepileptikum 3. Überlappende Umstellung auf Diazepam oder Clonazepam 4. Langsamer Abbau, Pausen möglich. Bsp. Diazepam: • Dosis > 40 mg/die: -10 mg-Schritte alle 1 -2 Wochen • Dosis > 20 mg/die: -5 mg-Schritte alle 1 -2 Wochen • Dosis > 10 mg/die: -2 mg-Schritte alle 1 -2 Wochen • Ab 10 mg: -1 mg-Schritte alle 1 -2 Wochen

Umrechnungstabelle (Auswahl) Substanz Äquivalenzdosis Alprazolam (Xanax®) 0, 5 mg Bromazepam (Lexotanil®) 6 mg Chlordiazepoxid (Librium®) 20 mg Clonazepam (Rivotril®) 0, 5 mg Diazepam (Valium®, Stesolid®) 10 mg Flunitrazepam (Rohypnol®) 0, 5 mg Flurazepam (Dalmadorm®) 30 mg Lorazepam (Temesta®) 2 mg Midazolam (Dormicum®) 7, 5 mg Oxazepam (Seresta®) 25 mg Triazolam (Halcion®) 0, 5 mg
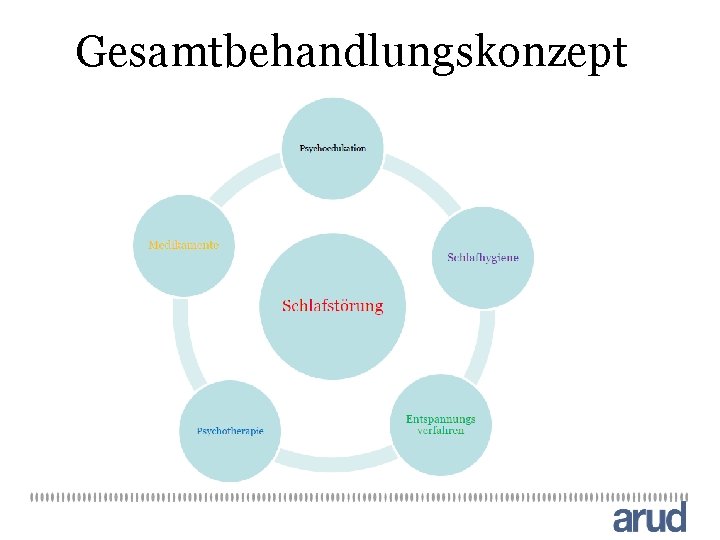
Gesamtbehandlungskonzept

Gibt es ein Benzodiazepin. Mangel-Syndrom? • Diabetes: Insulinmangel-Syndrom • Parkinsonismus: Dopaminmangel-Syndrom • Depression: Serotoninmangel-Syndrom • Opioidabhängigkeit: Morphinmangel-Syndrom ? Benzodiazepin-Mangelsyndrom

Tal Weizman et al. : Australian and New Zealand Journal of Psychiatry 2003; 37: 458 -463 Treatment of benzodiazepine dependence in methadone maintenance treatment patients: a comparison of two therapeutic modalities Objective: • Clonazepam (Rivotril®)-Entzug und Clonazepam. Substitution in offener klinischen Studie untersucht • 66 Personen eingeschlossen: Methadon-substituiert und BZD-abhängig ( 3 Jahre) und nach mehreren BZDEntzügen

Tal Weizman et al. : Australian and New Zealand Journal of Psychiatry 2003; 37: 458 -463 Schlussfolgerung • Benzodiazepin-Erhaltungsstrategie mit Clonazepam ist sinnvolle BZD-Behandlungsform bei dieser Patientengruppe • Psychiatrische Komorbidität kann eine wichtige Rolle bei der Wahl einer angemessenen Behandlungsform spielen

Faktoren für Schwere des Entzugs • Dauer Einnahme (Murphy et Tyrer, 1991): pos. Korrelat • Dosis (Lamb et Griffiths, 1985): pos. Korrelat • Eliminationshalbwertszeit: neg. Korrelat • Allgemeinzustand (Poser 1996): neg. Korrelat • Ko-Abhängigkeit und Ko-Morbidität: Pos. Korrelat Aber: Erfolg der Entzugsbehandlung korreliert nicht mit Schwere des Entzugs (Schweizer et Rickels, 1998) Abstinenzraten nach 1 Jahr: 30 -50%

Entzugssymptomatik vs. Rückkehr einer Angstsymptomatik „Gemeinsame“ Symptome: • Angst, Konzentrationsstörung • Unruhe, Schlafstörung Zeitunterschied Dosisschwankungen – Symptome: • Entzugssymptome: nach wenigen Tagen am stärksten, dann abnehmend • Licht- und Lärmempfindlichkeit • Tinitus, Tremor, Gefühlsstörungen • Gefühl elektr. Entladungen, Myoklonien, Krampfanfälle • Rückfall Angstsymptome: nach wenigen Tagen beginnend, Frequenz und Stärke nimmt zu

Benzodiazepinabhängigkeit und Opioidabhängigkeit • Kleine aber wichtige Untergruppe von Benzodiazepinabhängigen • Häufig Hochdosisabhängigkeit Unsicherheit • Methadondosis oft Einfluss auf Gebrauch von Benzodiazepin: Methadon hoch genug (> 80 mg) aufdosieren • Häufig mehrfache frustrane Benzodiazepin-Entzüge in Anamnese

Differenzierte Verschreibung Opioide
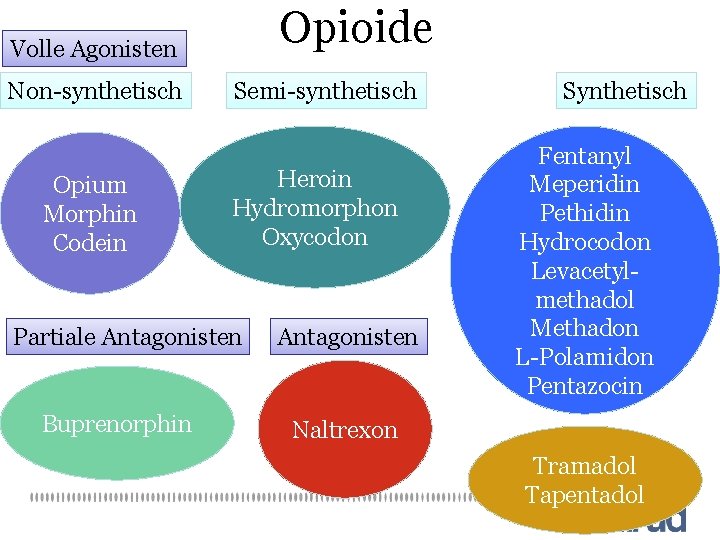
Opioide Volle Agonisten Non-synthetisch Opium Morphin Codein Semi-synthetisch Heroin Hydromorphon Oxycodon Partiale Antagonisten Buprenorphin Antagonisten Synthetisch Fentanyl Meperidin Pethidin Hydrocodon Levacetylmethadol Methadon L-Polamidon Pentazocin Naltrexon Tramadol Tapentadol

Opioide: Pharmakologie • 3 Hauptfamilien von Opioidrezeptoren (μ, κ, σ) • Agonisten wie Morphin, Heroin, Methadon, Polamidon μ-System • Partielle Agonisten wie Buprenorphin auch partieller Antagonist auf μ- und κ-Rezeptoren • Lokalisation von Opioid-Rezeptoren und Peptide: ZNS, PNS und Gastro-Intestinal-Trakt • Opioid-Rezeptor: Inhibitorisch (-): Freisetzung einiger Neurotransmitter (5 -HAT, GABA, Glutamat, Acetylcholin. Ermöglichen Freisetzung von Dopamin

Entzugssymptome • Nicht lebensbedrohlich • Beginn: 6 – 24 (+) Std. nach der letzten Einnahme • Höhepunkt: Bei etwa 24 – 48 Std. • Nachlassende Symptomatik: 5 – 7 Tage ! Existenz einer langwierigen Phase von Wochen oder Monaten mit reduziertem Wohlbefinden, Schlaflosigkeit, Dysthymie und Craving! • Methadonentzug: Beginn nach 24 – 48 Std. , manchmal >; Dauer 10 – 20 Tage

Entzugssymptome Objektiv Subjektiv • Gähnen • Schlaflosigkeit • Tränenfluss, Mydriasis • Schwitzen • Blähungen, Krämpfe, Bauchschmerzen • „Schnupfen“: Rhinorhoe, Niessen • Gelenk- und Muskelschmerzen • Tremor • Craving • Piloerektion „Gänsehaut“ • Warm-Kalt-Empfinden • Durchfall, Erbrechen • Appetitmangel, Übelkeit • Tachykardie, Hypertonie • Unruhe, Ängstlichkeit
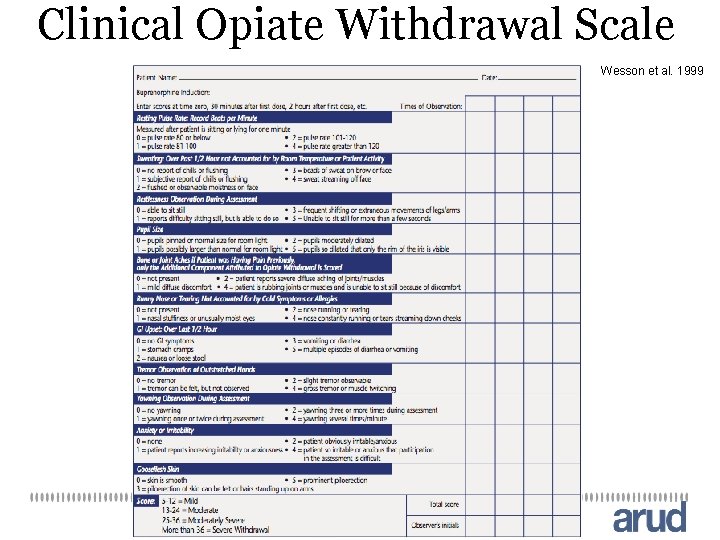
Clinical Opiate Withdrawal Scale Wesson et al. 1999
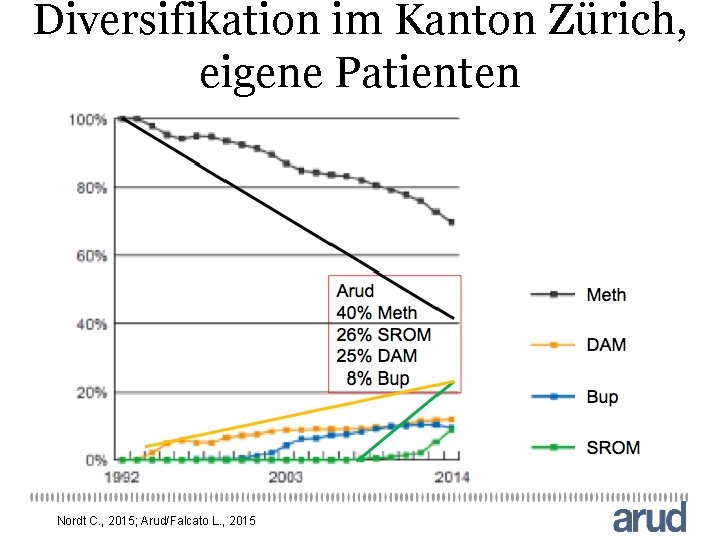
Diversifikation im Kanton Zürich, eigene Patienten Nordt C. , 2015; Arud/Falcato L. , 2015

Risiko-Profile und Indikationen R/S-Methadon R-Methadon (Polamidon) • Effektiv • Bewährt (am besten erforscht) • Weniger QTc. Verlängerung • Lineare Dosis-Wirkkurve • Voller Agonist • Razemat: voller Agonist, Interaktionen (Cy. P 450) • Flüssig • Kostengünstig • Teuer • QTc-Verlängerung Wikipedia

Risiko-Profile und Indikationen II Buprenorphin • Effektiv SROM (Retardiertes Morphin) • Ceiling Effekt • Effektiv • Partieller Agonist • Weniger QTc. Verlängerung • Kaum Interaktionen (Cy. P 450) • Razemat: voller Agonist, Interaktionen (Cy. P 450) • Weniger Nebenwirkungen • Flüssig • Teurer Wikipedia

Methadon • Hohe Bioverfügbarkeit (ca. 80%) • Plasmapeak nach 3 -4 stunden • Plasmahalbwertszeit ca. 25 Std. (13 – 47 Std. ) • Steady-State nach ca. 1 Woche • Metabolisierung: Leber, Cytochrome P 450 - CYP 3 A 4, CYP 2 B 6 hauptsächlich - CYP 2 D 6, CYP 1 A 2, CYP 2 C 9, CYP 2 C 19 genetisch variabel - CYP 3 A 4: baut 50% der Medikamente ab

Methadon: Nebenwirkungen • Atemdepression • Schwitzen Kurzfristig Langfristig • Herzreizleitungsstörung (QTc-Verlängerung) • Verlangsamte Magen-Darm-Passage –> Obstipation, Übelkeit • Testosteronmangel, Gynäkomastie, Amenorrhoe, Galaktorrhoe, Impotenz, Osteoporose, Dysphorie • Hyperalgesie (Doverty M. et al. , 2001) • Kognitive und psychische Defizite (Darke S. et al. 2000) • Hinweise auf strukturelle und funktionale Störungen des Gehirns (Andersen et al. , 2011)

Buprenorphin (Subutex®) • Bioverfügbarkeit: sublingual 50 -65%; peroral 25% • Kurze Plasmahalbwertszeit, aber lange Halbwertszeit in der Rezeptorbindung • Hohe Affinität an Morphinrezeptor: stärkere Bindung als Heroin und Methadon • Flache Dosis-Wirkungskurve. Dosen über 32 mg/die: Ceiling-Effekt • Metabolisierung: Leber, günstiger bei CYP 450 - Cy. P 45 o. CYP 3 A 4
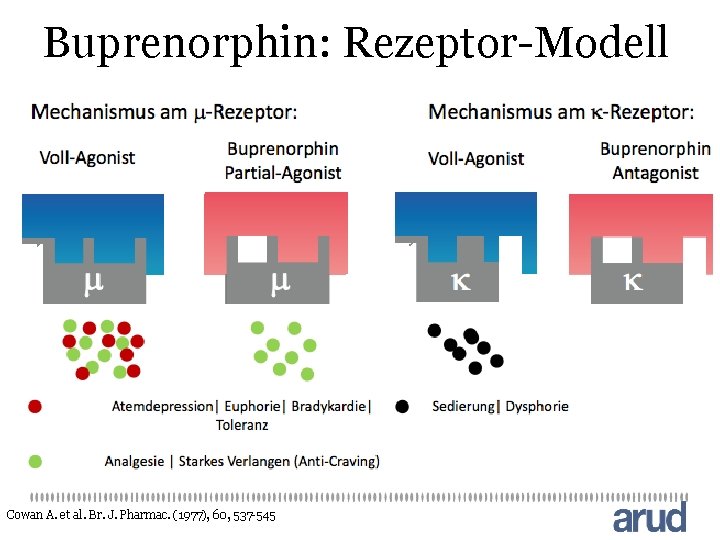
Buprenorphin: Rezeptor-Modell Cowan A. et al. Br. J. Pharmac. (1977), 60, 537 -545

SROM Slow Release Oral Morphine • Retardiert: Plasmaspiegel +/- stabil über 24 Std. , einmal tägliche Einnahme möglich • Kurze Plasmahalbwertszeit, Akkumulationsgefahr bei Induktion gering • Vergleichsstudien mit Methadon: - Gleichwertige Effektivität - Hinweise auf höhere Patientenzufriedenheit für SROM - Weniger Nebenwirkungen: Verstopfung; Schwitzen; Potenzstörungen; Libido; Schlaf; Amenorrhoe, Osteoporose Beck T. et al. 2013

R-Methadon (L-Polamidon) • Aktive Form • Agonist μ-Opioid-Rezeptor (IC 50 = 3 -7 μM) S-Methadon: Schwacher Agonist, (IC 50 = 26 -28 μM) • Nebenwirkung QTc-Verlängerung durch Methadon: - Blockade h. ERG-Kanal (repolarisation cardiac cell) verlängert QTc-Zeit -> Risiko einer Tachyarrhythmie, Torsade de Pointe - S-Methadon 3, 5 mal potenter für h. ERG-Kanal-Blockade als R-Methadon Eap et al. , 2007; Lin et al. , 2000 • Slow Metabolizer von CYP 2 B 6: Konzentration von S-Methadon -> sehr hohes Risiko für QTc. Verlängerung
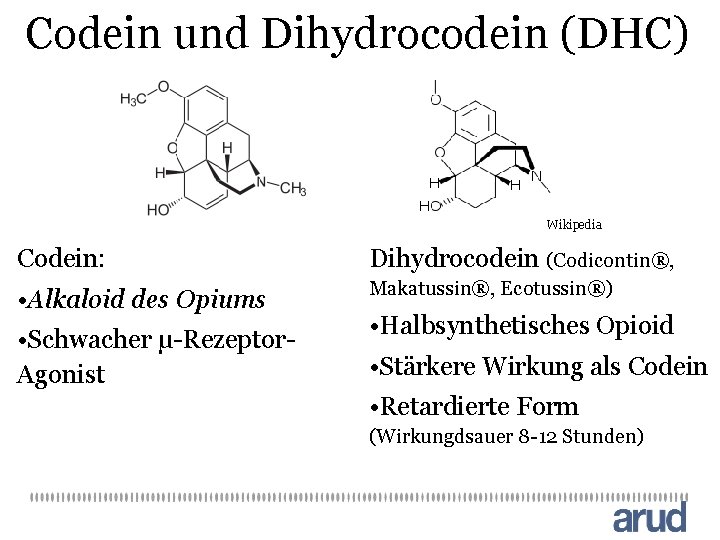
Codein und Dihydrocodein (DHC) Wikipedia Codein: Dihydrocodein (Codicontin®, • Alkaloid des Opiums Makatussin®, Ecotussin®) • Schwacher μ-Rezeptor. Agonist • Halbsynthetisches Opioid • Stärkere Wirkung als Codein • Retardierte Form (Wirkungdsauer 8 -12 Stunden)

Codein und Dihydrocodein (DHC) • Einnahme mehrmals täglich (mindestens 2 x/Tag) • Indikation: Analgetikum, Antitussivum • Als Substitutionsmittel: Im Einzelfall, Off-Lable use • Metabolisierung: Hoher First-Pass-Effekt –> aktiver Metaboliten mit starker individueller Variabilität • Nebenwirkungen: Sedierung, Juckreiz, Kopfschmerzen • 360 mg. DHC ≈ 90 mg Morphium per os (4: 1 bis 6: 1)

Opioidabhängigkeit nach iatrogener Schmerzmittelbehandlung • Länger dauernde Schmerzbehandlung mit Opioiden • Risiko einer Abhängigkeit erhöht bei - Schwierigkeiten Familie/Arbeitsplatz - Abnahme der schmerzstillenden Wirkung - Zunahme Nebenwirkungen - Eigenständige (nicht verordnete) Dosiserhöhung - Wunsch nach kurzwirksamen Opioiden - Verlieren von Rezepten, Versäumnis Termine - Häufiger Arztwechsel

Ausführlich: Vortrag 23. 03. 2016 https: //www. fosumos. ch/fosumos/index. php/de/referate-53
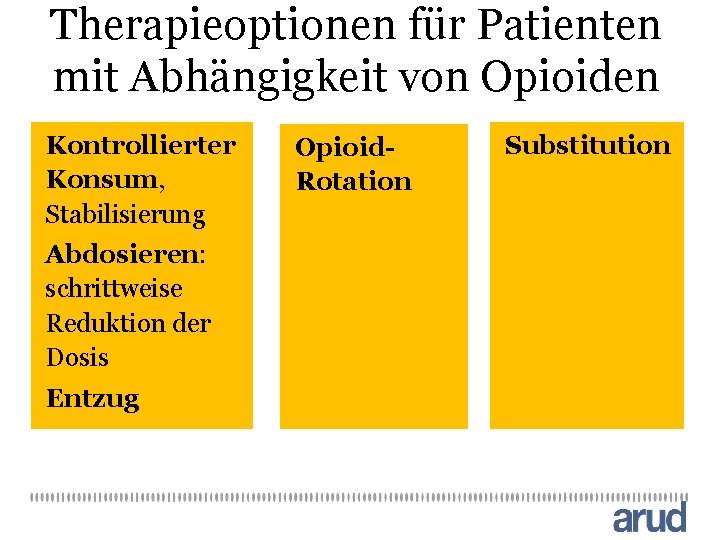
Therapieoptionen für Patienten mit Abhängigkeit von Opioiden Kontrollierter Konsum, Stabilisierung Abdosieren: schrittweise Reduktion der Dosis Entzug Opioid. Rotation Substitution
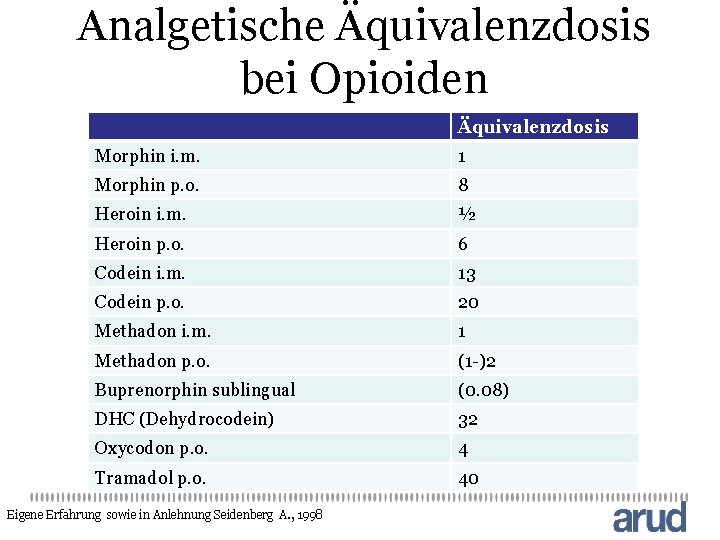
Analgetische Äquivalenzdosis bei Opioiden Äquivalenzdosis Morphin i. m. 1 Morphin p. o. 8 Heroin i. m. ½ Heroin p. o. 6 Codein i. m. 13 Codein p. o. 20 Methadon i. m. 1 Methadon p. o. (1 -)2 Buprenorphin sublingual (0. 08) DHC (Dehydrocodein) 32 Oxycodon p. o. 4 Tramadol p. o. 40 Eigene Erfahrung sowie in Anlehnung Seidenberg A. , 1998
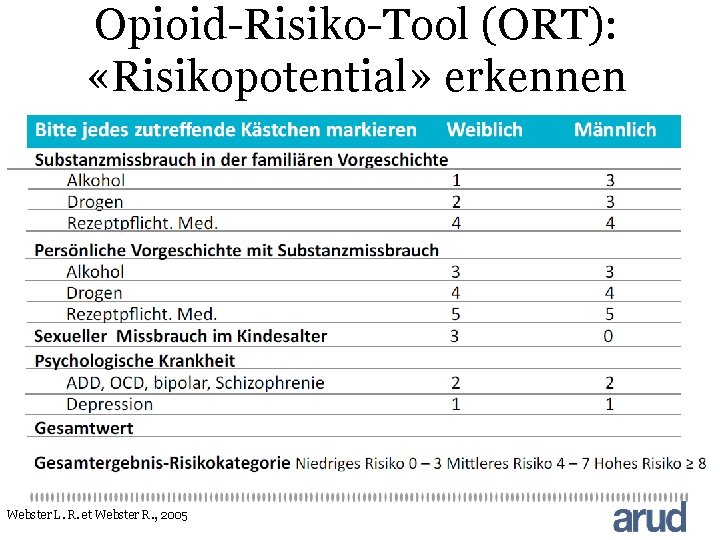
Opioid-Risiko-Tool (ORT): «Risikopotential» erkennen Webster L. R. et Webster R. , 2005

Danke für die Aufmerksamkeit! Fragen?
- Slides: 48