Medicinski fakultet Univerzitet u Beogradu Univerzitetska deja bolnica

Medicinski fakultet, Univerzitet u Beogradu. Univerzitetska dečja bolnica Beograd. Evropsko udruženje za razvoj perinatalne i pedijatrijske farmakologije Your Logo
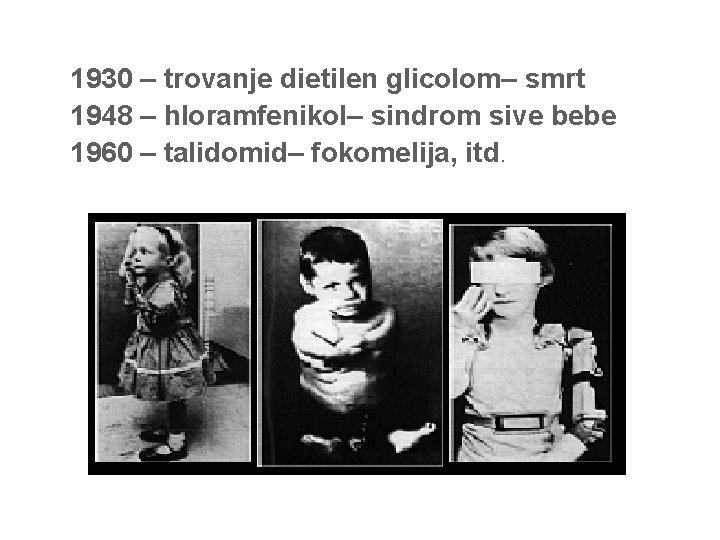
• 1930 – trovanje dietilen glicolom– smrt • 1948 – hloramfenikol– sindrom sive bebe • 1960 – talidomid– fokomelija, itd.

LICENCIRANJE LEKOVA REGULATIVA Efikasnost PROFIT ETIKA Kvalitet Bezbednost Your own footer Your Logo
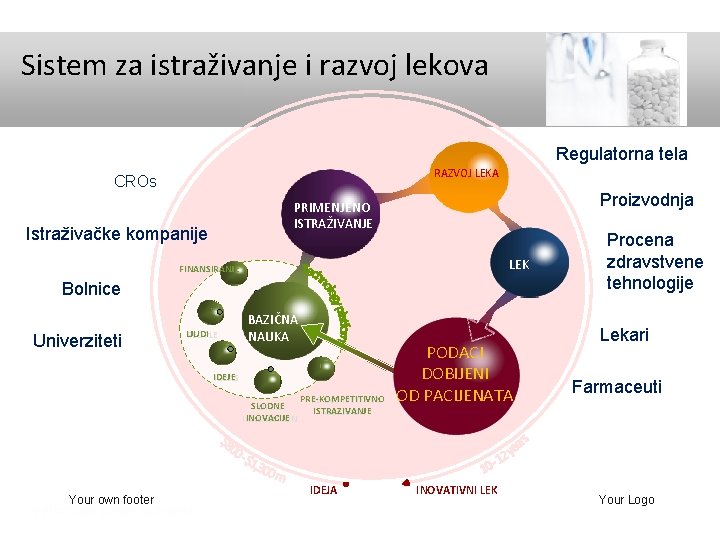
Sistem za istraživanje i razvoj lekova Regulatorna tela RAZVOJ LEKA CROs Proizvodnja PRIMENJENO ISTRAŽIVANJE Istraživačke kompanije LEK FINANSIRANJE FUNDING Bolnice Univerziteti LJUDI PEOPLE BAZIČNA NAUKA IDEJE IDEAS SLODNE OPEN INOVACIJE INNOVATION Your own footer PPP=Public private partnership PRE-KOMPETITIVNO PRE-COMPETITIVE ISTRAZIVANJE RESEARCH IDEJA PODACI DOBIJENI OD PACIJENATA INOVATIVNI LEK Procena zdravstvene tehnologije Lekari Farmaceuti Your Logo
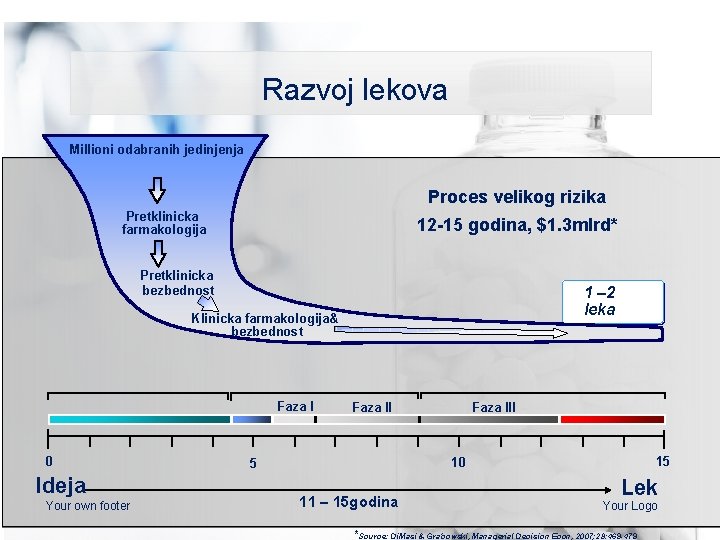
Razvoj lekova Millioni odabranih jedinjenja Proces velikog rizika Pretklinicka farmakologija 12 -15 godina, $1. 3 mlrd* Pretklinicka bezbednost 1 – 2 leka Klinicka farmakologija& bezbednost Faza I 0 Ideja Your own footer Faza III 15 10 5 11 – 15 godina Lek Your Logo *Source: Di. Masi & Grabowski, Managerial Decision Econ, 2007; 28: 469 -479
Sažetak karakteristika lekova (Sm. PC) Uputstvo za pacijenta (PIL) • Agencija za lekove i medicinska sredstva Republike Srbije www. alims. gov. rs • Evropska agencija za lekove www. ema. europa. eu • Agencija za lekove Velike Britanije www. medicines. org. uk

SAŽETAK KARAKTERISTIKA LEKA 1. 2. 3. 4. XXXXXXX, kapi za oči, rastvor, 5 mg/ml, 5 ml rastvora u bočici sa polietilenskom kapaljkom, Proizvođač: YYYYYY Consumer Health SA Аdresa: XXXXX Podnosilac zahteva: YYYYYY Consumer Health SA Adresa: XXXX IME LEKA KVALITATIVNI I KVANTITATIVNI SASTAV FARMACEUTSKI OBLIK KLINIČKI PODACI 4. 1 TERAPIJSKE INDIKACIJE 4. 2 DOZIRANJE I NAČIN PRIMENE 4. 3 KONTRAINDIKACIJE 4. 4 POSEBNA UPOZORENJA I MERE OPREZA 4. 5 INTERAKCIJE SA DRUGIM LEKOVIMA 4. 6 PRIMENA U PERIODU TRUDNOĆE I DOJENJA 4. 7 UTICAJ NA PSIHOFIZIČKE SPOSOBNOSTI 4. 8 NEŽELJENA DEJSTVA 4. 9 PREDOZIRANJE KO JE PROIZVOĐAČ AKTIVNE SUPSTANCE? 5. FARMAKOLOŠKI PODACI 5. 1 FARMAKODINAMSKI PODACI 5. 2 FARMAKOKINETIČKI PODACI 5. 3 PRETKLINIČKI PODACI O BEZBEDNOSTI LEKA GENERIKA ILI ORIGINAL? BIOEKVIVALENCA/STUDIJE EFIKASNOSTI 6. FARMACEUTSKI PODACI? 6. 1 LISTA POMOĆNIH SUPSTANCI 6. 2 INKOMPATIBILNOST 6. 3 ROK UPOTREBE 6. 4 POSEBNE MERE UPOZORENJA PRI ČUVANJU 6. 5 PRIRODA I SADRŽAJ KONTAKTNE AMBALAŽE 6. 6 POSEBNE MERE OPREZA PRI ODLAGANJU MATERIJALA KOJI TREBA ODBACITI NAKON PRIMENE LEKA ALIMS NEMA KAPACITETA DA VRŠI INSPEKCIJU CRO U DRUGIM ZEMLJAMA! 7. 8. 9. 10. NOSILAC DOZVOLE BROJ PRVE DOZVOLE I OBNOVE DOZVOLE DATUM REVIZIJE TEKSTA
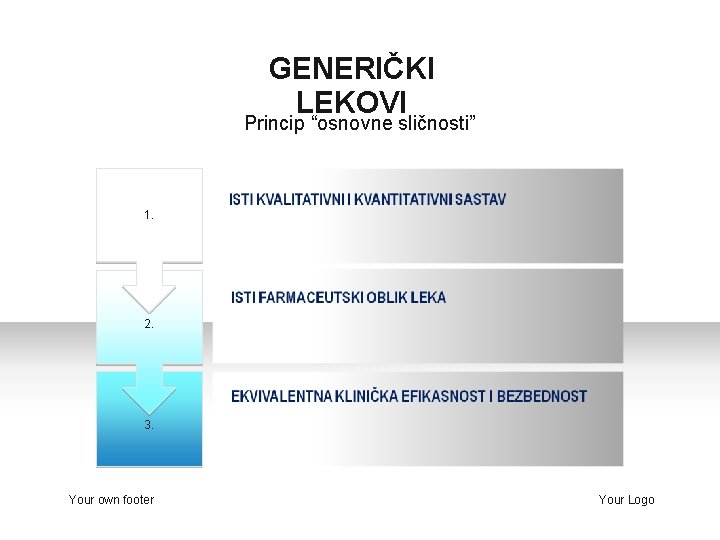
GENERIČKI LEKOVI Princip “osnovne sličnosti” 1. 2. 3. Your own footer Your Logo

ISTI KVALITATIVNI I KVANTITATIVNI SASTAV üODNOSI SE SAMO NA AKTIVNU SUPSTANCU üSASTAV POMOĆNIH SUPSTANCI MOŽE DA SE RAZLIKUJE ? ! Ekscipijensi – smatraju se inertnim supstancama propilen glikol – hiperosmolalitet benzil alkohol – toksičnost sorbitol – dijareja, intestinalna pneumatoza Your own footer Your Logo

Neonatalna izloženost ekscipijensima u Evropi- ESNEE • Evropska studija neonatalne izloženosti ekscipijensima uključuje 27 evropskih zemalja, Srbiju, Švajcarsku, Norvešku, i Island. • Cilj studije: Identifikovati individualnu izloženost ekscipijensima kod neonatusa i istaći potrebe i mogućnosti za proizvodnju zamena zasnovanih na statusu procene rizika svakog ekscipijensa. Your Logo

ISTI FARMACEUTSKI OBLIK üGalenske formule mogu biti različite üRazličite formulacije nekog leka za oralnu upotrebu sa brzim oslobađanjem smatraju se istim farmaceutskim oblikom! üNpr. tablete umesto kapsula i obrnuto üFilm tablete se ne smeju lomiti!! Your Logo

EKVIVALENTNA KLINIČKA EFIKASNOST I BEZBEDNOST üKoncentracija aktivne supstance mora imati ekvivalentni klinički efekat üZa lekove za sistemsko dejstvo određuje se bioekvivalentnost üDokumentacija bez bioekvivalence se odobrava u slučajevima gde je aktivna supstanca već rastvorena (oralni parenteralni rastvori) üZa generičke lekove nije potrebno dokazati terapijsku ekvivalentnost Your Logo
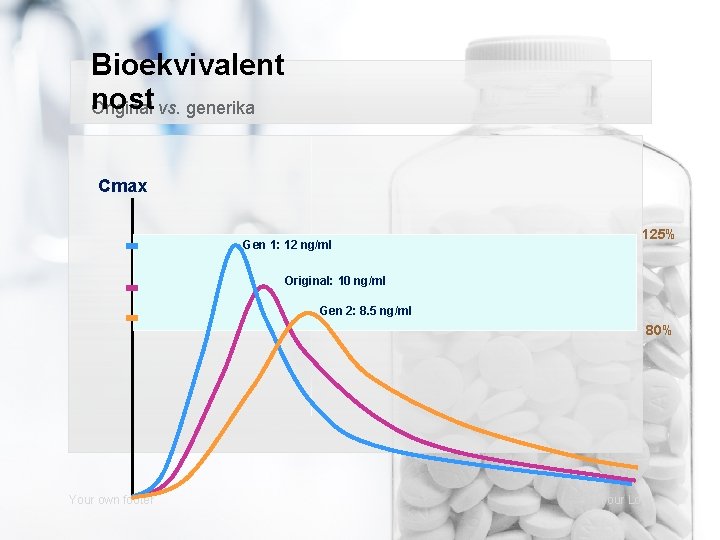
Bioekvivalent nost Original vs. generika Cmax 125% Gen 1: 12 ng/ml Original: 10 ng/ml Gen 2: 8. 5 ng/ml Cmax 80% Your own footer Your Logo
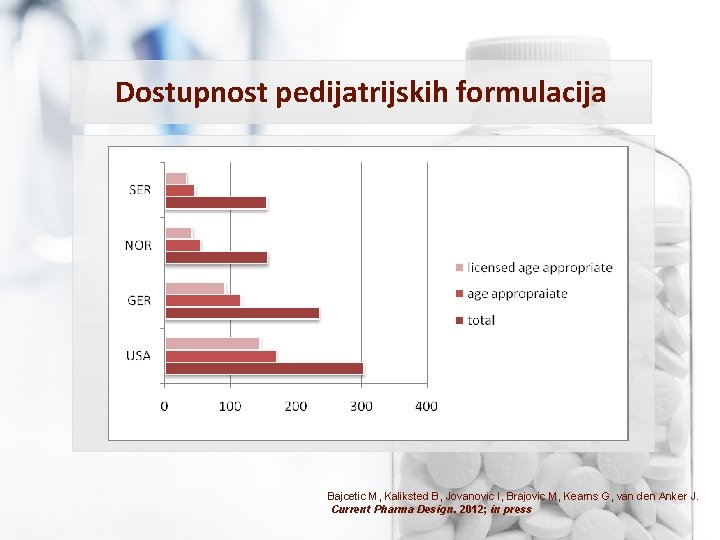
Dostupnost pedijatrijskih formulacija Bajcetic M, Kaliksted B, Jovanovic I, Brajovic M, Kearns G, van den Anker J. Current Pharma Design. 2012; in press

Extempore formulacije ? ! Potentnost aktivnih supstanci ? ! Bioraspoloživost ? ! Fizička i hemijska stabilnost pod normalnim uslovima i u toku čuvanja ? ! Sterilnost i pirogenost – za i. v. formulacije lekova ? ! Ekscipijensi Your Logo
Razviti originalne formulacije prikladne uzrastu
- Slides: 16