MEDICAMENTOS BIOSIMILARES aclarando conceptos Vol 24 n 3

MEDICAMENTOS BIOSIMILARES: aclarando conceptos Vol. 24, nº 3 - 2016 http: //www. osakidetza. euskadi. net

Sumario • Introducción • ¿Qué es un medicamento biológico? • ¿Qué es un medicamento biosimilar? • Diferencias entre medicamentos genéricos y biosimilares • ¿Son los biosimilares igual de seguros que los medicamentos de referencia? • ¿Se pueden extrapolar las indicaciones? • ¿Son intercambiables? • Conclusiones http: //www. osakidetza. euskadi. net

Introducción • La biotecnología ha hecho posible el desarrollo de nuevos medicamentos para enfermedades graves • Los primeros medicamentos biotecnológicos se aprobaron en los 80 y ahora están caducando sus patentes • En 2014 los medicamentos biológicos supusieron el 27% de las ventas en Europa • Los biosimilares pueden suponer una importante aportación a la sostenibilidad del sistema sanitario http: //www. osakidetza. euskadi. net

¿Qué es un medicamento biológico? • Contiene principios activos derivados de una fuente biológica (tejidos, microorganismos, fluidos, etc) u obtenidos por biosíntesis de células vegetales, animales, bacterias, virus, etc. mediante manipulación genética • La complejidad en su producción puede provocar variabilidad en las moléculas de un mismo principio activo • “El proceso es el producto” • Se autorizan por la Agencia Europea del Medicamento (EMA) mediante un procedimiento centralizado y con un marco regulatorio específico http: //www. osakidetza. euskadi. net

¿Qué es un medicamento biosimilar? • Es un medicamento biológico similar a uno ya comercializado, cuya patente ha caducado • El principio activo es esencialmente la misma sustancia biológica que el de referencia, pero pueden existir ligeras diferencias por la complejidad de su naturaleza y método de producción • La EMA exige estudios de comparabilidad (clínicos y no clínicos) de eficacia, seguridad y calidad • Permite el ahorro de costes por la reducción del precio respecto al medicamento de referencia http: //www. osakidetza. euskadi. net
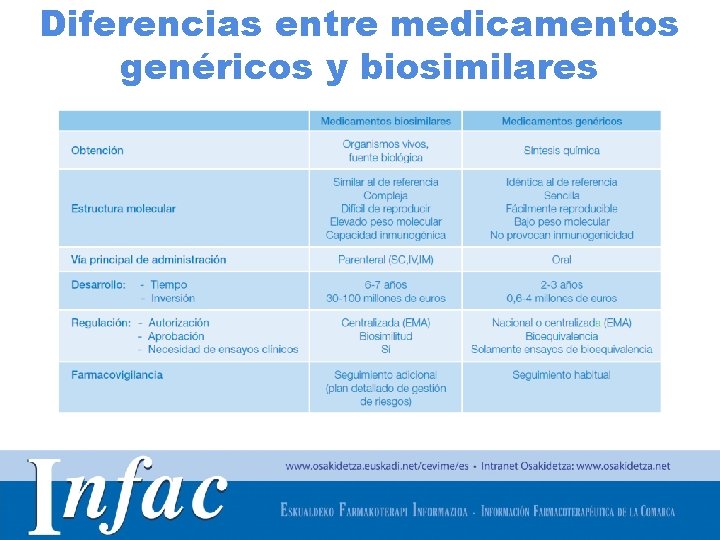
Diferencias entre medicamentos genéricos y biosimilares http: //www. osakidetza. euskadi. net

¿Son los biosimilares igual de seguros que los de referencia? • Las reacciones de inmunogenicidad pueden ser potencialmente graves y no son fácilmente previsibles • Los medicamentos biológicos (biosimilares y de referencia) están sujetos a un seguimiento adicional (▼) particularmente riguroso e intensivo • La inmunogenicidad depende del paciente (genética individual, enfermedad, etc. ) y del fármaco (proceso de producción, tipo de molécula, etc. ) • La inmunogenicidad puede afectar a su eficacia y a su seguridad; se exige Plan de Gestión de Riesgos postautorización • Los medicamentos biológicos deben prescribirse por marca para asegurar la trazabilidad de los lotes http: //www. osakidetza. euskadi. net

¿Se pueden extrapolar las indicaciones? • La extrapolación de la eficacia y seguridad de una indicación a otra es posible, pero no es automática • En ciertos casos, la EMA y FDA permiten extrapolar al biosimilar otras indicaciones del medicamento de referencia • La extrapolación de indicaciones requiere una adecuada justificación científica y un ejercicio de comparabilidad • La EMA publica guías específicas sobre extrapolación de indicaciones para cada biosimilar http: //www. osakidetza. euskadi. net

¿Son intercambiables? • La intercambiabilidad de los biosimilares es competencia de cada Estado de la Unión Europea • En nuestro país los medicamentos biológicos no son sustituibles en las oficinas de farmacia • Para la intercambiabilidad de los biosimilares se requiere el conocimiento y autorización del médico responsable del tratamiento • Hasta el momento no se han notificado problemas de seguridad en el intercambio de medicamentos biológicos http: //www. osakidetza. euskadi. net

Medicamentos biosimilares autorizados por la EMA en Europa http: //www. osakidetza. euskadi. net

CONCLUSIONES • Un biosimilar es un medicamento biológico similar, pero no idéntico, a un medicamento de referencia cuya patente ha caducado • La EMA es la encargada de asegurar la calidad, actividad biológica, eficacia y seguridad de los biosimilares • Los medicamentos biosimilares son una alternativa equivalente y más eficiente que contribuye la sostenibilidad del sistema y favorece el acceso de los pacientes a las nuevas terapias biológicas http: //www. osakidetza. euskadi. net

IDEAS CLAVE • En los medicamentos biológicos “el proceso es el producto” • Los biosimilares son fármacos similares, pero no idénticos, a los medicamentos de referencia • Los medicamentos biosimilares son igual de seguros que sus medicamentos biológicos de referencia http: //www. osakidetza. euskadi. net

Para más información y bibliografía… • INFAC Vol. 24 nº 3 Eskerrik asko!! http: //www. osakidetza. euskadi. net
- Slides: 13