MEDICAMENTOS BIOLGICOS Y BIOSIMILARES MITOS Y REALIDADES Crdoba

MEDICAMENTOS BIOLÓGICOS Y BIOSIMILARES. MITOS Y REALIDADES Córdoba, 22 de octubre de 2014 Prof. Francisco Zaragozá Catedrático de Farmacología Vocal Nacional de Investigación y Docencia del CGCOF
EL FARMACÉUTICO Y LA INNOVACIÓN n La innovación es imprescindible en materia de medicamento. n El farmacéutico tiene una gran responsabilidad: - Proporcionando ideas - En plan formativo n Las perspectivas profesionales demandan actualización permantente.

EL MEDICAMENTO Y SU FUNCIÓN EN LA SOCIEDAD n Es un instrumento para ser aplicado en el paciente. n Gracias a su empleo adecuado vivimos más y mejor: - Curan enfermedades - Cronifican algunas que eran hasta hace poco mortales - Proporcionan confort - Alargan la vida y generan esperanza

¿HACIA DÓNDE SE DIRIGE LA I+D+I? n Cáncer: Ac. Mo y moléculas pequeñas n Vacunas: oportunismo n Campos poco explorados v Mayoritariamente, hacia los productos biológicos: - Observación de efectos tóxicos - Búsqueda de nuevos dianas: la biotecnología

ANTECEDENTES Voronov n Glándulas de aminales n Opoterapia Corticoides Orina: hormonas n Jalea Real n Extractos hepáticos n Gangliósidos: el problema del Nevrotal® n Venenos de reptil: Reptilase® n Insulina de cerdo: purificación
EVOLUCIÓN MÁS RECIENTE n Los avances fisiopatológicos Factores proteicos, tróficos ó inhibidores Secuenciación aminoacídica n Irrupción de la Biotecnología – Descubrimiento de genes y su responsabilidad – Técnicas de ADN-recombinante

AVANCES INICIALES DE ORIGEN RECOMBINANTE n Insulina n Hormona de crecimiento (GH) n Somatostatina n Vasopresina n Factores de coagulación n Factor estimulador de crecimiento de colonias de neutrófilos n Eritropoyetina (EPO) n Los interferones (IFN)

SECUENCIA DE OBTENCIÓN (I) 1. Moléculas iguales a las “fisiológicas“ - Insulina, GH, IFN, etc 2. Factores tróficos - Becaplermina, SGCF 3. Fragmentos activos proteícos - Venenos de reptil: IECA, Eptifibatida

SECUENCIA DE OBTENCIÓN (II) 4. Anticuerpos monoclonales 5. Moléculas modificadas − Proteínas de fusión: etanercept − mab “humanos”: adalimumab − mab citotóxicos: brentuximab vedotin BÚSQUEDA DE LA DIANA: MEJORAS MOLECULARES

ALGUNAS REFLEXIONES PREVIAS n De la naturaleza a la síntesis……volviendo a la naturaleza n El descubrimiento e identificación de los principios activos vegetales n Síntesis orgánica n Semisíntesis n El aprendizaje de las pequeñas modificaciones estructurales y su trascendencia
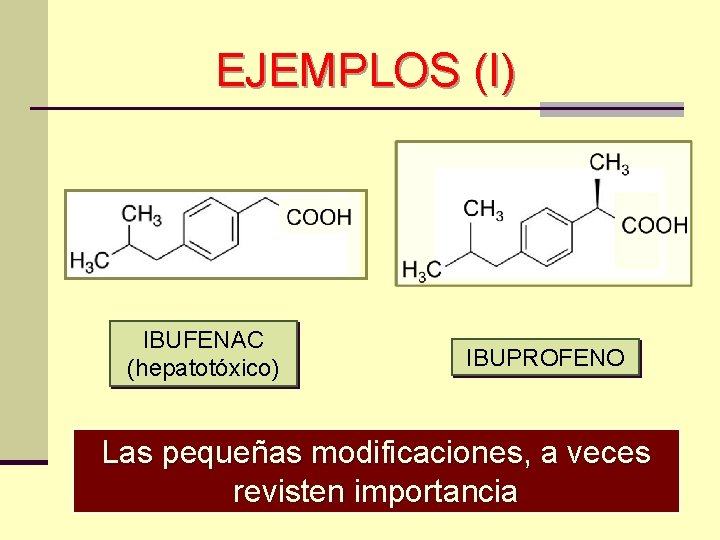
EJEMPLOS (I) IBUFENAC (hepatotóxico) IBUPROFENO Las pequeñas modificaciones, a veces revisten importancia
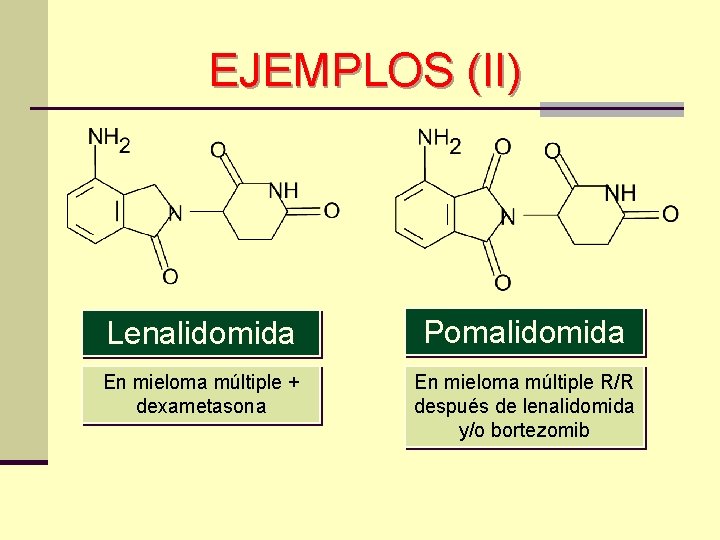
EJEMPLOS (II) Lenalidomida Pomalidomida En mieloma múltiple + dexametasona En mieloma múltiple R/R después de lenalidomida y/o bortezomib

OBTENCIÓN DE FÁRMACOS BIOTECNOLÓGICOS n Claras diferencias entre fármacos “de sustitución” y anticuerpos monoclonales (Ac. Mo) n Los Ac. Mo se diseñan a partir de una diana: generalmente, sobreexpresión n El “mecanismo” de acción es diferente n La obtención de los Ac. Mo es más compleja

CAUTELAS EN LA ADMINISTRACIÓN n Escaso conocimiento de algunos mediadores celulares n ¿Otras vías de señalización de las citoquinas? n El problema de los no respondedores
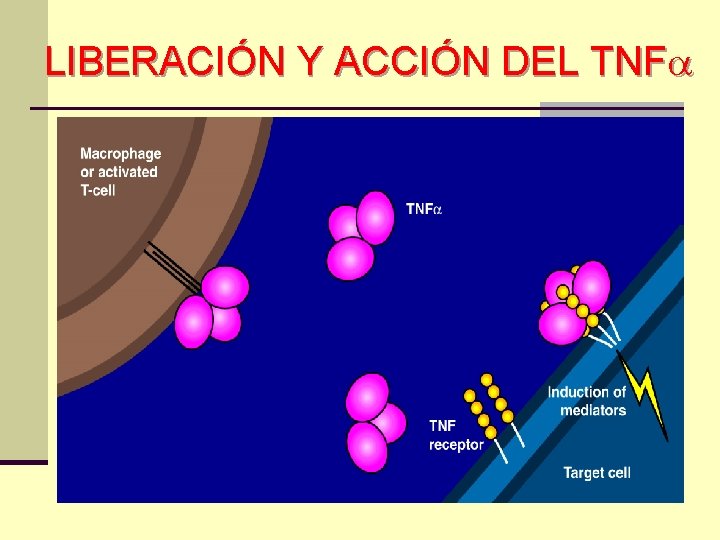
LIBERACIÓN Y ACCIÓN DEL TNF
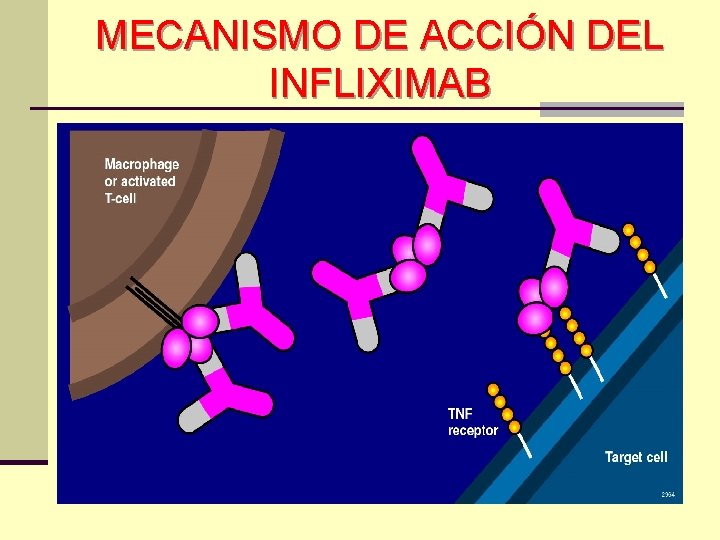
MECANISMO DE ACCIÓN DEL INFLIXIMAB

LOS MEDICAMENTOS BIOSIMILARES n Son copias de medicamentos biotecnológicos, producidos por un fabricante diferente mediante otras líneas celulares, nuevos procesos y nuevos métodos analíticos. n Registro centralizado europeo (EMA). Pruebas mucho más exigentes que las requeridas para un genérico. n Aprobación: datos originales de ensayos clínicos y certificación de bioequivalencia (“similar” al producto original) con estudios de seguridad, eficacia y calidad. Las aparentes ligeras diferencias con respecto al original pueden tener consecuencias clínicas: reconocimiento, cinética, estabilidad, inmunogenicidad, diferente eficacia, etc.

BIOLÓGICOS Y BIOSIMILARES n Cierta heterogeneidad por modificaciones post-transduccionales: glicosilación, metilación, etc. n Diferencias en la obtención n CHO (células de ovario de hámster chino) n NSO n E. coli, S. cerevisiae n Otras fuentes celulares: mosquitos, vegetales, etc. n Casi un 20% de los registros centralizados son de este tipo

EN CONCLUSIÓN (I) n Existe clara diferenciación entre Ac. Mo y el resto de los productos biológicos n Los Ac. Mo son difíciles de replicar n Existen diferencias entre los quiméricos, humanizados y humanos n Es enormemente dificultoso encontrar dianas de interés por desconocimiento de la fisiopatología y/o de las rutas bioquímicas que pueden verse afectadas, lo que genera incertidumbre

EN CONCLUSIÓN (II) n Las diferencias entre los Ac. Mo innovadores y sus biosimilares pueden ser importantes n No se puede predecir la inmunogenicidad n No se puede prever la repercusión clínica de pequeñas modificaciones estructurales n No deben considerarse idénticos los Ac. Mo innovadores y sus biosimilares

- Slides: 21