MEDICAMENT ET COMMUNICATION CELLULAIRE C L BENHAMOU Service

MEDICAMENT ET COMMUNICATION CELLULAIRE C. L. BENHAMOU Service de Rhumatologie Unité Inserm U 658 CHR d’ORLEANS

MEDICAMENT ET COMMUNICATION CELLULAIRE § Différentes phases de développement d’un médicament § Mise sur le marché § Suivi Réglementation § Génériques – Domaine public § Grandes classes thérapeutiques § Effet placebo

DIFFERENTES PHASES DE DEVELOPPEMENT Recherche de molécule active : § § § Découverte empirique Molécules d’origine végétale Screening des molécules Modélisation des molécules à screener Questions des brevets

Protection du Brevet = 20 ans
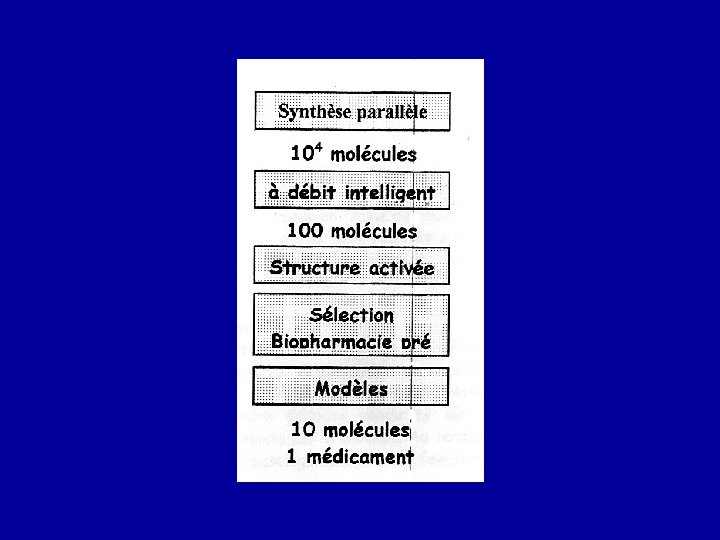

MODELISATION Un exemple : On veut bloquer un récepteur Ou se fixer sur un récepteur On connaît sa conformation stéréologique Modélisation stéréologique « in silico » Série de molécules à tester

SCREENING DES MOLECULES PUIS PREMIERES EXPERIMENTATIONS Sur modèles in vitro Par ex : § Cellules osseuses in vitro § Cellules myocardiques in vitro § Cellules nerveuses in vitro Puis on retient la (ou les) molécules qui ont des propriétés intéressantes en matière d’efficacité, sans effet délétère évident
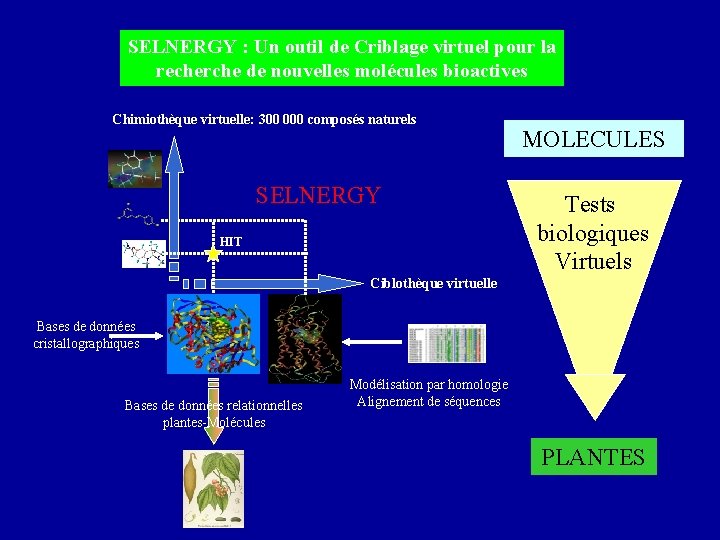
SELNERGY : Un outil de Criblage virtuel pour la recherche de nouvelles molécules bioactives Chimiothèque virtuelle: 300 000 composés naturels SELNERGY HIT MOLECULES Tests biologiques Virtuels Ciblothèque virtuelle Bases de données cristallographiques Bases de données relationnelles plantes-Molécules Modélisation par homologie Alignement de séquences PLANTES
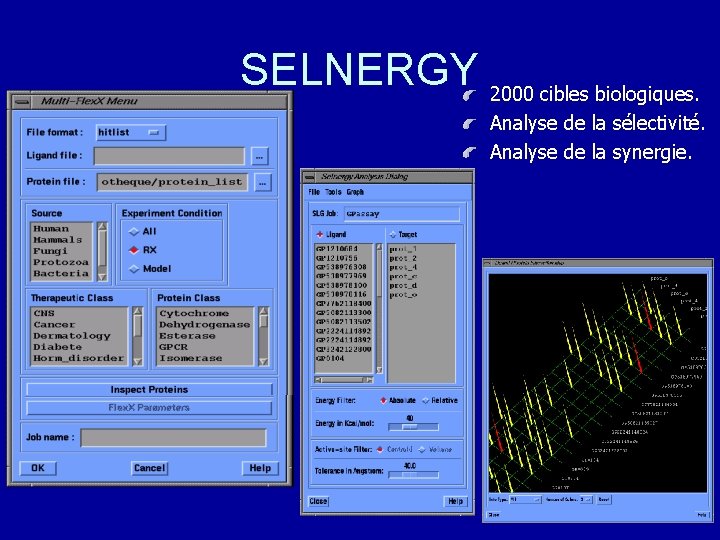
SELNERGY 2000 cibles biologiques. Analyse de la sélectivité. Analyse de la synergie.

Exemple 1: application de l’approche par pharmacognosie inverse
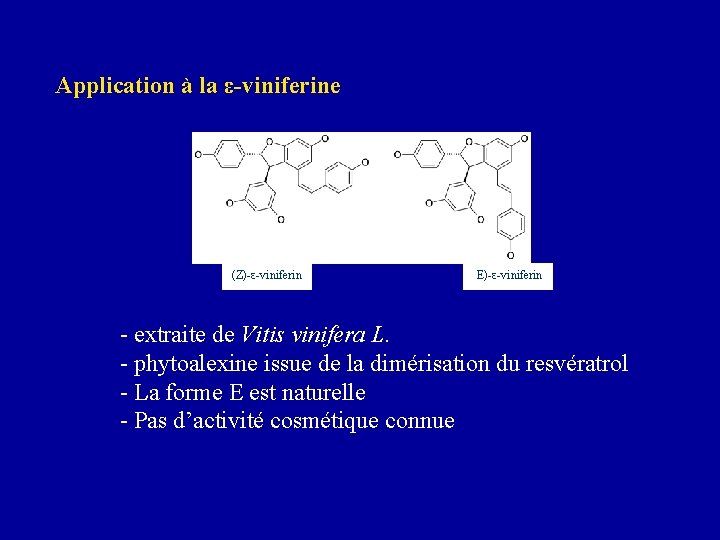
Application à la ε-viniferine (Z)-ε-viniferin (E)-ε-viniferin - extraite de Vitis vinifera L. - phytoalexine issue de la dimérisation du resvératrol - La forme E est naturelle - Pas d’activité cosmétique connue

(E)- -viniferine dans le site actif de la phosphodiestérase 4
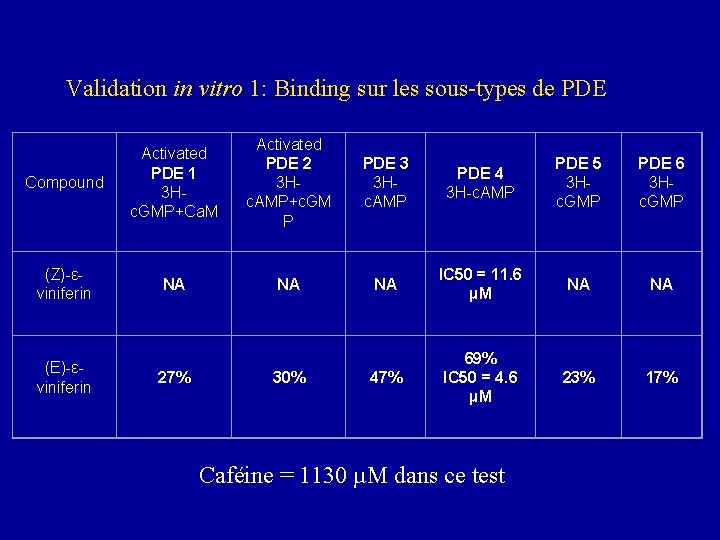
Validation in vitro 1: Binding sur les sous-types de PDE Compound Activated PDE 1 3 Hc. GMP+Ca. M Activated PDE 2 3 Hc. AMP+c. GM P PDE 3 3 Hc. AMP PDE 4 3 H-c. AMP PDE 5 3 Hc. GMP PDE 6 3 Hc. GMP (Z)-εviniferin NA NA NA IC 50 = 11. 6 µM NA NA 47% 69% IC 50 = 4. 6 µM 23% 17% (E)-εviniferin 27% 30% Caféine = 1130 µM dans ce test
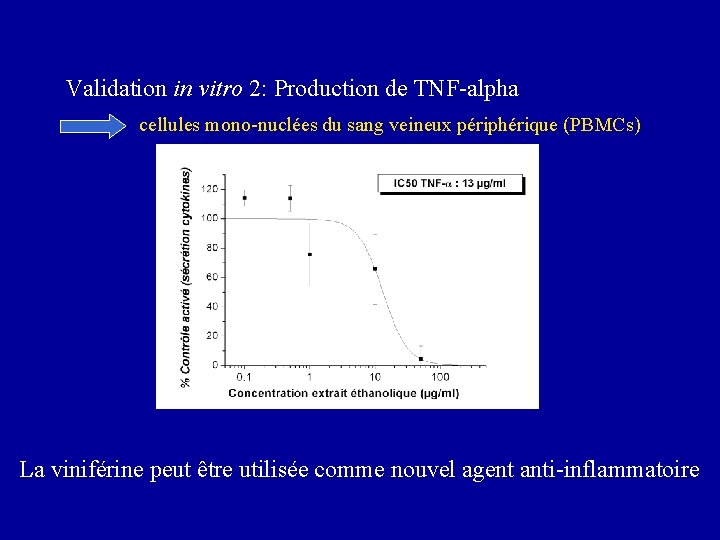
Validation in vitro 2: Production de TNF-alpha cellules mono-nuclées du sang veineux périphérique (PBMCs) La viniférine peut être utilisée comme nouvel agent anti-inflammatoire

RAPPORT BENEFICE - RISQUE § Souci présent à toutes les étapes du développement § Mais aussi rapport coût – bénéfice clinique § Et coût – bénéfice… financier Problème des maladies orphelines

EXPERIMENTATION ANIMALE Premières expérimentations in vivo pour vérifier les effets préalablement testés in vitro Selon les maladies et les médicaments : § rat - souris § cobayes § parfois lapins § rarement chiens moutons singes

NOMBRE D’ANIMAUX § Petits rongeurs : souvent quelques dizaines § Gros animaux : nombre plus limité Souvent premières expériences sur petits groupes Puis confirmation si intéressant Groupes plus vastes

Toxicologie et Pharmacologie chez l’animal § Toxicité § Fonction de reproduction § Potentielle mutagenèse § Potentiel cancérogène de la molécule § Pharmacodynamique § Intéractions médicamenteuses

Développement préclinique (animal) § Toxicité à court terme § Toxicité à long terme Durée environ 36 mois

EXPERIMENTATION HUMAINE § Phase I : volontaire sain - tolérance § Phase II : choix de dose § Phase III : Etude pivot (efficacité – tolérance) § Phase IV : Etudes complémentaires

ETUDES DE PHASE I Volontaire sain § Jeunes – souvent étudiants § Consentement éclairé § Financement Première expérimentation humaine § Précautions maximum milieu hospitalier § Peu de centres § Peu de sujets (environ 5 à 20)

Buts des phases I Tolérance : toxicité chez l’homme § Mais aussi : § Pharmacodynamique § Pharmacocinétique

Principes Phase I § Souvent cross over § Ou dose ranging Exception aux volontaires sains : cancérologie

PHASE II : CHOIX DE DOSE 2 ou 3 doses § Versus placebo § Sujets = malades § Nombre de sujets = dizaines ou centaines Durée variable § Rôle capital ex du tiludronate

PHASE II : CHOIX DE DOSE Notion de placebo § Produit inactif § Effet placebo § Effet nocebo

PHASE III : ETUDES PIVOTS Toujours contre placebo Et/ou contre produit de référence § Une seule dose parfois deux § Nombre suffisant de malades § Echantillonnage clair permettant de répondre à la question § Critères idem

PHASE III : ETUDES PIVOTS Généralement multicentriques § ± internationales ± § Durée variable § Etudes très encadrées

PHASE III : ETUDES PIVOTS Question principale § efficacité - tolérance Décisif pour l’intérêt réel du médicament

PHASE IV : QUESTIONS COMPLEMENTAIRES Par exemple § Sujet âgé § Insuffisance rénale modérée § Enfant - adolescent § Effets complémentaires du produit § Impact épidémiologique Nombre variable - durée variable Plus proche de la « vraie vie »

PHASE IV : QUESTIONS COMPLEMENTAIRES ≠ Phase IV « à l ’ancienne » Questions importantes en rapport avec la pratique courante

MISE SUR LE MARCHE § AFSSAPS Agence Française de Sécurité Sanitaire des Aliments et des Produits de Santé § Agence européenne § FDA Food and Drug Administration Soumission européenne française américaine

AFSSAPS § AFSSAPS Agence Française de Sécurité Sanitaire des Aliments et des Produits de Santé § Agence européenne § FDA Food and Drug Administration Soumission européenne française américaine

DUREE GLOBALE § De la molécule à la mise sur le marché ≈ 10 ans § De la mise sur le marché au générique ≈ 10 ans § Coûts en rapport

Coût des différentes phases de développement § Phase I (quelques mois) § 1 à 4 millions d’euros pour 20 à 100 volontaires § Phase II (jusqu’à 2 ans) § 7 à 21 millions d’euros pour 100 à 1000 participants § Phase III (quelques années - 3 à 5) § 50 à 100 millions d’euros pour 1000 à 5000 patients § Phase IV (après l’AMM) § Coût très variable non évaluable

Enregistrement § Autorisation de Mise sur le Marché § AMM § Transparence : Amélioration du service Médical Rendu § ASMR 1, 2, 3, 4 § Prix § Négociation en fonction de l’ASMR

Pharmaco-vigilance § Recensement des évènements indésirables § Rôle très important § Surtout pour les accidents rares § Parfois demande d’étude complémentaire

Génériques § Au bout de 10 ans après l’AMM Le médicament « tombe dans le domaine public » § Il peut être légalement fabriqué par qui le souhaite (de l’industrie pharmaceutique) § Il porte le nom générique de la molécule. § Il repasse une AMM (simplifiée)

Exemples Dafalgan Doliprane Paracétamol Mopral Oméprazole Di. Antalvic Paracétamol Dextropropoxyfène

Pour se défendre contre les génériques § § § Autres modes de présentation Association de produits Non génériques dans l’immédiat Mais nécessité d’obtenir AMM transparence prix Ou le laboratoire lui même fabrique le générique (prolongation)

Déremboursements Moindres remboursements § Médicaments classés en 3 groupes § A Efficaces § B Moins efficaces § C Peu efficaces Avec pourcentage de remboursement en fonction Exemple : les veinotoniques

Les essais § Essais contrôlés # Observation Épidémio-pharmacologie Série historique

Randomisation § Pourquoi ? Diminuer les biais § Quand ? Le plus tard possible à l’inclusion § Comment ? § Simple § En bloc § Stratification

L’insu ou l’aveugle § Simple aveugle : seul le malade ne sait pas ce qu’il reçoit § Double aveugle : le malade et l’investigateur ne savent pas § Triple aveugle : malade, investigateur et analyste des données ne savent pas

Essai en ouvert § Pas de traitement de comparaison Pas d’aveugle Ou § Traitement de comparaison Mais pas d’aveugle

Randomisation § Répartition aléatoire des traitements Randon Randomisation Français Anglais

Essais cliniques § Effet mesuré = effet thérapeutique + effet du hasard + effet des biais La randomisation a pour but de supprimer ou de minimiser les biais

Randomisation § Par tirage au sort § Traitement imprévisible § Choix du traitement indépendant de l’état du patient

Stratification encore supprimer les biais après la randomisation § § Stratification par centre Stratification par sexe Age + sexe Par niveau de TA En général pas plus de deux strates

Code de randomisation § Qui le possède ? § § Les investigateurs Le coordinateur Les centres anti-poison Le promoteur Levée d’aveugle uniquement en cas de nécessité

Événements indésirables graves § Décès § Événement indésirable avec mise en jeu du pronostic vital § Hospitalisation ou prolongation d’hospitalisation § Invalidité ou incapacité Tout événement indésirable grave doit être déclaré dans les 24 heures au Centre de Vigilance et au promoteur.

Pharmacovigilance après AMM § Soit études phase IV § Soit pratique courante § Pratique courante = signalements spontanés à des centres de pharmaco-vigilance § Effets des grands nombres sur les événements indésirables rares mais parfois graves § Études complémentaires parfois nécessaires

La Pharmacovigilance § Détection – Évaluation – Prévention des effets indésirables des médicaments Avant l’AMM : seulement essais cliniques mais profil incomplet de la tolérance § Effet attendu § Effet inattendu

Avant l’AMM § Dans les essais, on signale TOUS les évènements indésirables, même si le rapport avec le médicament est douteux § On classe rapport § § Certain Probable Douteux improbable

Le consentement éclairé § § § Écrit Détaillé Très informatif Avec délai de réflexion Retrait de consentement possible à tout moment

CCPPRB Comité Consultatif de Protection des Personnes se Prêtant à la Recherche Biomédicale Anciens comités d’éthiques Répondent des « conditions de validité de la recherche en regard de la protection des personnes »

CCPPRB Également respect du secret médical de la confidentialité

CCPPRB Composition § 4 personnes de la recherche biomédicale (dont 3 médecins) § § § § 1 MG 2 Pharmaciens 1 « éthicien » (religieux, mère de famille) 1 sociologue 1 juriste 1 psychologue 1 infirmier(e)

Missions des CCPPRB Donne son avis sur § l’information des personnes incluses ou à inclure § Le consentement éclairé écrit § Les indemnités versées § La pertinence scientifique du projet § L’adéquation entres les moyens et les buts du travail § L’existence d’une assurance § L’ABSENCE de dangerosité inacceptable

Notion de Bénéfice Individuel Direct Etudes toujours classées § avec BID § sans BID Exigences plus fortes quand étude sans BID

Recommandations de groupes de travail internationaux Concernant la conduite des études dans un domaine donné Par exemple, Ostéoporose Þ concernant la durée le nombre de malades les points de comparaison…. Osteoporosis International, 2006, 17, 1 -7


CCPPRB Soumission ÞÉventuellement aller-retours ÞÉventuellement approbation 1 CCPPRB pour 1 étude multicentrique Au moins 1 en France pour étude internationale

Protocole thérapeutique § § § Tout doit être écrit Rationnel Objectif principal Objectifs secondaires Critères de jugement Recrutement : § Critères d’inclusion § Critères d’exclusion § Déroulement calendrier examens à chaque visite

Objectifs § Objectif principal § Objectifs secondaires § § Définis très clairement dans le protocole On n’a pas le droit d’en changer Pour enregistrement : objectif principal Analyse non citée aux objectifs = travail posthoc, peu ou pas de valeur

Exemples de protocoles § 2 groupes parallèles § A § B § 4 groupes parallèles § § A B C Placebo

Essai de phase III en groupes parallèles § 3 conditions fortes § Randomisation double insu § Groupes comparables au départ § Respect du double insu

Schémas plus complexes § Par exemple : cross over § Cross over avec wash out § Plus complexe avec trois groupes

Notion de marqueur intermédiaire (surrogate endpoint) § par exemple cholestérolémie § Accidents coronariens § Mortalité § Par exemple, densitométrie osseuse § Fractures ostéoporotiques

Critères d’inclusion et de non inclusion § Très détaillés : Tout doit être écrit

Déclaration des personnes Se prêtant à la recherche biomédicale Volontaires sains Fichier centralisé anonymisé (CNIL)

Homéopathie Le principe est qu’une dose infinitésimale d’une produit (10 -3 10 -10) pourrait avoir un effet thérapeutique Pas de preuve d’efficacité basée sur des essais répondant aux exigences décrites précédemment Rôle de l’effet placebo

Phytothérapies Médecines « douces » Médecines naturelles Style de vie Relaxation – hypnose….
- Slides: 72