Mecnica quntica e os orbitais atmicos Schrdinger props

Mecânica quântica e os orbitais atômicos Schrödinger propôs uma equação que incorpora o comportamento ondulatório e o comportamento de partícula do elétron. Erwin Schrödinger - Físico Prêmio Nobel de Física (1933)

Mecânica quântica e os orbitais atômicos A posição do elétron é especificada por uma “função de onda” (x, y, z) As diferentes funções de onda possíveis serão identificadas por 4 números quânticos: n, l, ml e ms E. Schorödinger

A Equação de Onda • Schrödinger propôs uma equação que contém os termos onda e partícula. • A resolução da equação leva às funções de onda. • A função de onda fornece o contorno da nuvem eletrônica (orbital). • O quadrado da função de onda fornece a probabilidade de se encontrar o elétron, isto é, dá a densidade eletrônica para o átomo.

A Equação de Onda Não tem significado físico 2 É uma expressão matemática de como a probabilidade de encontrar a partícula varia de lugar para lugar. Conforme o princípio da incerteza na mecânica quântica, as trajetórias exatas do elétron não aparecem

Orbitais e Números Quânticos Distribuição da Densidade Eletrônica no Estado Fundamental do Átomo de Hidrogênio
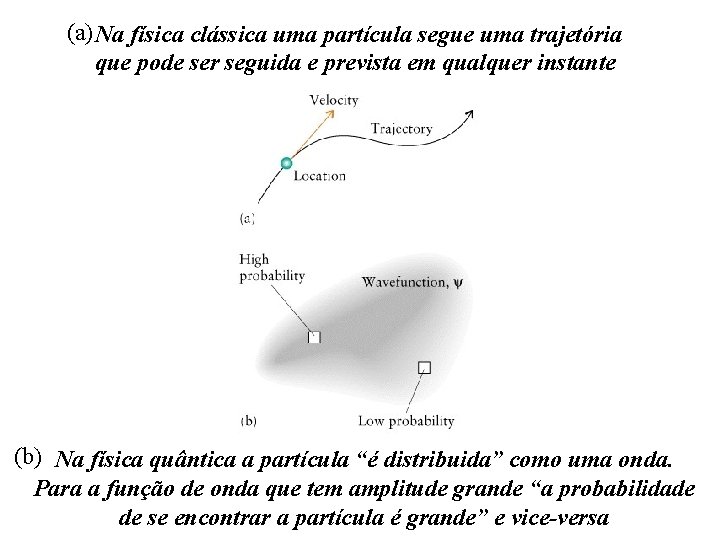
(a) Na física clássica uma partícula segue uma trajetória que pode ser seguida e prevista em qualquer instante (b) Na física quântica a partícula “é distribuida” como uma onda. Para a função de onda que tem amplitude grande “a probabilidade de se encontrar a partícula é grande” e vice-versa

1 - O Orbitais e Números Quânticos número quântico principal (n) Este número quântico pode ter qualquer valor inteiro, positivo, exceto zero. A medida que n aumenta o orbital torna-se maior, e o elétron passa mais tempo distante do núcleo. Portanto n indica a distância média do elétron ao núcleo. Um aumento de n indica também que o elétron tem energia mais alta e por isso esta mais fracamente preso ao núcleo.

Orbitais e números quânticos 2. O número quântico azimutal, l. Esse número quântico depende do valor de n. Os valores de l começam de 0 e aumentam até n -1. O valor de l é representado pela letras s, p, d, f correspondendo aos valores = 0, 1, 2, e 3. l fornece informação sobre o formato do orbital

Orbitais e números quânticos 3. O número quântico magnético, ml. É um número inteiro que fornece informação sobre a orientação de um orbital no espaço. Esse número quântico depende de l. O número quântico magnético tem valores inteiros entre -l e +l.

Orbitais e Números Quânticos 4 -Número Quântico de Spin (ms) Esse número determina o sentido do giro de rotação do elétron em torno do seu próprio eixo. Valores : ms = +1/2 e ms = -1/2
Orbitais e números quânticos Spin eletrônico


Orbitais e números quânticos Ex. : 1 s 2 ___ n = 1; l = 0(subcamada s); ml = 0; ms = +½ n = 1; l = 0(subcamada s); ml = 0; ms = -½

Orbitais e números quânticos 2 p 1 ___ ___ n = 2; l = 1(subcamada p); ml = -1; ms = +½ 2 p 2 ___ ___ n = 2; l = 1(subcamada p); ml = -1; ms = +½ n = 2; l = 1(subcamada p); ml = 0; ms = +½ 2 p 3 ___ ___ n = 2; l = 1(subcamada p); ml = -1; ms = +½ n = 2; l = 1(subcamada p); ml = 0; ms = +½ n = 2; l = 1(subcamada p); ml = +1; ms = +½
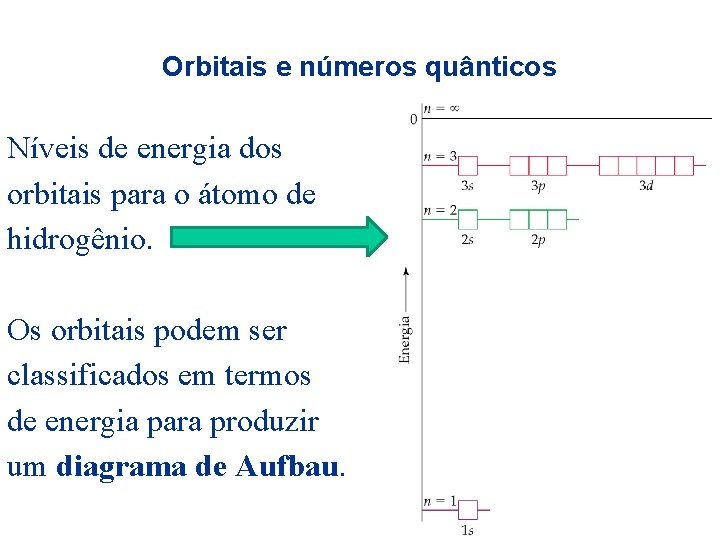
Orbitais e números quânticos Níveis de energia dos orbitais para o átomo de hidrogênio. Os orbitais podem ser classificados em termos de energia para produzir um diagrama de Aufbau.
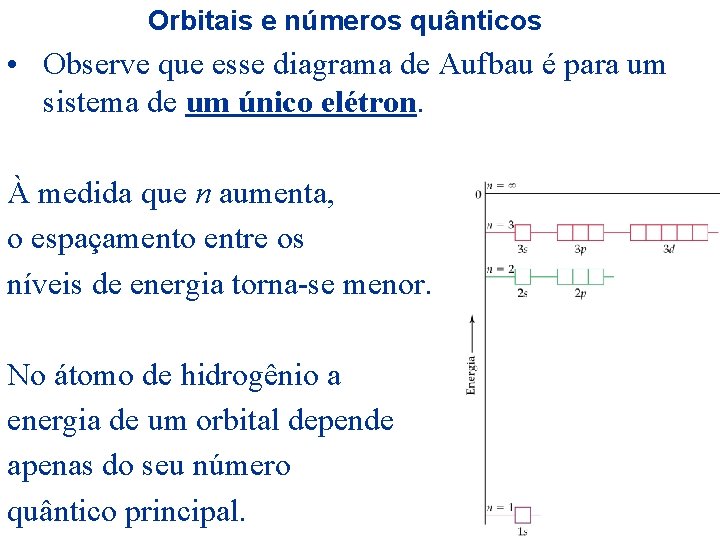
Orbitais e números quânticos • Observe que esse diagrama de Aufbau é para um sistema de um único elétron. À medida que n aumenta, o espaçamento entre os níveis de energia torna-se menor. No átomo de hidrogênio a energia de um orbital depende apenas do seu número quântico principal.

Representação dos Orbitais : Orbitais s • • • Todos os orbitais s são esféricos. À medida que n aumenta, os orbitais s ficam maiores. À medida que n aumenta, aumenta o número de nós. Um nó é uma região no espaço onde a probabilidade de se encontrar um elétron é zero. Em um nó, 2 = 0 Orbitais s possuem apenas nós esféricos.
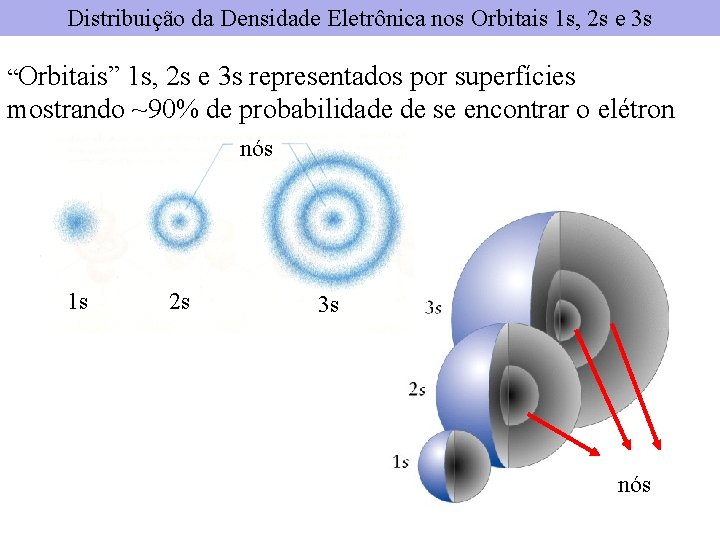
Distribuição da Densidade Eletrônica nos Orbitais 1 s, 2 s e 3 s “Orbitais” 1 s, 2 s e 3 s representados por superfícies mostrando ~90% de probabilidade de se encontrar o elétron nós 1 s 2 s 3 s nós
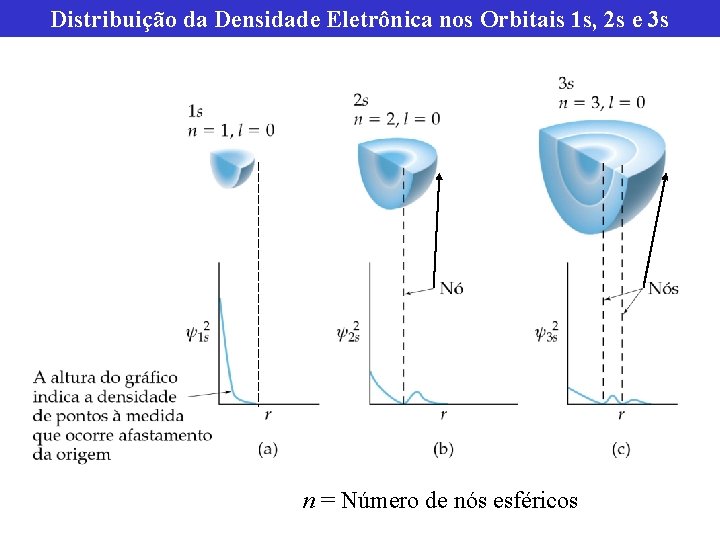
Distribuição da Densidade Eletrônica nos Orbitais 1 s, 2 s e 3 s n = Número de nós esféricos

Distribuição da Densidade Eletrônica nos Orbitais 1 s, 2 s e 3 s

Orbitais p • Existem três orbitais p: px, py, e pz. • Os três orbitais p localizam-se ao longo dos eixos x, y e z de um sistema cartesiano. • As letras correspondem aos valores permitidos de ml, -1, 0, e +1. • Os orbitais têm a forma de halteres. • À medida que n aumenta, os orbitais p ficam maiores.
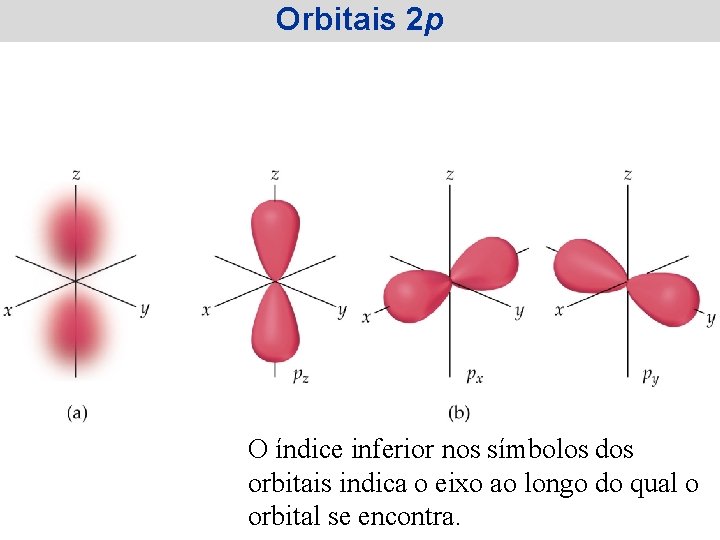
Orbitais 2 p O índice inferior nos símbolos dos orbitais indica o eixo ao longo do qual o orbital se encontra.
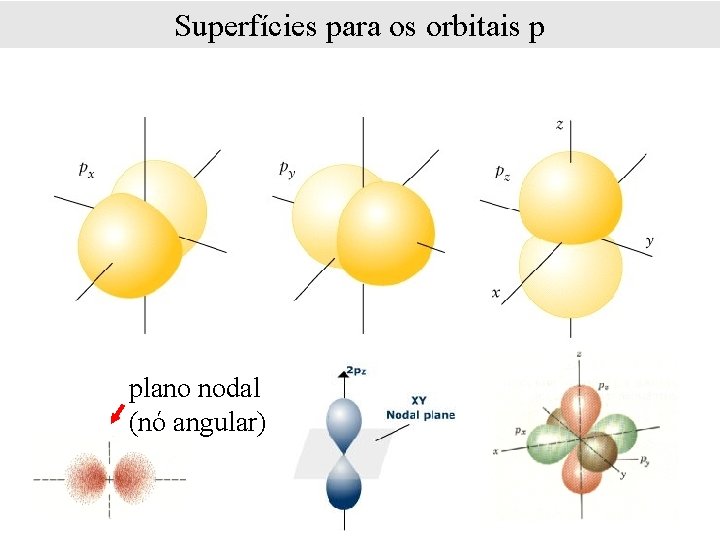
Superfícies para os orbitais p plano nodal (nó angular)

Orbitais d • Existem cinco orbitais d: dxy , dzx , dyz , dx 2 -y 2 e dz 2 • Três dos orbitais d encontram-se em um plano bissecante aos eixos x-, y- e z. • Dois dos orbitais d se encontram em um plano alinhado ao longo dos eixos x-, y- e z. • Quatro dos orbitais d têm quatro lóbulos cada. • Um orbital d tem dois lóbulos e um anel.
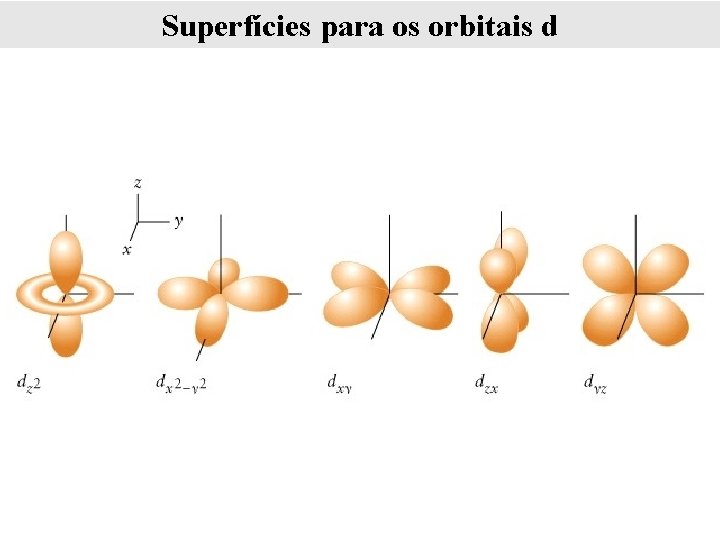
Superfícies para os orbitais d
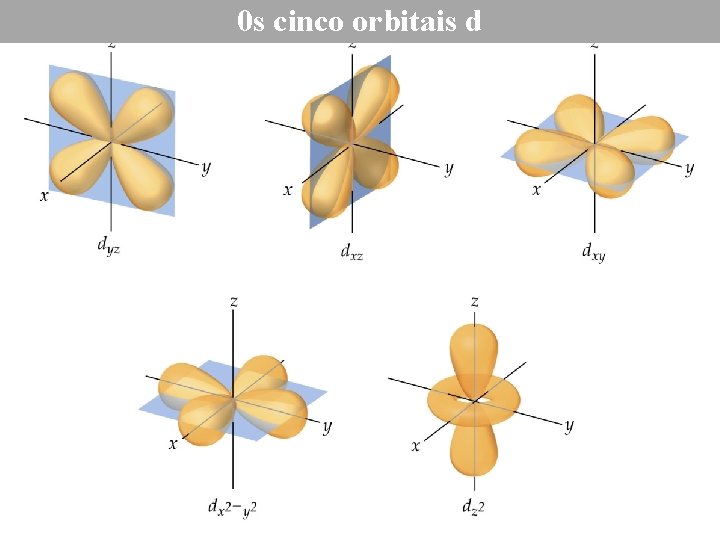
0 s cinco orbitais d
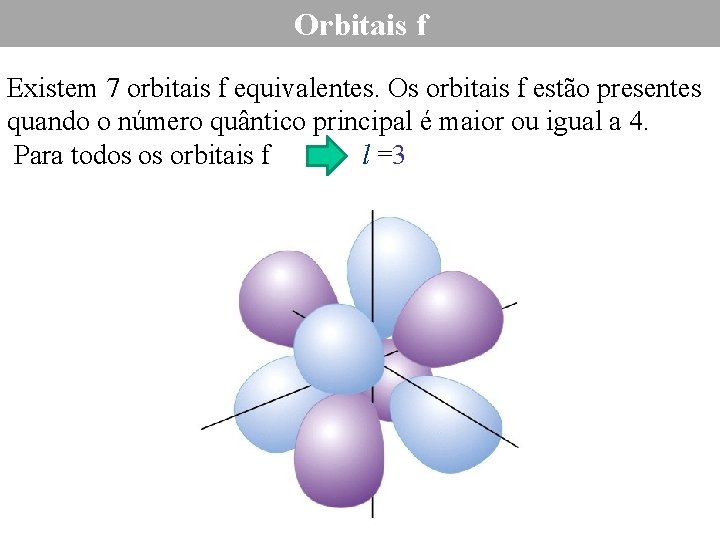
Orbitais f Existem 7 orbitais f equivalentes. Os orbitais f estão presentes quando o número quântico principal é maior ou igual a 4. Para todos os orbitais f l =3
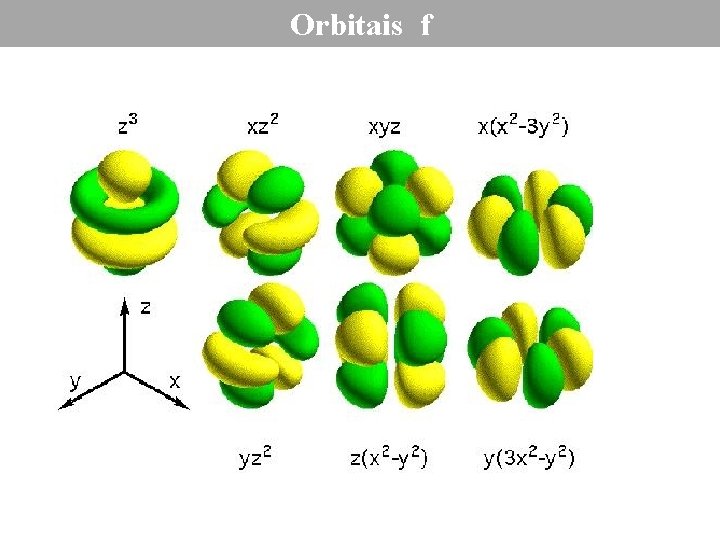
Orbitais f

Átomos polieletrônicos Orbitais e suas energias • Orbitais de mesma energia são conhecidos como degenerados. • Para n 2, os orbitais s e p não são mais degenerados porque os elétrons interagem entre si. • Portanto, o diagrama de Aufbau apresenta-se ligeiramente diferente para sistemas com muitos elétrons.
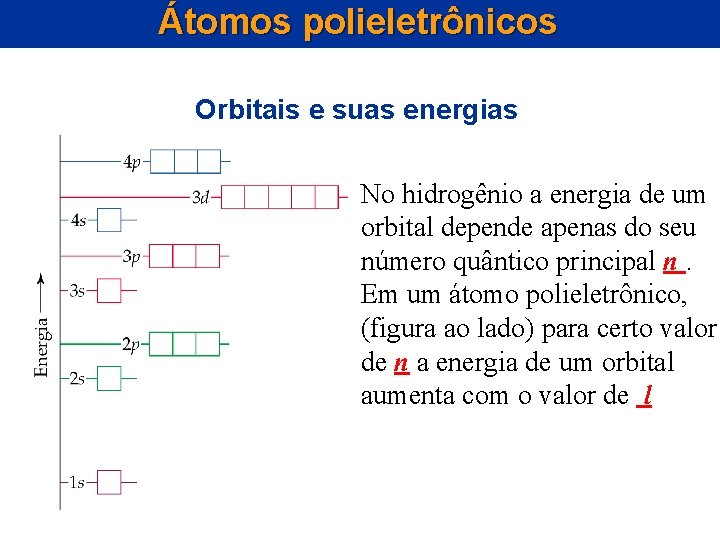
Átomos polieletrônicos Orbitais e suas energias No hidrogênio a energia de um orbital depende apenas do seu número quântico principal n. Em um átomo polieletrônico, (figura ao lado) para certo valor de n a energia de um orbital aumenta com o valor de l
- Slides: 30