Mechanismus der basischen Hydrolyse Unterscheidet sich stark von

Mechanismus der basischen Hydrolyse • Unterscheidet sich stark von dem der sauren Hydrolyse • Co 3+ Komplexe mit NH 3 oder Aminen als Liganden hydrolysieren oberhalb p. H=4 wesentlich rascher als in sauren Lösungen • Das Geschwindigkeitsgesetz ist immer 2. Ordnung: • Würde auf einen assoziativen Mechanismus hinweisen, dies ist aber nicht der Fall! Beweis für einen dissoziativen Mechanismus: Sterischer Effekt Je größer der Amin-Ligand, desto rascher die Reaktion.

Wieso kann ein dissoziativer Mechanismus zu einem Geschwindigkeitsgesetz 2. Ordnung führen? • Der NH 3 Ligand wird dadurch, dass er an Co 3+ koordiniert ist, fähiger, ein H+ abzuspalten • In wässr. Lsg ist das OH- -Ion nicht imstande, NH 3 zum NH 2 - Ion zu deprotonieren. Ist aber das NH 3 Molekül an das Co 3+ koordiniert, so zieht das positiv geladene Metallion Elektronendichte vom NH 3 ab, sodass es saurer wird und ein Amid-Ion entstehen kann • Dies ist sehr oft die Art Änderung der Liganden-Reaktivität, die in Übergangsmetall-Katalysatoren und Metalloenzymen wirksam ist.


Liganden-Substitution unter Beteiligung mehrzähniger Liganden • Der Ersatz von 2 koordinierten Wassermolekülen durch einen zweizähnigen Liganden L-L erfolgt in zwei aufeinanderfolgenden Schritten. • Man kann die Steady-State Näherung auf die Zwischenverbindung anwenden:
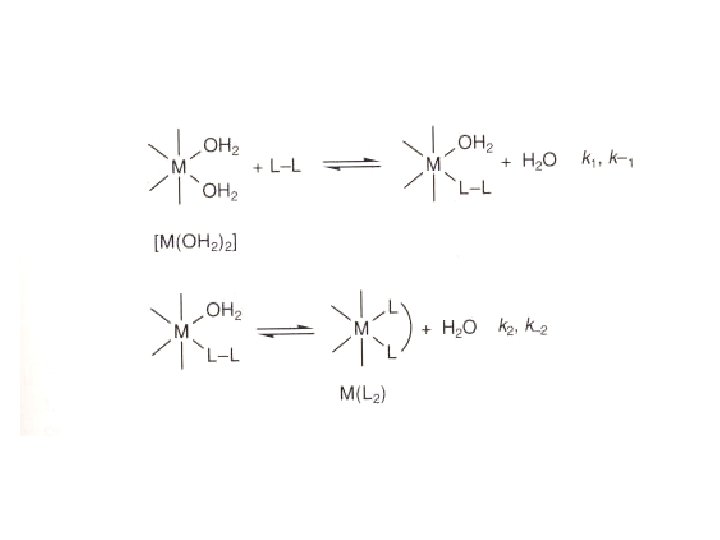
L-L
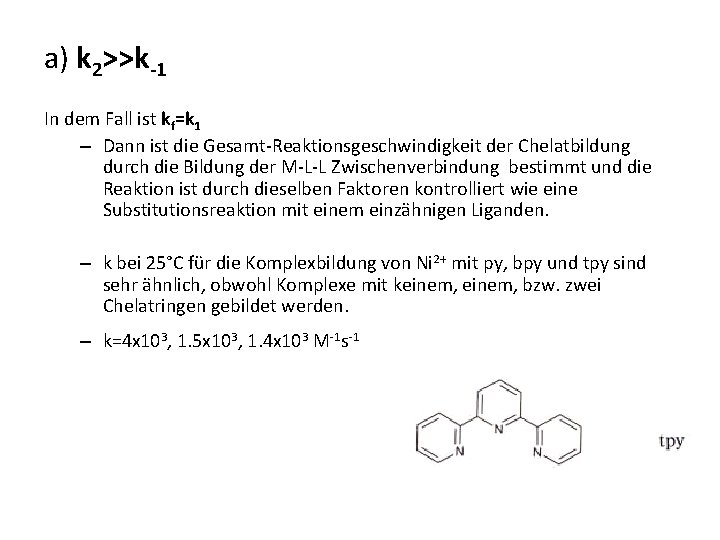
a) k 2>>k-1 In dem Fall ist kf=k 1 – Dann ist die Gesamt-Reaktionsgeschwindigkeit der Chelatbildung durch die Bildung der M-L-L Zwischenverbindung bestimmt und die Reaktion ist durch dieselben Faktoren kontrolliert wie eine Substitutionsreaktion mit einem einzähnigen Liganden. – k bei 25°C für die Komplexbildung von Ni 2+ mit py, bpy und tpy sind sehr ähnlich, obwohl Komplexe mit keinem, bzw. zwei Chelatringen gebildet werden. – k=4 x 103, 1. 5 x 103, 1. 4 x 103 M-1 s-1
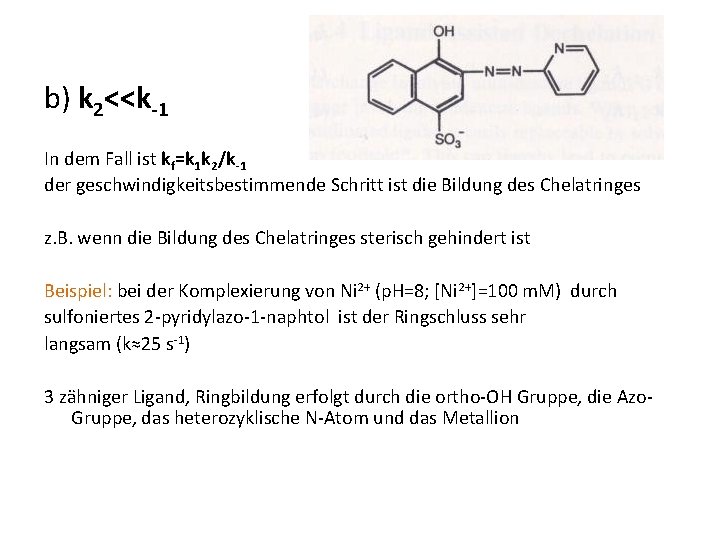
b) k 2<<k-1 In dem Fall ist kf=k 1 k 2/k-1 der geschwindigkeitsbestimmende Schritt ist die Bildung des Chelatringes z. B. wenn die Bildung des Chelatringes sterisch gehindert ist Beispiel: bei der Komplexierung von Ni 2+ (p. H=8; [Ni 2+]=100 m. M) durch sulfoniertes 2 -pyridylazo-1 -naphtol ist der Ringschluss sehr langsam (k≈25 s-1) 3 zähniger Ligand, Ringbildung erfolgt durch die ortho-OH Gruppe, die Azo. Gruppe, das heterozyklische N-Atom und das Metallion
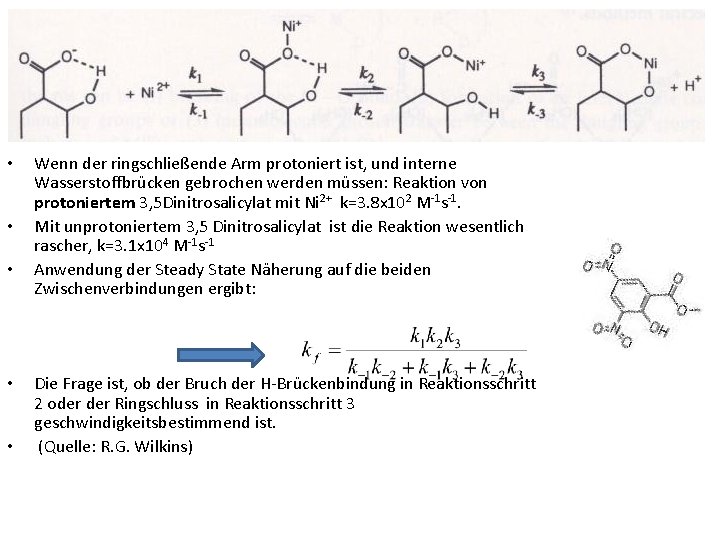
• • • Wenn der ringschließende Arm protoniert ist, und interne Wasserstoffbrücken gebrochen werden müssen: Reaktion von protoniertem 3, 5 Dinitrosalicylat mit Ni 2+ k=3. 8 x 102 M-1 s-1. Mit unprotoniertem 3, 5 Dinitrosalicylat ist die Reaktion wesentlich rascher, k=3. 1 x 104 M-1 s-1 Anwendung der Steady State Näherung auf die beiden Zwischenverbindungen ergibt: Die Frage ist, ob der Bruch der H-Brückenbindung in Reaktionsschritt 2 oder Ringschluss in Reaktionsschritt 3 geschwindigkeitsbestimmend ist. (Quelle: R. G. Wilkins)

Effekt des p. H auf die Geschwindigkeit der Substitution bei Chelatkomplexen • Das Verhalten eines Chelatliganden L und seiner protonierten Form LH+ ist unterschiedlich • Sowohl die Bildung als auch die Hydrolyse von Chelatkomplexen ist daher in der Regel p. H-abhängig weil gewöhnlich K 1<<1, gilt: K 2>>K 3 kinetischen Messungen an Metallkomplexen (Ni 2+, Cr 3+) von Polyaminen zeigten, dass auch k 2>>k 3 In der umgekehrten Richtung kann ein Proton die Ringöffnung direkt unterstützen, oder auf dem Weg reaktiver protonierter Spezies

Metallionen-unterstützte Dissoziation (Hydrolyse) von Chelatkomplexen • Metallionen können die Dissoziation von Komplexen mit multidentaten Liganden beschleunigen • Der Reaktionsweg ist kompliziert und umfasst zweikernige Zwischenverbindungen, die M und M 1 enthalten
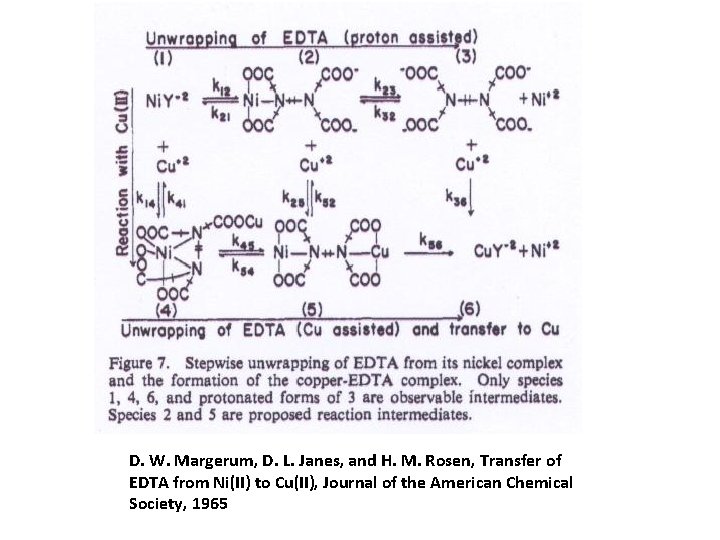
D. W. Margerum, D. L. Janes, and H. M. Rosen, Transfer of EDTA from Ni(II) to Cu(II), Journal of the American Chemical Society, 1965
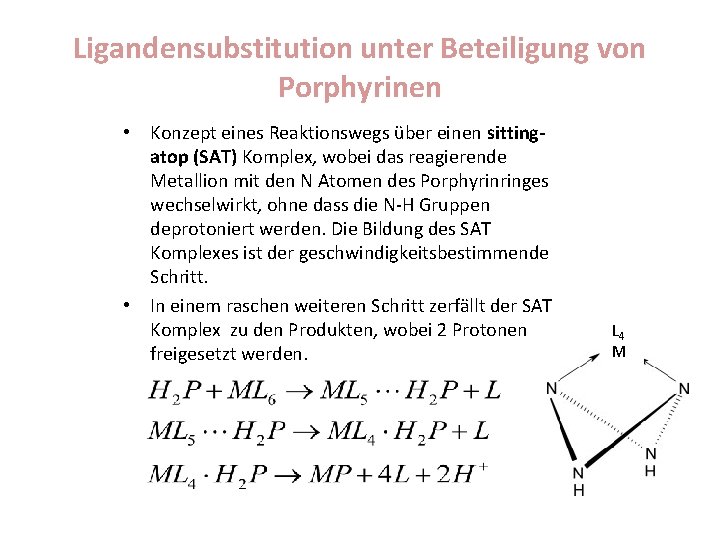
Ligandensubstitution unter Beteiligung von Porphyrinen • Konzept eines Reaktionswegs über einen sittingatop (SAT) Komplex, wobei das reagierende Metallion mit den N Atomen des Porphyrinringes wechselwirkt, ohne dass die N-H Gruppen deprotoniert werden. Die Bildung des SAT Komplexes ist der geschwindigkeitsbestimmende Schritt. • In einem raschen weiteren Schritt zerfällt der SAT Komplex zu den Produkten, wobei 2 Protonen freigesetzt werden. L 4 M
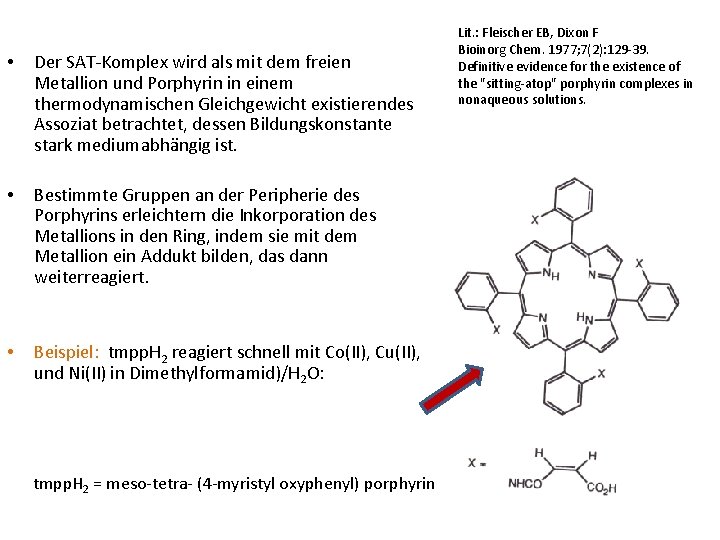
• Der SAT-Komplex wird als mit dem freien Metallion und Porphyrin in einem thermodynamischen Gleichgewicht existierendes Assoziat betrachtet, dessen Bildungskonstante stark mediumabhängig ist. • Bestimmte Gruppen an der Peripherie des Porphyrins erleichtern die Inkorporation des Metallions in den Ring, indem sie mit dem Metallion ein Addukt bilden, das dann weiterreagiert. • Beispiel: tmpp. H 2 reagiert schnell mit Co(II), Cu(II), und Ni(II) in Dimethylformamid)/H 2 O: tmpp. H 2 = meso-tetra- (4 -myristyl oxyphenyl) porphyrin Lit. : Fleischer EB, Dixon F Bioinorg Chem. 1977; 7(2): 129 -39. Definitive evidence for the existence of the "sitting-atop" porphyrin complexes in nonaqueous solutions.
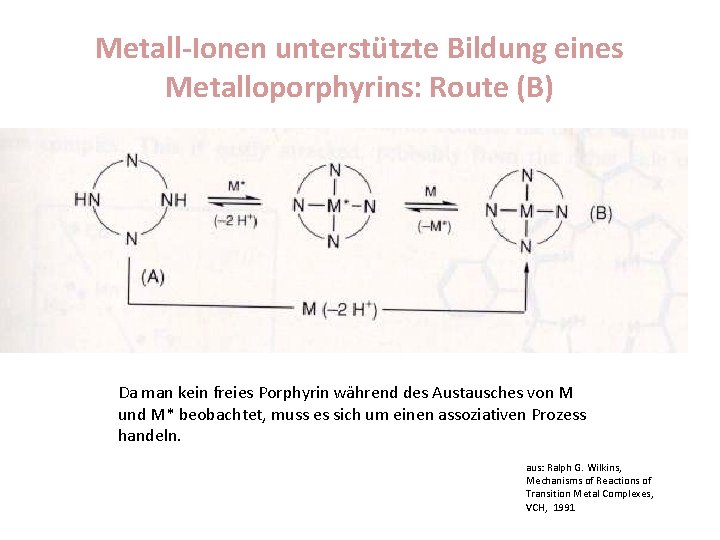
Metall-Ionen unterstützte Bildung eines Metalloporphyrins: Route (B) Da man kein freies Porphyrin während des Austausches von M und M* beobachtet, muss es sich um einen assoziativen Prozess handeln. aus: Ralph G. Wilkins, Mechanisms of Reactions of Transition Metal Complexes, VCH, 1991

Isobestische Punkte bei UV-VIS Spektren Isobestische Punkte sind Wellenlängen, bei denen die Absorption konstant bleibt, während sich die Konzentrationen der Reaktanden und Produkte ändern: weisen darauf hin, dass keine nachweisbaren Zwischenverbindungen auftreten: synchroner Prozess. z. B. Reaktion von Hg(tpp) mit Zn 2+ in Pyridin. Hier tritt die freie tpp Base nicht auf, sie hätte ein von beiden Komplexen unterschiedliches Spektrum. tpp = Tetraphenylporphyrin aus: Ralph G. Wilkins, Mechanisms of Reactions of Transition Metal Complexes, VCH, 1991
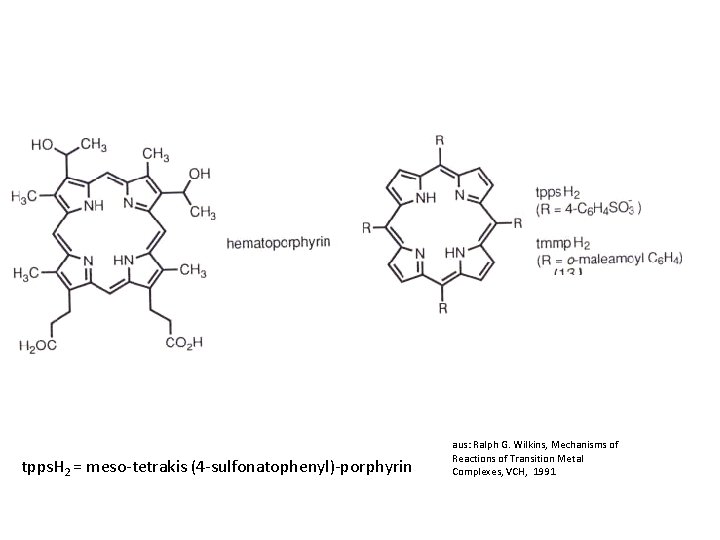
13 tpps. H 2 = meso-tetrakis (4 -sulfonatophenyl)-porphyrin aus: Ralph G. Wilkins, Mechanisms of Reactions of Transition Metal Complexes, VCH, 1991

• Die Reaktion von Mn 2+ mit tpps. H 24 - in Wasser ist sehr langsam. • Die Aufnahme von Mn 2+ in den Porphyrinring wird jedoch stark beschleunigt durch die Gegenwart kleiner Mengen von Cd 2+ Ionen, die als Katalysator wirken

• Die Reaktion von Cd 2+ mit tpps. H 24 - ist rasch, denn das größere Metallion bildet einen out-of-plane Komplex. Dieser kann wiederum leicht durch das stärker bindende Mn 2+ attackiert werden. -------------------------------- • Die Dissoziation der meisten Metall-Porphyrine M(II)P ist sehr langsam. • H+ beschleunigen die Entfernung des Metallions. Häufig findet man folgendes Geschwindigkeitsgesetz:
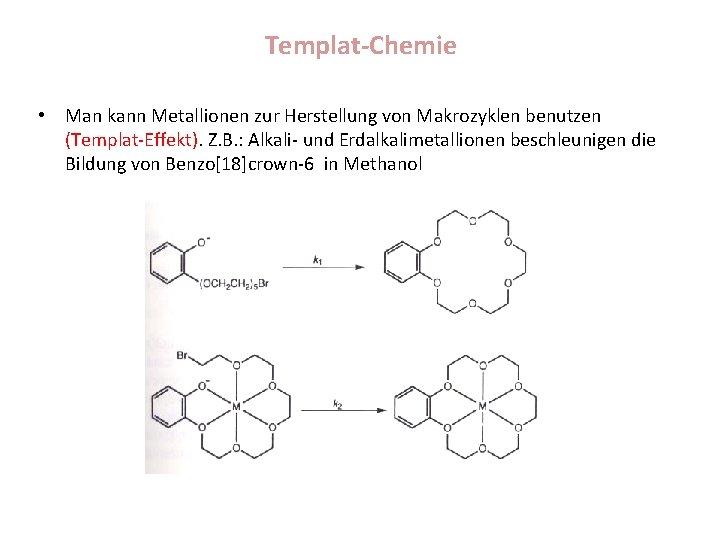
Templat-Chemie • Man kann Metallionen zur Herstellung von Makrozyklen benutzen (Templat-Effekt). Z. B. : Alkali- und Erdalkalimetallionen beschleunigen die Bildung von Benzo[18]crown-6 in Methanol

Stereochemie der oktaedrischen Substitution • Die normale oktaedrische Substitution erfolgt unter Retention der Konfiguration • Dies deutet darauf hin, dass die normale fünffach koordinierte Zwischenverbindung eine tetragonal pyramidale Struktur beibehält (quadratische Pyramide) • In manchen Fällen ist der Substitutionsvorgang jedoch von einer stereochemischen Umwandlung begleitet, z. B. • trans-[Co(NH 3)4 Cl 2]+ + H 2 O ergibt 55% cis- und 45% trans-Produkt • trans-[Co(en)2(OH)Cl]+ + H 2 O ergibt 75% cis und 25% trans-Produkt • trans-[Co(en)2 Br 2]+ + H 2 O ergibt 30% cis und 70% trans-Produkt

• Das Auftreten stereochemischer Umlagerungen kann durch die Annahme einer trigonal-bipyramidalen Struktur der fünffach koordinierten Zwischenverbindungen erklärt werden. • Der Austritt von X wird durch die Bewegung eines Paares ursprünglich trans zueinander stehender Liganden begleitet, von denen jeder cis zur austretenden Gruppe X steht • Es gibt 2 Möglichkeiten zur Bildung einer trigonalen Bipyramide • Die eintretende Gruppe Y tritt entlang einer der trigonalen Kanten ein • 6 mögliche Reaktionswege, 2 davon führen zur Wiederherstellung der relativen Positionen der Liganden im Komplex


Welche Liganden ermöglichen stereochemische Umwandlung? • Voraussetzung ist das Vorhandensein eines Elektronenpaares in einem Orbital, dessen Symmetrie eine π-Bindung vom Liganden zum Metall ermöglicht, sobald das Umklappen von der quadratischen Pyramide zur trigonalen Bipyramide erfolgt ist: • Stabilisierung des trigonalen ÜZ
- Slides: 23