Mecanismo de accin de los lactmicos Inhibidores de

Mecanismo de acción de los lactámicos
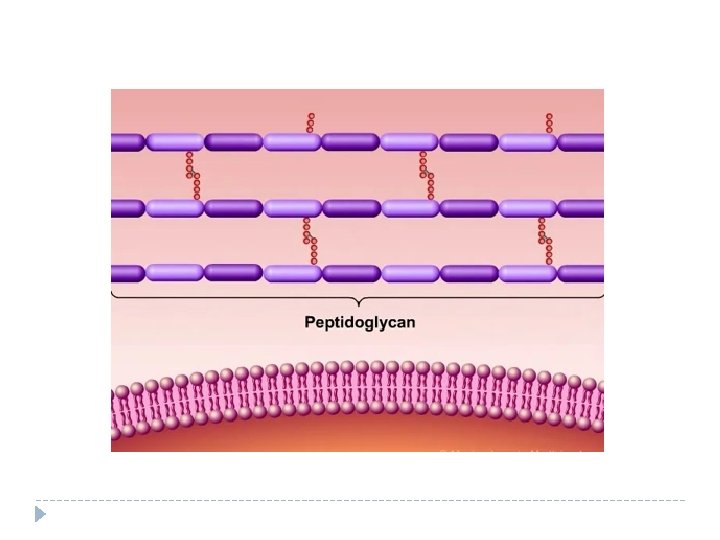
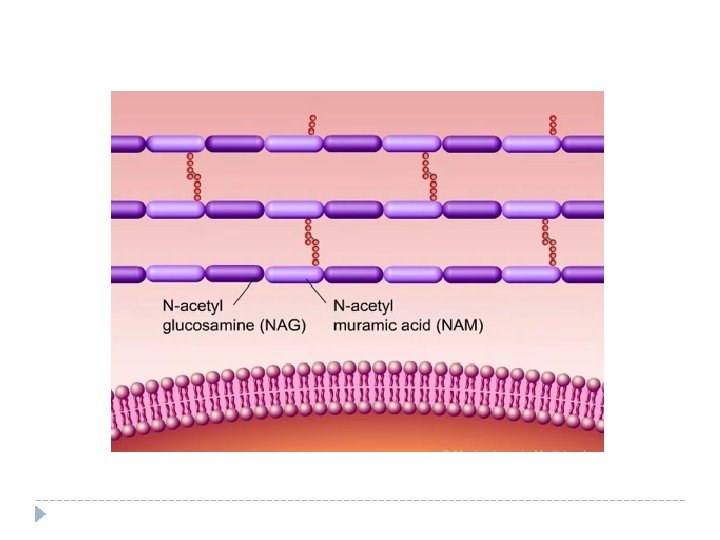
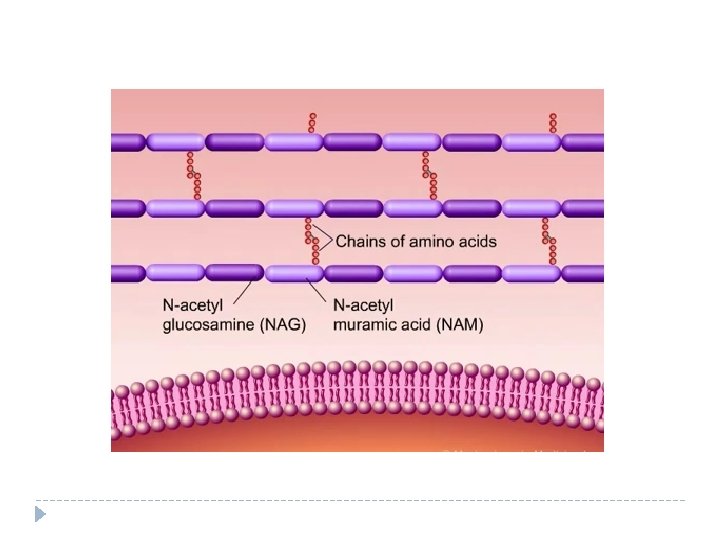
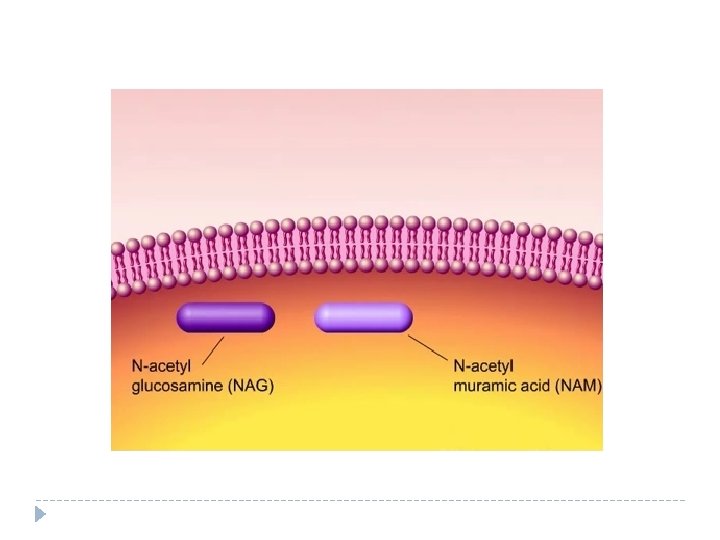
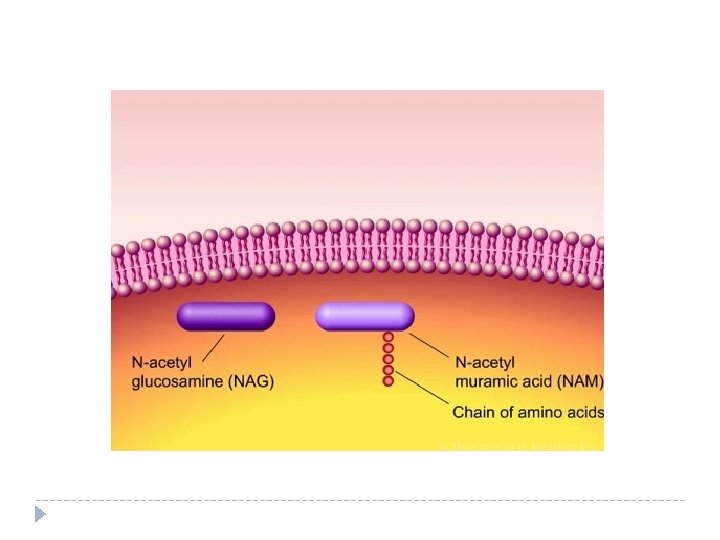
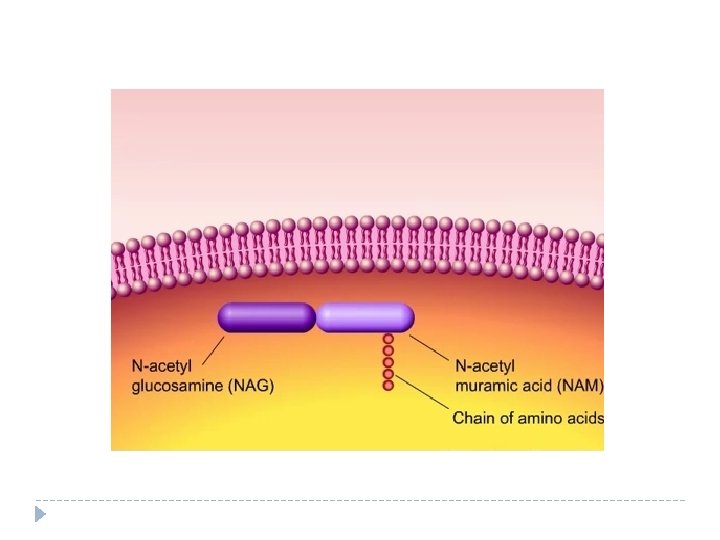
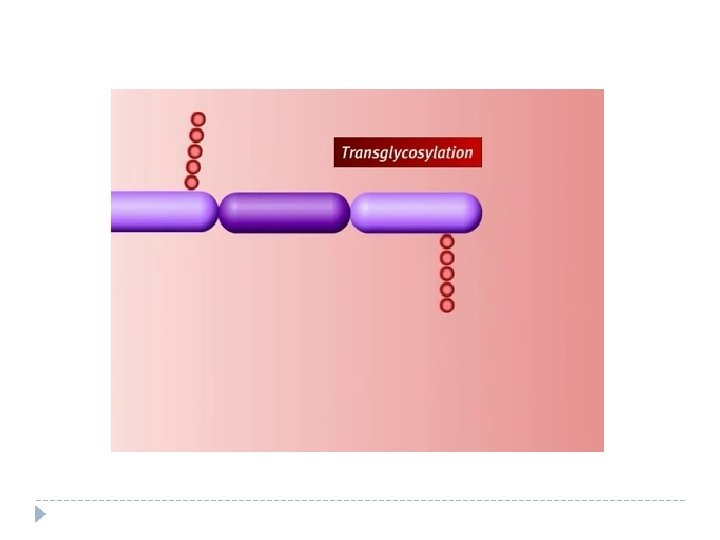
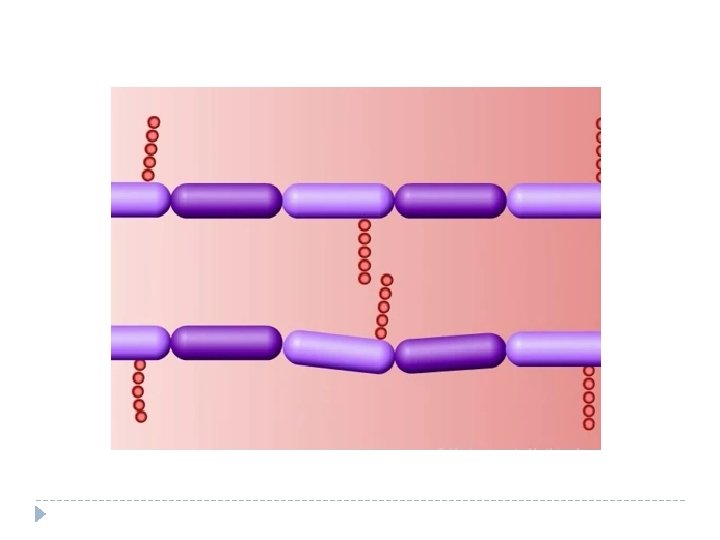
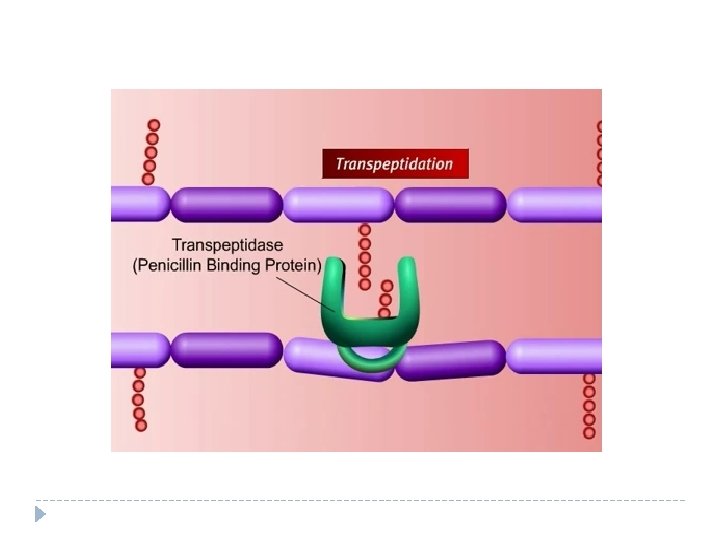
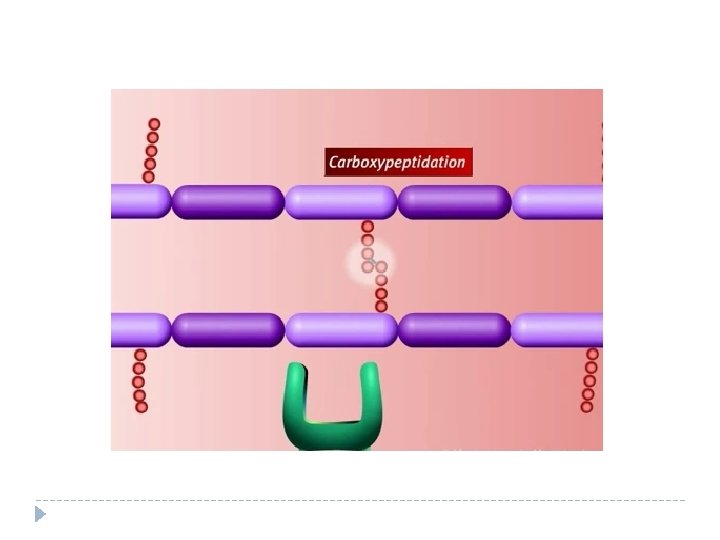
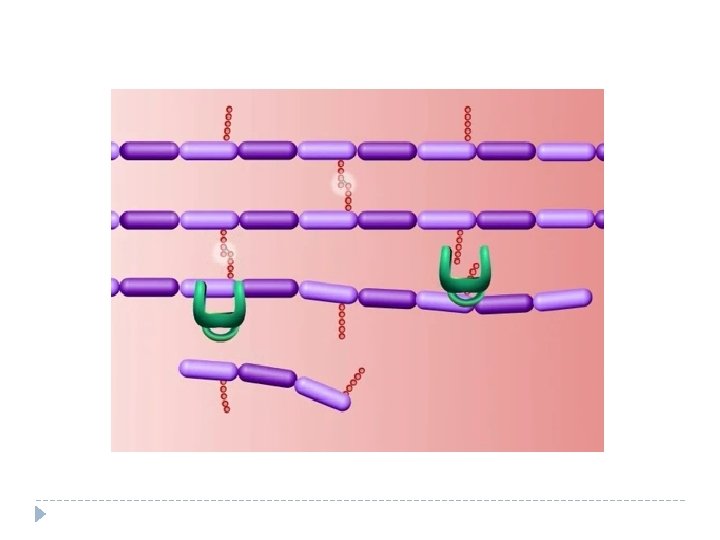
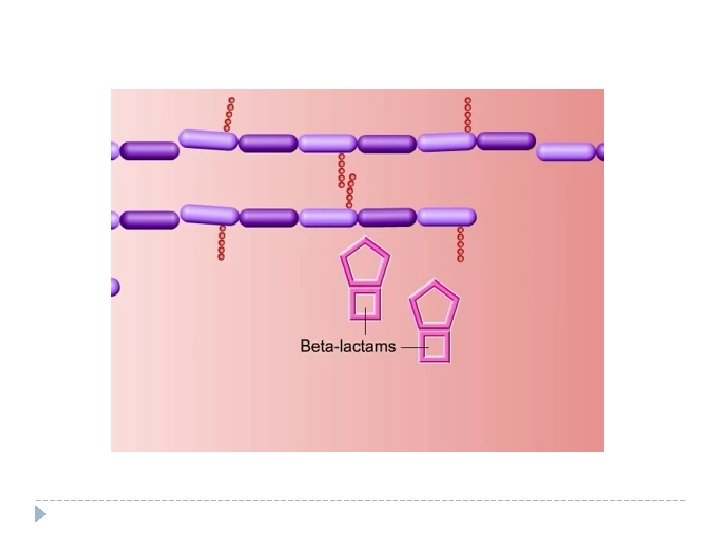

Inhibidores de la síntesis proteica

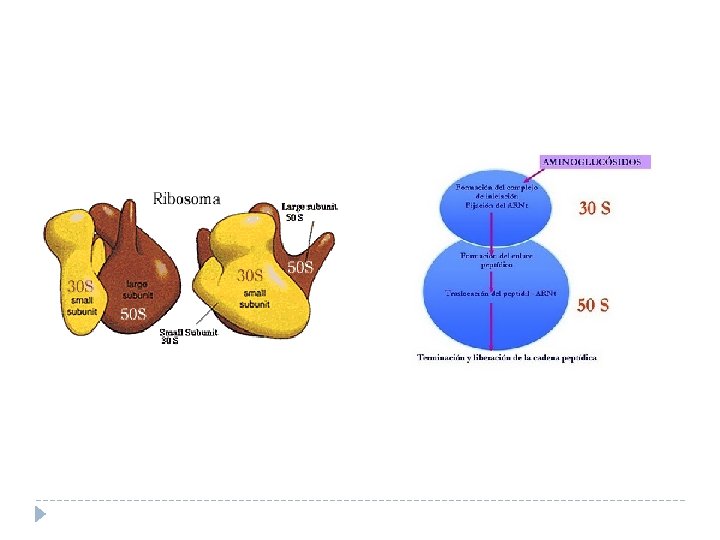
Inhibidores de la síntesis proteica � Ribosomas microbianos: 70 S � Se subidividen en dos fracciones � 30 S � 50 S � Las dos fracciones son sitios de acción de antimicrobianos que buscan alterar la síntesis proteica para función (enzimática) o reparación (estructural)
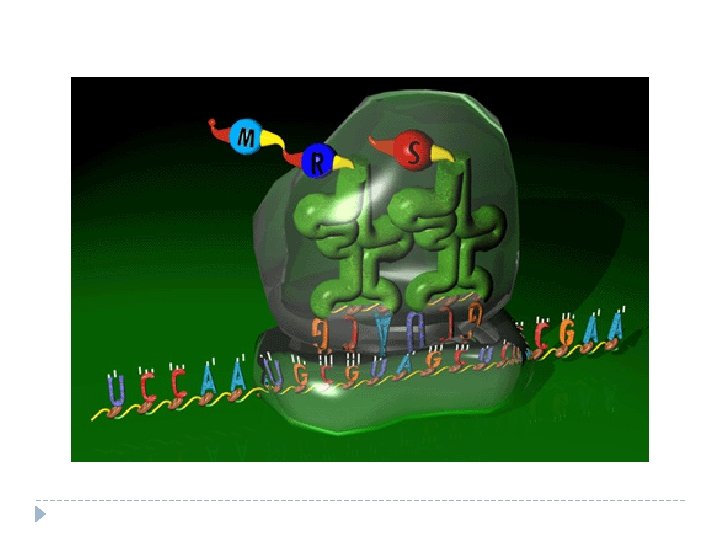
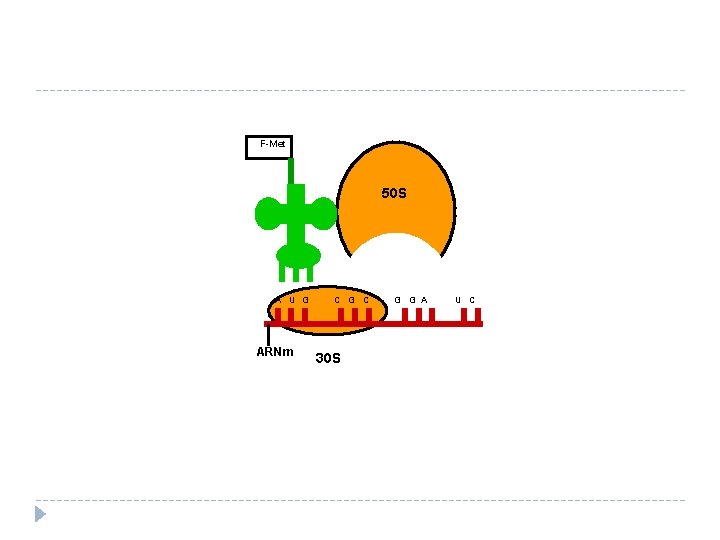
F-Met 50 S A U G ARNm C G C 30 S G G A U C
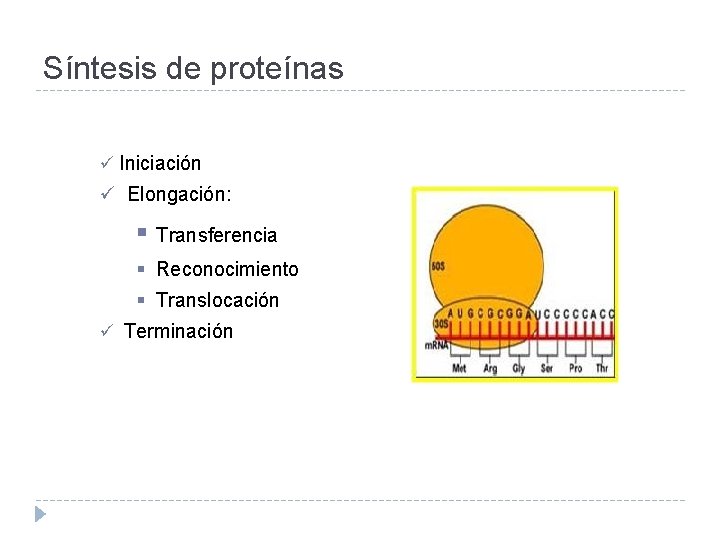
Síntesis de proteínas ü Iniciación ü Elongación: § Transferencia § Reconocimiento § Translocación ü Terminación

Fracción 30 S

Fracción 30 S � Aminoglucósidos � Tetraciclinas

Aminoglucósidos

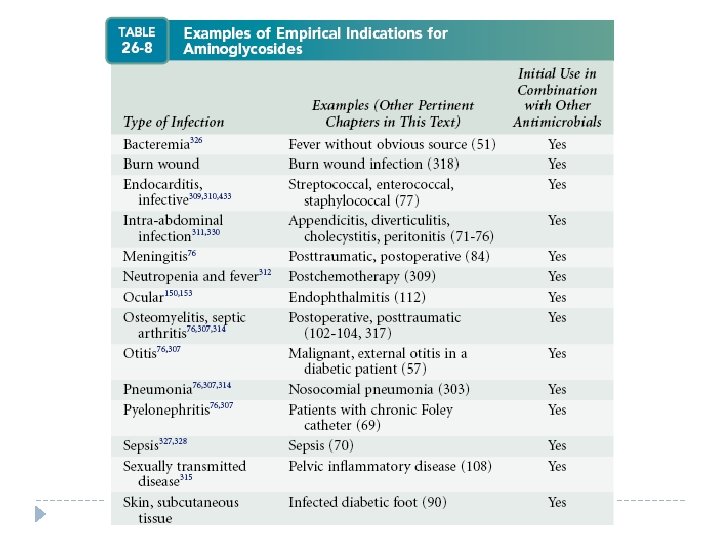
Aminoglucósidos � Actividad concentración dependiente � Actividad contra Pseudomonas � Algunos son útiles contra micobacterias o contra protozoarios � Algunos pueden ser sinergísticos con lactámicos (penicilinas o cefalosporinas) contra cocos aerobios positivos o bacilos positivos negativos � Poca resistencia � Toxicidad renal, ótica y de bloqueo neuromuscular � Alergia es rara

Estructura � Todos tienen un anillo aminociclitol, de 6 miembros con sustituciones amino � Están unidos a azúcares que pueden o no tener amino ácidos � Para todos, excepto para estreptomicina, el aminociclitol es el 2 -desoxiestreptamina � Para estreptomicina es desoxiestreptadina
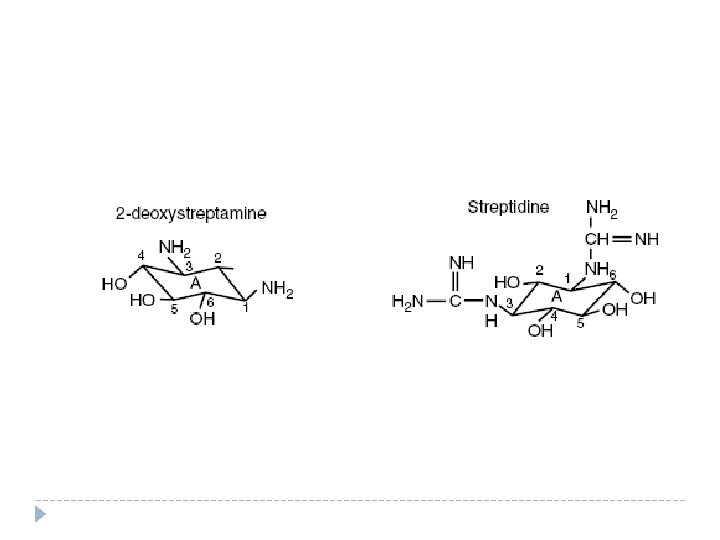
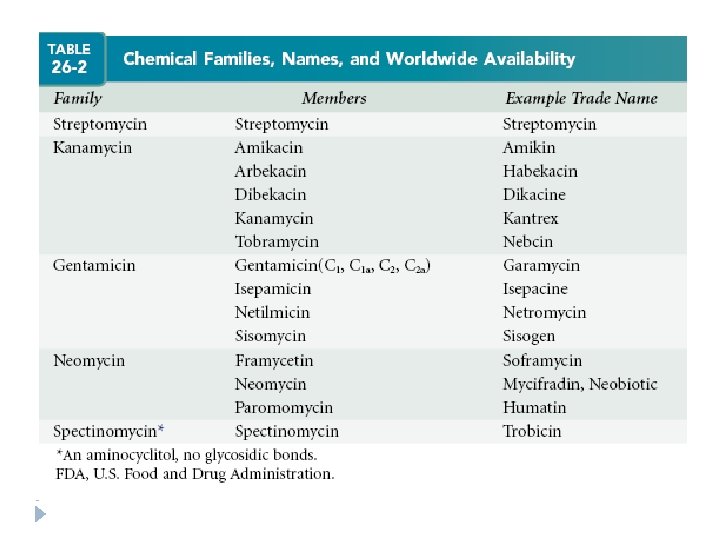

Mecanismo de acción � Se ligan con gran afinidad a una región de nucleótidos altamente conservada en la región decodificadora del ARNm de la subunidad 30 S de los ribosomoas procarióticos � La avidez depende del aminoglucósido � Una variable es el número de grupos amino y su estado de protonización � Unión � No reversible es el único mecanismo para lesionar bacterias � Son BACTERICIDAS

Propiedades químicas � Altamente hidrosolubles � Insolubles en solventes orgánicos � Limitación para atravesar barreras lipídicas � En p. H fisiológico son altamente catiónicos, con altas cargas positivas � Influye tanto en actividad como en toxicidad � La actividad antimicrobiana: Aumenta en medio alcalino � Se disminuye en medio ácido � coadministración conjunta con lactámicos inactiva ambas drogas: � La Abre el núcleo lactámico � Acila el grupo amino del AG �

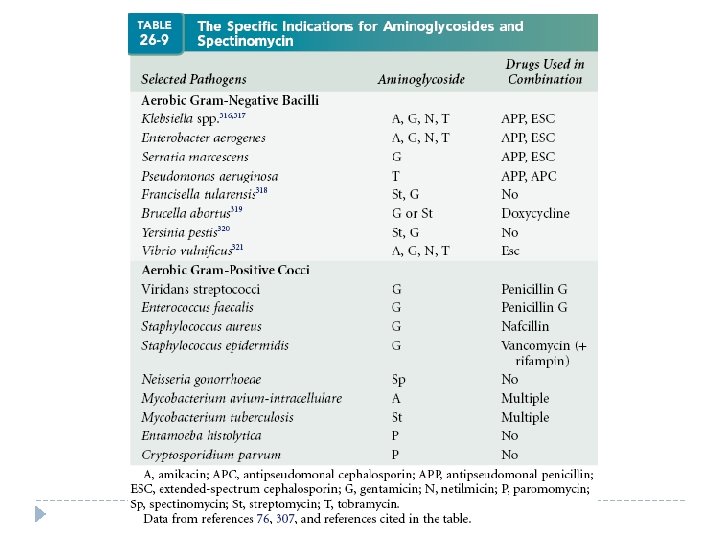
Espectro � Predominante contra BGN � MSSA son susceptibles � MRSA son resistentes � Anaerobios son resistentes � Pseudomonas � Amikacina � Micobacterias � Estreptomicina � Amebas � Paramomicina � Gonorrea � Espectinomicina

Actividad antimicrobiana – Mecanismos � Ligadura inicial � Reversible � Independiente de energía � Al inicio, la ligadura es a la membrana � Desplaza calcio y magnesio � Hay ruptura, desordenamiento y fuga � Alteración � Captura de las funciones normales de pared por dos mecanismos dependientes de energía � Ligadura a proteínas

Actividad antimicrobiana – Mecanismos � Fases � I: dependientes de energía lenta � Inhibida � II: por: Cationes divalentes Osmolalidad elevada Bajo p. H Anaerobiosis acelerada � Representa ligadura a ribosomas � Acumulación intracelular: Ligadura a ribosomas Alteración en la traducción del ARNm, produciendo proteínas alteradas Disrrupción de la pared con eflujo Inhibición de la replicación de ADN

Resistencia � Intrínseca � Enzimática � Metilación � No en el ARNm 16 S enzimática � Anaerobiosis � Adquirida � Ingreso disminuido � Eflujo � Modificación enzimática � Transmitidas por plásmidos o transposones

Propiedades farmacológicas � Administración parenteral, i. m. o i. v. � Baja ligadura a proteínas � Pobre absorción oral, prácticamente nula � Administración tópica � Efecto post antibiótico de hasta 3 horas � Otras vías: � Intrapleural � Intrapericárdica � Intraperitoneal � Intratecal � Irrigación vesical � Nebulización

Distribución � Amplia porque hay mala ligadura a proteínas � Varía con estados de edema � Altas concentraciones urinarias

Metabolismo � Inexistente

Excreción � Renal dominante � 99% � Resto por heces y saliva � Mayoría en las primeras 24 horas � Evidencia de residuos hasta 20 días después de la administración

Farmacocinética � FC de 3 fases: � : distribución del intravascular al espacio celular � : eliminación; excresión de la droga del plasma y del espacio extravascular �T � : ½ de 1, 5 a 3, 5 horas eliminación lenta de droga acumulada en riñón

Toxicidad � Depende de los niveles residuales Daño en túbulos contorneados proximales � Daño en cóclea � Bloqueo neuromuscular � � Todos correlacionan con sus cargas positivas a p. H fisiológico � Infrecuentes: Alergia e hipersensibilidad � Flebitis, dolor en sitio de inyección i. m. � � No hay irritación por instilación en serosas o LCR � No es hepatotóxico ni mielotóxico � No producen fotosensibilidad ni alteraciones en coagulación

Daño renal � Depende del calcio � La respiración mitocondrial se altera � Las células tubulares liberan enzimas de las células en borde de cepillo al contenido tubular � Fallan los transportadores de membrana � Se disminuye la absorción de magnesio y calcio a partir del filtrado glomerular � Se activa la apotosis � Inicia como oliguria para progresar a falla renal � Recupera con el paso de los días a pesar de continuar con el estímulo
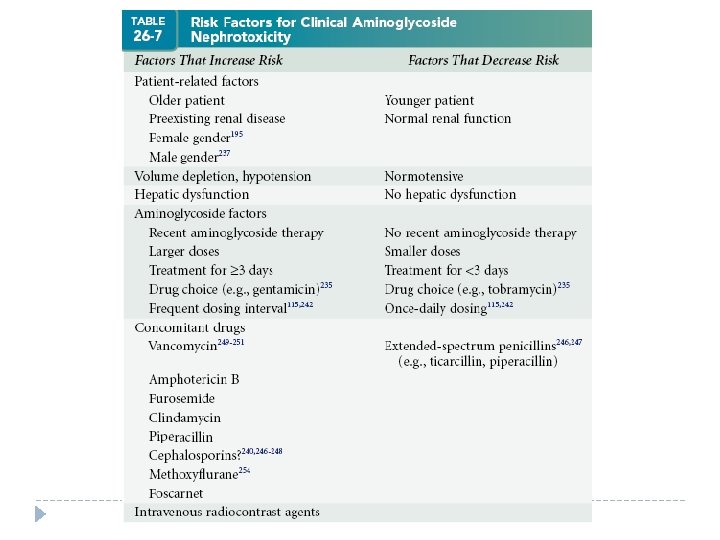
![Cálculo del aclaramiento de creatinina ACC = [140 – Edad (años)] X Peso (kg) Cálculo del aclaramiento de creatinina ACC = [140 – Edad (años)] X Peso (kg)](http://slidetodoc.com/presentation_image/517c7d12534e97db44a24fce2ce9d528/image-44.jpg)
Cálculo del aclaramiento de creatinina ACC = [140 – Edad (años)] X Peso (kg) Cr X 72 Mujer: ACC X 0, 85

Daño ótico � En ocasiones coclear y en otras vestibular � Rara vez ambos � Depende de exposición repetida � Efecto sumativo � Daño irreversible � Mecanismo preciso no conocido � Se propone que hay toxicidad de las células ciliadas

Bloqueo neuromuscular � Raro; serio potencialmente � Debilidad respiratoria � Parálisis flácida � Midriasis � Potenciado por drogas que afectan transmisión de la placa neuromuscular � Atribuible a bloqueo � Inhibición de la liberación de ACh presináptica � También a bloqueo de los receptores de ACh postsináptica � Internalización de calcio presináptico � Tratable con calcio parenteral
Regímenes de dosificación � Una dosis diaria � Mayor pico � Mayor letalidad � Menor toxicidad � Varias dosis diarias � Menor pico � Letalidad disminuida � Mayor toxicidad por niveles residuales mayores
Tetraciclinas

Tetraciclinas � Antibióticos de amplio espectro � Gram positivos � Gram negativos � Intracelulares � Clamidias � Rickettsias � Micoplasmas � Protozoarios: amebas y plasmodios � Bajo costo � Pocos efectos � Excepto niños y embarazadas

Clasificación � Primera � Corta generación vida media � Segunda � Vida generación media más larga � Tercera generación (? ) � Glicilciclinas
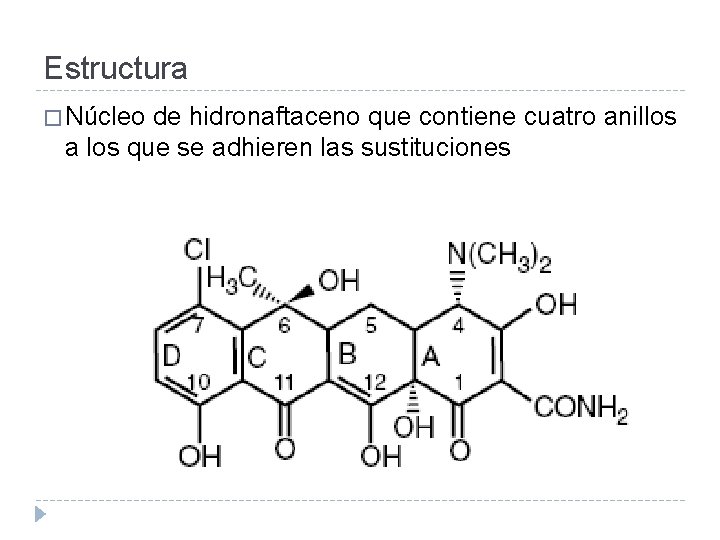
Estructura � Núcleo de hidronaftaceno que contiene cuatro anillos a los que se adhieren las sustituciones

Mecanismo de acción � Inhiben síntesis proteica al unirse a la fracción 30 S del ribosoma bacteriano, pero lo hacen en forma reversible � BACTERIOSTATICO � Esta unión bloquea la asociación del ARNt al sitio aceptor en el complejo ribosomal del ARNm � Impide la agregación o adición de nuevos amino ácidos a la cadena peptídica en elongación � Ingresan a la membrana externa de los GN por difusión pasiva a través de proinas, probablemente como moléculas cargadas positivamente asociadas con Mg � Luego, en el espacio periplásmico, el complejo se disocia y las TC ingresan a la membrana interna por difusión

Espectro amplio � No Cocos positivos � Cocos negativos � � Muy � � N. � gonorrhoeae Bacilos negativos � Vibrios Bacilos positivos � Espiroquetas � Clamidas � Micoplasmas � Micobacterias � Plasmodios � Amebas � Algunos anaerobios � incluyen Pseudomonas � Proteus

Mecanismos de resistencia � Genes adquiridos por elementos móviles de transferencia � Dos mecanismos básicos � Eflujo � Proteinas de protección ribosomal (RPP) � Dan cambios conformacionales que impiden la asociación de la TC sin que se altere la síntesis proteica � Resistencia a I y II G � En ocasiones están presentes ambos

Farmacología � Absorbidos en el intestino delgado � Presentaciones i. v. producen tromboflebitis � Presentaciones i. m. producen intenso dolor local � Las de II G tienen muy buena biodisponibilidad � Las de I G se afectan en absorción al ingerirse con alimentos � Reducción en la absorción con cationes (Mg, Ca, Fe) � Quelación, impedimento en absorción � I G no se debe dar con leche; II G en investigación � Podrían clasificarse en 3 grupos con base en la duración de su T ½, poco útil en la clínica

Distribución � Pequeñas � Depende cantidades en diversos líquidos de la liposolubilidad � Altas concentraciones en líquido sinovial y SPN � Minociclina es lipofílica � Eliminación de meningococo en estados de portación crónica � Atraviesan � Se placenta y leche materna depositan en huesos y dientes – CONTRAINDICADOS � Se eliminan en leche, pero en forma de complejos inactivos

Eliminación � Variable � Depende de cada droga � Incluye tanto renal como biliar y fecal � Insuficiencia � No renal se deberían usar � Excepciones: Doxiciclina y Tigeciclina

Toxicidad � Hematológica – eosinofilia � SNC � Gastrointestinal � Sobreinfección – diarrea inducida por AB � Riñón – IR, nefritis intersticial (algunas) � Hígado – rara � Esquelético – Pigmentación de dientes � Depositación en huesos de neonatos prematuros � � Piel - fotosensibilidad � Endocrino – antianabólico � Hipersensibilidad � Reacción de Jerish – Herxheimer
Glicilciclinas

Glicilciclinas � Tigeciclina � Derivado modificado de la minociclina � Administración parenteral � Espectro muy amplio � Activa contra Gram positivos, Gram negativos, anaerobios y atípicos, incluyendo microorganismos resistentes a múltiples antimicrobianos
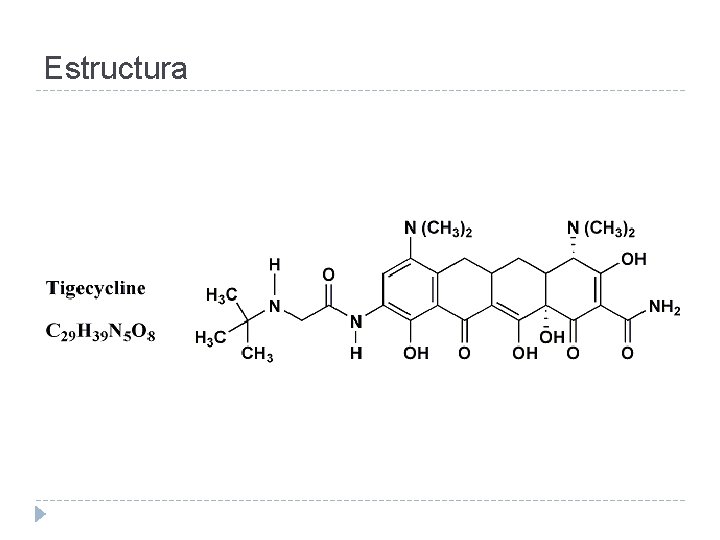
Estructura

Mecanismo de acción � Bacteriostático � Se une a la subunidad 30 S, y bloquea el ingreso del aminoacil RNAt dentro del sitio A del ribosoma, con lo cual inhibe la síntesis de proteínas bacterianas

Mecanismos de resistencia � Similares a las tetraciclinas � Eflujo � Proteínas de protección ribosomal � Modificaciones químicas (menos importante)

Farmacología � Amplio volumen de distribución � Bajo aclaramiento total � Larga vida media � Baja disponibilidad oral � Ligadura a proteinas de 71 a 89% � Penetra poco SNC � Metabolismo es limitado � Eliminación principalmente fecal, inalterada � Efecto post antibiótico variable

Efectos adversos � Principalmente gastrointestinales � Descritos, pero menos frecuentes � Cefalea � Hipertensión � Trombocitopenia

Fracción 50 S

Fracción 50 S � Anfenicoles � Macrólidos � Azálidos � Ketólidos � Anhidrólidos � Lincosaminas � Oxazolidinonas � Estreptograminas
Anfenicoles

Anfenicoles � Cloramfenicol � Tiamfenicol

Cloramfenicol � Muy amplio espectro � Gram positivos � Gram negativos � Anaerobios � Espiroquetas � Rickettsias � Clamidias � Micoplasmas � En desuso por aparente toxicidad medular
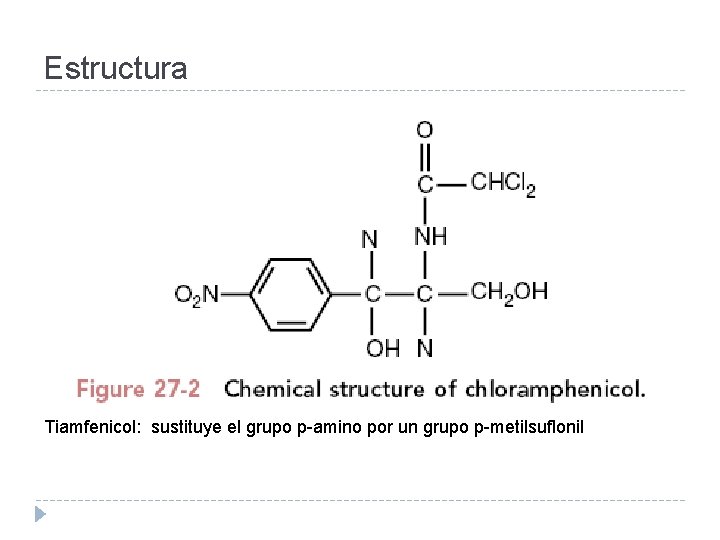
Estructura Tiamfenicol: sustituye el grupo p-amino por un grupo p-metilsuflonil

Mecanismo de acción � Ingresa a la célula por un mecanismo energía dependiente � Inhibe reversiblemente la síntesis proteica al ligarse a la fracción 50 S en un locus que previene la ligadura del ARNm en el extremo que contiene amino ácido a su región de unión � Sin esta unión, la asociación del substrato de amino ácido con la peptidiltransferasa no ocurre y por tanto se previene la formación de uniones peptídicas � Este bloqueo produce un efecto de tipo estático

Mecanismos de resistencia � Permeabilidad reducida � Mutación ribosomal � Producción de cloramfenicol acil transferasa

Farmacología � Muy buena absorción oral � Mejores niveles que cuando se da i. v. � Metabolismo hepático � Se conjuga con ácido glucurónico � Hace ciclo enterohepático de forma inactiva � La mayoría de la eliminación es renal

Toxicidad � Hematológica: � Anemia aplásica; resultado de la inhibición de síntesis de proteínas mitocondriales � Reversible, dosis dependiente � Irreversible: idiopática � Síndrome de niño gris � Neonatos � Distensión abdominal, vómitos, flacidez, cianosis, colapso circulatorio y muerte � Resultado de una habilidad disminuida para conjugar el AB en hígado y excretar la forma activa por vía renal � Neuritis óptica
Macrólidos, azálidos y ketólidos

Macrólidos y azálidos � Bacteriostáticos � Estructuras de 14 y 16 átomos � Eritromicina � Claritromicina � Azálidos tienen estructuras de 15 átomos � Azitromicina
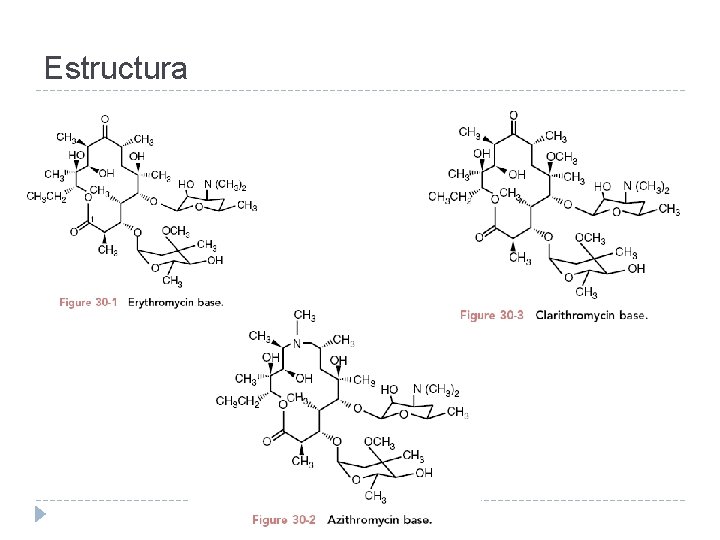
Estructura

Mecanismo de acción � Inhiben la síntesis de proteínas ARN dependiente en el paso de elongación de la cadena � Como consecuencia, el ARNt se disocia del ribosoma

Mecanismos de resistencia � Impermeabilidad � Eflujo � Alteraciones del sitio objetivo � Inactivación enzimática � Fosfotransferasas

Espectro � Amplio � Gram positivos � Estreptococos � Gram � No negativos son útiles para enterobacterias � Actinomicetes � Micobacterias � Treponemas � Micoplasmas � Clamidias � Rickettsias Gran utilidad en IVRI

Farmacología � Eritromicina Pobre absorción oral � Destrucción por ácidos gástricos � Estolato � � Correlación con litiasis vesiculares � Amplia distribución � Concentración intracelular en macrófagos � Ligadura a proteínas variable � 40 a 90% � Penetra LCR y atraviesa placenta � Propiedades no antimicrobianos Propiedades procinéticas � Propiedades antiinflamatorias �

Farmacología � Claritromicina � Bien y azitromicina absorbidos � Evitar con antiácidos con Mg o Al � Metabolismo � Metabolito � Ligadura hepático activo, sinergístico: 14 -OH claritromicina a proteínas � 65 – 70% para claritromicina � 7 – 50% para azitromicina �T ½ � Claritromicina 5 a horas � Azitromicina 68 horas � Ajuste de dosis en IR terminal por acúmulo de droga � Amplia distribución, buena penetración a tejidos

Reacciones adversas � Irritativas intestinales � Alérgicas cutáneas � Colestasis – rara (estolato) � Trastornos del ritmo � Torsades pointes � Prolongación del QT � Sobreinfección � Colitis pseudomembranosa

Ketólidos � Semisintéticos � Bacteriostáticos � Mayor estabilidad frente a los ácidos � No inducen resistencia de tipo MLSB � Tienen grupo ceto en posición 3
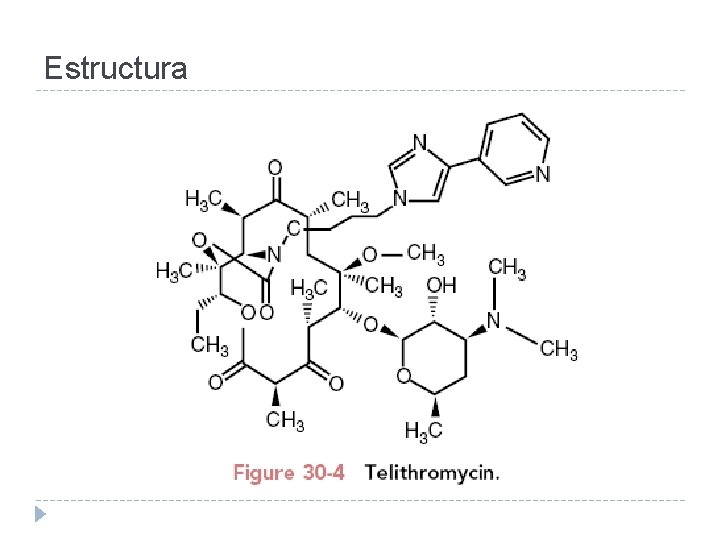
Estructura

Mecanismo de acción � Similar al de los macrólidos � La diferencia está en la naturaleza de su interacción con el ribosoma: � Mayor afinidad � Mecanismos que se sobreponen a la metilación de los sitios de unión � Adicionalmente, inhibe la formación de la subunidad 50 S y aún más, en altas concentraciones (a diferencia de los macrólidos) puede inhibir la formación de la subunidad ribosomal 30 S

Mecanismos de resistencia � Raros � No inducen genes que codifiquen para MLSB

Espectro � Similar al de los macrólidos � Muy útiles contra estreptococos resistentes � Útiles contra Enterococcus faecalis pero no contra E. faecium

Farmacología � Se absorben bien con o sin comidas � Biodisponibilidad de aprox. 60% � Buena distribución en todos los compartimentos � Incluidos � Se macrófagos metaboliza el 70% en hígado

Reacciones adversas � Similares � Hepatitis � Baja fulminante frecuencia � Afectación a personas con Miastenia Gravis
Lincosaminas

Lincosaminas � Clindamicina � Lincomicina
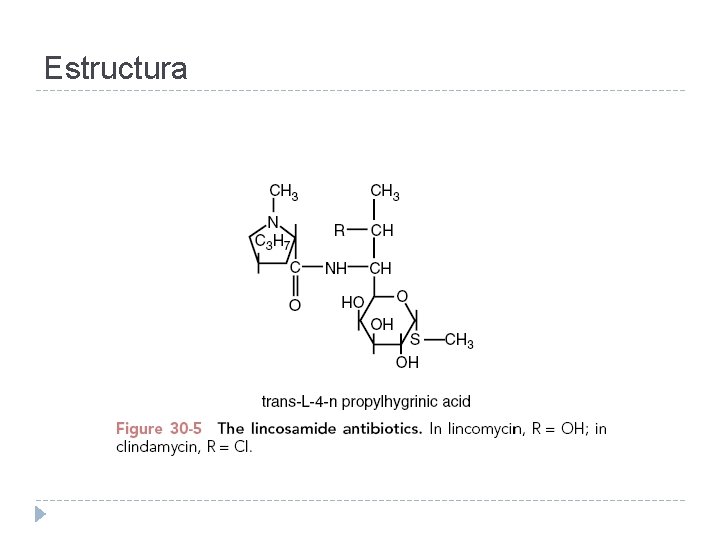
Estructura

Mecanismo de acción � Es el mismo mecanismo que para macrólidos y cloramfenicol � Hay competencia por el substrato � La síntesis proteica se inhibe primariamente en la elongación temprana de la cadena por interferencia con la reacción de transpeptidación � También pueden estimular la disociación del ARNt de los ribosomas

Mecanismos de resistencia � Alteración en el ARNm de la subunidad 23 S del ribosoma 50 S (metilación de la adenina) � Mutaciones en el ARNr bacteriano � Alteración en las proteínas de receptor de la subunidad 50 S � Inactivación enzimática (rara, escasa) � Impermeabilidad (enterobacterias)

Espectro � Cocos positivos � Anaerobios � Algunos bacilos negativos anaerobios

Farmacología � Absorción de 90% � Retrasada pero no impedida por alimentos (clindamicina; lincosamina si es bloqueada) � Administración i. m. , i. v. , tópico, vaginal � Buena penetración, excepto SNC incluso en meningitis � Metabolismo hepático � T ½ 2, 4 horas � Sin modificación por función renal

Reacciones adversas � Dermatológicas � Exantemas, eritema multiforme, anafilaxia � Diarrea � Colitis inducida por antibióticos � Colitis � Leve pseudomembranosa alteración de PFH ocasionalmente � Raro: neutropenia, leucopenia, trombocitopenia

Oxazolidinonas

Oxazolidinonas � Clase completamente sintética � Empezó como un grupo con actividad antibiótica vegetal � Sólo hay un elemento de uso clínico aprobado
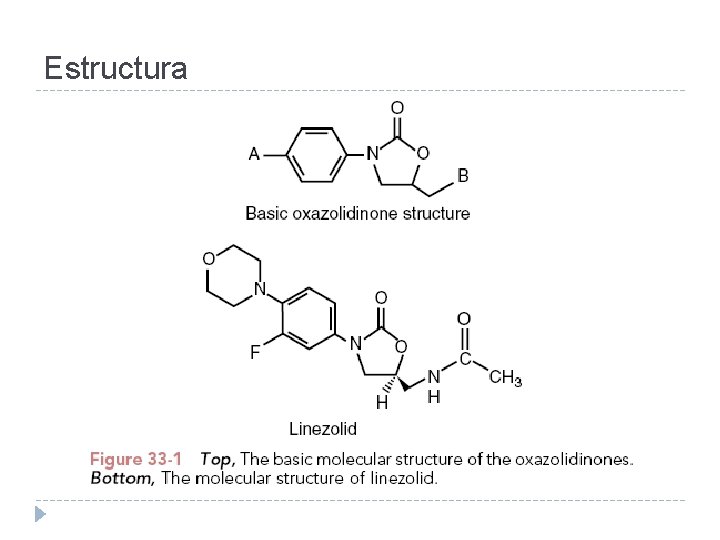
Estructura

Mecanismo de acción � Inhiben síntesis proteica � Son bacteriostáticos � Mecanismo único: inhibición de etapas tempranas de síntesis proteica, al ligarse al ribosoma 50 S en su interfase con la fracción 30 S, lo que previene la formación del complejo de iniciación del ribosoma bacteriano 70 S � La ligadura es inhibida competitivamente por cloramfenicol y lincomicina, lo que propone que el sitio se sobrepone o se comparte, aunque no hay resistencia cruzada entre estas drogas � Las oxazolidinonas no inhiben la formación del iniciador del ARNt

Espectro � La mayoría de los cocos positivos � Incluidos � Alguna sensibles y resistentes actividad contra Neisseriae � Sin actividad contra Gram negativos � Sin actividad contra intracelulares � Actividad contra Nocardia y Mycobacteria en estudio

Espectro

Farmacología � Buena � Casi absorción oral, rápida 100% � Metabolizado por oxidación � Eliminación renal del 85% � 30 – 40% sin metabolizar � Ligadura a proteínas 31% � Distribución a líquidos adecuada, incluso SNC

Resistencia � Mutación en 23 S � Metiltransferasa de ARNt � Afecta múltiples clases

Toxicidad � Digestivos � Diarrea � Raros: � Cefalea � Hipertensión � Hematológicos � Mielosupresión � Inhibición transitoria, reversible de la MAO � Síndromes serotoninérgicos en pacientes usando drogas serotoninérgicas � Ocasional neurotoxicidad periférica

Estreptograminas

Estreptograminas � Diferentes compuestos, que incluyen: � Mikamicina � Virginiamicina � Pristinamicina � Quinupristin � Cada – dalfopristin uno posee dos anillos macrocíclicos de lactona peptólido, que son referidos como estreptogramina A (poliinsaturado) y estreptogramina B (hexadepsipéptidos cíclicos)

Mecanismo de acción � Inhibe la síntesis en el ribosoma en la fracción 50 S en la segunda fase, de elongación � Estreptogramina A (dalfopristin) bloquea la adición de nuevos amino ácidos a la molécula en crecimiento � Estreptogramina B (quinupristin), parecido a los macrólidos, actúa en una fase tardía previniendo la elongación y causando la liberación de cadenas peptídicas incompletas � La unión de dalfopristin ejerce una alteración conformacional que favorece la unión de quinupristin � Complejo irreversible � Actividad bactericida

Espectro � Contra Gram positivos � Algunos Gram negativos

Mecanismos de resistencia � Diferentes para cada componente � 3 tipos generales de resistencia: � Cambios conformacionales � Inactivación enzimática � Eflujo por transporte activo

Farmacología � Tiene efecto post antibiótico variable, según la especie � T ½ corta � Administración i. v. � Amplio volumen de distribución � Eliminación fecal � No atraviesa SNC ni placenta

Efectos adversos � Flebitis � Mialgias � Artralgias � Digestivos � Cutáneos � Inhibición significativa del P 450 3 A 4
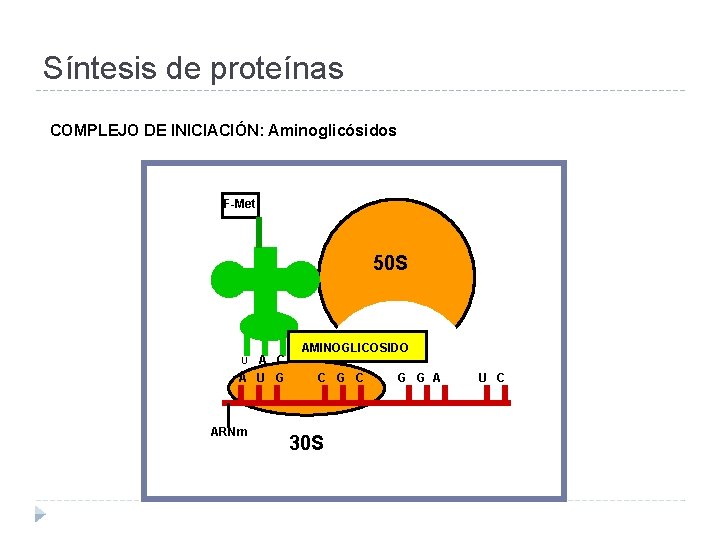
Síntesis de proteínas COMPLEJO DE INICIACIÓN: Aminoglicósidos F-Met 50 S A C A U G AMINOGLICOSIDO U ARNm C G C 30 S G G A U C
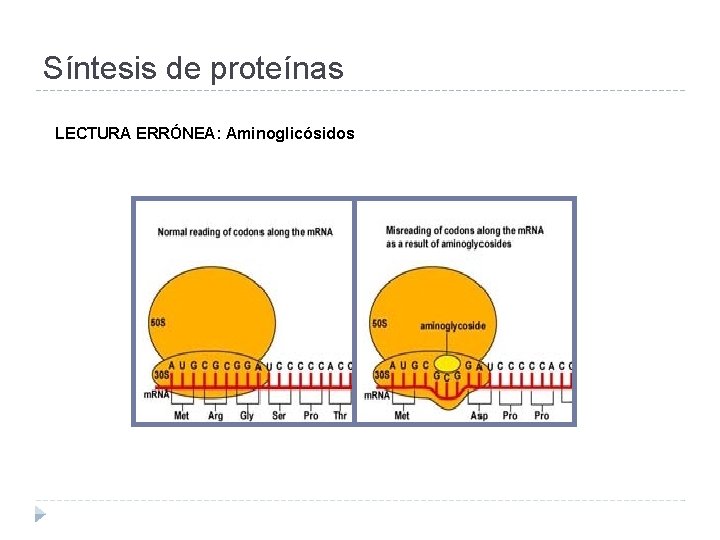
Síntesis de proteínas LECTURA ERRÓNEA: Aminoglicósidos
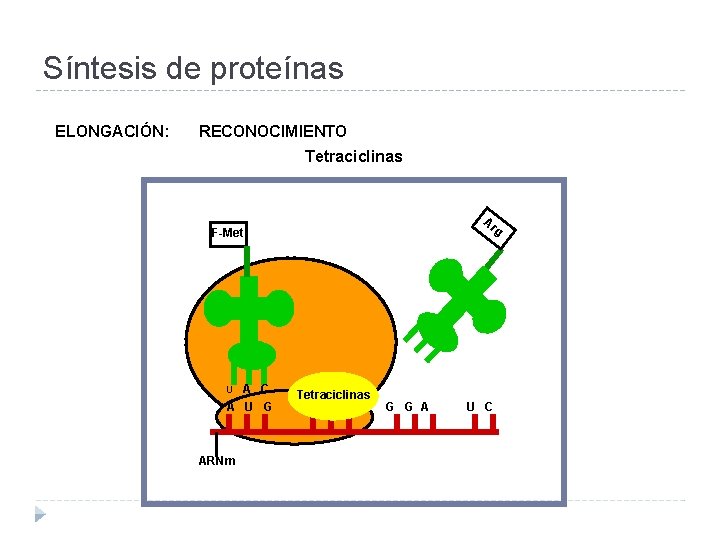
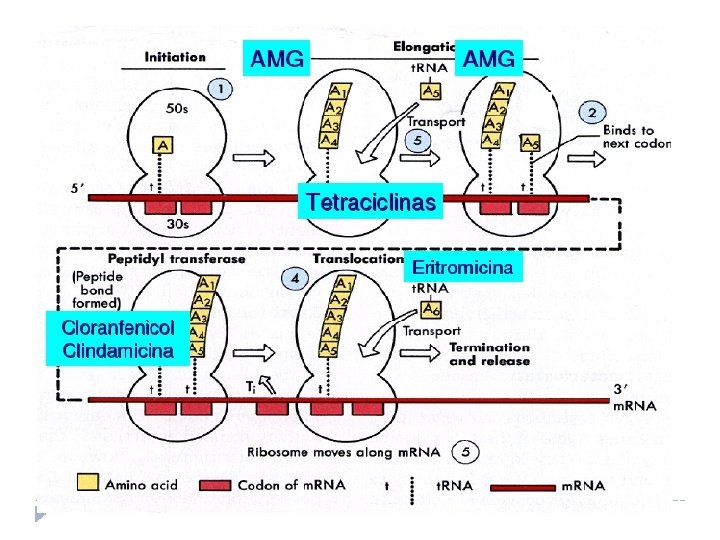
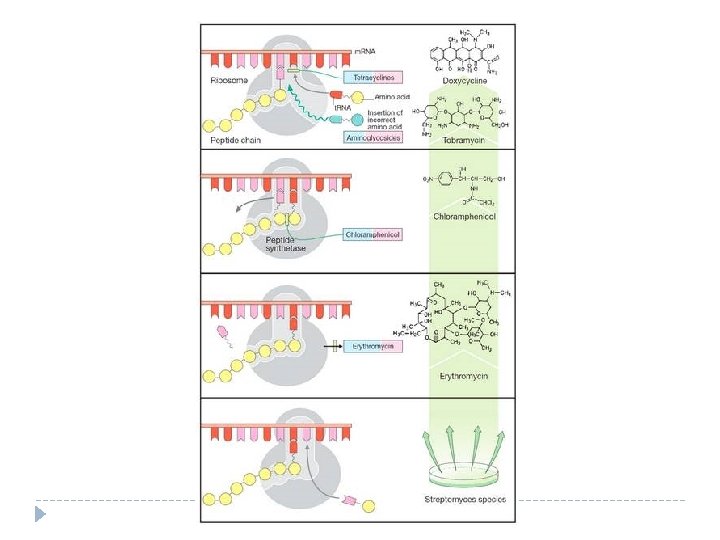
Síntesis de proteínas ELONGACIÓN: RECONOCIMIENTO Tetraciclinas Ar g F-Met A C A U G U ARNm Tetraciclinas C G G A U C
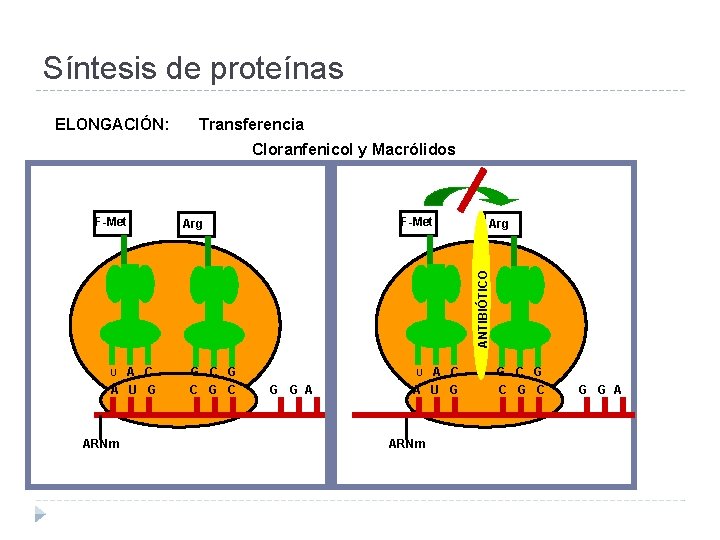
Síntesis de proteínas ELONGACIÓN: Transferencia Cloranfenicol y Macrólidos F-Met Arg ANTIBIÓTICO F-Met A C A U G U ARNm G C G C A U G G A U C ARNm G C G C G G A
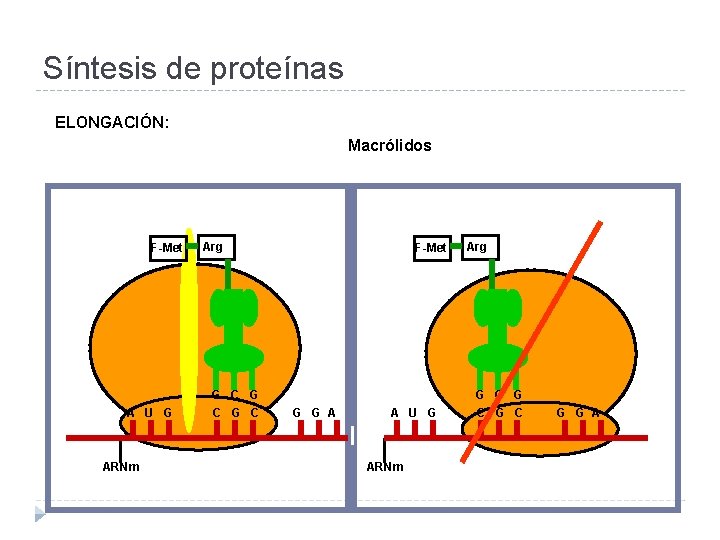
Síntesis de proteínas ELONGACIÓN: Macrólidos F-Met A U G ARNm Arg G C G C F-Met G G A A U G ARNm Arg G C G C G G A
- Slides: 123