Mcanismes molculaires des rsistances aux fongicides chez Botrytis

Mécanismes moléculaires des résistances aux fongicides chez Botrytis cinerea Unité de Phytopharmacie & Médiateurs Chimiques INRA Versailles - Pierre Leroux Catherine Albertini René Fritz Annick Arnold Michel Gredt Jocelyne Bach Catherine Lanen Florence Chapeland Frédérique Tellier Danièle Debieu Sabine Fillinger

Botrytis cinerea - agent de la pourriture grise z Pathogène polyphage z Impact économique sur viticulture h. Moyens de lutte: prophylaxie (entretien des vignes), lutte biologique, résistance variétale et lutte chimique à raison de 3 applications maximales par an.

Critères des pesticides ÚEfficacité à faibles doses (résidus limités) Ø pas de toxicité vis à vis des organismes non-cibles (ex. : levures) Ø faible impact environnemental Ø risque de résistance minime! r nécessité de stratégies anti-résistances
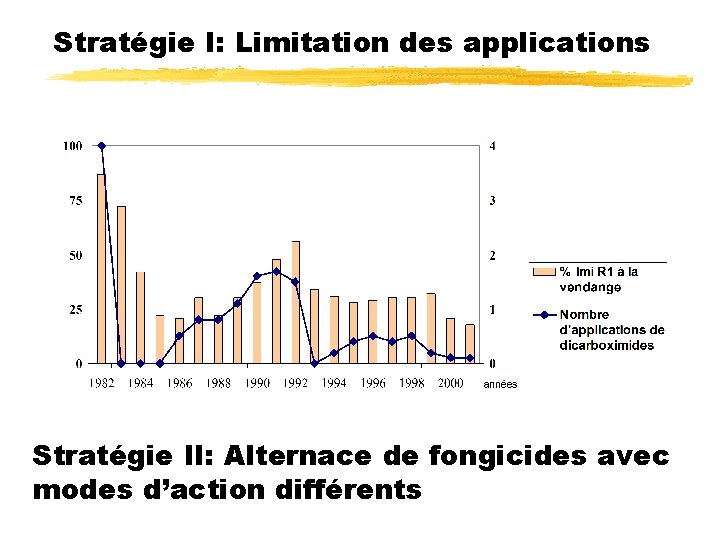
Stratégie I: Limitation des applications Stratégie II: Alternace de fongicides avec modes d’action différents
![Sites d’action des fongicides ? stérols RESPIRATION Multi-sites minéraux [Cu] thirame, folpel Chaine respiratoire Sites d’action des fongicides ? stérols RESPIRATION Multi-sites minéraux [Cu] thirame, folpel Chaine respiratoire](http://slidetodoc.com/presentation_image_h2/4741e388244e3854d60052be1efdc27c/image-5.jpg)
Sites d’action des fongicides ? stérols RESPIRATION Multi-sites minéraux [Cu] thirame, folpel Chaine respiratoire [carboxamides, strobilurines, famoxadone] polyols O 2 SBIs imidazoles (prochloraze, …) triazoles (tébuconazole, …) amines [fenpropimorphe, . . . ] hydroxyanilides (fenhexamide) CO 2 Phosphorylation oxydative ADN découplants (fluazinam) précurseurs ARN Anti - microtubules ? benzimidazoles (carbendazime, ) phénylcarbamates (diéthofencarbe) acides aminés vacuole cytosquelette
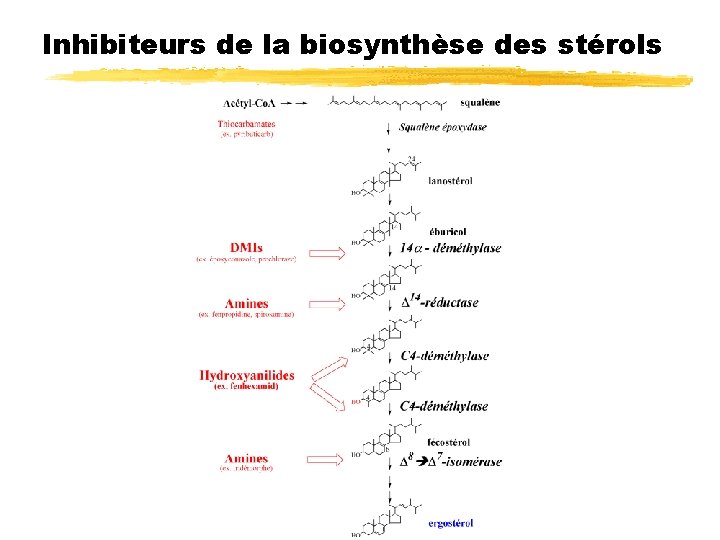
Inhibiteurs de la biosynthèse des stérols
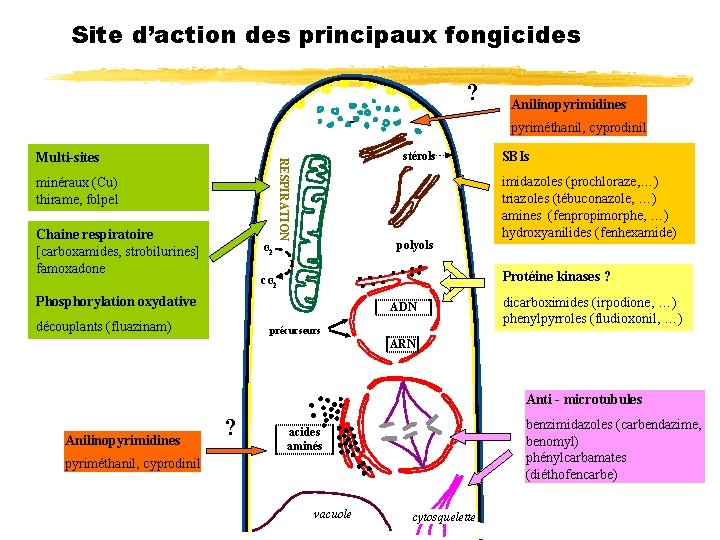
Site d’action des principaux fongicides ? Anilinopyrimidines pyriméthanil, cyprodinil stérols RESPIRATION Multi-sites minéraux (Cu) thirame, folpel Chaine respiratoire [carboxamides, strobilurines] famoxadone polyols O 2 imidazoles (prochloraze, …) triazoles (tébuconazole, …) amines (fenpropimorphe, …) hydroxyanilides (fenhexamide) Protéine kinases ? CO 2 Phosphorylation oxydative ADN découplants (fluazinam) SBIs précurseurs dicarboximides (irpodione, …) phenylpyrroles (fludioxonil, …) ARN Anti - microtubules Anilinopyrimidines ? benzimidazoles (carbendazime, benomyl) phénylcarbamates (diéthofencarbe) acides aminés pyriméthanil, cyprodinil vacuole cytosquelette

Mécanismes de résistance 1/Mutation de la cible ou surproduction 2/Diminution de l’accumulation du fongicide yimport réduit /export actif ydétoxification 3/Système de contournement yvoie enzymatique “alternative” ymutation dans protéine-kinase ou autre régulateur 4/Mécanismes inconnus
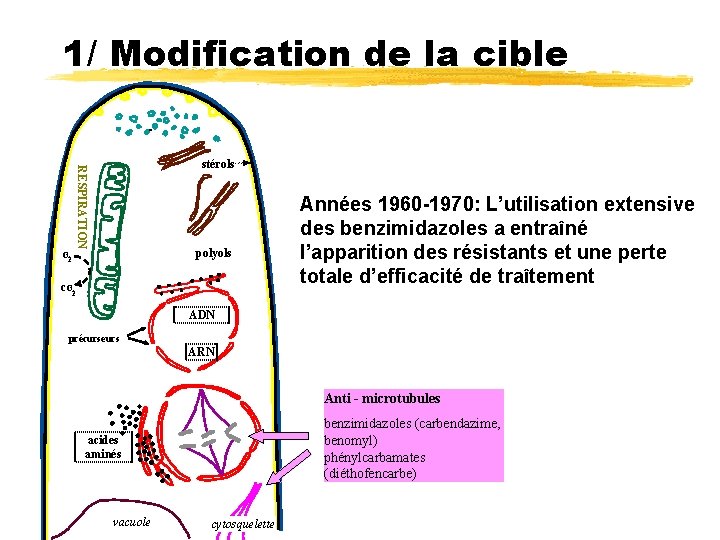
1/ Modification de la cible RESPIRATION stérols polyols O 2 CO 2 Années 1960 -1970: L’utilisation extensive des benzimidazoles a entraîné l’apparition des résistants et une perte totale d’efficacité de traîtement ADN précurseurs ARN Anti - microtubules benzimidazoles (carbendazime, benomyl) phénylcarbamates (diéthofencarbe) acides aminés vacuole cytosquelette
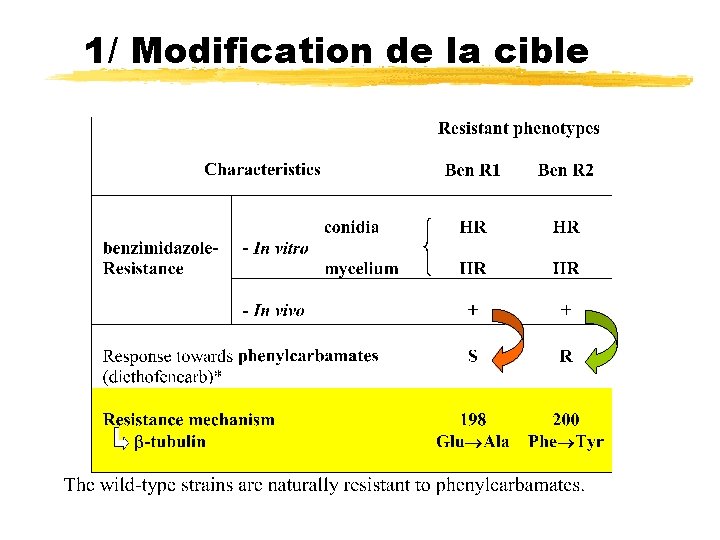
1/ Modification de la cible
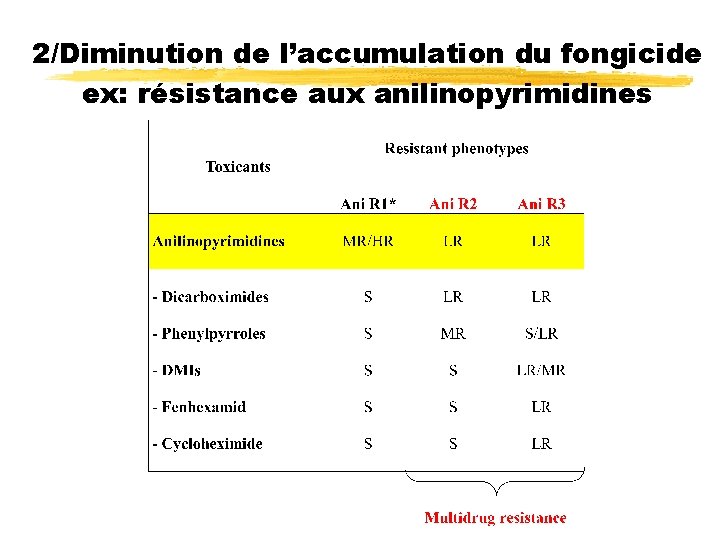
2/Diminution de l’accumulation du fongicide ex: résistance aux anilinopyrimidines
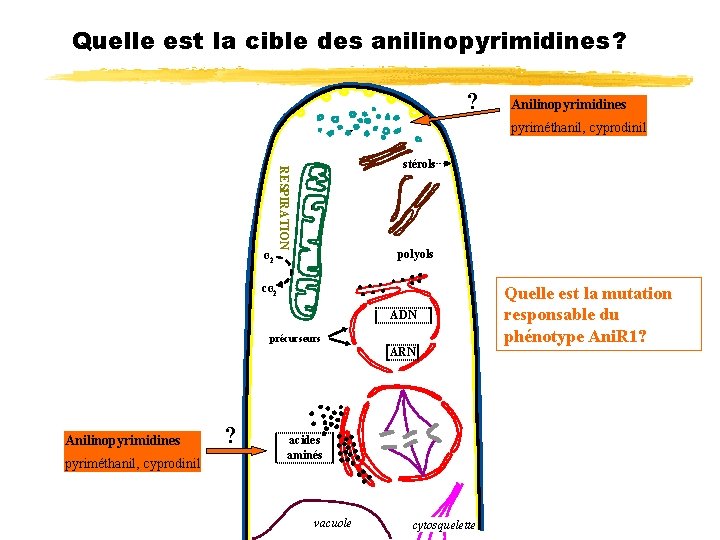
Quelle est la cible des anilinopyrimidines? ? Anilinopyrimidines pyriméthanil, cyprodinil RESPIRATION stérols polyols O 2 CO 2 ADN précurseurs ARN Anilinopyrimidines pyriméthanil, cyprodinil ? acides aminés vacuole cytosquelette Quelle est la mutation responsable du phénotype Ani. R 1?
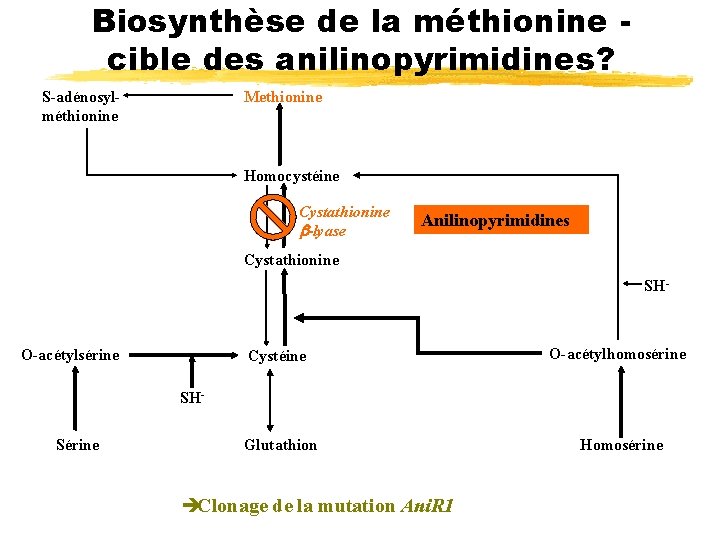
Biosynthèse de la méthionine cible des anilinopyrimidines? S-adénosylméthionine Methionine Homocystéine Cystathionine b-lyase Anilinopyrimidines Cystathionine SH- O-acétylsérine Cystéine O-acétylhomosérine Glutathion Homosérine SHSérine èClonage de la mutation Ani. R 1
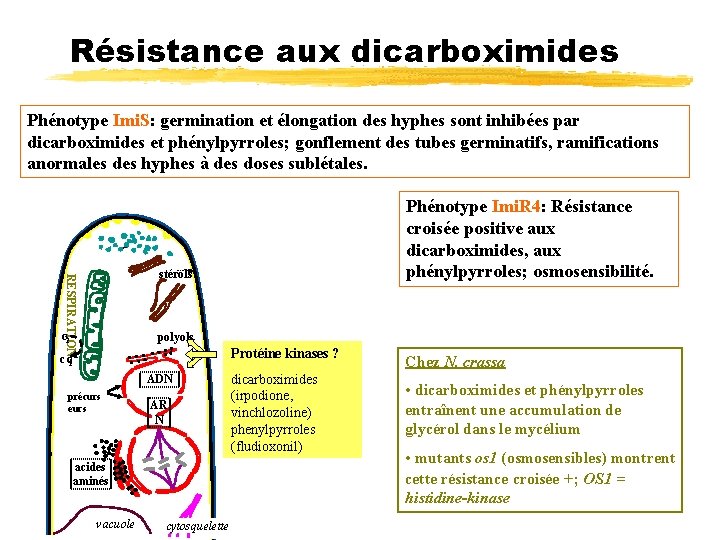
Résistance aux dicarboximides Phénotype Imi. S: germination et élongation des hyphes sont inhibées par dicarboximides et phénylpyrroles; gonflement des tubes germinatifs, ramifications anormales des hyphes à des doses sublétales. Phénotype Imi. R 4: Résistance croisée positive aux dicarboximides, aux phénylpyrroles; osmosensibilité. RESPIRATION stérols polyols O 2 Protéine kinases ? CO 2 ADN précurs eurs AR N acides aminés vacuole cytosquelette dicarboximides (irpodione, vinchlozoline) phenylpyrroles (fludioxonil) Chez N. crassa • dicarboximides et phénylpyrroles entraînent une accumulation de glycérol dans le mycélium • mutants os 1 (osmosensibles) montrent cette résistance croisée +; OS 1 = histidine-kinase
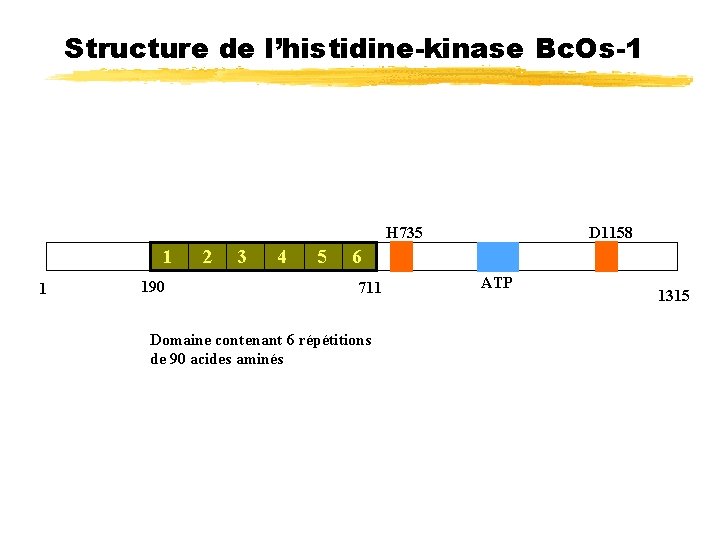
Structure de l’histidine-kinase Bc. Os-1 H 735 1 1 190 2 3 4 5 D 1158 6 711 Domaine contenant 6 répétitions de 90 acides aminés ATP 1315
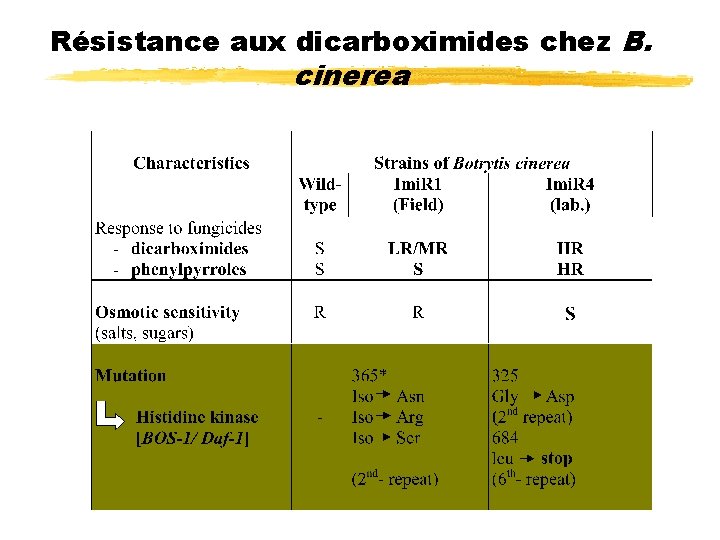
Résistance aux dicarboximides chez B. cinerea

Perspectives z. Résistances aux dicarboximides: y. Verification des mutations Imi. R (dicarboximides) par génétique réverse. y. Démonstration de l’interaction Bc. Os 1/Iprodione z Développement de nouveaux marqueurs de sélection sur la base des résistances (btubuline) z. Caractérisation des résistances «noncaractérisées» par clonage directe (p. FAC 1? )
- Slides: 17