Mcanismes daction des Bisphonates Vronique Breuil CHU de

Mécanismes d’action des Bisphonates Véronique Breuil – CHU de Nice

La découverte Connu dès 1865 Utilisé dans l’industrie anti-calcaire 1968 : H Fleisch In vitro : précipitation du phosphate de calcium dissolution du phosphate de calcium In vivo : calcifications vasculaires résorption osseuse +++

Action des bisphonates • Puissants inhibiteurs de la résorption osseuse • AMM dans pathos asso à résorption osseuse – – – Hypercalcémies Métastases osseuses Myélome multiple Maladie de Paget Ostéoporose
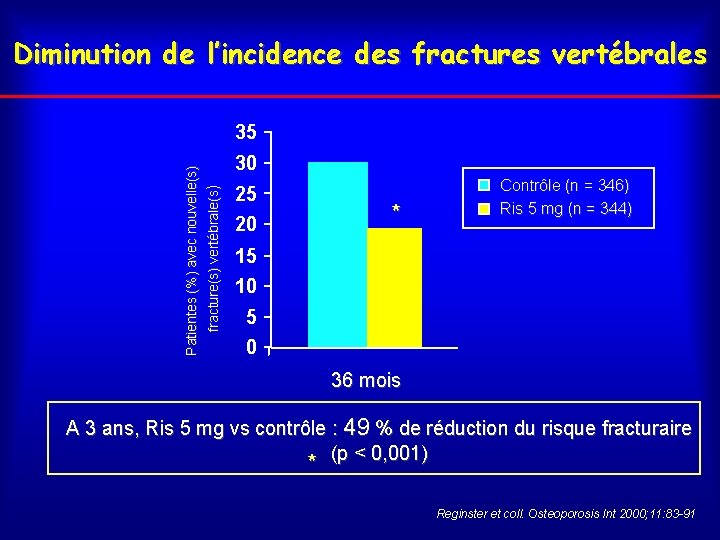
Diminution de l’incidence des fractures vertébrales Patientes (%) avec nouvelle(s) fracture(s) vertébrale(s) 35 30 25 * 20 Contrôle (n = 346) Ris 5 mg (n = 344) 15 10 5 0 36 mois A 3 ans, Ris 5 mg vs contrôle : 49 % de réduction du risque fracturaire (p < 0, 001) * Reginster et coll. Osteoporosis Int 2000; 11: 83 -91
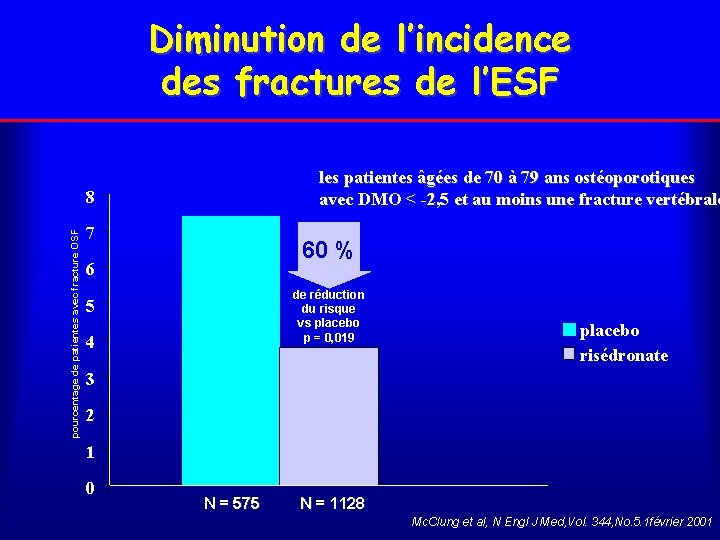
Diminution de l’incidence des fractures de l’ESF les patientes âgées de 70 à 79 ans ostéoporotiques avec DMO < -2, 5 et au moins une fracture vertébrale pourcentage de patientes avec fracture OSF 8 7 60 % 6 de réduction du risque vs placebo p = 0, 019 5 4 placebo risédronate 3 2 1 0 N = 575 N = 1128 Mc. Clung et al, N Engl J Med, Vol. 344, No. 5. 1 février 2001

Mécanismes d’action • Tissulaires • Cellulaires • Moléculaires
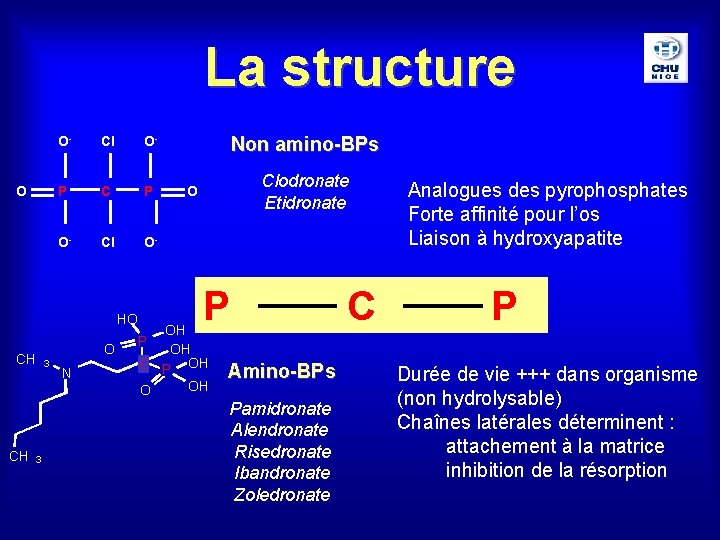
La structure O O- Cl O- P C P O- Cl O- HO CH CH 3 O 3 N Non amino-BPs Clodronate Etidronate O P OH OH C P OH OH O C Analogues des pyrophosphates Forte affinité pour l’os Liaison à hydroxyapatite P P Amino-BPs Pamidronate Alendronate Risedronate Ibandronate Zoledronate Durée de vie +++ dans organisme (non hydrolysable) Chaînes latérales déterminent : attachement à la matrice inhibition de la résorption

Caractéristiques chimiques • Liaison P-C-P • Analogues des pyrophosphates • Forte affinité pour l’os • Liaison à hydroxyapatite • Chaîne P-C-P résistante à l’hydrolyse enzymatique : non catabolisés, libérés sous forme intacte • Durée de vie importante dans organisme • Propriétés fonction des chaînes latérales (attachement à la matrice, inhibition de la résorption)
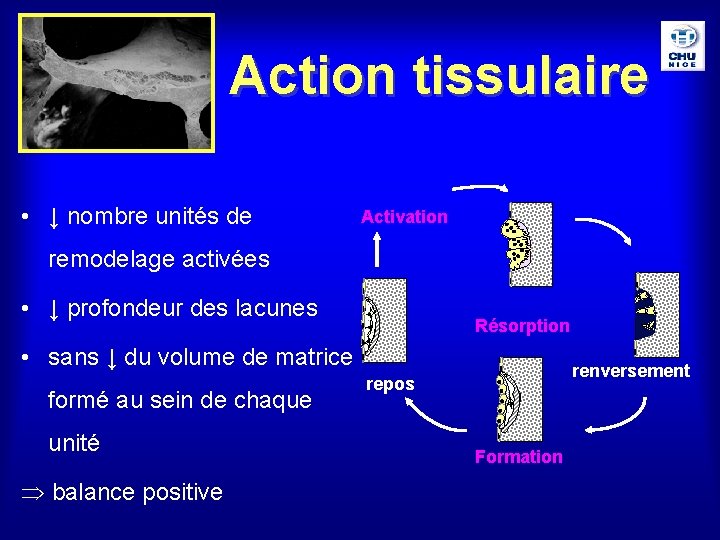
Action tissulaire • ↓ nombre unités de Activation remodelage activées • ↓ profondeur des lacunes Résorption • sans ↓ du volume de matrice formé au sein de chaque unité balance positive renversement repos Formation
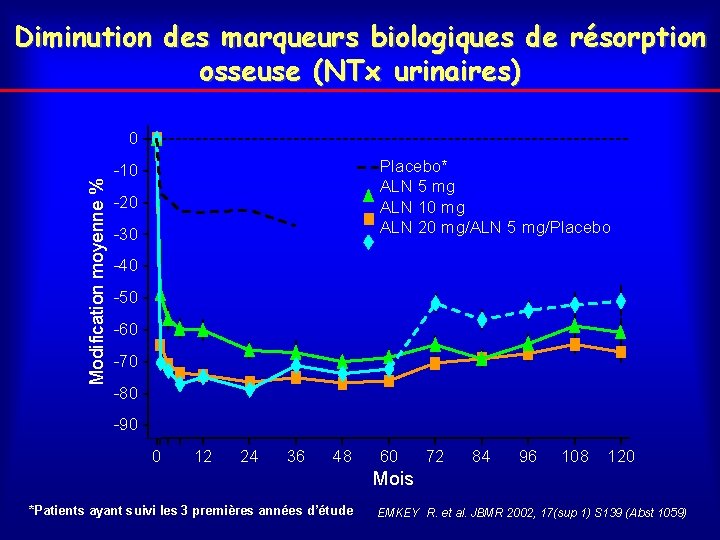
Diminution des marqueurs biologiques de résorption osseuse (NTx urinaires) Modification moyenne % 0 Placebo* ALN 5 mg ALN 10 mg ALN 20 mg/ALN 5 mg/Placebo -10 -20 -30 -40 -50 -60 -70 -80 -90 0 12 24 36 48 60 72 84 96 108 120 Mois *Patients ayant suivi les 3 premières années d’étude EMKEY R. et al. JBMR 2002, 17(sup 1) S 139 (Abst 1059)
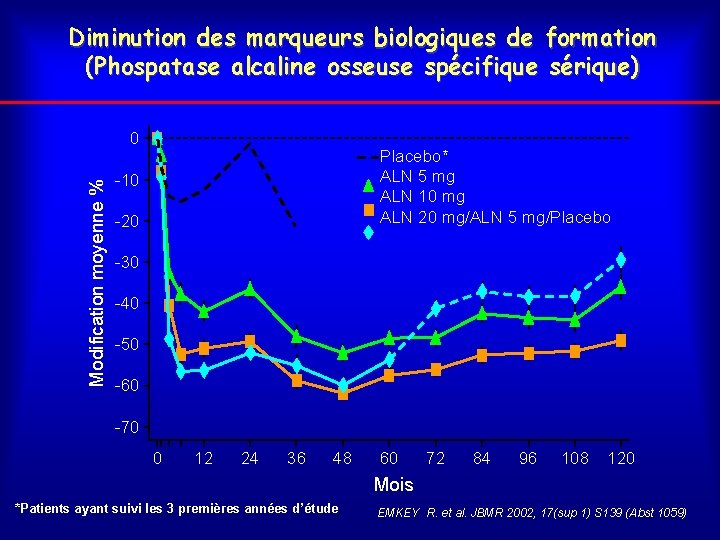
Diminution des marqueurs biologiques de formation (Phospatase alcaline osseuse spécifique sérique) Modification moyenne % 0 Placebo* ALN 5 mg ALN 10 mg ALN 20 mg/ALN 5 mg/Placebo -10 -20 -30 -40 -50 -60 -70 0 12 24 36 48 60 72 84 96 108 120 Mois *Patients ayant suivi les 3 premières années d’étude EMKEY R. et al. JBMR 2002, 17(sup 1) S 139 (Abst 1059)
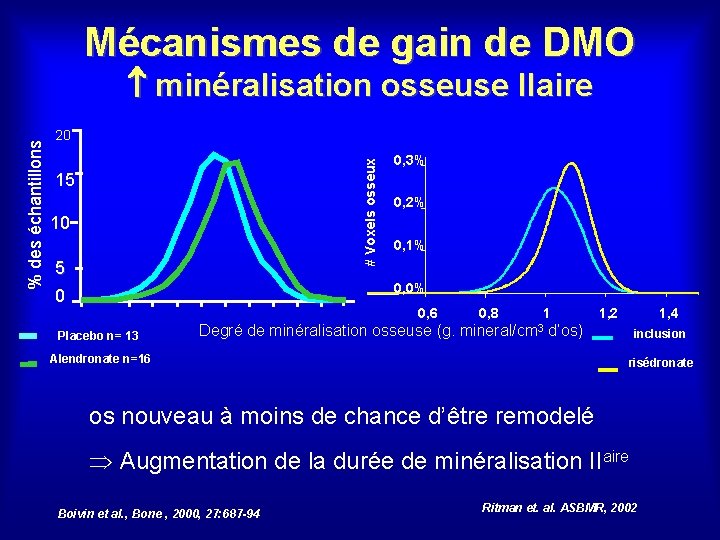
Mécanismes de gain de DMO 20 # Voxels osseux % des échantillons minéralisation osseuse IIaire 15 10 5 0, 3% 0, 2% 0, 1% 0, 0% 0 0, 6 Placebo n= 13 Degré de minéralisation osseuse (g. 0, 8 1 mineral/cm 3 1, 2 1, 4 d’os) Alendronate n=16 inclusion risédronate os nouveau à moins de chance d’être remodelé Augmentation de la durée de minéralisation IIaire Boivin et al. , Bone , 2000, 27: 687 -94 Ritman et. al. ASBMR, 2002

Augmentation de la DMO 5 persistance de formation dans les unités activées : gain précoce de DMO (4 - DMO vertébrale • ↓ de la résorption et 6 mois) 4 3 2 1 0 6 mois • minéralisation secondaire : gain tardif Risédronate 35 mg 12 mois 5 mg 50 mg Brown et al. , Calcif Tissue Int 2002, 71: 103 -111

Ostéoporose post- ménopausique : détérioration de la micro-architecture Femme non ostéoporotique Femme ostéoporotique (avec fr. vert. ) Diminution de la masse osseuse et perte des travées horizontales Sept 2002 Borah, et al. Anat. Rec.

Préservation de la micro-architecture Direction de charge Echantillons de vertèbres de cochon nain après 18 mois Contrôle OVX RIS 2. 5 mg/kg/j Borah et al. , J Bone Miner Res. 2002 Jul; 17(7): 1139 -47

Qualité osseuse DMO : explique qu’une partie de l’augmentation de la résistance osseuse induite par les BPs préservation de la micro-architecture Ø travées horizontales Contrôle Ø volume osseux Ø nombre de travées Ø espaces intertravées Risédronate 5 mg Ø connectivité Inclusion Recker R et al. 2005 Benhamou CL et al. , 2005 +1 an Borah et al. , Bone 2004
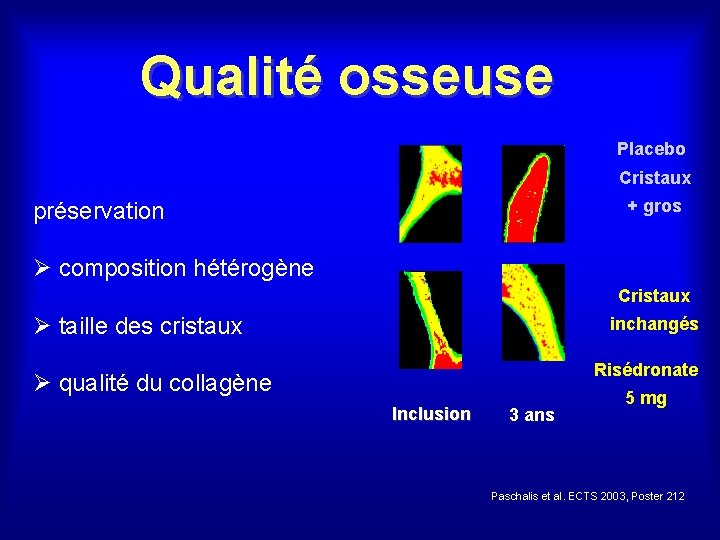
Qualité osseuse Placebo Cristaux + gros préservation Ø composition hétérogène Cristaux Ø taille des cristaux inchangés Risédronate Ø qualité du collagène Inclusion 3 ans 5 mg Paschalis et al. ECTS 2003, Poster 212
Action cellulaire Ostéoclaste Cellule spécialisée dans la résorption osseuse cible privilégiée de l’action des BPs
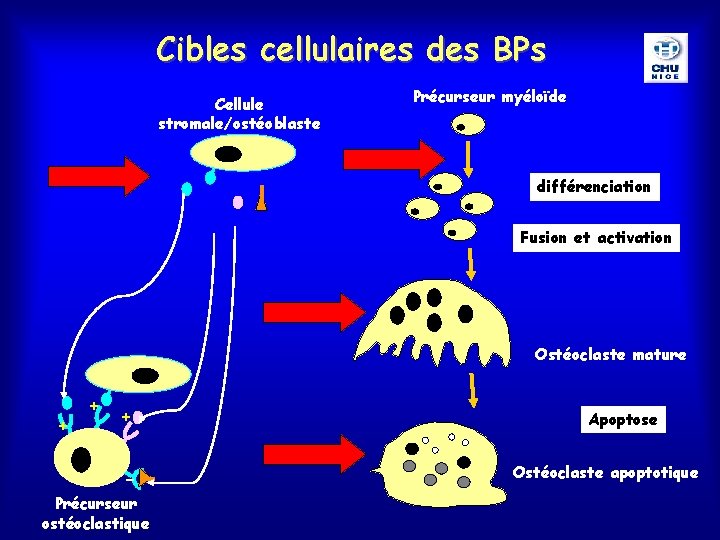
Cibles cellulaires des BPs Cellule stromale/ostéoblaste Précurseur myéloïde différenciation Fusion et activation Ostéoclaste mature + + + - Précurseur ostéoclastique Apoptose Ostéoclaste apoptotique

Au niveau cellulaire mécanismes d ’action intriqués !!! Résultats selon les modèles et les BP testés - altération physico-chimique : ↓la dissolution de l ’os - inhibition recrutement - inhibition de l ’adhésion - ↓ durée de vie - inhibition de l ’activité Directe sur OC ou indirecte via les OB

Altération de la structure osseuse par un phénomène physico-chimique Ø analogues des pyrophosphates fixés à l ’hydroxyapatite : ↓de la dissolution de l ’hydroxyapatite ? ? Ø mais ne rend pas compte de la puissance pharmacologique des BP observée in vivo : - à forte C, ↓ de la dissolution de l ’hydroxyapatite - à faible C, nouveaux BP inhibent la résorption sans modification des propriétés de dissolution minérale Fleisch H et al. Science, 1969

Interactions BP- hydroxyapatite • Fn de la composition de la chaîne latérale • Degré d’affinité : ZOL > ALN > IBD > RIS > ETI > CLO • Modifications variables : - de la structure des cristaux HA selon la charge électrique des chaînes latérales (RIS ALN, ZOL, IBD) - de l’interface solide / liquide Explique certaines différences d’action (rapidité d’action, degré de rétention) au sein même des amino-BPs Nancollas GH et al. Bone 2006

Inhibition du recrutement des OC Ø Action directe sur les précurseurs : - modèles murins (Schmidt 1996, Boonekamp 1986) - modèle humain (culture de moelle, Hughes 1989) - Inhibition de la prolifération macrophages +++ lignée monocytes -macrophages (Cecchini 1987, 1990, modèle murin souris) - effet à un stade terminal de différentiation (TRAP) (Löwik 1988 : modèle murin) Ø Action indirecte : sécrétion par les OB d ’un facteur inhibiteur du recrutement ou de la durée de vie des OC (Shani 1993, Vitté 1996)

Inhibition de l’adhésion cellulaire Ø Diminution de l ’adhésion des OC à la matrice : étidronate (Colucci S 1995) inhibition de la formation de l ’anneau d ’actine nécessaire à la polarisation et l ’adhésion : Alendronate, Tiludronate (Sato 1991, Murakami 1995) Ø Diminution de l’adhésion des cellules tumorales: cancer du sein et de la prostate (Boissier 1997, Van Der Pluijm G 1996)

Diminution durée de vie des OC Ø Effet cytotoxique : ssi fortes C ne reflète pas effets des BP aux doses usuelles Ø Induction de l ’apoptose des OC : Hughes (1995) : risédronate, pamidronate, alendronate - in vitro, modèle murin - in vivo : souris saine/ nude + ostéolyse méta/saine + IL 1 Rogers (1996) : in vitro, lignée macrophagiques pamidronate, ALN, ibandronate, clodronate mais pas étidronate

Inhibition de l ’activité des OC matures • Inhibition de l ’activité des OC démontré dans modèles - murins : souris (Van Beek 1997), rat (Sato 1991) - humain : culture primaire (Breuil 1998) Interaction entre OC et ALN lié à la matrice osseuse - résorption osseuse avec initiale du nombre d ’OC, mais inactifs tardive du nombre OC stimulation formation pour compenser activité OC ? Schenk (1973), Miller (1979), Endo (1993)
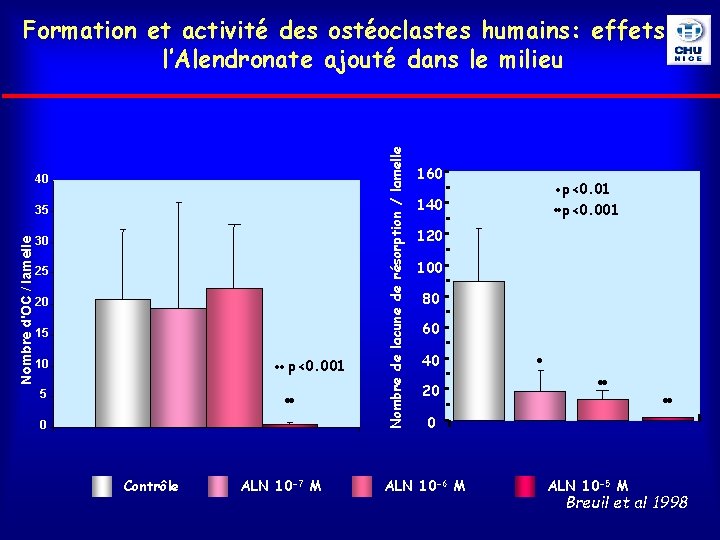
40 Nombre d'OC / lamelle 35 30 25 20 15 p<0. 001 10 • • 5 0 Contrôle ALN 10 -7 M Nombre de lacune de résorption / lamelle Formation et activité des ostéoclastes humains: effets de l’Alendronate ajouté dans le milieu 160 • p<0. 01 • • p<0. 001 140 120 100 80 60 40 20 • • • 0 ALN 10 -6 M ALN 10 -5 M • • Breuil et al 1998
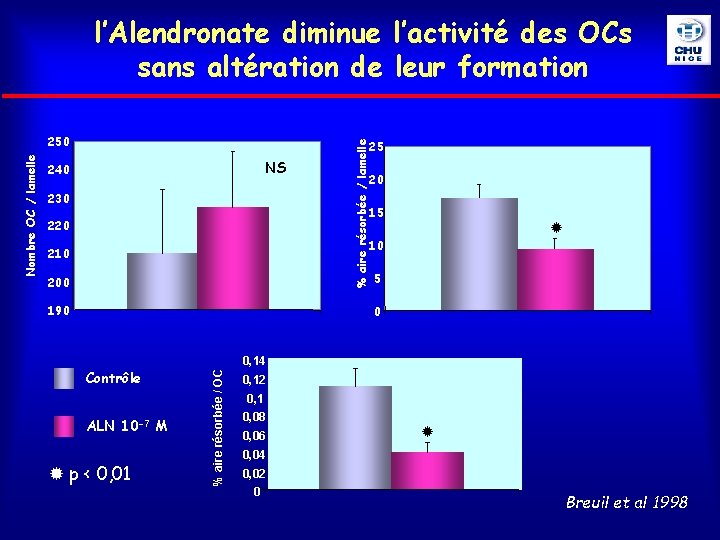
l’Alendronate diminue l’activité des OCs sans altération de leur formation NS 240 230 % aire résorbée / lamelle 25 20 15 220 10 200 190 5 0 Contrôle ALN 10 -7 M p < 0, 01 0, 14 % aire résorbée / OC Nombre OC / lamelle 250 0, 12 0, 1 0, 08 0, 06 0, 04 0, 02 0 Breuil et al 1998
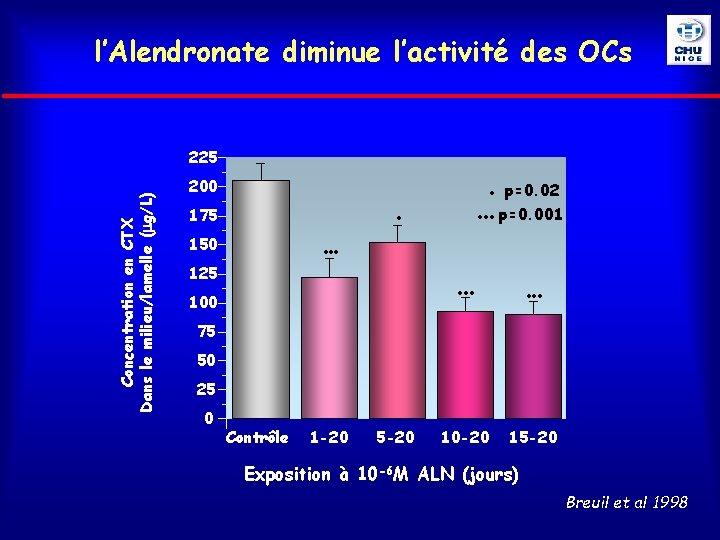
l’Alendronate diminue l’activité des OCs Concentration en CTX Dans le milieu/lamelle ( g/L) 225 200 175 • 150 • p=0. 02 • • • p=0. 001 • • • 125 100 • • • 10 -20 15 -20 75 50 25 0 Contrôle 1 -20 5 -20 Exposition à 10 -6 M ALN (jours) Breuil et al 1998
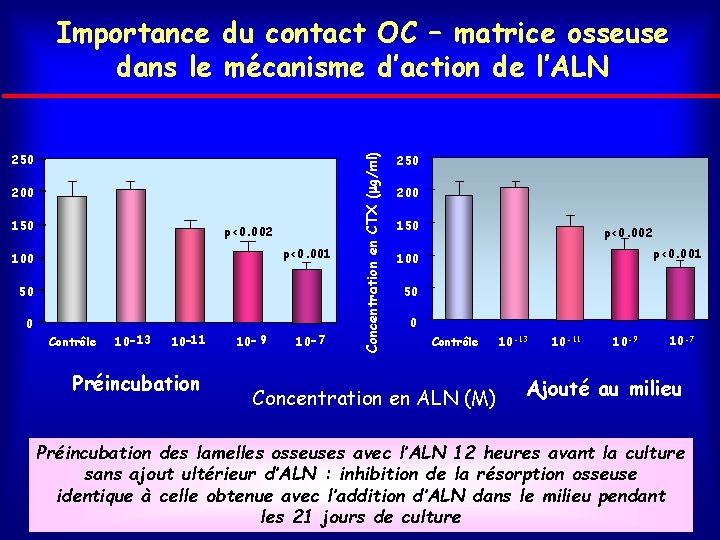
250 200 150 p<0. 002 p<0. 001 100 50 0 Contrôle 10 -13 10 -11 Préincubation 10 - 9 10 -7 Concentration en CTX ( g/ml) Importance du contact OC – matrice osseuse dans le mécanisme d’action de l’ALN 250 200 150 p<0. 002 p<0. 001 100 50 0 Contrôle Concentration en ALN (M) 10 -13 10 -11 10 -9 10 -7 Ajouté au milieu Préincubation des lamelles osseuses avec l’ALN 12 heures avant la culture sans ajout ultérieur d’ALN : inhibition de la résorption osseuse identique à celle obtenue avec l’addition d’ALN dans le milieu pendant les 21 jours de culture

Action directe sur les OC matures • Modifications morphologiques: in vivo et in vitro Cytosquelette : actine, vinculine, membrane plissée ( Sato 90 et 91, Murakami 95, Selander 94, Plasmans 80, Miller 79) seult sur OC actifs résorbant os / BP injectés dans cell. • Ingestion des BP par les OC Felix 84 • Dépôt préférentiel des BP sous les OC et os nouvellement formé (Sato 91, Azuma 95) Fortes C intra-C de BP OC incorporent les BP liés à os entraînant une inhibition de l ’activité des OC

Action sur les ostéoblastes Sécrétion facteurs inhibiteurs de la différenciation ou la survie OC (cf) synthèse de collagène par OB et chondrocytes clodronate (Guenther 1981) nodules de minéralisation Alendronate dans culture de moelle (Giulani 1995)

Au niveau moléculaire • Action des BP peut être médiée par : – liaison à un R de surface ou site de liaison induisant transduction du signal : OB exposés seult 5 mn à de faibles C de BP induit sécrétion d ’un F inhibiteur des OC. Mais R non identifié. – Ingestion dans la cellule par pinocytose : interaction avec enzymes / molécules du métabolisme cellulaire.

Effets sur sécrétions OC et OB • Modifications morphologiques de la bordure en brosse : excrétion acide des OC (Sato 1991) – Na+ indpte (Zimolo 1995) – Inhibition de la pompe à protons H+ATPase par tiludronate mais pas autres BP (David 1996) • ac. lactique des OC (pamidronate) (Shinoda 1983) • Inhibition enzymes lysosomiales (Delaissé 1985) • Inhibition de la prostaglandines par OB (Felix 1981, Ohya 1985) • Clivage de RANKL membranaire (+ TACE) (Zolédronate) (PAN B. 2004) expression de RANKL par OB et C. stromale (amino. BP) (Nishida 2005)

Effets des BP sur enzymes utilisant pyrophosphates et ATP • Pas d’inhibition des phosphatases acides ou alcalines (sauf fortes C. ) • Inhibition de tyrosines phosphatases : – régulent activité des tyrosines kinases : contrôle croissance, différenciation et activité cellulaire – PTP , CD 45, PTPs – ALN (Schmidt 96, Skorey 97), étidronate (Endo 96) , pamidronate, tiludronate (Murakami 97) – pas de corrélation entre cette inhibition et puissance in vivo.

Induction d’apoptose par les amino-BP la voie du mévalonate ALN, ibandronate, risédronate, pamidronate inh. voie du mévalonate : farnesyl diphosphate ase modification prénylation post-traductionnelle de protéines fixant le GTP (ras, rho, rac, rab) : + gpt géranyl ou farnesyl perte fn (cytosquelette, bordure plissée, trafic vésiculaire) activation de la caspase 3 Apoptose (Hughes 95, Bergstrom 2000, Benford 99, Luckman 98, Roger 96, Fisher 99, Coxon 2000, Van Beek 99)
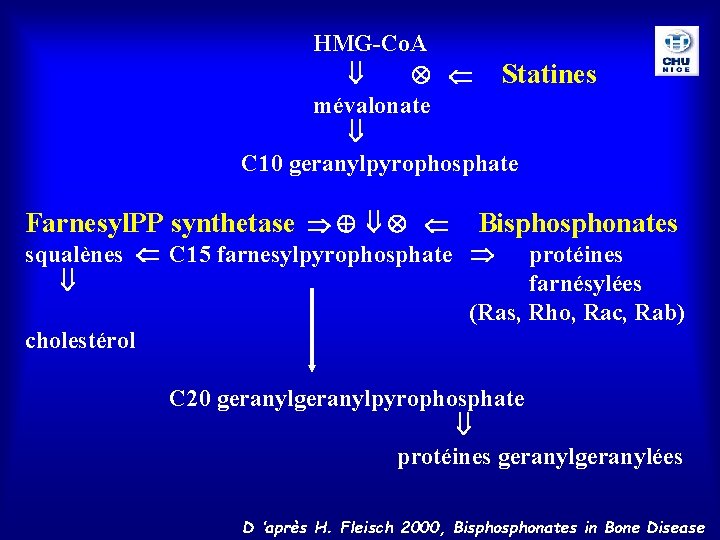
HMG-Co. A Statines mévalonate C 10 geranylpyrophosphate Farnesyl. PP synthetase Bisphonates squalènes C 15 farnesylpyrophosphate protéines farnésylées (Ras, Rho, Rac, Rab) cholestérol C 20 geranylpyrophosphate protéines geranylées D ’après H. Fleisch 2000, Bisphonates in Bone Disease

Induction d’apoptose par les non amino-bisphonates Etidronate, tiludronate, clodronate - similitude ++ avec pyrophosphates - se substituent aux gpts phosphates de l ’ATP analogues non hydrolysables apoptose - pas d ’inhibition de la caspase 3, ni de la prénylation (Benford 99, Mönkkönen 98, Makkonen 99, Luckman 98,

Effet anti-apoptotique des BP sur les ostéoblastes et ostéocytes OP cortisonique - apoptose des OB et ostéocytes - BP efficaces dans prévention OP cortisonique JCI 1999 : Plotkin LI et al. Etidronate, ALN, pamidronate, olpadronate prévention apoptose osteocytes (MLO-Y 4 murin) et osteoblastes (calvaria souris) rapide de ERKs

BP et tumeurs Inhibition de l ’ostéolyse induite par C. tumorales (sein et prostate) (Jung 84, Hall 94, Sasaki 95) Pas d ’inhibition in vitro de prolifération des cellules tumorales, mais inhib. in vivo de la masse tumorale (Boissier 97, Hall 94, Sasaki 95, Yoneda 97) Ø adhésion des C. tumorales à la matrice osseuse (Boissier 97, Van der Pluijm 96) Ø MMP-2 et 9 (dégradation matrice nécessaire à l ’invasion tumorale) (Boissier, Makowski 99, Stearns 98) Ø interaction plaquettes-C. tumorales (Marion 98) Apoptose des plasmocytes tumoraux (Shipman 97 -98, Aparicio 98) Effets anti-angiogéniques (Zol, Ris, IBD) (Caraglia 2006)
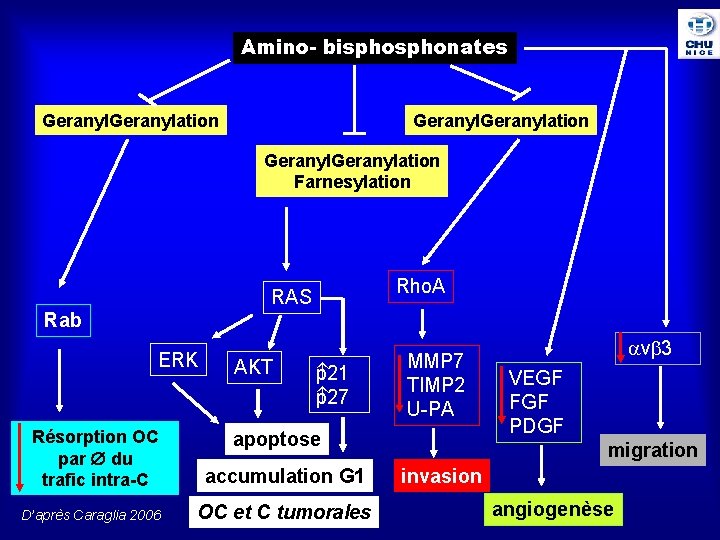
Amino- bisphonates Geranylation Farnesylation Rho. A RAS Rab ERK AKT 21 p p 27 Résorption OC par du trafic intra-C accumulation G 1 D’après Caraglia 2006 OC et C tumorales MMP 7 TIMP 2 U-PA apoptose v 3 VEGF FGF PDGF migration invasion angiogenèse

BP et système immunitaire Lignée monocytes-macrophages - prolifération et activité migration des macrophages - ALN synthèse IL 1 , IL 6 et TNF (Raw 264) - Pamidronate production IL 6 - Clodronate & pamidronate (pas ALN) production de NO. - Clodronate : production par macrophage TNF , IL-1 induisant apoptose (NF B), PKC monocytes/macrophages. expression mol. d’adhésion C bordantes synoviales

Nouvelles cibles thérapeutiques ? • OC reconnu comme coupable de la destruction articulaire de la PR • Physiopathologie de l’arthrose : rôle de l’os sous-chondral • Investigations sur les effets potentiels des BPs sur la destruction et l’inflammation des Rhumatismes inflammatoires et arthrose

Non Amino-bisphonates Animal : Arthrite à adjuvent chez rat Clodronate : ↓ Production synoviale de TNFα Doses pharmaco : ↓ Inflammation ↓ Hyperplasie des cellules synoviales bordantes Doses élevées cytotoxiques: Effet pro-inflammatoire Étidronate : Mécanisme incertain (↓ du remodelage de l'os sous-chondral ? ) ↓ Inflammation clinique Clinique : clodronate PR – amélioration clinique Mécanisme : ↓ IL-1 , TNF- , 2 microglobuline sécrétés par synoviocytes ↓ expression molécules d’adhésion ↓ nombre de macrophages Corrado A et al. 2007

Amino-bisphonates Alendronate Animal : Arthrite à l'adjuvant (rat)-↓ Inflammation Apoptose des ostéoclastes Clinique : Polyarthrite rhumatoïde - Amélioration clinique Arthrose - ↓ douleurs articulaires mécanismes : ↓IL 1, IL 6; TNFα, β 2 microglobuline ↓ Œdème de l'os sous-chondral Ibandronate Arthrite au collagène (souris) - pro-inflammatoire ↑ Migration leucocytaire ↑ Densité capillaire ↑Vélocité érythrocytaire Zolédronate : Arthrite au collagène (rat) : Effet structurel sur les articulations Arthrite TNF-transgénique (souris) : ↓ Érosions osseuses Arthrose induite par le carréganane (rat) : Effet chondroprotecteur Mécanismes : ↓ du nombre d'ostéoclastes ↓ de la dégradation du collagène de type I ↓ De l'appauvrissement en protéoglycanes ↓ Du remodelage de l'os sous-chondral Effet sur le métabolisme des chondrocytes Corrado A et al. 2007

Amino-bisphonates Pamidronate : Polyarthrite rhumatoïde - Amélioration clinique Spondylarthrite ankylosante - ↓ érosions articulaires Syndrome Sapho - Amélioration clinique, radiologique mécanismes : ↓ IL 1β ↑apoptose des monocytes ↓ Œdème péri-articulaire, Hyperostose, Ostéite Risédronate : Arthrose Effet structurel sur les articulations, ↓ douleurs articulaires non confirmés mécanismes : ↓ Dégradation du cartilage ↓ Remodelage de l'os sous-chondral INTERET DES BPs RESTE A CONFIRMER DANS CES PATHOLOGIES Corrado A et al. 2007

CONCLUSIONS Mécanismes d’action d’inhibition de la résorption osseuse par les bisphoantes bien connus. Encore beaucoup à apprendre sur les effets extra-osseux. Perspectives intéressantes dans Arthrose et PR A confirmer
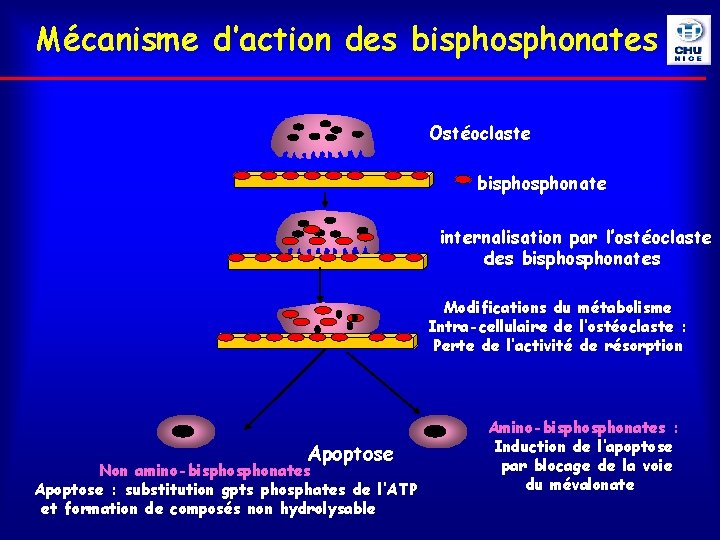
Mécanisme d’action des bisphonates Ostéoclaste bisphonate internalisation par l’ostéoclaste des bisphonates Modifications du métabolisme Intra-cellulaire de l’ostéoclaste : Perte de l’activité de résorption Apoptose Non amino-bisphonates Apoptose : substitution gpts phosphates de l’ATP et formation de composés non hydrolysable Amino-bisphonates : Induction de l’apoptose par blocage de la voie du mévalonate
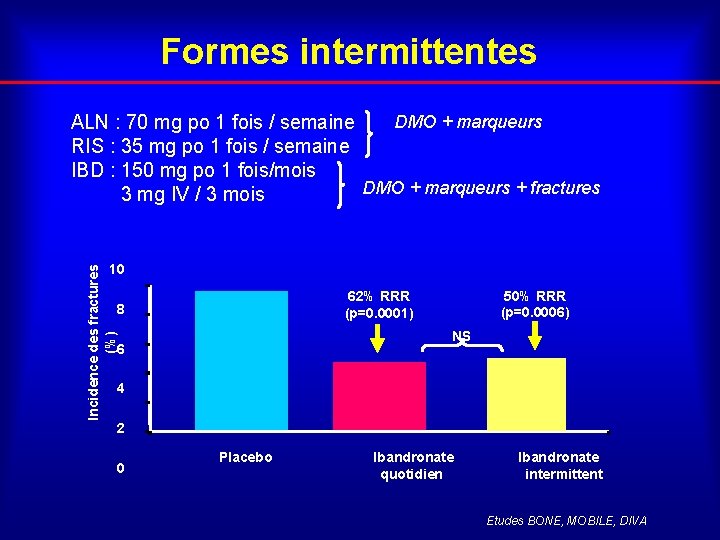
Formes intermittentes DMO + marqueurs ALN : 70 mg po 1 fois / semaine RIS : 35 mg po 1 fois / semaine IBD : 150 mg po 1 fois/mois DMO + marqueurs + fractures 3 mg IV / 3 mois Incidence des fractures (%) 10 50% RRR (p=0. 0006) 62% RRR (p=0. 0001) 8 NS 6 4 2 0 Placebo Ibandronate quotidien Ibandronate intermittent Etudes BONE, MOBILE, DIVA
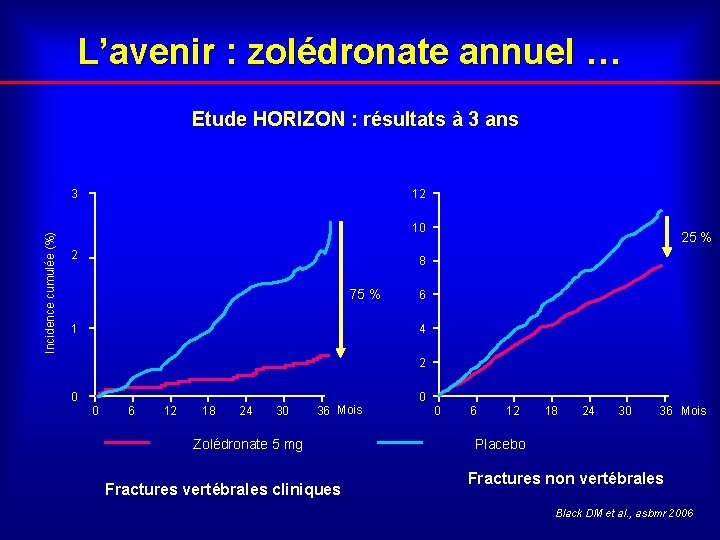
L’avenir : zolédronate annuel … Etude HORIZON : résultats à 3 ans Incidence cumulée (%) 3 12 10 2 25 % 8 75 % 1 6 4 2 0 0 0 6 12 18 24 30 36 Mois Zolédronate 5 mg Fractures vertébrales cliniques 0 6 12 18 24 30 36 Mois Placebo Fractures non vertébrales Black DM et al. , asbmr 2006

Tolérance des bisphonates Ostéoporose • maladie chronique • Espérance de vie après la ménopause : > 30 ans Bisphonates • Fixation forte à la matrice osseuse (accumulation) • Inhibition puissante du remodelage osseux • Au long cours : os gelé (ostéopétrose) avec effet paradoxal d’augmentation du risque de fracture ? • Le recul : Alendronate : 10 ans Risédronate : 7 ans Ibandronate : 3 ans • Données : DMO, qualité osseuse, Fractures
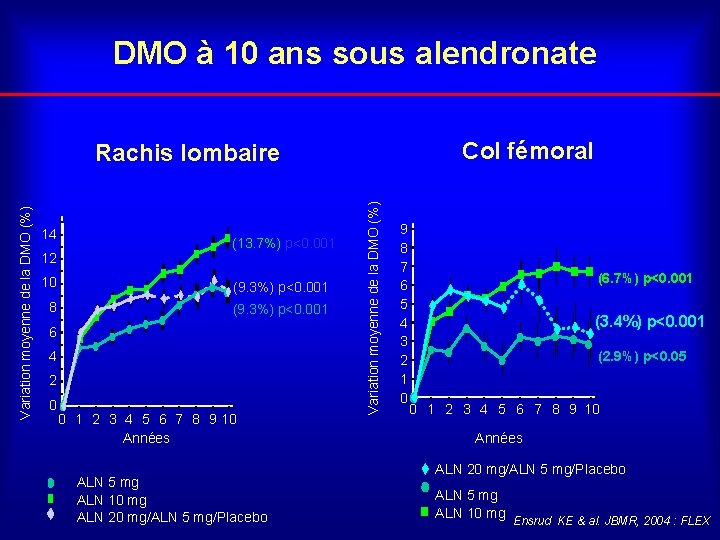
DMO à 10 ans sous alendronate Col fémoral 14 12 (13. 7%) p<0. 001 10 (9. 3%) p<0. 001 8 (9. 3%) p<0. 001 6 4 2 0 0 1 2 3 4 5 6 7 8 9 10 Années ALN 5 mg ALN 10 mg ALN 20 mg/ALN 5 mg/Placebo Variation moyenne de la DMO (%) Rachis lombaire 9 8 7 6 5 4 3 2 1 0 (6. 7%) p<0. 001 (3. 4%) p<0. 001 (2. 9%) p<0. 05 0 1 2 3 4 5 6 7 8 9 10 Années ALN 20 mg/ALN 5 mg/Placebo ALN 5 mg ALN 10 mg Ensrud KE & al. JBMR, 2004 : FLEX
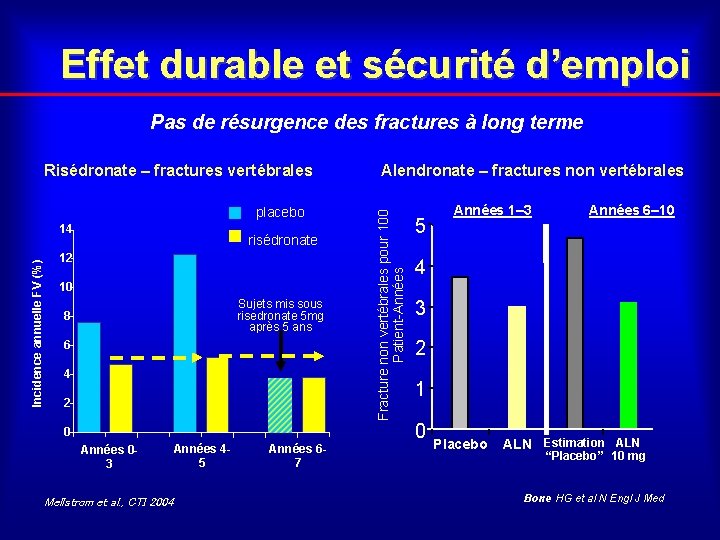
Effet durable et sécurité d’emploi Pas de résurgence des fractures à long terme placebo Incidence annuelle FV (%) 14 risédronate 12 10 Sujets mis sous risedronate 5 mg après 5 ans 8 6 4 2 0 Années 03 Mellstrom et al. , CTI 2004 Années 45 Années 67 Alendronate – fractures non vertébrales Fracture non vertébrales pour 100 Patient-Années Risédronate – fractures vertébrales 5 Années 1– 3 Années 6– 10 4 3 2 1 0 Placebo ALN Estimation ALN “Placebo” 10 mg Bone HG et al N Engl J Med

Tolérance osseuse Paramètres micro-architecture et hétérogénéïté de l’os conservés (données ALN et Ris) Microcrack Etude humaine Femmes traitées par ALN, risé ou pamidronate > 3 ans (en moyenne 6, 5 ans) Témoin = cadavres Évaluation de la fréquence des microcracks Spongieux (trop rare dans os cortical) Pas de différence avec le groupe témoin de • densité des microcracks • longueur des microcraks Pas de relation entre fréquence des craks et • fréquence d’activation • âge • durée du traitement Courtoisie du Pr Chapurlat R, Chapurlat et al. ASBMR 2006
Et les ostéonécroses de la mâchoire? Mai 2006 30 cas recensé dans traitement per os pour ostéoporose (<5% cas recensés) ? Recommandations : pas de données suffisantes pour élaborer un consensus. v- informer le/la patiente et le dentiste v examen dentaire systématique v si traitement invasif nécessaire, si possible avant la mise en route du traitement par BPs v arrêt quelques semaines avant des soins dentaires invasifs v hygiène bucco-dentaire ++ et soins habituels (détartrage) JBMR – octobre 2006, Shane E et al.
- Slides: 55