MB 541 KMYA BLG TAZELEME Ne Gryorsunuz Tablo

ÇMB 541 KİMYA BİLGİ TAZELEME

Ne Görüyorsunuz?
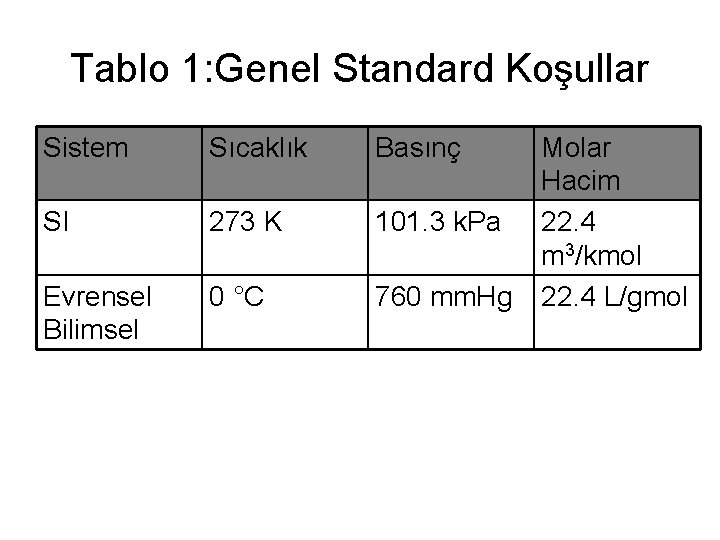
Tablo 1: Genel Standard Koşullar Sistem Sıcaklık Basınç SI 273 K 101. 3 k. Pa Evrensel Bilimsel 0 °C 760 mm. Hg Molar Hacim 22. 4 m 3/kmol 22. 4 L/gmol
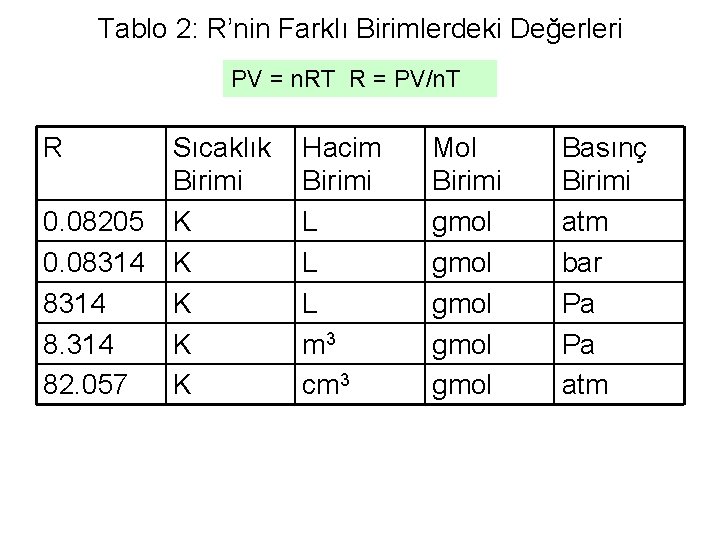
Tablo 2: R’nin Farklı Birimlerdeki Değerleri PV = n. RT R = PV/n. T R 0. 08205 0. 08314 82. 057 Sıcaklık Birimi K K K Hacim Birimi L L L m 3 cm 3 Mol Birimi gmol gmol Basınç Birimi atm bar Pa Pa atm
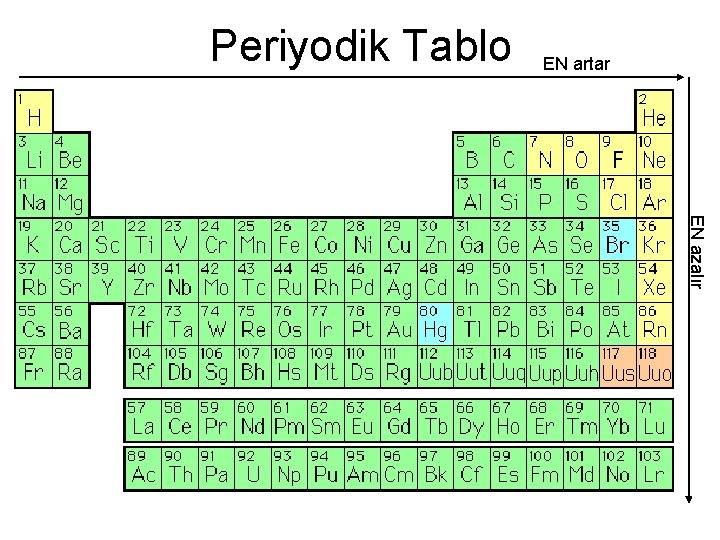
Periyodik Tablo EN artar EN azalır

Molekül Yapısı • Bağlar C-C 83 kcal/mol C=C 146 kcal/mol Kararlı bağlar genellikle bağın oluşması sırasında enerji verirler. Bu enerji ne kadar büyükse bağ o kadar sağlamdır. Bağ sayısı arttıkça açığa çıkan enerji de artar. Bağ nötr bir atomun en dış kabuğundaki elektronları ile olur. (değerlik elektronları) Bir atomun yapacağı bağ sayısı değerlik elektronlarının sayısına bağlıdır.

Soru • Aşağıdaki elementlerdeki değerlik elektronu kaçtır? a) 14 Si b)10 Ne c)11 Na d) 17 Cl

İyonik Bağ Elektronlar bir atomdan diğer atoma transfer edilir. Her zaman ekzotermiktir. Na+ + Cl- Na. Cl (s) DH = -787. 3 kj/mol

Kovalent Bağlar Atomların bir ya da daha fazla çift elektronlarını paylaşarak oluşturdukları bağdır. Cl 2, CO 2, Çoğunlukla elektron paylaşımı da ekzotermiktir.
Diğer Bağlar • Polar Kovalent Bağ: Atomlar elektronları paylaşır ancak elektronlar zamanlarının çoğunu bir atomun çevresinde harcarlar. En tipik örneği sudur. • Koordinat Kovalent Bağı (Paylaşılan elektron çifti tek bir atomdan gelir.

Oksidasyon Hali • Madde(atom/molekül) - elektron= Yükseltgenme – Nao Na+1 + e 1. Tüm atomlar element hallerinde 0 oksidasyon nosuna sahiptir. 2. İyonik Moleküllerde oksidasyon nosu iyon yüküne eşittir. 3. Kovalentler için daha belirsiz ve elektronegativitiye (EN) göre değişiklik gösterir. EN arttıkça elektron çekme gücü artar. CH 4, H=+1, C = -4 4. Metallerle olan bileşikler dışında H’in oksidasyon nosu +1, Oksijen ise genellikle -2 (üç hal dışında) 1. Florlu bileşiklerde +1 2. Hidrojen peroksid (H 2 O 2) ve peroksid (O 2 -2 ) için -1 3. I. Grup metal oksitlerde -1/2

• Atmosferde oksidasyon nosunu yükseltme eğilimi görülür. • Örnekler: O 2 0 Li. H H: -1 Li: +1 HCl H: +1 Cl: -1 NH 3 H: +1 N: -3 Soru: Aşağıdakilerin oksidasyon nolarını yazın. a) H 2 SO 4 b) SO 2 c)H 2 O 2

Serbest Radikaller Eşlenmemiş elektronu olan atom ya da molekül. Bu nedenle aşırı reaktiftirler. Yükselticidirler. H H O-2 H+ 1 elektron: ·OH· CH 3 · H C H Organik Moleküller: Alkanlar Cn. H 2 n+2 Metan CH 4 (1 bağ) Alkenler Cn. H 2 n Etilen C 2 H 4 (2 bağ) Alkinler Cn. H 2 n-2 Acetilin C 2 H 2 (3 bağ) Halka Alkanlar (Cn. H 2 n) Cyclohexane (C 6 H 12) Halka Alkenler Aromatikler (Cn. H 2 n-6) Benzene: C 6 H 6 Çoklu Halkalı Aromatik Hidro Karbonlar (PAH): Birden fazla benzen halkasına sahip maddeler (Naftalin gibi)
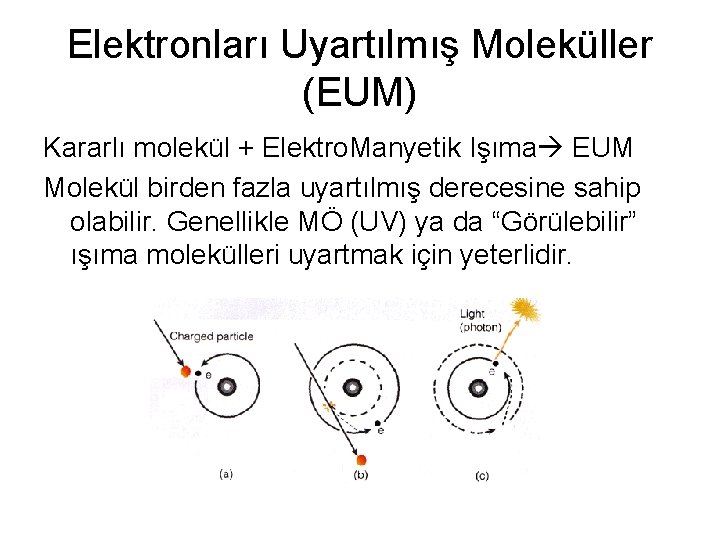
Elektronları Uyartılmış Moleküller (EUM) Kararlı molekül + Elektro. Manyetik Işıma EUM Molekül birden fazla uyartılmış derecesine sahip olabilir. Genellikle MÖ (UV) ya da “Görülebilir” ışıma molekülleri uyartmak için yeterlidir.

Işıma Uyartma İyonlaştırma Atom ya da moleküllerin soğrulan enerji ile bir elektronu bulunduğu orbitalden bir üstteki yüksek enerjili orbitale atar. Atom ya da molekülden elektron çıkarır. Enerji (kj/mol) Kozmik Işınlar 2. 4 x 109 X ışınları 1. 2 x 105 MÖ 1200 Görülebilir 200 Radyo Dalgaları 1. 2 x 10 -5 Tip İyonlaştırıcı
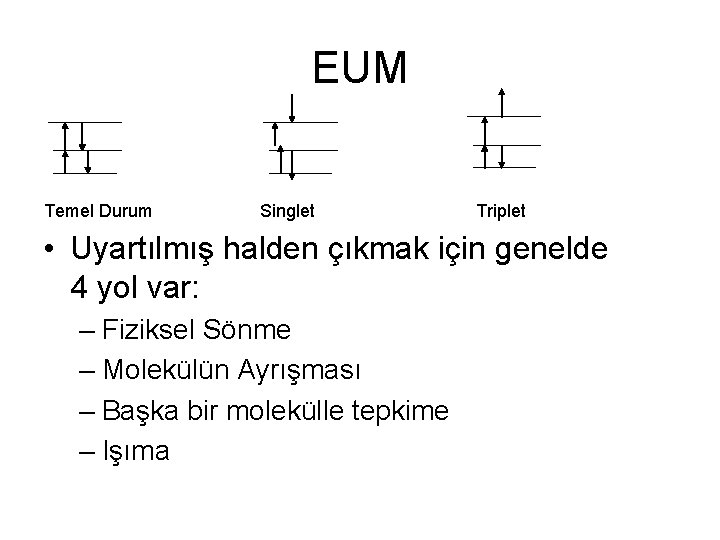
EUM Temel Durum Singlet Triplet • Uyartılmış halden çıkmak için genelde 4 yol var: – Fiziksel Sönme – Molekülün Ayrışması – Başka bir molekülle tepkime – Işıma

Tepkime Eşitleme • __C 4 H 10 + __O 2 __CO 2 + __H 2 O Tepkimeyi eşitleyin. 2 mol bütan yandığında kaç kg CO 2 üretilir? Kütle korundu mu?

Enerji Hesaplamaları • Ekzotermik: ∆H < 0 • Endotermik: ∆H > 0 ∆Hf°: oluşum entalpisi: Elementlerin termodinamik olarak en kararlı oldukları durum için 0 alınır. O 2 (g), en kararlı hali. ∆Hf° = 0 A + B C + D ∆H = Tepkime Entalpisi = (∆HD + ∆HC ) – (∆HA +∆HB ) SORU: Aşağıdakilerden hangisinin ∆Hf° si 0 dır? a) Hg (l) b) Br 2 (g) c) H(g)

YANIT: kj/mol a) Hg (l) ∆Hf° = 0 Standard şartlarda en kararlı hali sıvı b) Br 2 (g) ∆Hf° = 30. 91 Standard şartlarda en kararlı hali sıvı. (sıvıdan gaz haline geçtiği için +30. 91) c) H(g) ∆Hf° = 217. 65 Standard şartlarda en kararlı hali gaz H 2. (H 2 bağının kırılması için +217. 65) Örnek 2 Aşırı zehirli doğasından ve hava ile temas ettiğinde yeşil alevler çıkararak yandığından “yeşil canavar” da denir. B 5 H 9 (pentaboran) bir süre roket yakıtı olarak düşünüldü. B 5 H 9’un yanmasıyla ne kadar enerji açığa çıkar? 2 B 5 H 9(g) + 12 O 2(g) 5 B 2 O 3 (s)+ 9 H 2 O(g) H 2 ve O 2’nin birleşip bağ oluşturduğundan oluşum entalpisi negatif Bileşik ∆Hf° (kj/mol) B 5 H 9(g) 73. 2 O 2(g) 0 H 2 O(g) -24. 82 B 2 O 3(s) -1272. 77

YANIT: ∆H° =5∆Hf°(B 2 O 3) + 9∆Hf°(H 2 O) –(12∆Hf° (O 2) + 2∆Hf° (B 5 H 9) ∆H° = -8686. 6 kj (2 mol B 5 H 9 için) Bir mol için ∆H° = -8686. 6/2 = -4343. 3 kj/mol Bir mol metan yandığında açığa çıkan enerji bunun yaklaşık 5’de biri kadardır.

Gibbs Serbest Enerji • Gibbs Serbest enerji : iş yapma enerjisinin ölçütü • ∆G = ∆H-T∆S Entropi Sıcaklık (K) • ∆G < 0 Tepkime yazıldığı yönde kendiliğinden • ∆G = 0 dengede • ∆G >0 Tepkime yazıldığı yönde kendiliğinden değil

Örnek Aşağıdaki tepkime için ∆H° ve ∆S° değerleri -92. 22 k. J ve -198. 75 J/K’dir. Standard şartlarda Amonyak bu tepkime ile oluşur mu? N 2(g) + 3 H 2(g) 2 NH 3(g) TK = 25° C + 273. 15 = 298. 15 K ∆G = ∆H-T∆S ∆G°= ∆H° - T∆ S° = -92, 220 J - (298. 15 K x -198. 75 J/K) = -92, 220 J + 59, 260 J = -32, 960 J ∆G° = -32. 96 k. J <0 25°C’de tepkime yazıldığı yönde kendiliğinden olur. • ∆G° tabloda standart şartlar için verilmiş serbest oluşum enerjilerini (∆Gf°) kullanarak hesaplanabilir.

∆G° • ∆G° tanım gereği tüm tepkimeye giren ve çıkanların standard şartlardaki durumlarını dikkate alarak aradaki enerji farkını ölçer. Örneğin aşağıdaki tepkime için, tüm katılanlar 1 atm basınçtadır. Yani • N 2(g) + 3 H 2(g) 2 NH 3(g)

∆G ‘yi bilmek yeterli mi? • ∆G ‘den tepkimenin mümkün olup olmadığını tahmin edebiliriz. Ancak tepkimenin olup olmayacağını bilmek o tepkimenin ne kadar hızla olacağını bilmediğimizde, çok fazla anlam içermez.

Tepkime Hızları • Tepkime Hızı: Tepkimede çıkan ürünlerin veya tepkimeye girenlerin birim zamanda molar derişimlerindeki artma ya da azalma. • Tepkime hızı sabit mi? • R = d. A/dt = f( » » Tepkimeye girenlerin derişimi Sıcaklık Tepkimeye girenlerin fiziksel durumu Katalizör (veya inhibitör)’ün varlığı » Işık)

2 N 2 O 5 4 NO 2 + O 2 Tepkime hızı sabit değildir. Girenlerin derişimi azaldıkça azalır.

Hız Kanunları • Elementer tepkimeler için tepkimenin hızı tepkimeye girenlerin derişimiyle doğru orantılı A + B C Hız: R = k[A][B] Derecesi = 2 (A’ya göre 1, B’ye göre 1) A + A B R = k[A]2 Derecesi = 2
![Hız Kanunları A + B C d. A/dt = -k[A][B] d. C/dt = k[A][B] Hız Kanunları A + B C d. A/dt = -k[A][B] d. C/dt = k[A][B]](http://slidetodoc.com/presentation_image_h/cfa4801d9b01ae328f680cf12a22a5ed/image-28.jpg)
Hız Kanunları A + B C d. A/dt = -k[A][B] d. C/dt = k[A][B] A + A B d. B/dt = R=k[A]2 d. A/dt = -2 R=-2 k[A]2

Hız Kanunları • Hız denklemi herhangi bir tepkime için tepkime yazılımından belirlenemez. Deneysel olarak elde edilir. Çünkü bazı tepkimeler birden fazla adımda gerçekleşir. Her bir gerçek adım “elementer” tepkime olarak adlandırılır ve elementer tepkimelerin toplamı tepkime mekanizmasını verir. Tepkimenin toplamda hızını en yavaş olan basamak belirler.

Tepkime Mekanizması • Tek Adım – Cl. NO 2(g) + NO(g) NO 2(g) + Cl. NO(g) • 3 adım • N 2 O 5 NO 2 + NO 3 • NO 2 + NO 3 NO 2 + NO+ O 2 • NO + NO 3 2 NO 2 – 2 N 2 O 5(g) 4 NO 2(g) + O 2(g)
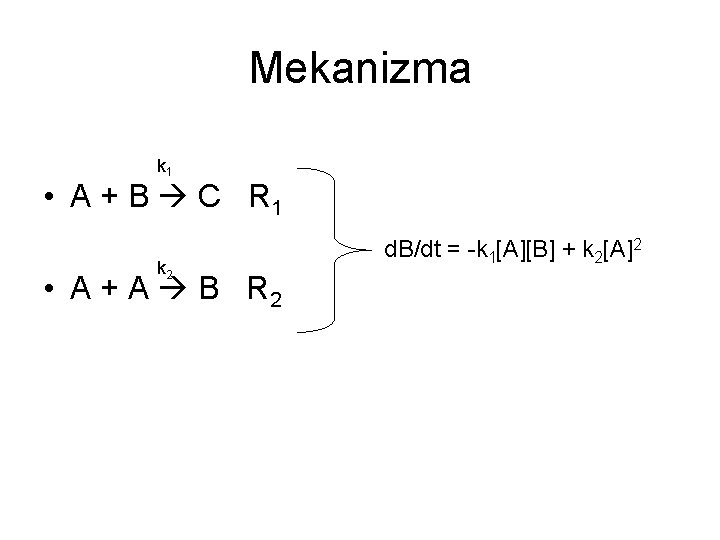
Mekanizma k 1 • A + B C R 1 k 2 • A + A B R 2 d. B/dt = -k 1[A][B] + k 2[A]2
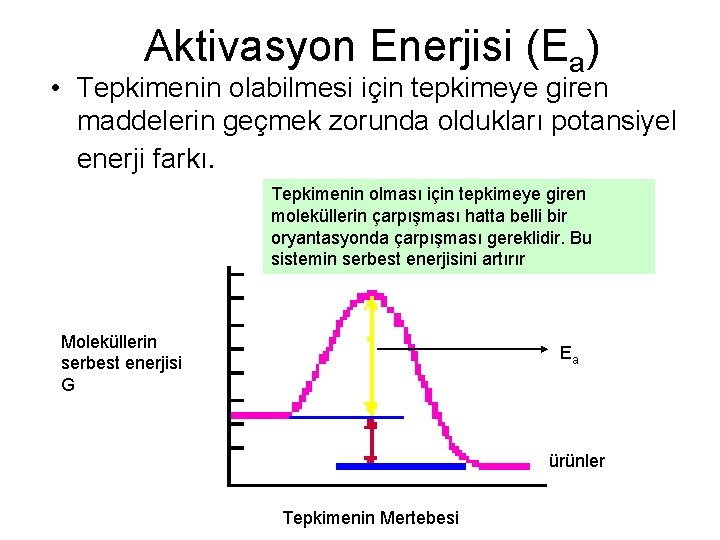
Aktivasyon Enerjisi (Ea) • Tepkimenin olabilmesi için tepkimeye giren maddelerin geçmek zorunda oldukları potansiyel enerji farkı. Tepkimenin olması için tepkimeye giren moleküllerin çarpışması hatta belli bir oryantasyonda çarpışması gereklidir. Bu sistemin serbest enerjisini artırır Moleküllerin serbest enerjisi G Ea ürünler Tepkimenin Mertebesi

Tepkime Hızını Artırmak 1. Tepkimeler genellikle sıcaklığın artmasıyla hızlanırlar. Her 10 ˚C lik artışla hız iki katına çıkar. -Katalizör: Ea’yı düşürerek tepkime hızını artırır. (kırmızı çizgi) Tepkimede tükenmezler. Denge sabitini değiştirmezler. Tepkimeye girenlerin derişimine kıyasla çok düşük miktarlarda yeterli olurlar

KİMYASAL DENGE • Birçok tepkime geriye dönüşlü olup tamamalanmazlar. • k 1 • A + B C + D k_1 • Dengede • R 1 = k 1[A][B] • R 1 = R 2 • R 2 = k-1[C][D] Kd büyükse, k 1 >>k-1 A ve B tamamen C ve D’ye dönüşür. Kd küçükse k 1<<k-1 Çok az A ve B tüketilir. • k 1[A][B] = k-1[C][D]

Le Chatelier (1850 -1936) Prensibi • Sistemde bir değişim olduğunda (derişim, basınç, sıcaklık vb), denge bu stresin etkisini azaltacak yöne kayar. • A + B C + D C ve D ekle

Denge Halinde Gazlar • Gazlarda ideal gaz kanunu kabul edersek, denge ifadesinde derişim yerine her gazın kısmi basıncı kullanılabilir. N 2(g) + 3 H 2(g) 2 NH 3(g) Le Chatelier, bu tepkimeyle basıncı artırarak amonyak sentezlemeye çalıştı. Basınç artarsa tepkime neden amonyak oluşma yönünde ilerler ?

Denge Sabitinin Hesaplanması • Tepkimenin herhangi bir zamanındaki serbest enerjisi (∆G) ile standart serbest enerjisi(∆G° ) arasında şu bağ vardır. R: ideal gaz sabiti (J/mol-K ∆G = ∆G° + RTln. Q T: Sıcaklık (K) Q: Tepkime Kesri (ürünler/girenler) Tepkime dengede ise, ∆G = 0 ∆G° = -RTln. Kd ∆G° ‘nın büyüklüğü standart halin dengeden ne kadar uzakta olduğunun bir göstergesidir. ∆G° küçükse, tepkime dengeye o kadar yakın.

Örnek Tepkime ∆G° (kj) Kd 2 SO 3 2 SO 2(g) + O 2(g) 141. 7 1. 4 x 10 -25 H 2 O(l) H+ (aq) + OH-(aq) 79. 9 1. 0 x 10 -14 N 2(g) + 3 H 2(g) 2 NH 3(g) -32. 9 5. 8 x 105 Zn(s) + Cu 2+ Zn 2+ + Cu(s) -2118 1. 4 x 1037 ∆G° < 0 , tepkime kendiliğinden yazıldığı yönde, K>1

Denge Sabiti ve Sıcaklık • Farklı sıcaklıklardaki denge sabitini bulmak için: • van't Hoff Eşitliği:
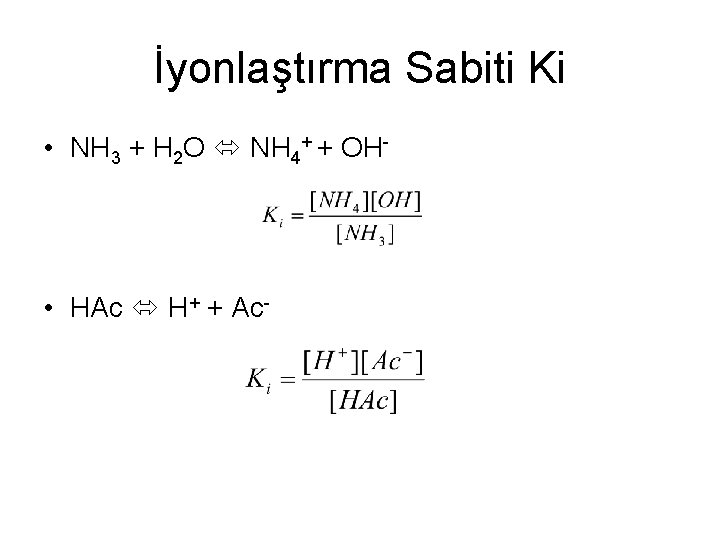
İyonlaştırma Sabiti Ki • NH 3 + H 2 O NH 4+ + OH- • HAc H+ + Ac-
![Faz Dengeleri • 1. Çözünebilirlik Ag. Cl(s) Ag+ + Cl[Ag][Cl] = Ksp = 1. Faz Dengeleri • 1. Çözünebilirlik Ag. Cl(s) Ag+ + Cl[Ag][Cl] = Ksp = 1.](http://slidetodoc.com/presentation_image_h/cfa4801d9b01ae328f680cf12a22a5ed/image-41.jpg)
Faz Dengeleri • 1. Çözünebilirlik Ag. Cl(s) Ag+ + Cl[Ag][Cl] = Ksp = 1. 82 x 10 -10 2. İki faz arasında paylaşım – Suda ve organik karışmayan bir organik sıvıdaki dağılım – X(aq) X(org) K=[Xorg]/[Xaq] • 3. Gaz ve sulu fazda dağılım (Henry Kanunu) A(g) + H 2 O AH 2 O KH=[AH 2 O]/PA=HA NH 3(g) + H 2 O NH 3(aq)

Sabit Hal (Steady State) • Birçok tepkime çok aktif bileşikler içerir. (Serbest kökler gibi). Oluşur oluşmaz diğer tepkime tarafından kullanılır. Tepkimenin hızı belirlenirken yalancı sabit hal yaklaşımı kullanılır. (Pseudo Steady State)

Yalancı Sabit Hal • Oluşma hızı ile tükenme hızı birbirine eşit. • d. A*/dt = 0 (A*’nın derişimi zamanla değişmiyor demek değil, sadece A*’nın değişimi diğerlerine oranla öyle hızlı ki, onu sabit halde kabul edebiliriz. )

Serbest Kökler ve Zincirleme Tepkimeler • H 2 + Br 2 2 HBr (elementer tepkime değil) • • Başlatma Yayılma Engelleme Sonlanma Serbest kökleri oluşturan basamak Tükettiği kadar serbest kök üreten basamaklar Br 2 2 Br· ka Br· + H 2 HBr + H· kb H· + Br 2 HBr + Br· kc Ürünün oluşmasına yol açmayan basamak H· + HBr H 2 + Br· kd Serbest köklerin tüketildiği basamak Br· + Br· Br 2 ke
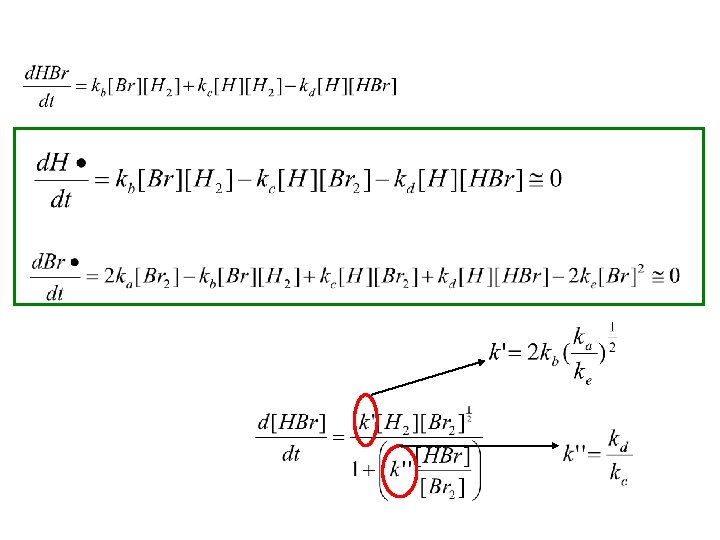

Dikkat Edilecek Durumlar • C 2 H 6 C 2 H 4+H 2 tepkimesi (etanın eten oluşturması) tepkimesi birinci dereceden tepkime kinetiği izler. Bu durumda etanın direkt etene dönüştüğü düşünülebilir. Ancak etanın etene dönüşmesi gerçekte daha karmaşık bir tepkime kinetiğine sahiptir.

Etan Eten • Başlama C 2 H 6 2 CH 3· • Yayılma • Sonlanma ka CH 3· + C 2 H 6 CH 4 + C 2 H 5· kb C 2 H 5· C 2 H 4 + H· kc H· + C 2 H 6 H 2 + C 2 H 5· kd H· + C 2 H 5· C 2 H 6 ke Tüm kök türler için yalancı sabit hal varsayımı yapılarak hız denklemleri oluşturulup mekanizma çözüldüğünde, tepkimenin birinci derece kinetiği ortaya çıkar. k 1

Zincir Tepkime Örneği • A + M A· + M • A· + M A + M • A· B+C
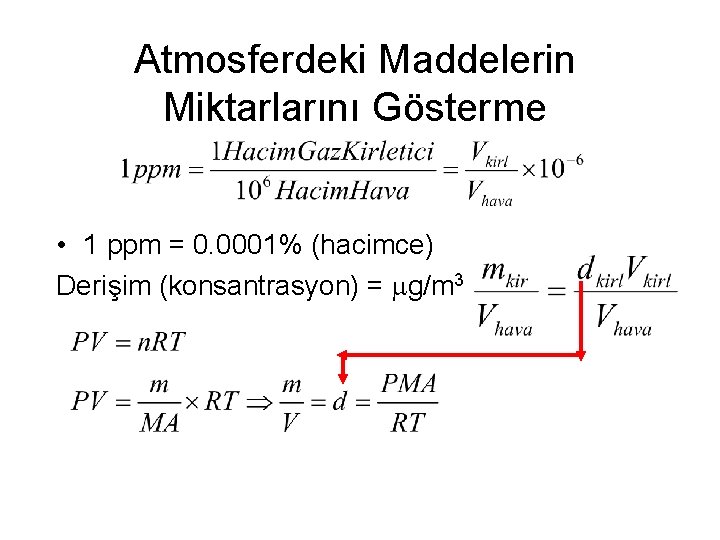
Atmosferdeki Maddelerin Miktarlarını Gösterme • 1 ppm = 0. 0001% (hacimce) Derişim (konsantrasyon) = mg/m 3
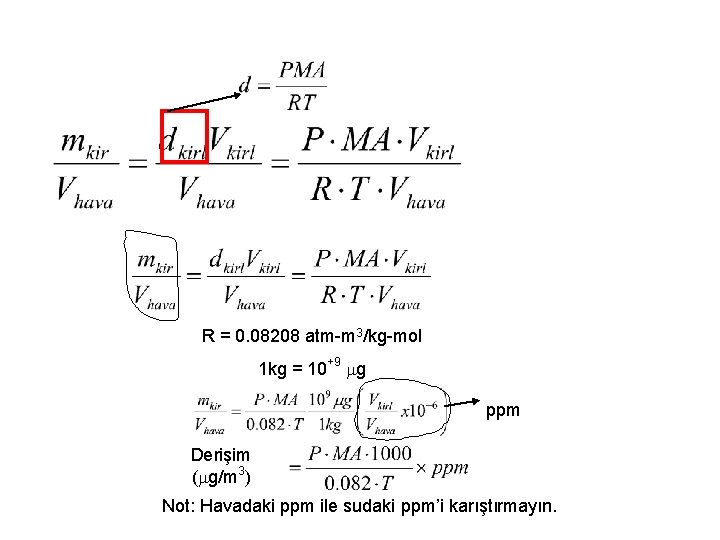
R = 0. 08208 atm-m 3/kg-mol 1 kg = 10+9 mg ppm Derişim (mg/m 3) Not: Havadaki ppm ile sudaki ppm’i karıştırmayın.

Diğer Konsantrasyon Birimleri • molekül/cm 3 : Genellikle kimyasal hız denklemlerini yazarken çok aktif olan türlerin konsantrasyonlarını ifade ederken kullanılır. Molar konsantrasyona çevirmek için Avogadro’s Sayısı 6. 023 x 1023 molekül/gr-mol kullanılır. • mg/m 3

Sorular: • Van’t Hoff eşitliğini aşağıdaki eşitlikleri kullanarak elde ediniz.

Sorular: • N 2 + 3 H 2 2 NH 3(g) tepkimesinin 500 K’daki denge sabitini nasıl hesaplarsınız? • Dengedeki bir karışımdaki N 2 ve H 2 kısmi basıncını biliyorsanız NH 3’un kısmi basıncını nasıl hesaplarsınız? • Belli miktarlarda N 2 ve H 2’den oluşan bir karışımın bir tanka konulduğunu ve dengeye ulaştığını biliyorsunuz diyelim. Dengedeki karışım bileşimini nasıl belirlersiniz?

Sorular • Sudaki ppm ile atmosferdeki ppm’in farkı nedir? • 2 HI H 2 + I 2 için deneysel olarak I 2’nin oluşum hız denklemi : • d. I 2/dt = k[HI]2 • Buna göre aşağıdaki ifadeleri oluşturun. • d. H 2/dt = • d. HI/dt =

Atmosfer Kimyası -Terminoloji • Kirletici: İnsan faaliyetleri sonucu ortaya çıkan ve normal konsantrasyon değerlerinin üstünde bir miktarda bulunan ve çevre üzerinde net olarak bozucu etkisi olan madde • Bulaşkan (kontaminant): Çevrede bulunan normal bileşimden sapmaya neden olan ancak kirletici olarak sınıflandırılmamış madde • Kaynak: Kirleticinin ortaya çıktığı yer • Alıcı: Kirleticiden etkilenen her şey (insanlar, yerler, ciğerler vs. ) • Alıcı Havuz: Kirleticinin uzun süreli depolandığı yer

Atmosfer Kimyası -Terminoloji • Birincil Kirletici: Kaynaktan doğrudan yayılan kirletici, SO 2 • İkincil Kirletici: Birincil kirleticilerin atmosferdeki kimyasal tepkimeleri sonucu oluşan kirleticiler, O 3

Atmosfer Kimyası -Terminoloji • Atmosfer: Sıcaklık profiline göre bölümlere bölünmüş, troposfer yeryüzüne en yakın olanı. Bu derste çoğunlukla bu tabakada olan kimyasal tepkimeleri konuşacağız. Ayrıca Troposferin üzerindeki stratosferdeki Ozon ile ilgili tepkimelere de bakacağız. • Hidrosfer: Yeryüzündeki tüm su ortamları (okyanus, göl, deniz, ırmak, buzullar, buz dağları ve yer altı suyu) • Litosfer: Yeryüzünün dış kısımları, yerkabuğundaki mineraller ve toprak • Biyosfer: Yaşayan organizmalar ve onların bulunduğu yakın çevre
- Slides: 57