Maturazione dei linfociti B La storia dei linfociti

Maturazione dei linfociti B
La “storia” dei linfociti B

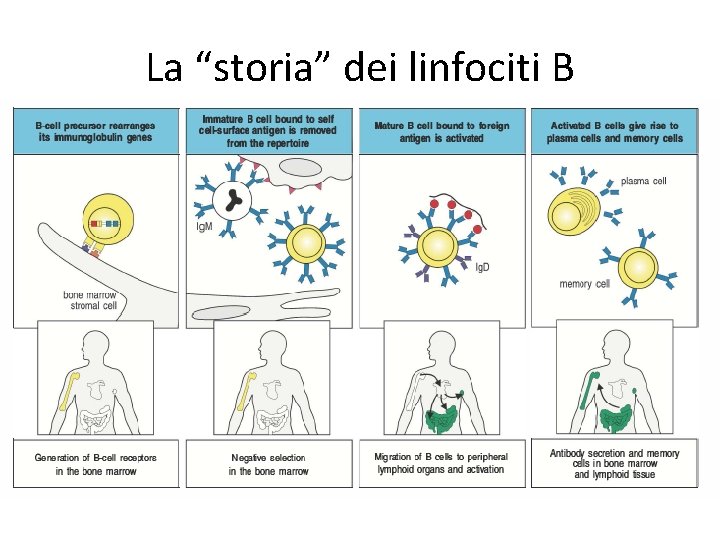
La “storia” dei linfociti B • I vari stadi di maturazione linfocitaria sono definiti dalle varie fasi di riarrangiamento ed assemblaggio del BCR • Superamento dei checkpoint di controllo per il passaggio alla fase successiva di maturazione • I linfociti derivano da un precursore (CLP, common lymphoid progenitor) che origina dalle cellule staminali ematopoietiche del midollo osseo • Il microambiente del midollo osseo contribuisce in maniera determinante a fornire I segnali necessari per la maturazione • Le cellule stromali del midollo osseo: • interagiscono con I precursori dei linfociti B mediante specifiche molecule di adesione • Producono citochine che stimolano proliferazione e differenziamento • Per esempio le cellule stromali del midollo osseo esprimono il ligando di Flt 3, che è un recettore presente su progenitori ematopoietici che dopo il legame con il ligando attiva il differenziamento a CLP
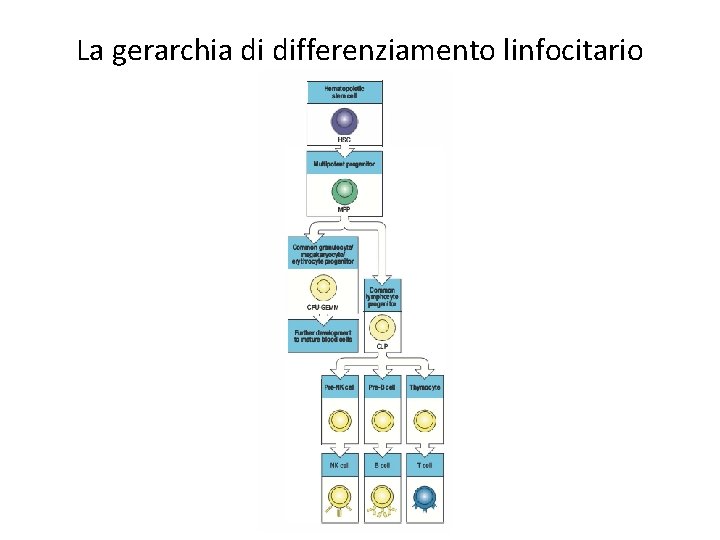
La gerarchia di differenziamento linfocitario
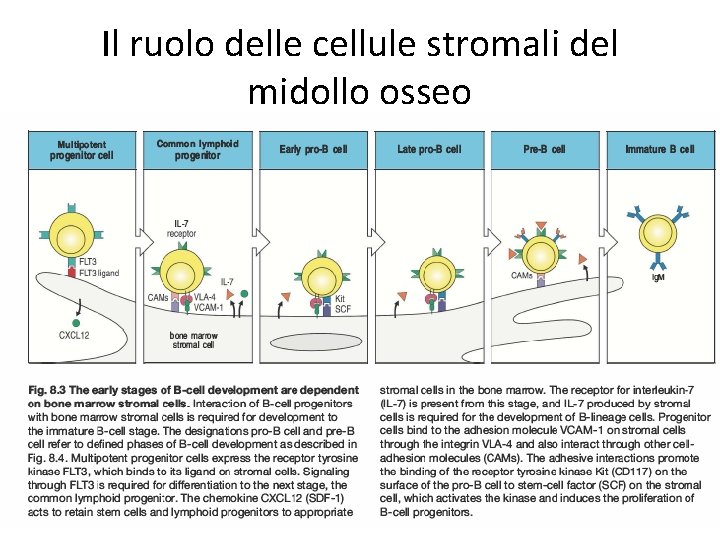
Il ruolo delle cellule stromali del midollo osseo
Il ruolo delle cellule stromali del midollo osseo
Le cellule B si localizzano in zone diverse del midollo osseo in funzione dello stadio di differenziamento Le cellule migrano verso l’asse centrale del midollo osseo, dove la presenza di larghi sinusoidi favorisce l’export dal midollo osseo
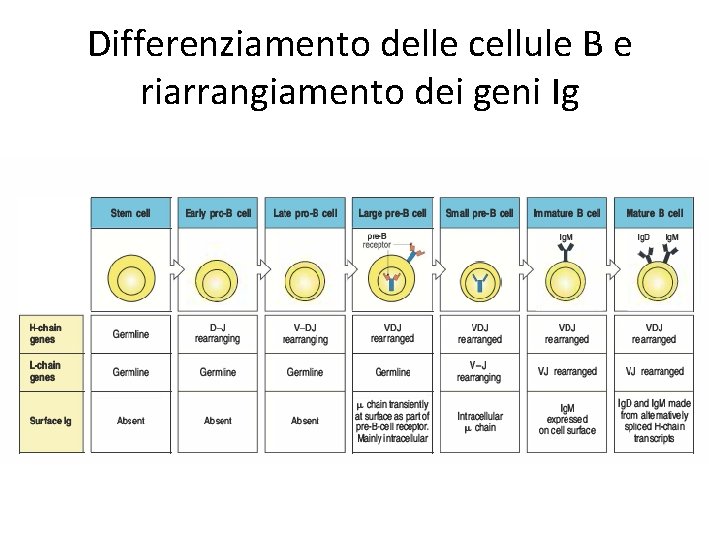
Differenziamento delle cellule B e riarrangiamento dei geni Ig
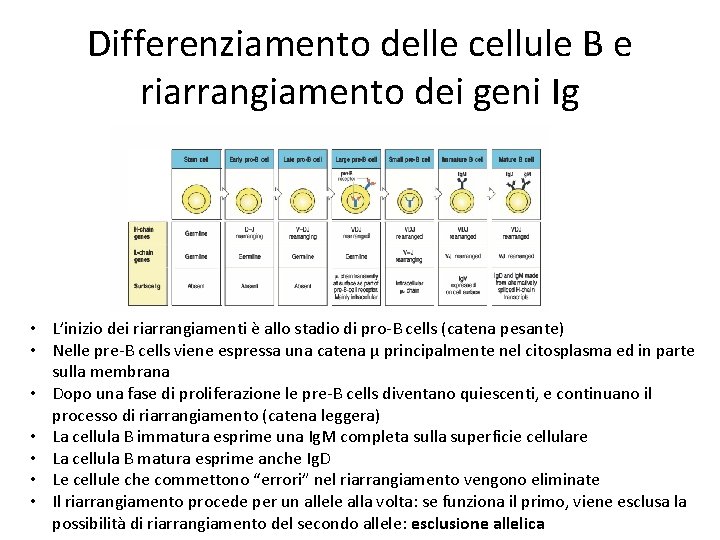
Differenziamento delle cellule B e riarrangiamento dei geni Ig • L’inizio dei riarrangiamenti è allo stadio di pro-B cells (catena pesante) • Nelle pre-B cells viene espressa una catena µ principalmente nel citosplasma ed in parte sulla membrana • Dopo una fase di proliferazione le pre-B cells diventano quiescenti, e continuano il processo di riarrangiamento (catena leggera) • La cellula B immatura esprime una Ig. M completa sulla superficie cellulare • La cellula B matura esprime anche Ig. D • Le cellule che commettono “errori” nel riarrangiamento vengono eliminate • Il riarrangiamento procede per un allele alla volta: se funziona il primo, viene esclusa la possibilità di riarrangiamento del secondo allele: esclusione allelica

Il differenziamento delle cellule B correla con l’espressione di proteine di superficie
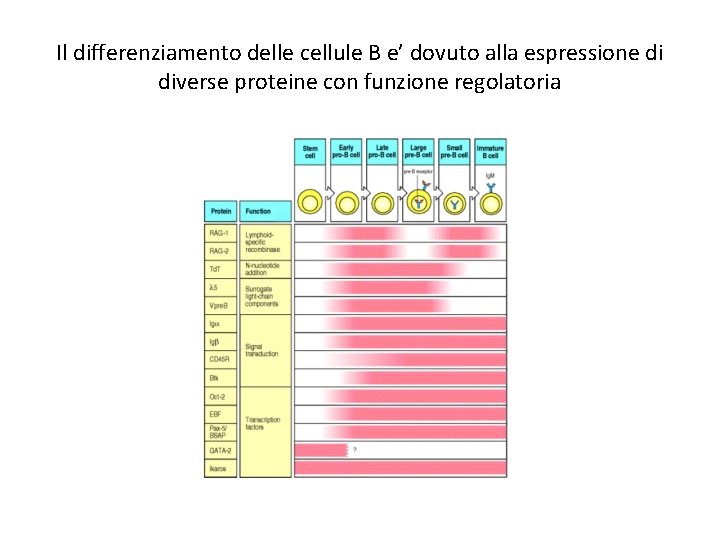
Il differenziamento delle cellule B e’ dovuto alla espressione di diverse proteine con funzione regolatoria
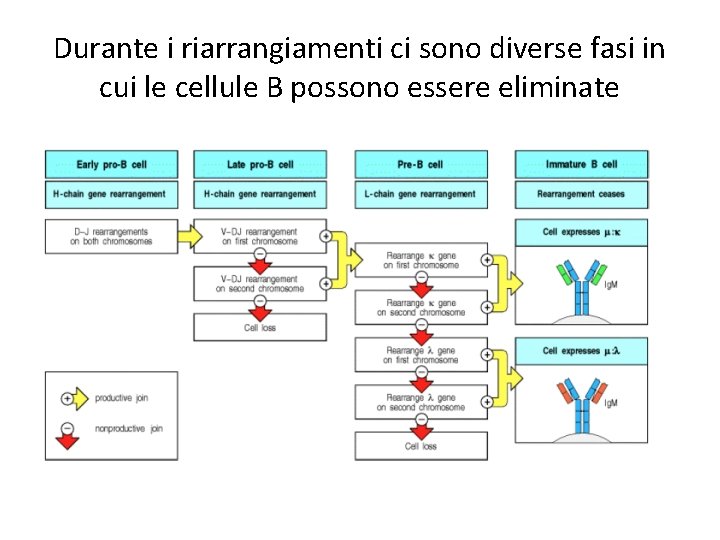
Durante i riarrangiamenti ci sono diverse fasi in cui le cellule B possono essere eliminate
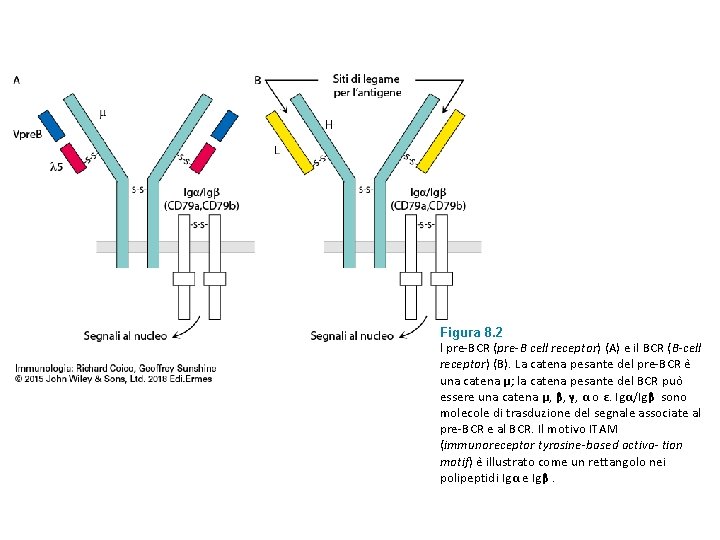
Figura 8. 2 l pre-BCR (pre-B cell receptor) (A) e il BCR (B-cell receptor) (B). La catena pesante del pre-BCR e una catena μ; la catena pesante del BCR puo essere una catena μ, β, γ, α o ε. Igα/Igβ sono molecole di trasduzione del segnale associate al pre-BCR e al BCR. Il motivo ITAM (immunoreceptor tyrosine-based activa- tion motif) e illustrato come un rettangolo nei polipeptidi Igα e Igβ.
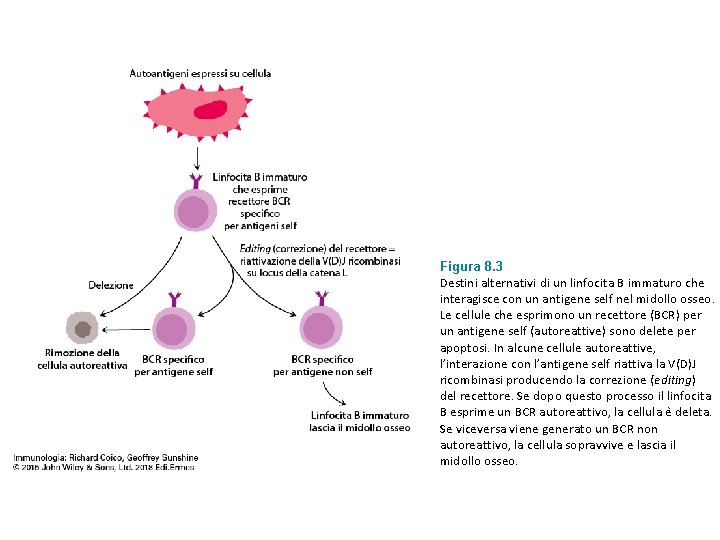
Figura 8. 3 Destini alternativi di un linfocita B immaturo che interagisce con un antigene self nel midollo osseo. Le cellule che esprimono un recettore (BCR) per un antigene self (autoreattive) sono delete per apoptosi. In alcune cellule autoreattive, l’interazione con l’antigene self riattiva la V(D)J ricombinasi producendo la correzione (editing) del recettore. Se dopo questo processo il linfocita B esprime un BCR autoreattivo, la cellula e deleta. Se viceversa viene generato un BCR non autoreattivo, la cellula sopravvive e lascia il midollo osseo.
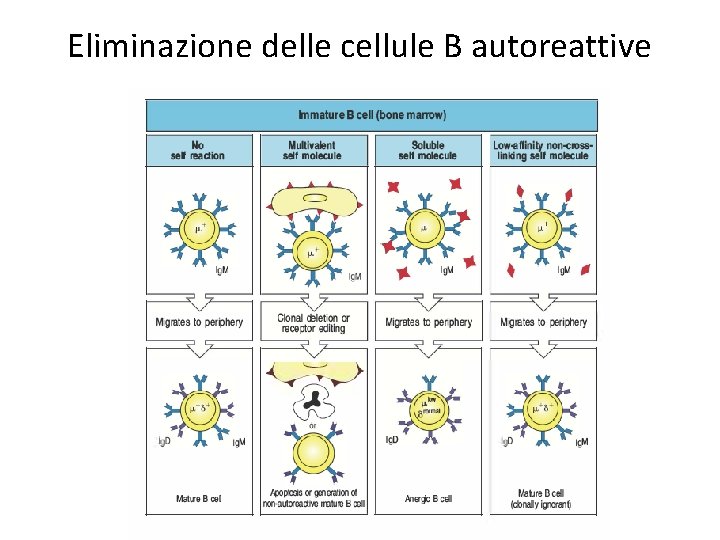
Eliminazione delle cellule B autoreattive

Eliminazione delle cellule B immature autoreattive • Cellule non autoreattive: migrazione ai tessuti linfatici periferici dove maturano • Cellule autoreattive verso antigeni multivalenti (esempio MHC): o avviene un “receptor editing” per cambiare specificità antigenica, oppure le cellule vanno incontro a morte programmata • Se la molecola “self” è solubile, le cellule possono maturare in periferia ma esprimono poche Ig sulla superficie e sono dette anergiche, non possono essere attivate dal legame con l’antigene • Se l’antigene “self” è inaccessibile o ha affinità scarsa per il BCR, la cellula B matura normalmente ma è potenzialmente autoreattiva
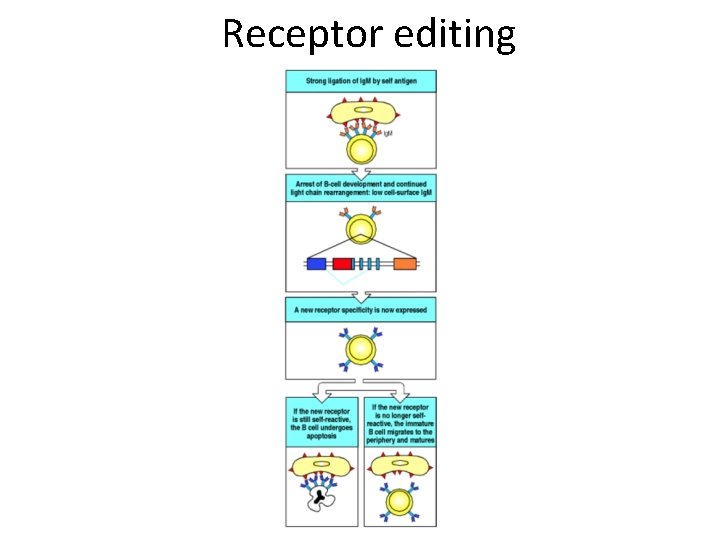
Receptor editing

Maturazione dei linfociti T
La “storia” dei linfociti /
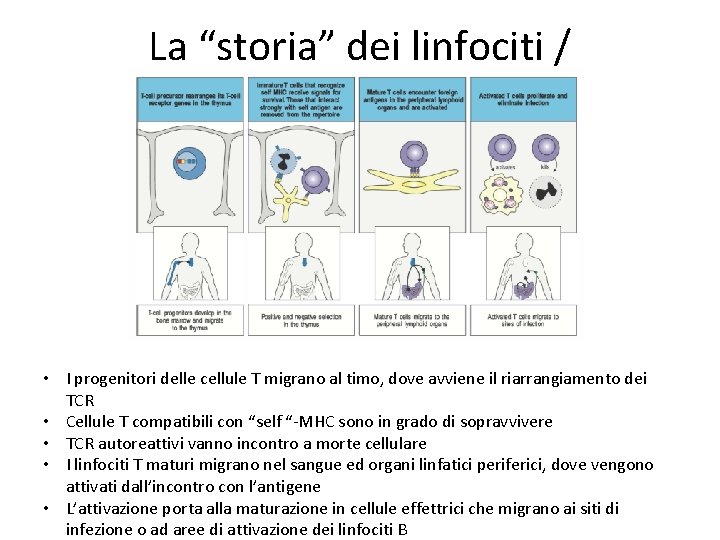
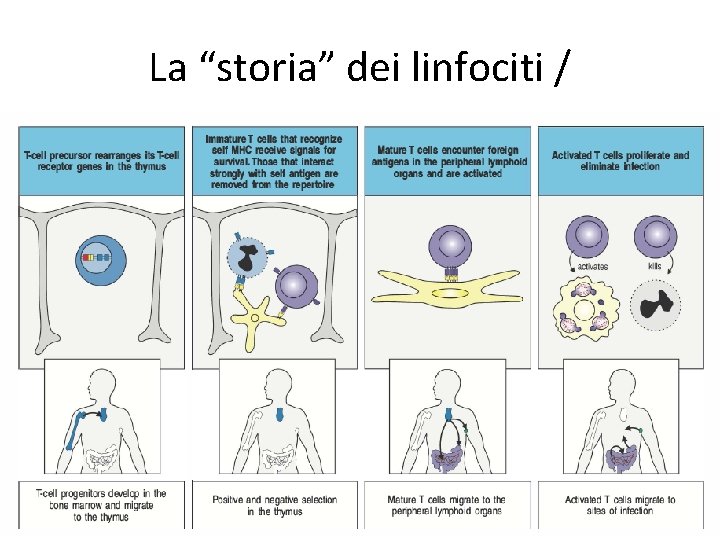
La “storia” dei linfociti / • I progenitori delle cellule T migrano al timo, dove avviene il riarrangiamento dei TCR • Cellule T compatibili con “self “-MHC sono in grado di sopravvivere • TCR autoreattivi vanno incontro a morte cellulare • I linfociti T maturi migrano nel sangue ed organi linfatici periferici, dove vengono attivati dall’incontro con l’antigene • L’attivazione porta alla maturazione in cellule effettrici che migrano ai siti di infezione o ad aree di attivazione dei linfociti B
Struttura del timo

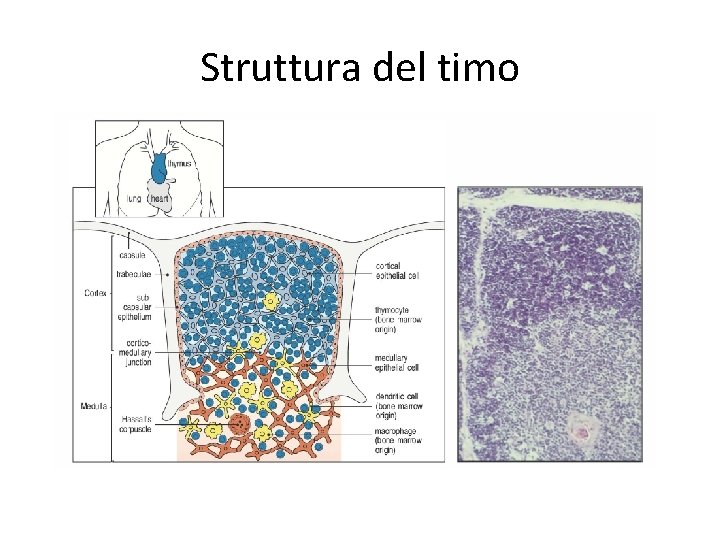
Struttura del timo • Zona corticale: timociti immaturi, con cellule epiteliali corticali, e macrofagi per rimuovere le cellule che vanno incontro a morte • Zona midollare: timociti maturi, cellule epiteliali midollari, macrofagi e cellule dendritiche. I corpuscoli di Hassall sono probabilmente areee di distruzione cellulare • I timociti nella zona corticale interna sono le cellule T che vanno incontro a selezione (>98% dei timociti totali), mentre nella zona esterna c’è proliferazione • IN assenza di timo non c’è sviluppo dei linfociti T (sindrome di De George nell’uomo, topi “nude”)

Il network delle cellule epiteliali del timo

Il timo è critico per lo sviluppo dei linfociti T
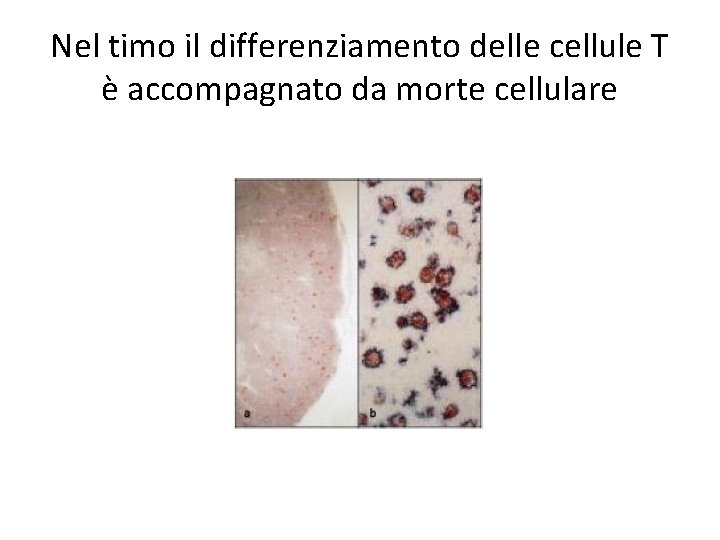
Nel timo il differenziamento delle cellule T è accompagnato da morte cellulare
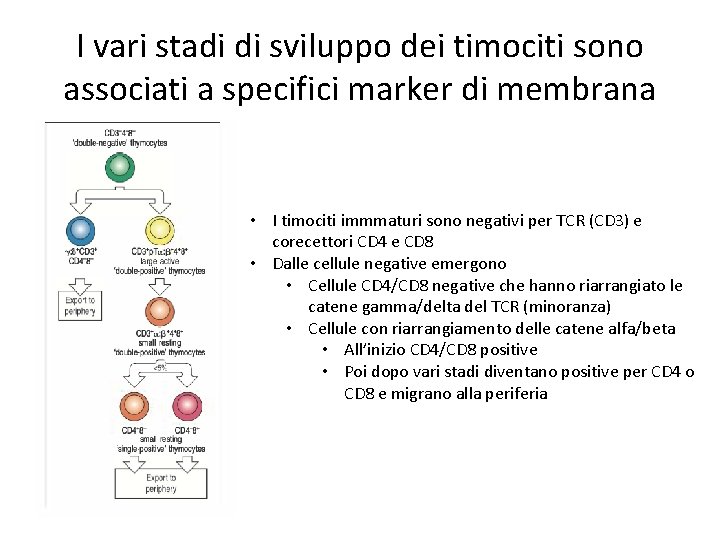
I vari stadi di sviluppo dei timociti sono associati a specifici marker di membrana • I timociti immmaturi sono negativi per TCR (CD 3) e corecettori CD 4 e CD 8 • Dalle cellule negative emergono • Cellule CD 4/CD 8 negative che hanno riarrangiato le catene gamma/delta del TCR (minoranza) • Cellule con riarrangiamento delle catene alfa/beta • All’inizio CD 4/CD 8 positive • Poi dopo vari stadi diventano positive per CD 4 o CD 8 e migrano alla periferia
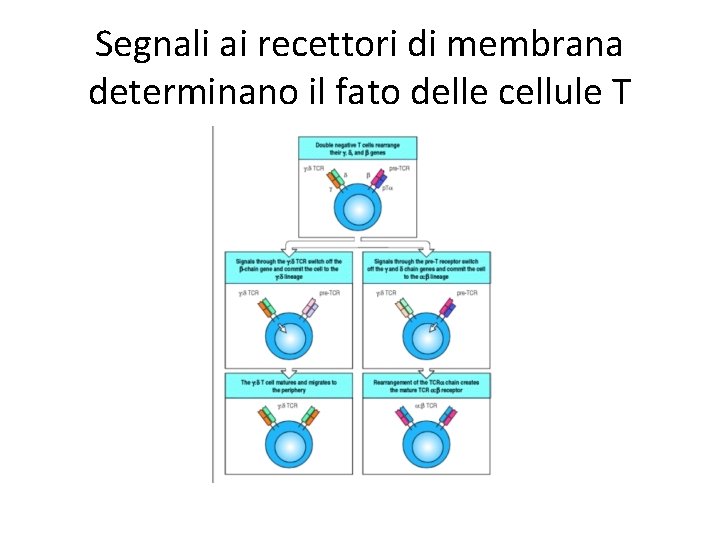
Segnali ai recettori di membrana determinano il fato delle cellule T

Correlazione degli stadi di sviluppo con riarrangiamento genico ed espressione di proteine di membrana
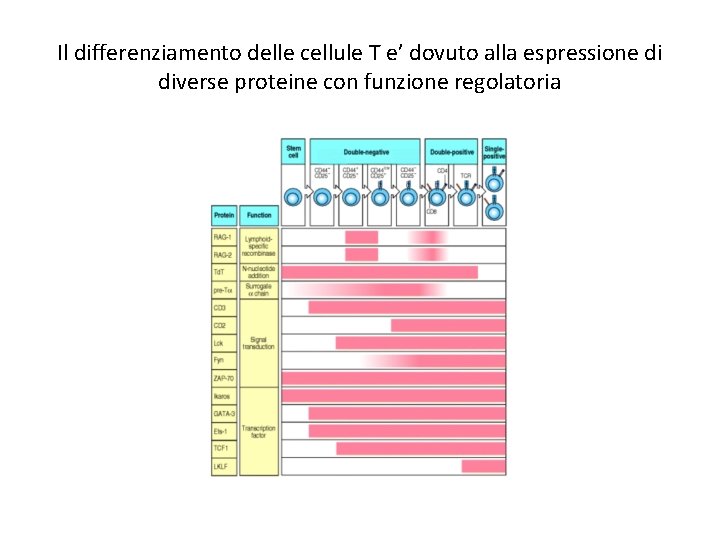
Il differenziamento delle cellule T e’ dovuto alla espressione di diverse proteine con funzione regolatoria
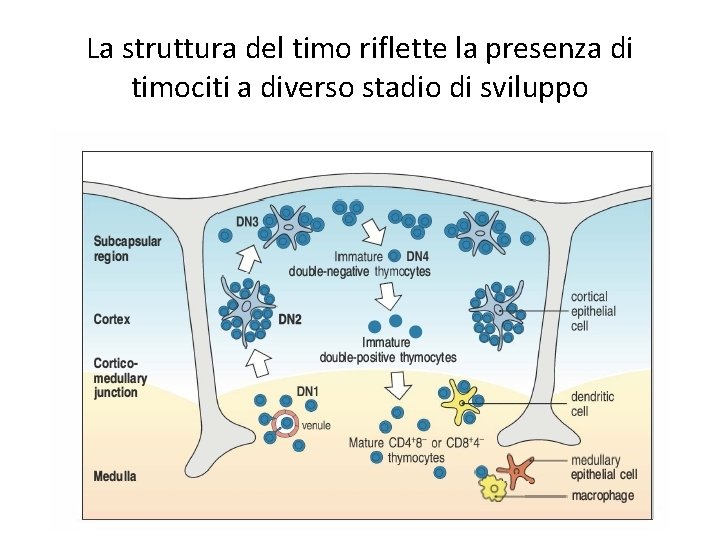
La struttura del timo riflette la presenza di timociti a diverso stadio di sviluppo

Caratteristiche del processo di selezione • Solo I timociti I cui recettori interagiscono con complessi self-MHC/peptide possono sopravvivere e maturare • Il repertorio di TCR ha una intrinseca specificità per molecole MHC • L’interazione dei timociti con le cellule epiteliali corticali timiche determina il processo di selezione positiva • I timociti che reagiscono fortemente con antigeni self/MHC vengono eliminati

Come viene distinto il processo di selezione negativa da quella positiva? • Sia la selezione positiva che quella negativa dipendono dall’interazione di TCR con peptidi/MHC self • Teoricamente, devono esistere meccanismi in grado di distinguere timociti potenzialmente capaci di danneggiare I tessuti self da quelli che possono sfruttare il riconoscimento del self per diventare efficaci linfociti T effettori • L’ipotesi corrente è che la discriminazione fra I due fati è data dalla forza dell’interazione del TCR con peptide/MHC self – Interazione debole: selezione positiva – Interazione forte: selezione negativa
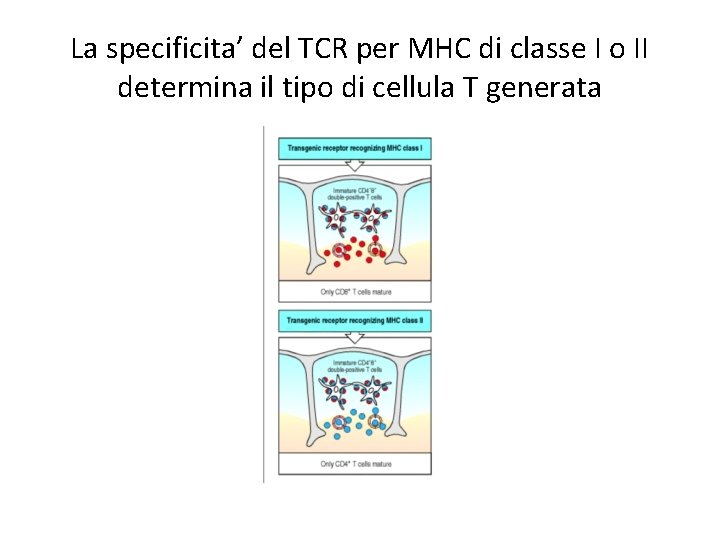
La specificita’ del TCR per MHC di classe I o II determina il tipo di cellula T generata
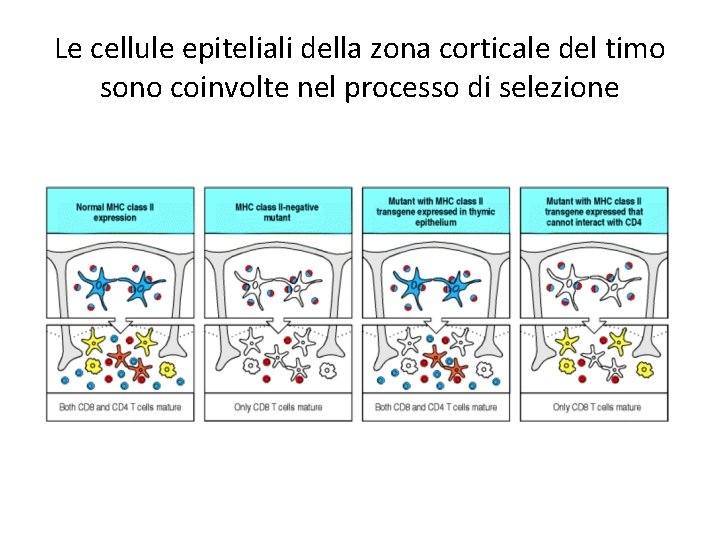
Le cellule epiteliali della zona corticale del timo sono coinvolte nel processo di selezione
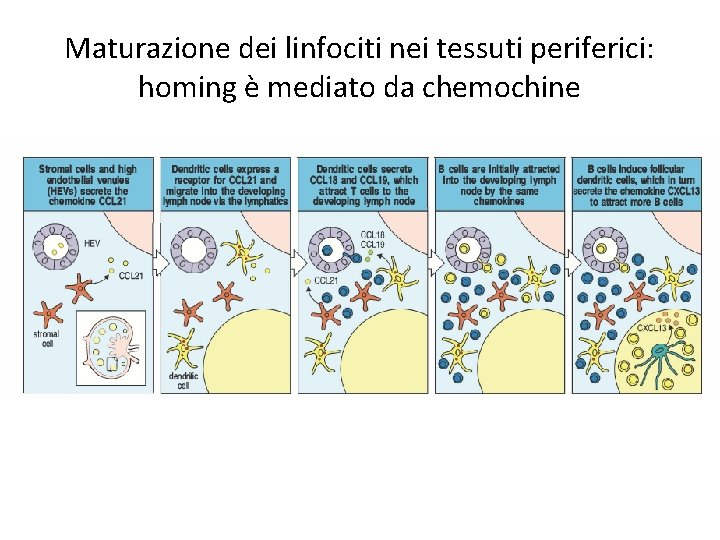
Maturazione dei linfociti nei tessuti periferici: homing è mediato da chemochine
- Slides: 35